ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ПРИРОДОПОЛЬЗОВАНИЯ
|
УТВЕРЖДАЮ
__________ А.Н. Кичемасов «21» марта 2012 г. |
КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ
АТМОСФЕРНОГО ВОЗДУХА И ВЫБРОСОВ В АТМОСФЕРУ
МЕТОДИКА ИЗМЕРЕНИЙ МАССОВЫХ
КОНЦЕНТРАЦИЙ СЕРОВОДОРОДА И МЕТИЛМЕРКАПТАНА
В ПРОМЫШЛЕННЫХ ВЫБРОСАХ ПРЕДПРИЯТИЙ
МЕТОДОМ ПОТЕНЦИОМЕТРИЧЕСКОГО
АРГЕНТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
ПНД Ф 13.134-2002
(ФР.1.31.2007.03824)
Методика допущена для целей
государственного
экологического контроля
МОСКВА 2002 г.
(издание 2012 г.)
Методика рассмотрена и одобрена федеральным бюджетным учреждением «Федеральный центр анализа и оценки техногенного воздействия» (ФБУ «ФЦАО»).
1 ВВЕДЕНИЕ
Настоящая методика предназначена для измерения массовых концентраций сероводорода (H2S) и метилмеркаптана (ММ) в промышленных выбросах предприятий в диапазоне концентраций 5 - 50000 мг/м3 по сероводороду и 5 - 100000 мг/м3 по метилмеркаптану.
Сероводород - бесцветный газ с резким характерным запахом, температура плавления tпл = -85,54 °С, температура кипения tкип = -60,35 °C, растворим в спирте, воде, сильный восстановитель.
Порог ощущения запаха сероводорода 0,000012 мг/дм3, однако, в высоких концентрациях ввиду паралича обонятельного нерва запах сероводорода не ощущается и это очень опасно для жизни. ПДК в воздухе рабочей зоны 10 мг/м3, ПДКм.р. в атмосферном воздухе населенных мест 0,008 мг/м3. Сильный яд, вызывающий смерть от остановки дыхания, раздражает дыхательные пути и глаза.
Метилмеркаптан (CH3SH) - газ с резким сильным запахом, температура плавления tпл = -122,97 °C, температура кипения tкип = 5,95 °C, растворим в воде, спирте, эфире.
Порог ощущения запаха метилмеркаптана 0,0001 мг/м3. ПДК в воздухе рабочей зоны 0,8 мг/м3, ПДКм.р. в атмосферном воздухе населенных мест 9 × 10-6 мг/м3. При концентрации 0,001 - 0,002 мг/дм3 и вдыхании в течение 5 минут работоспособность нарушается, но потом восстанавливается.
Методика селективная. Определению мешает этил- и пропил- меркаптаны, осаждаясь вместе с метилмеркаптаном, но их концентрация в выбросах предприятий незначительна и ими можно пренебречь.
Продолжительность анализа 15 минут, а с учетом отбора пробы - 40 - 60 минут.
2 ПРИПИСАННЫЕ ХАРАКТЕРИСТИКИ ПОКАЗАТЕЛЕЙ ТОЧНОСТИ ИЗМЕРЕНИЙ
Значения показателя точности методики используют при:
- оформлении результатов измерений, выдаваемых лабораторией;
- оценке деятельности лабораторий на качество проведения испытаний;
- оценке возможности использования результатов измерений при реализации методики измерений в конкретной лаборатории.
Таблица 1 - Диапазон измерений, значения показателей повторяемости, точности, и правильности методики
|
Наименование определяемого компонента, диапазон измерений, мг/м3 |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr, % |
Показатель правильности (границы относительной систематической погрешности при Р = 0,95), ± δc, % |
Показатель точности1 (границы относительной погрешности методики при вероятности Р=0,95), ± δ, % |
|
Сероводород От 5 до 50000 вкл. |
7 |
14 |
20 |
|
Метилмеркаптан От 5 до 100000 вкл. |
7 |
14 |
20 |
______________
1 Соответствует расширенной стандартной неопределенности при коэффициенте охвата k = 2
3 СРЕДСТВА ИЗМЕРЕНИЙ, ВСПОМОГАТЕЛЬНОЕ ОБОРУДОВАНИЕ, РЕАКТИВЫ И МАТЕРИАЛЫ
При выполнении измерений должны быть применены следующие средства измерений, вспомогательное оборудование, реактивы и материалы:
3.1 Средства измерений и вспомогательное оборудование
- Мономер универсальный типа И-130 по ТУ 25.05.11044-84 или другой с погрешностью не более ± 1 мВ.
- Весы лабораторные специального или высокого класса точности с ценой деления не более 0,1 мг, наибольшим пределом взвешивания не более 210 г по ГОСТ Р 53228-2008.
- Весы технические среднего или обычного класса точности по ГОСТ Р 53228-2008
- Гири по ГОСТ 7328-2001
- Мешалка магнитная по ТУ 25.11.834-80.
- Электрод сульфид серебряный ЭСС-01 по ТУ 25.05.1742-80.
- Электрод хлорсеребряный насыщенный ЭВЛ-1МЗ по ГОСТ 17792-72.
- Вакуумметр жидкостный U-образный по ГОСТ 27758-88.
- Электроаспиратор по ТУ 20.11.1414 или другой аспиратор
- Дифманометр-тягомер типа ДТмМП по ГОСТ 2405-88
- Барометр по ТУ 25-04-1797-75
- Термометр жидкостной лабораторный по ГОСТ 29224-91
- Поглотитель Рыхтера по ГОСТ 25336-82.
- Склянки с нижним тубусом вместимостью 5 дм3 по ГОСТ 25336-82.
- Цилиндры 1-25, 1-50 по ГОСТ 1770-74.
- Стаканы В, 11-2-100, 150 ТС по ГОСТ 25336-82.
- Пипетки градуированные 6-2-5, 5-2-2, 2-2-10, 4-2-1 по ГОСТ 29227-91.
- Колбы мерные 1-50-2, 1-100-2, 1-500-2, 1-1000-2 по ГОСТ 1770-74.
- Бюретки 6-2-5, 6-2-2, 3-2-25 по ГОСТ 29252-91.
Примечания.
1 Допускается использование других средств измерений утвержденных типов, обеспечивающих измерения с установленной точностью.
2 Допускается использование другого оборудования с метрологическими и техническими характеристиками, аналогичными указанным.
3 Средства измерений должны быть поверены в установленные сроки.
3.2 Реактивы
- Серебро азотнокислое по ГОСТ 1277-75, чда.
- Калий хлористый по ГОСТ 4234-77, хч.
- Калий азотнокислый по ГОСТ 4217-77, хч.
- Аммиак водный по ГОСТ 3760-79, хч., 25 % раствор.
- Натрия гидрокись по ГОСТ 4328-77, хч.
- Метиловый оранжевый
- Фенолфталеин по ТУ 6-09-4530-77
- Кислота соляная по ГОСТ 3118-77, хч.
- Калий йодистый по ТУ 6-09-2540-72, хч, стандарт-титр С(КI) = 0,1 моль/дм3.
- Вода дистиллированная по ГОСТ 6709-72.
- Рутин по ТУ 6-09-10-498-76.
- Натрий сернистый 9-ти водный (сульфид натрия) по ГОСТ 2053-77, хч.
- Натрий хлористый по ГОСТ 4233-77, хч.
- Спирт этиловый ректификованный по ГОСТ 18300-87.
Примечание.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных.
4 МЕТОД ИЗМЕРЕНИЙ
Метод основан на выделении сероводорода и метилмеркаптана щелочным поглотительным раствором и измерении концентрации сульфид- и меркаптид-ионов методом ионометрического титрования при селективном осаждении сульфид- и меркаптид-ионов в виде нерастворимых солей серебра.
Массовую концентрацию компонентов в растворе находят по резкому изменению (скачку) потенциала измерительного электрода, соответствующему эквивалентной затрате титранта. Присутствие элементарной серы в выбросных газах приводит к образованию в щелочном растворе органополисульфидов в результате реакции серы с метилмеркаптаном. Ее количество необходимо учитывать при расчете концентрации метилмеркаптана в промвыбросах. Сероводород и метилмеркаптан не мешают потенциометрическому определению друг друга, так как произведения растворимости образующихся осадков сульфида и меркаптида серебра различаются на 27 порядков (ПР Ag2S = l,36 × 10-49, ПР CH3SAg = l,3 × 10-22).
Первыми количественно из раствора осаждаются сульфид-ионы, так как осадок сульфида серебра менее растворим.
В качестве поглотительного раствора используют растворы гидроксида натрия C(NaOH) = 5 моль/дм3 (20 %) или C(NaOH) = 8 моль/дм3 (32 %). После поглощения порции газов массовая концентрация щелочи должна быть не менее C(NaOH) = 2 моль/дм3 (8 %), так как дальнейшее уменьшение щелочности раствора приведет к уменьшению его поглотительной способности по отношению к метилмеркаптану.
Массовую концентрацию титранта (серебра азотнокислого) определяют потенциометрическим титрованием фиксанальным раствором йодистого калия.
Данные по полноте поглощения компонентов приведены в Приложении А.
5 ТРЕБОВАНИЯ БЕЗОПАСНОСТИ, ОХРАНЫ ОКРУЖАЮЩЕЙ СРЕДЫ
При работе в лаборатории необходимо соблюдать следующие требования техники безопасности.
5.1 При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76.
5.2 Электробезопасность при работе с электроустановками соблюдается по ГОСТ Р 12.1.019-2009.
5.3 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83.
5.4 Организация обучения работающих безопасности труда производится по ГОСТ 12.0.004-90.
5.5 Содержание вредных веществ в воздухе не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005-88.
5.6 Работы на высоте следует проводить в соответствии с требованиями СНиП III-4-80.
При отборе проб должны соблюдаться общие правила безопасности для предприятий и организаций соответствующей отрасли.
К отбору проб допускаются операторы технологических установок и пробоотборщики, прошедшие специальный инструктаж.
6 ТРЕБОВАНИЯ К КВАЛИФИКАЦИИ ОПЕРАТОРОВ
К выполнению измерений и обработке их результатов допускают специалистов, имеющих высшее или среднее специальное химическое образование, имеющих опыт работы на потенциометрической установке и стаж работы в химической лаборатории не менее одного года, прошедших соответствующий инструктаж и получивших удовлетворительные результаты при выполнении контроля процедуры измерений.
7 ТРЕБОВАНИЯ К УСЛОВИЯМ ИЗМЕРЕНИЙ
При выполнении измерений должны быть соблюдены следующие условия:
- температура окружающего воздуха (20 ± 5) °С;
- относительная влажность не более 80 % при t = 25 °С;
- атмосферное давление от 97,3 до 104,6 кПа;
- напряжение переменного тока (220 + 22/-33) В;
- частота переменного тока (50 ± 1) Гц;
- механические воздействия, внешние электрические и магнитные поля, влияющие на работоспособность оборудования, должны быть исключены.
8 ПОДГОТОВКА К ВЫПОЛНЕНИЮ ИЗМЕРЕНИЙ
При подготовке к выполнению измерений массовых концентраций сероводорода и метилмеркаптана в промышленных выбросах выполняют следующие операции: собирают связку поглотителей Рыхтера для выделения сероводорода и метилмеркаптана из газового потока; потенциометрическую установку; готовят растворы и устанавливают концентрацию титранта, выбирают способ установления точки эквивалентности.
8.1 Подготовка поглотителей
Готовят связку поглотителей Рыхтера, соединенных резиновыми или полиэтиленовыми муфтами: первый поглотитель пустой для улавливания пыли и паров жидкости; второй, третий и четвертый поглотители заполняют по 10 см3 раствора гидроксида натрия C(NaOH) = 5 моль/дм3 (или 8 моль/дм3) для поглощения сероводорода и метилмеркаптана.
Если после поглощения порции газов концентрация раствора щелочи менее 2 моль/дм3 (8 %), то необходимо увеличить исходную концентрацию щелочи до 8 моль/дм3 (32 %) и повторить отбор.
Раствор хранят в полиэтиленовой таре, концентрацию проверяют титриметрически не реже одного раза в три месяца.
Поглотительные растворы гидроксида натрия предварительно охлаждают смесью льда или снега с хлористым натрием.
Систему поглотителей проверяют на герметичность.
8.2 Подготовка потенциометрической установки
Собирают потенциометрическую установку, состоящую из иономера, бюретки, магнитной мешалки и двух электродов (сульфид- и хлорид серебряных), соединенных электролитическими мостиками, заполненными раствором калия азотнокислого С (KNO3) = 0,1 моль/дм3.
8.3 Приготовление растворов
8.3.1 Приготовление раствора соляной кислоты с молярной концентрацией 0,5 моль/дм3
1. Раствор соляной кислоты готовят из стандарт-титра 0,1 н раствора, добавляя его к дистиллированной воде в мерной колбе на 200 дм и доводя до метки дистиллированной водой.
2. В колбу вместимостью 1 дм3 наливают 500 см3 дистиллированной воды, добавляют 41 см3 концентрированной соляной кислоты (пл. 1,19) и доводят до метки дистиллированной водой.
Срок хранения в таре из темного стекла шесть месяцев.
8.3.2 Приготовление раствора гидроксида натрия с молярной концентрацией 5 моль/дм3
200 г гидроксида натрия взвешивают на технических весах. Навеску при постоянном перемешивании стеклянной палочкой растворяют в 1 дм3 дистиллированной воды. После охлаждения раствора до комнатной температуры определяют его концентрацию (суммарно с карбонатами). Для этого 1 см3 раствора гидроксида натрия С (NaOH) = 5 моль/дм3 титруют раствором соляной кислоты С (НСl) = 0,5 моль/дм3 в присутствии 1 - 2 капель фенолфталеина до исчезновения розовой окраски в течение 1 минуты титрованием.
Раствор хранят в полиэтиленовой таре не более двух месяцев.
8.3.3 Приготовление раствора гидроксида натрия с молярной концентрацией 8 моль/дм3
320 г гидроксида натрия взвешивают на технических весах. Навеску при постоянном перемешивании стеклянной палочкой растворяют в 1 дм3 дистиллированной воды. После охлаждения раствора до комнатной температуры определяют его концентрацию, как указано в п. 8.3.2.
Раствор хранят в полиэтиленовой бутыли не более двух месяцев.
8.3.4 Приготовление растворов калия йодистого с молярной концентрацией 0,1 моль/дм3, 0,02 моль/дм3 и 0,002 моль/дм3
Исходный раствор калия йодистого С(КI) = 0,1 моль/дм3 готовят из стандарт-титра. Растворяют его в дистиллированной воде в мерной колбе вместимостью 1 дм3 и доводят до метки дистиллированной водой. Хранят в течение одного месяца.
Рабочие стандартные растворы С(КI) = 0,02 и 0,002 моль/дм3 готовят последовательным разбавлением в 5 и 50 раз исходного раствора дистиллированной водой в мерных колбах непосредственно перед определением.
8.3.5 Приготовление раствора азотнокислого калия с молярной концентрацией 0,1 моль/дм3
10 г калия азотнокислого помещают в мерную колбу вместимостью 1 дм3 и доводят до метки дистиллированной водой.
Срок хранения 3 месяца.
8.3.6 Приготовление водного раствора метилового оранжевого с массовой долей 0,1 %
0,1 г метилового оранжевого помещают в колбу вместимостью 100 см3 и доводят до метки дистиллированной водой.
Раствор хранят в защищенном от света месте до внешних изменений.
8.3.7 Приготовление раствора фенолфталеина с массовой долей 0,1 % в 60 % растворе этилового спирта
0,1 г фенолфталеина помещают в колбу вместимостью 100 см3 и доводят до метки 60 % этиловым спиртом.
Раствор хранят в защищенном от света месте до внешних изменений.
8.3.8 Приготовление раствора серебра азотнокислого с молярной концентрацией 0,1 моль/дм3, 0,02 моль/дм3 и 0,02 моль/дм3
Для приготовления раствора серебра азотнокислого C(AgNO3) = 0,l моль/дм3 в мерную колбу вместимостью 1 дм3 помещают навеску серебра азотнокислого 17 г, взвешенную на технических весах. Доливают в колбу до метки дистиллированную воду. Хранят в темной склянке, периодически проверяя концентрацию по п. 8.4.
Раствор серебра азотнокислого C(AgNO3) = 0,02 и 0,002 моль/дм3 готовят последовательным разбавлением в 5 и 50 раз исходного раствора дистиллированной водой в мерных колбах непосредственно перед определением.
8.4 Установление концентрации серебра азотнокислого
В стакан для титрования вместимостью 100 - 150 см3 помещают 5 см раствора калия йодистого С(КI) = 0,1 моль/дм3, приготовленного из стандарт-титра, и 15 - 20 см3 дистиллированной воды.
Стакан ставят на магнитную мешалку, опускают в него магнит, два электрода (сульфид- и хлорсеребряные), включают мешалку. Бюретку вместимостью 25 см3 заполняют раствором серебра азотнокислого C(AgNO3) = 0,l моль/дм3.
Потенциал сульфидсеребряного электрода изменяется от -150 мВ до 150 мВ (величины Енач и Екон зависят от концентрации растворов серебра азотнокислого и калия йодистого).
На рис. Г.1 (приложение Г) приведена типичная кривая титрования.
Концентрацию раствора серебра азотнокислого рассчитывают по уравнению:
![]() (1)
(1)
где СKI - концентрация раствора калия йодистого, С(КI) = 0,1 моль/дм3;
VkI - объем раствора калия йодистого, взятого для анализа, Vki = 5 см3;
![]() - объем раствора серебра азотнокислого, пошедший на
осаждение йодид-ионов, см3.
- объем раствора серебра азотнокислого, пошедший на
осаждение йодид-ионов, см3.
Концентрацию титранта серебра азотнокислого проверяют при приготовлении новой порции по фиксанальному раствору йодистого калия.
8.5 Установление точки эквивалентности при осаждении сульфид- и меркаптид-ионов раствором серебра азотнокислого
При поглощении сероводорода и метилмеркаптана образуются сульфид- и меркаптид-ионы, которые осаждаются ионами серебра.
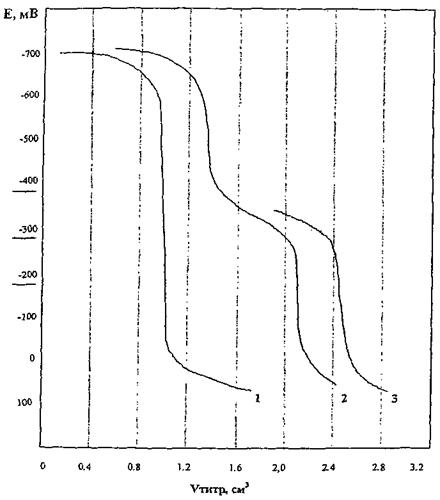
Типичные кривые титрования приведены на рис. Г.2 (приложение Г).
Эквивалентный объем титранта находят по методу Хаана-Вейлера расчетным путем по формуле:
![]() (2)
(2)
|
Объем титранта, см3 |
Потенциал, Е, мВ |
|
V1 |
Е1 |
|
v2 |
Е2 Х1 = Е2 - Е1 |
|
v3 |
Е3 Х2 = Е3 - Е2 |
|
v4 |
Е4 Х3 = Е4 - Е3 |
при этом X1 £ X2 £ X3
Для расчета эквивалентного объема титранта необходимо в районе точки эквивалентности титрант добавлять одинаковыми порциями. В расчет берут измерения до скачка (V1, Е1), скачок (V2, Е2) и после скачка (V3, Е3; V4, Е4) потенциала электрода.
8.6 Отбор газовых проб
Объем газа, проходящего через газоход при рабочих и нормальных условиях, определяют согласно ГОСТ 17.2.4.06-90 «Охрана природы. Атмосфера. Методы определения скорости и расхода газопылевых потоков, отходящих от стационарных источников загрязнения».
Исследуемую пробу газа отбирают с помощью газозаборной трубки через штуцер, установленный на прямолинейном участке газохода на достаточном удалении от вентиляторов, задвижек, отводов и других подобных устройств, а также с учетом безопасного проведения работ и удобства пробоотбора. Другой конец газозаборной трубки встык присоединяют к четырем последовательно соединенным поглотителям Рыхтера.
Поглотители Рыхтера соединяют встык резиновыми или полиэтиленовыми муфтами.
Выходную трубку четвертого поглотителя Рыхтера подсоединяют к электроаспиратору. Если давление в исследуемой системе превышает 101,3 кПа, выходную трубку четвертого поглотителя Рыхтера соединяют с газовым счетчиком (ГСБ-400).
Когда установка собрана, систему проверяют на герметичность. Для этого плотно закрывают с помощью винтового зажима вход в установку и открывают зажим на резиновой трубке, соединяющей систему с аспиратором. Если система герметична, уровень ротаметра электроаспиратора остается неизменным. С помощью мыльного раствора устанавливают места, где нарушена герметичность.
Исследуемую пробу газа аспирируют с объемным расходом 0,4 дм3/мин в течение 10 - 30 мин. Отбирают 4 - 12 дм3 газа в зависимости от содержания в исследуемых выбросах сероводорода и метилмеркаптана. Во время отбора проб регистрируют температуру, атмосферное давление и давление (или разрежение) в газоходе.
По окончании пробоотбора необходимо определить конечную концентрацию щелочи в поглотительном растворе, которая должна быть не менее 2 моль/дм3. Для этого 1 см3 раствора гидроксида натрия С(NaOH) = 5 моль/дм3 титруют раствором соляной кислоты С(НСl) = 0,5 моль/дм3 в присутствии 1 - 2 капель фенолфталеина до исчезновения розовой окраски в течение 1 минуты. Фиксируют объем соляной кислоты, пошедший на титрование (V1). К бесцветному раствору добавляют 1 каплю метилоранжа (раствор желтый) и продолжают титровать раствором соляной кислоты до перехода от желтой окраски к оранжевой. Фиксируют объем соляной кислоты, пошедший на титрование щелочного раствора с метилоранжем.
Концентрацию гидроксида натрия (моль/дм3) рассчитывают по формуле:
![]() (3)
(3)
где V1 - количество соляной кислоты, пошедшее на титрование пробы щелочного раствора с индикатором фенолфталеином, см3;
V2 - количество соляной кислоты, пошедшее на титрование пробы щелочного раствора с индикатором метилоранжем, см3;
СHCl - массовая концентрация соляной кислоты,
СHCl = 0,5 моль/дм3;
Va - объем пробы щелочного раствора, отобранный для анализа, см3.
Если конечная концентрация щелочи после отбора проб составляет менее 2 моль/дм3, то пробоотбор повторяют с использованием поглотительного раствора с концентрацией щелочи 8 моль/дм3.
После пропускания порции газа поглотители отсоединяют от системы и закрывают свободные отростки заглушками. Пробы анализируют в день отбора или консервируют 0,001 %-ным раствором рутина (арабино-галактана) на 5 - 7 дней.
9 ВЫПОЛНЕНИЕ ИЗМЕРЕНИЙ
Щелочные поглотительные растворы из поглотителей Рыхтера переносят в цилиндр и измеряют объем (Vo), перемешивают.
В зависимости от предполагаемой концентрации 1 - 20 см3 объединенного поглотительного раствора (Va) помещают в стакан вместимостью 100 см3, добавляют 2 см3 25 %-ного водного раствора аммиака и раствор гидроксида натрия2 C(NaOH) = 5 моль/дм3 до общего объема 20 см3. В стакан опускают электроды, включают магнитную мешалку и измеряют начальный потенциал сульфидсеребряного электрода (Еo).
______________
2 Если предполагаемая концентрация сероводорода неизвестна, то используют раствор гидроксида натрия концентрации 8 моль/дм3.
Если значение потенциала Еo = -780 мВ и более отрицательное, то объем пробы (Va) уменьшают или титруют раствором серебра азотнокислого с C(AgNO3) = 0,02 моль/дм3 до потенциала (-710 ÷ -720) мВ. Затем концентрацию титранта меняют на C(AgNO3) = 0,002 моль/дм3 и продолжают титровать.
При добавлении порции титранта потенциал изменяется на 20 - 30 мВ. В точках эквивалентности потенциал резко изменяется на 500 - 700 мВ при добавлении одной капли (0,03 - 0,04 см3) титранта.
Если начальный потенциал электрода составляет (-700 ÷ -500) мВ, то в качестве титранта сразу используют раствор азотнокислого серебра C(AgNO3) = 0,002 моль/дм3. Титрование проводят, как описано выше.
В зависимости от содержания в растворе сульфид-, меркаптид-ионов, а также элементарной серы, на кривых титрования появляются скачки потенциала, которые соответствуют определенному иону (см. таблицу 2).
Таблица 2
|
Количество скачков |
Изменение потенциала сульфидсеребряного электрода, мВ |
Потенциал эквивалентности, мВ |
|||
|
сероводород |
метил-меркаптан |
полисульфиды |
|||
|
Сульфид-ион |
1 |
-710 ÷ -690 до +60 ÷ 100 |
-300 ÷ -320 |
- |
- |
|
Сульфид-ион и меркаптид-ион |
2 |
-710 ÷ -690 до -450 |
-500 ÷ -560 |
- |
|
|
-140 ÷ -170 |
|||||
|
-420 ÷ -380 до +60 ÷ 100 |
|||||
|
Сульфид-ион, меркаптид-ион, полисульфид (элемент сера) |
3 |
-710 ÷ -560 |
-670 ÷ -660 |
||
|
-560 ÷ -350 |
-140 ÷ -170 |
||||
|
-250 ÷ -100 |
-560 ¸ -570 |
||||
|
Меркаптид-ион |
1 |
-420 ÷ -480 до +60 |
-200 ÷ -270 |
||
Если в растворе присутствуют только сульфид-ионы, то потенциал сульфидсеребряного электрода изменяется от (-710 ÷ -690) мВ до (+60 ÷ 100) мВ. Потенциал точки эквивалентности для сероводорода (-300 ÷ -320) мВ (рис. Г.2, кривая 1, приложение Г).
Если в поглотительном растворе кроме сульфид-ионов присутствуют меркаптид-ионы, то сразу же после осаждения сульфида серебра начинает осаждаться меркаптид серебра и на кривой титрования появляется второй скачок потенциала. Начальный потенциал электрода при осаждении меркаптид-иона составляет (-420 ÷ -380) мВ. В этом случае потенциал точки эквивалентности для сероводорода смещается в область (-520 ÷ -560) мВ и скачок потенциала составляет (200 ÷ 300) мВ (рис. Г.2, кривая 2, приложение Г).
Если начальное значение потенциала электрода меньше (-600) мВ, но отрицательней, чем потенциал точки эквивалентности сероводорода (-320 ÷ -300) мВ в случае отсутствия метилмеркаптана или (-500 ÷ -560) мВ в случае присутствия последнего), то увеличивают объем пробы поглотительного раствора. Титруют по каплям раствором азотнокислого серебра C(AgNO3) = 0,002 моль/дм3.
Если начальный потенциал электрода менее отрицателен, чем потенциал точки эквивалентности сероводорода, аналитически определяемое количество сульфид-ионов в растворе отсутствует.
Если начальный потенциал электрода составляет (-420 ÷ -480) мВ, то в поглотительном растворе содержится только меркаптид-ионы (рис. Г.2, кривая 3, приложение Г).
Потенциал сульфидсеребряного электрода при осаждении меркап-тид-ионов изменяется от (-420) мВ до (+60) мВ (потенциал титранта). Потенциал точки эквивалентности для метилмеркаптана (-200 ÷ -170) мВ.
Если в промвыбросах содержится элементарная сера, то поглотившись щелочью, она может вступать в реакцию с метилмеркаптаном, образуя органо-полисульфид, который осаждается после осаждения сульфидов:
CH3SNa + S -> CH3SSNa
В этом случае на интегральной кривой титрования появляется третий скачок потенциала в области (-560 ÷ -570) мВ. В этом случае потенциал точки эквивалентности для сероводорода смещается в область (-670 ÷ -660) мВ, а метилмеркаптана (-140 ÷ -170) мВ.
В случае, когда на интегральных кривых титрования получаются нечетко выраженные скачки потенциалов, необходимо построить дифференцированные кривые титрования, по числу максимумов которых можно определить число оттитрованных компонентов.
Обычно для расшифровки потенциометрических данных достаточно построения интегральных кривых титрования.
10 ОБРАБОТКА РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
10.1 Расчет концентрации сероводорода
Содержание сероводорода (CН2S), мг/пробе, в поглотительном растворе рассчитывают по формуле:
где V0 - общий объем поглотительного раствора, см3;
С' - концентрация «концентрированного» раствора серебра азотнокислого, моль/дм3;
V' - объем «концентрированного» раствора серебра азотнокислого, пошедший на осаждение сульфид-ионов до потенциала, приблизительно (-700) мВ, см3;
С'' - концентрация «разбавленного» раствора серебра азотнокислого, моль/дм3;
V'' - объем «разбавленного» раствора серебра азотнокислого, пошедший на осаждение сульфид-ионов, см3;
ГЭ - грамм-эквивалент сероводорода, 17 г;
Va - объем пробы поглотительного раствора, взятой для анализа, см3.
Массовую концентрацию сероводорода в
газовых выбросах (![]() , мг/м3) рассчитывают по формуле:
, мг/м3) рассчитывают по формуле:
![]() (5)
(5)
где ![]() - содержание сероводорода в пробе, мг;
- содержание сероводорода в пробе, мг;
Wo - объем отобранных газов, приведенный к нормальным условиям, дм3.
Объем газа, приведенный к нормальным условиям (Wo) вычисляют по формуле:
![]() (6)
(6)
где Wr - объем пропущенного через поглотители газа при условиях отбора, дм3;
Р - атмосферное давление, кПа;
ΔР - избыточное давление (разряжение) у счетчика или водяного аспиратора, кПа;
t - температура газа при отборе перед ротаметром, °С.
10.2 Расчет концентрации метилмеркаптана
Концентрацию метилмеркаптана (Смм, мг/пробе) вычисляют по формуле:
![]() (7)
(7)
где Vо и Va - то же, что в формуле (4);
С - концентрация раствора серебра азотнокислого, моль/дм ;
V - объем раствора серебра азотнокислого, пошедший на осаждение меркаптид-ионов, см3;
ГЭ - грамм-эквивалент метилмеркаптана, ГЭ = 48 г.
Если в растворе присутствуют сероводород и метилмеркаптан и на кривой титрования имеются два скачка потенциала (см. рис. Г.2, приложение Г), то объем титранта, израсходованного на осаждение меркаптид-ионов (V3), определяют как разность между объемом, пошедшим на титрование смеси ионов (V2), и объемом, затраченным на осаждение сульфид-ионов (V1), а концентрацию метилмеркаптана в пробе вычисляют по формуле:
![]() (8)
(8)
где Vо и Vа - то же, что в формуле (4);
С - концентрация раствора азотнокислого, моль/дм3;
V3 - объем раствора серебра азотнокислого, пошедший на осаждение меркаптид-ионов, V3 = V2 - V1, см3;
ГЭ - грамм-эквивалент метилмеркаптана, 48 г.
Массовую концентрацию метилмеркаптана в газовых выбросах (Хмм, мг/м3) рассчитывают по формуле:
![]() (9)
(9)
где Смм - концентрация метилмеркаптана в пробе, мг/пробе;
Wо - объем газа, приведенный к нормальным условиям, дм3.
При титровании щелочных проб, содержащих сульфид-, меркаптид-, и органополисульфид-ионы объем титранта (V1), соответствующий содержанию меркаптидов, рассчитывают по разности между объемами титранта по третьему (меркаптидному) и первому (сероводородному) скачкам потенциала.
За результат измерения массовой концентрации сероводорода и метилмеркаптана в парогазовых выбросах принимают среднее арифметическое значение двух наблюдений, для которых выполняется условие:
При невыполнении условия (10) и/или условия (11) могут быть использованы методы проверки приемлемости результатов параллельных определений и установления окончательного результата согласно разделу 5 ГОСТ Р ИСО 5725-6.
Значение предела повторяемости r, приведено в табл. 3.
Таблица 3 - Значения предела повторяемости при вероятности Р = 0,95
|
Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений), r, % |
|
|
Сероводород От 5 до 50000 вкл. |
20 |
|
Метилмеркаптан От 5 до 100000 вкл. |
20 |
11 ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Результат измерений X в документах, предусматривающих его использование, может быть представлен в виде: X ± Δ, Р = 0,95,
где Δ - показатель точности методики.
Величину Д рассчитывают по формуле: Δ = 0,01 × δ × X. Значение δ приведено в таблице 1.
Допустимо результат измерений в документах, выдаваемых лабораторией, представлять в виде: Х ± Δл, Р = 0,95, при условии Δл < Δ, где
X - результат измерений, полученный в соответствии с прописью методики;
± Δл - значение характеристики погрешности результатов анализа, установленное при реализации методики в лаборатории и обеспечиваемое контролем стабильности результатов анализа.
12 КОНТРОЛЬ ТОЧНОСТИ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
- контроль стабильности результатов измерений путем контроля стабильности среднеквадратического отклонения повторяемости, погрешности;
- оперативный контроль процедуры измерений путем оценки погрешности при реализации отдельно взятой контрольной процедуры.
Периодичность оперативного контроля процедуры выполнения измерений и алгоритмы контрольных процедур, а также реализуемые процедуры контроля стабильности результатов измерений регламентируют во внутренних документах лаборатории.
Периодичность оперативного контроля процедуры анализа, а также реализуемые процедуры контроля стабильности результатов анализа регламентируют в Руководстве по качеству лаборатории.
Разрешение противоречий между результатами двух лабораторий проводят в соответствии с 5.3.3 ГОСТ Р ИСО 5725-6-2002.
ПРИЛОЖЕНИЕ А
ПРОВЕРКА ПОЛНОТЫ ПОГЛОЩЕНИЯ СЕРОВОДОРОДА И МЕТИЛМЕРКАПТАНА РАСТВОРОМ ГИДРОКСИДА НАТРИЯ С(NaOH) = 5 моль/дм3
А.1 Средства измерений, вспомогательное оборудование, реактивы и материалы
- Колбы плоскодонные по ГОСТ 25336-82.
- Азот особой чистоты по ГОСТ 2293-74.
- Медь сернокислая по ГОСТ 4165-78.
- Кислота серная по ГОСТ 4204-77.
- Склянки Тищенко по ГОСТ 25336-82.
А.2 Приготовление растворов
А.2.1 Приготовление 2 моль/дм3 раствора гидроксида натрия
40 г гидроксида натрия помещают в колбу вместимостью 500 дм3 и доводят до метки дистиллированной водой.
Раствор хранят в полиэтиленовой посуде в течение двух месяцев.
А.2.2 Раствор серной кислоты (1:1)
Смешивают равные количества воды и концентрированной серной кислоты (кислоту осторожно приливают к воде).
Срок хранения 6 месяцев.
А.3 Проверка полноты поглощения сероводорода
С целью проверки полноты поглощения, сероводород предварительно получают по методу Бауэра, который поглощают раствором гидроксида натрия C(NaOH) = 2 моль/дм3.
Концентрацию полученного раствора сероводорода находят потенциометрически.
Затем собирают установку, состоящую из баллона с азотом особой чистоты, плоскодонной колбы с капельницей, в которой получают анализируемый газ, трех последовательно соединенных поглотителей Рыхтера, заполненных раствором гидроксида натрия C(NaOH) = 5 моль/дм3 по 10 см3 каждый и склянки Тищенко, заполненной насыщенным раствором меди сернокислой для предотвращения попадания в атмосферу не поглотившихся газов.
Пробу полученного раствора натрия сульфида нейтрализуют рассчитанным количеством серной кислоты (1:1) в плоскодонной колбе и продувают в течение 15 минут азотом через поглотительные растворы.
Распределение сероводорода в поглотителях контролируют потенциометрическим методом.
Результаты измерений представлены в таблице 1.
Таблица А.1 - Результаты исследований поглотительной способности раствора гидроксида натрия С (NaOH) = 5 моль/дм3
|
Среда |
Взято H2S, мг |
Найдено H2S, мг |
Найдено H2S, % |
|
Колба с исходным раствором |
20,0 |
1,00 |
5,00 |
|
1 поглотитель Рыхтера 5 моль/дм3 NaOH |
20,0 |
18,20 |
91,00 |
|
2 поглотитель Рыхтера 5 моль/дм3 NaOH |
20,0 |
0,79 |
3,97 |
|
3 поглотитель Рыхтера 5 моль/дм3 NaOH |
20,0 |
0,01 |
0,03 |
Примечание: За результат измерения принимают среднее арифметическое значение из пяти наблюдений.
А.4 Проверка полноты поглощения метилмеркаптана
С целью проверки полноты поглощения, метилмеркаптан предварительно получают разложением сульфата метилизотиомочевины при действии щелочи.
Концентрацию полученного раствора метилмеркаптана находят потенциометрически.
Собирают установку, как указано в п. 8 МВИ.
Меркаптан продувают азотом через поглотительные растворы, так же как и сероводород. Распределение метилмеркаптана в поглотителях контролируют потенциометрически. Результаты измерений представлены в таблице А.2.
Таблица А.2 - Результаты исследований поглотительной способности раствора гидроксида натрия С(NaOH) = 5 моль/дм3
|
Взято ММ, мг |
Найдено ММ, мг |
Найдено ММ, % |
|
|
Колба с исходным раствором |
20,0 |
1,20 |
6,0 |
|
1 поглотитель Рыхтера 5 моль/дм3 NaOH |
20,0 |
15,6 |
78,0 |
|
2 поглотитель Рыхтера 5 моль/дм3 NaOH |
20,0 |
2,68 |
13,4 |
|
3 поглотитель Рыхтера 5 моль/дм3 NaOH |
20,0 |
0,52 |
2,6 |
Примечание: За результат измерения принимают среднее арифметическое значение из пяти наблюдений.
Проведенные опыты позволяют сделать вывод, что раствор C(NaOH) = 5 моль/дм3 натрия гидроксида применим для поглощения сероводорода и метилмеркаптана из парогазовых выбросов, а связка из трех поглотителей Рыхтера соответствует наиболее полному поглощению этих газов.
ПРИЛОЖЕНИЕ Б
ПОДГОТОВКА ЭЛЕКТРОДОВ
Б.1 Средства измерений, вспомогательное оборудование, реактивы и материалы
- Натрий сернистый (сульфид натрия) по ГОСТ 2053-77.
- Кислота азотная по ГОСТ 4461-77.
- Стаканы стеклянные, химические, 50 см3 по ГОСТ 25336-82.
Б.2 Приготовление растворов
Б.2.1 Приготовление 0,1 моль/дм3 раствора сульфида натрия
7,8 г сульфида натрия помещают в колбу на 1 дм3 и доводят до метки раствором гидроксида натрия концентрацией 5 моль/дм3.
Б.2.2 Приготовление 0,01 моль/дм3 раствора сульфида натрия
Готовят разбавлением раствора приготовленного по п. Б.2.1 в 10 раз раствором гидроксида натрия концентрацией 5 моль/дм3.
Б.3 Подготовка электродов к работе
Электрод сравнения (хлорид серебряный) готовят в соответствии с прилагаемым к нему паспортом.
Каждые 7 - 10 суток электрод заполняют свежим насыщенным раствором хлористого калия.
Индикаторный электрод (сульфид серебряный ЭСС-01) вымачивают при комнатной температуре в течение 1 часа в дистиллированной воде. Для градуировки электрода используют потенциометрическую установку. В стакан вместимостью 50 см3 наливают 20 см3 раствора сульфида натрия концентрацией 0,01 моль/дм3 в растворе натрия гидроксида С(NaOH) = 5 моль/дм3 и помещают сульфид серебряный электрод.
Хлоридсеребряный электрод помещают в насыщенный раствор хлористого калия. Соединяют систему электрическим мостиком. После погружения электродов в раствор включают мешалку и через 5 минут записывают установившееся значение потенциала измерительного электрода. Затем измеряют потенциал сульфидсеребряного электрода в растворе сульфида натрия не более С(Na2S) = 0,1 моль/дм3, приготовленного на растворе натрия гидроксида С(NaOH) = 5 моль/дм3. Если при изменении концентрации сульфид-иона на порядок разница потенциалов ΔЕ составляет 80 - 100 мВ, данный электрод может быть использован для потенциометрического титрования. Если ΔЕ меньше, электрод необходимо регенерировать по методике, приведенной ниже.
Аналогично проверяется чувствительность электрода по отношению к меркаптид-иону (в растворах метилмеркаптана натрия, приготовленном в растворе натрия гидроксида С(NaOH) = 5 моль/дм3 или гидроксида свинца). Если при изменении концентрации меркаптид-иона на порядок разница потенциалов ΔЕ составляет 60 - 80 мВ, данный электрод может быть использован для потенциометрического титрования.
Электрод ЭСС-01 проверяют не реже одного раза в месяц.
После каждого определения электроды (сравнения и индикаторный) тщательно промывают дистиллированной водой и вытирают фильтровальной бумагой. В промежутках между определениями электроды хранят в дистиллированной воде.
Б.4 Способ регенерации сульфидсеребряного электрода ЭСС-01
Сульфид серебряные электроды, у которых нарушена поверхностная пленка и невелика величина ΔЕ, регенерируют следующим образом. Пленка сульфида серебра растворяют в концентрированной азотной кислоте, после чего электролитически получают новую поверхностную пленку сульфида серебра.
В стакан емкостью 50 см3 помещают 20 см3 раствора сульфида натрия концентрацией 0,02 - 0,04 моль/дм3 и опускают медную проволочку, присоединенную другим концом к отрицательному полюсу элемента 373 (анод). К положительному полюсу присоединяют регенерируемый электрод (катод). Во второй стакан емкостью 50 см3 наливают концентрированную азотную кислоту, в третий - дистиллированную воду.
В стакан с кислотой опускают на 30 - 40 секунд электрод, вынимают его и опускают в стакан с дистиллированной водой. Черная пленка сульфида серебра должна раствориться. Если она не растворилась, эту операцию повторяют несколько раз. Небольшие кусочки рыхлого осадка сульфида серебра снимают с поверхности электрода легким прикосновением фильтровальной бумаги. Когда поверхность электрода будет абсолютно чистой (матовая серая поверхность), его опускают на 5 - 10 секунд в концентрированную азотную кислоту, а затем хорошо ополаскивают дистиллированной водой.
Для нанесения новой поверхностной пленки сульфида серебра электрод опускают в раствор сульфида натрия. Он начинает покрываться черной пленкой сульфида серебра. Через 1 - 2 минуты электрод вынимают, ополаскивают в стакане с дистиллированной водой и проверяют равномерность и плотность нанесенной пленки сульфида серебра (легко прикасаются к электроду фильтровальной бумагой). Если нанесенная пленка рыхлая, то на фильтровальной бумаге остаются черные кусочки сульфида серебра. В этом случае с электрода необходимо снять пленку сульфида серебра описанным выше способом. Затем повторить процесс нанесения пленки, уменьшив концентрацию раствора сульфида натрия или время контакта электрода с раствором (0,5 - 1 мин). Нормально нанесенная пленка сульфида серебра должна оставлять легкий след на фильтровальной бумаге и равномерно покрывать поверхность электрода.
ПРИЛОЖЕНИЕ В
(Рекомендуемое)
Таблица В.1 - Расчет объема отобранных газов, приведенный к нормальным условиям
|
Скорость отбора, дм3/мин |
Время отбора, мин. |
Объем пропущенного через поглотители газа, дм3 |
Атмосферное давление, кПа |
Избыточное давление (разряжение у счетчика), кПа |
Температура газа при отборе, °С |
Объем газа, приведенный к нормальным условиям, дм3 |
|
V |
t |
Wr |
Р |
ΔР |
t |
wо |
Таблица В.2 - Результаты измерений массовой концентрации сероводорода и метилмеркаптана в поглотительном растворе
|
Общий объем поглотительного раствора, см3 |
Объем поглотительного раствора, взятый для анализа, см3 |
Количество добавленного титранта AgHО3, см3 |
Потенциал электрода, мВ |
Х1-3, мВ (по методу Хаана-Вейлера) |
Концентрация H2S и MM в поглотительном растворе, г/пробе |
Таблица В.3 - Результаты измерения массовой концентрации сероводорода и метилмеркаптана в парогазовых выбросах
|
Объем отобранного газа, приведенный к нормальным условиям, дм3 |
Концентрация H2S и ММ в поглотительном растворе, г/пробе |
Концентрация H2S и ММ в парогазовых выбросах, г/дм3 |
ПРИЛОЖЕНИЕ Г
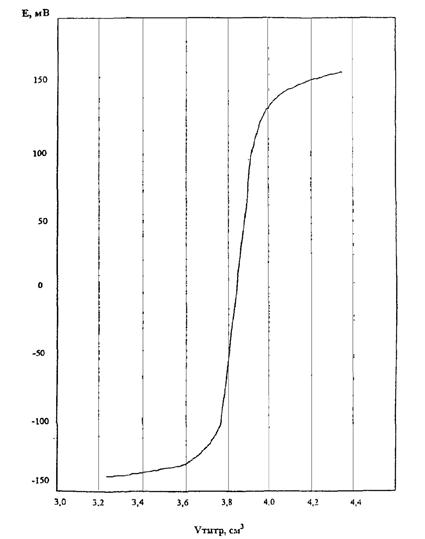
РИС. Г.1
КРИВАЯ ТИТРОВАНИЯ AgNО3
КРИВЫЕ ТИТРОВАНИЯ
РИС. Г.2
1 - Кривая титрования натрия сернистого.
2 - Кривая титрования смеси натрия сернистого и меркаптида натрия.
3 - Кривая титрования меркаптида натрия
СОДЕРЖАНИЕ