ГОСТ 11362-96
(ИСО 6619-88)
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
НЕФТЕПРОДУКТЫ И СМАЗОЧНЫЕ
МАТЕРИАЛЫ.
ЧИСЛО НЕЙТРАЛИЗАЦИИ
МЕТОД ПОТЕНЦИОМЕТРИЧЕСКОГО
ТИТРОВАНИЯ
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ
ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
Минск
Предисловие
1 РАЗРАБОТАН МТК 31, Всероссийским научно-исследовательским институтом по переработке нефти (ВНИИ НП)
ВНЕСЕН Госстандартом России
2 ПРИНЯТ Межгосударственным Советом по стандартизации, метрологии и сертификации (протокол № 9-96 от 12 апреля 1996 г.)
За принятие проголосовали:
|
Наименование государства |
Наименование национального органа по стандартизации |
|
Азербайджанская Республика |
Азгосстандарт |
|
Республика Белоруссия |
Белстандарт |
|
Республика Казахстан |
Казгосстандарт |
|
Российская Федерация |
Госстандарт России |
|
Республика Таджикистан |
Таджикский государственный центр по стандартизации, метрологии и сертификации |
|
Туркменистан |
Туркменглавгосинпекция |
|
Украина |
Госстандарт Украины |
3 Постановлением Комитета Российской Федерации по стандартизации, метрологии и сертификации от 30 июля 1996 г. № 496 межгосударственный стандарт ГОСТ 11362-96 введен в действие непосредственно в качестве государственного стандарта Российской Федерации с 1 июля 1997 г.
4 Настоящий стандарт представляет собой полный аутентичный текст международного стандарта ИСО 6619-88 «Нефтепродукты и смазочные материалы. Число нейтрализации. Метод потенциометрического титрования» с дополнительными требованиями, отражающими потребности экономики страны
5 ВЗАМЕН ГОСТ 11362-76
ГОСТ 11362-96
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
|
НЕФТЕПРОДУКТЫ И СМАЗОЧНЫЕ МАТЕРИАЛЫ. ЧИСЛО НЕЙТРАЛИЗАЦИИ Метод потенциометрического титрования Petroleum products and lubricants. Neutralization number. Potentiometric titration method |
Дата введения 1997-07-01
1. НАЗНАЧЕНИЕ И ОБЛАСТЬ ПРИМЕНЕНИЯ
1.1. Настоящий стандарт устанавливает метод определения общего кислотного числа, кислотного числа сильных кислот, кислотности, общего щелочного числа, щелочного числа сильных щелочей в нефтепродуктах и смазочных материалах. Он применим для определения кислот с константой диссоциации больше 10-9; слабые кислоты с константой диссоциации менее 10-9 не мешают определению.
Примечание - В товарных и отработанных маслах соединения кислого характера включают органические и минеральные кислоты, эфиры, фенольные соединения, лактоны, смолы, соли тяжелых металлов, соли аммония и других слабых оснований, соли многоосновных кислот, а также ингибиторы и детергенты.
1.2. Этот метод характеризует относительное изменение масел в процессе окисления, не зависящее от цвета и других свойств масел.
Несмотря на то, что титрование проводят в условиях равновесия, метод не применяют для измерения абсолютного кислотного или щелочного числа, по которому можно определить поведение масла в условиях эксплуатации. Не установлена зависимость между поведением масла при коррозии и кислотными и щелочными числами.
Примечание - Метод цветного индикаторного титрования указан в ГОСТ 28255. Кислотные числа, полученные потенциометрическим методом, могут соответствовать или нет полученным по методу ГОСТ 28255, но обычно они того же порядка.
1.3. Товарные и отработанные нефтепродукты могут содержать кислотные компоненты, присутствующие как присадки или как продукты распада, образовавшиеся в условиях эксплуатации, например продукты окисления. Относительное количество этих веществ может быть определено титрованием щелочами.
Кислотное число позволяет оценить количество кислотных компонентов масла в условиях испытания. Кислотное число применяется в качестве руководства для контроля качества смазочного масла.
Иногда его используют как оценку характера изменения смазочного материала при эксплуатации.
Содержание компонентов следует устанавливать опытным путем. Так как множество продуктов окисления является причиной повышения кислотного числа и органические кислоты обладают различными коррозионными свойствами, представленный метод нельзя применять для определения коррозионности масла в условиях эксплуатации. Не установлена зависимость между кислотным числом и коррозионной агрессивностью масла по отношению к металлам.
Кислотное число можно определить в компаундированных моторных маслах.
Настоящий стандарт не распространяется на электроизоляционные масла.
Дополнения, отражающие потребности народного хозяйства, выделены курсивом.
2. НОРМАТИВНЫЕ ССЫЛКИ
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Технические условия
ГОСТ 2517-85 Нефть и нефтепродукты. Методы отбора проб
ГОСТ 3118-77 Кислота соляная. Технические условия
ГОСТ 4107-78 Бария гидроокись 8-водная. Технические условия
ГОСТ 4204-74 Кислота серная. Технические условия
ГОСТ 4220-75 Калий двухромовокислый. Технические условия
ГОСТ 4234-74 Калий хлористый. Технические условия
ГОСТ 5789-78 Толуол. Технические условия
ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
ГОСТ 24363-80 Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 25794.1-82 Реактивы. Методы приготовления титрованных растворов для кислотно-основного титрования
ГОСТ 29255-91 Нефтепродукты и смазочные материалы. Определение числа нейтрализации методом цветного индикаторного титрования
ГОСТ 29228-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 2. Пипетки градуированные без установленного времени ожидания
ГОСТ 29252-91 Посуда лабораторная стеклянная. Бюретки. Часть 2. Бюретки без времени ожидания
3. ОПРЕДЕЛЕНИЯ
В настоящем стандарте применяют следующие термины:
3.1. Общее кислотное число К1 (суммарное кислотное число сильных и слабых кислот) - количество щелочи, выраженное в миллиграммах гидроокиси калия (KOH) на 1 г образца, необходимое для потенциометрического титрования испытуемой массы в определенном растворителе от начального показания измерительного прибора до показания свежеприготовленного щелочного неводного буферного раствора или четкой точки перегиба, как указано в стандарте.
3.2. Кислотное число сильных кислот К2 - количество щелочи, выраженное в миллиграммах гидроокиси калия (KOH) на 1 г образца, необходимое для потенциометрического титрования испытуемой массы в определенном растворителе от начального показания измерительного прибора до показания свежеприготовленного кислотного неводного раствора или четкой точки перегиба, как указано в стандарте.
3.3. Кислотность К3 - количество щелочи, выраженное в миллиграммах гидроокиси калия (KOH) на 100 см3 образца, необходимое для потенциометрического титрования испытуемой массы в определенном растворителе - от начального показания измерительного прибора до показания свежеприготовленного щелочного неводного буферного раствора или четкой точки перегиба, как указано в стандарте.
3.4. Общее щелочное число Щ2 - количество щелочи, выраженное в миллиграммах гидроокиси калия (KOH) на 1 г образца, необходимое для потенциометрического титрования испытуемой массы в определенном растворителе от начального показания измерительного прибора до показания свежеприготовленного кислого неводного буферного раствора или четкой точки перегиба, как указано в стандарте.
3.5. Щелочное число сильных оснований Щ1 - количество щелочи, выраженное в миллиграммах гидроокиси калия (KOH) на 1 г образца, необходимое для потенциометрического титрования испытуемой массы в определенном растворителе от начального показания измерительного прибора до показания свежеприготовленного щелочного неводного буферного раствора или четкой точки перегиба, как указано в стандарте.
4. СУЩНОСТЬ МЕТОДА
Массу для испытания растворяют в определенном растворителе и титруют потенциометрически спиртовым раствором гидроокиси калия или соляной кислоты при использовании стеклянного, каломельного или хлорсеребряного электродов.
Показания измерительного прибора наносят на график вручную или автоматически относительно соответствующих объемов титрующего раствора. Берут только четкие точки перегиба на кривой титрования. В случае, когда на кривой нет четкой точки перегиба, конечные точки берут по показаниям измерительного прибора, соответствующим показаниям для неводных кислотных и щелочных буферных растворов.
5. РЕАКТИВЫ
Для анализа применяют реактивы х.ч. или ч.д.а. и только дистиллированную воду или воду эквивалентной чистоты.
5.1. Неводный кислый буферный раствор
5.1.1. 10 см3 буферного исходного раствора А (5.5.1) добавляют к 100 см3 растворителя для титрования. Применяют в течение 1 ч.
5.1.2. 50 см3 буферного исходного раствора А (5.5.2).
5.2. Неводный щелочной буферный раствор
10 см3 буферного исходного раствора В (5.6) добавляют к 100 см3 растворителя для титрования. Применяют в течение 1 ч.
5.3. 2,4,6-триметилпиридин (γ-коллидин)
(Мr = 121,18), бесцветный, с
пределами кипения 168 - 170 °С и коэффициентом преломления (![]() ) 1,4982 ± 0,0005. Реактив хранят над активированным
алюминием в темной склянке.
) 1,4982 ± 0,0005. Реактив хранят над активированным
алюминием в темной склянке.
5.3.1. Калий фталевокислый кислый (бифталат калия) по соответствующей нормативной документации.
5.4. М-нитрофенол (Мr = 139,11), бледно-желтый, с температурой плавления 96 - 97 °С или с требованиями к качеству по соответствующей нормативной документации. Реактив хранят в темной склянке.
5.5. Буферный исходный раствор А
5.5.1. Тщательно взвешивают (24,2 ± 0,1) г 2,4,6-триметилпири-дина (γ-коллидина) и переносят в мерную колбу вместимостью 1 дм3, содержащую 100 см3 безводного пропан-2-ола (5.9 и 5.9.1) или этанола (5.9.2). Затем из мерного цилиндра вместимостью 1 дм3 добавляют в колбу при непрерывном перемешивании (150/с1 ± 5) см3 0,2 моль/дм3 спиртового раствора соляной кислоты (5.8) (c1 - истинная концентрация раствора соляной кислоты, установленная при градуировке). Добавляют до 1 дм3 пропан-2-олом или этанолом и тщательно перемешивают. Применяют в течение одного месяца.
5.5.2. При отсутствии γ-коллидина готовят кислый буферный раствор бифталата калия (pH - 4). Для приготовления 1 дм3 буферного раствора (10,20 ± 0,01) г перекристаллизованного бифталата калия растворяют в 20 - 50 см3 свежепрокипяченной дистиллированной воды, раствор количественно переносят в мерную колбу вместимостью 1 дм3 и при постоянном перемешивании доводят объем до метки прокипяченной дистиллированной водой. Допускается готовить буферный раствор из фиксанала бифталата калия для pH-метрии.
5.6. Буферный исходный раствор В
Тщательно взвешивают (27,8 ± 0,1) г м-нитрофенола и переносят в. мерную колбу вместимостью 1 дм3, содержащую 100 см3 безводного пропан-2-ола (5.9 и 5.9.1) или этанола (5.9.2). Затем из мерного цилиндра вместимостью 500 см3 при непрерывном перемешивании добавляют в колбу (50/с2 ± 1) см3 0,2 моль/дм3 спиртового раствора гидроокиси калия (5.12) (с2 - истинная концентрация раствора, установленная при градуировке). Доливают до метки 1 дм3 пропан-2-олом или этанолом и тщательно перемешивают. Используют раствор в течение одного месяца.
5.7. Соляная кислота, спиртовый раствор, с (HCL) = 0,1 моль/дм3.
5.7.1. 9 см3 соляной кислоты по ГОСТ3118 (ρ20 = 1,17 - 1,19 г/см3) смешивают с 1 дм3 безводного пропан-2-ола (5.9) или с 1 дм3 этилового спирта.
Молярную концентрацию (с4) проверяют не реже одного раза в 2 недели с погрешностью не более 0,0005 моль/дм3 потенциометрическим титрованием (8 ± 0,25) см3 0,1 моль/дм3 спиртового раствора гидроокиси калия (5.11), растворенного в 125 см3 воды, не содержащей углекислого газа.
Молярную концентрацию раствора соляной кислоты определяют по ГОСТ 25794.1.
5.8. Соляная кислота, спиртовый раствор, с (HCL) = 0,2 моль/дм3. Готовят раствор и устанавливают молярную концентрацию, как указано в 5.7.1, при этом берут 18 см3 соляной кислоты (ρ20 = 1,17 - 1,19 г/см3).
1) Сита типа Линде 4А являются примером пригодной продукции, имеющейся в наличии. Сведения даны для всех, кто пользуется настоящим стандартом
5.9.1. Спирт этиловый по ГОСТ 18300, высшего сорта, перегнанный в колбе с дефлегматором.
5.9.2. Толуол по ГОСТ 5789.
5.10. Калий хлористый по ГОСТ 4234.
Готовят насыщенный раствор хлористого калия (KCL) в воде.
5.11. Гидроокись калия, спиртовый раствор, с (KOH) = 0,1 моль/дм3.
5.11.1 Добавляют (6 ± 0,1) г гидроокиси калия (KOH) по ГОСТ 24363 приблизительно к 1 дм3 безводного пропан-2-ола (5.9) или к 1 дм3 этанола в колбе вместимостью 2 дм3. Аккуратно кипятят с обратным холодильником в течение 10 мин, после чего встряхивают до полного растворения. Добавляют не менее 2 г гидроокиси бария Ba(OH)2 и снова аккуратно кипятят 5 - 10 мин.
Раствор оставляют на 2 дня и фильтруют жидкость через стеклянный или бумажный фильтр. Хранят раствор в химически стойкой склянке.
Бюретка должна быть снабжена трубкой с натронной известью или неволокнистым силикатным абсорбентом, поглощающим CO2.
Раствор не должен контактировать с резиновой пробкой, закрывающей склянку, или со смазкой, уплотняющей стеклянную пробку.
Для установки молярной концентрации растворяют 0,1 - 0,15 г бифталата калия (высушенного в течение 2 ч при температуре 105 °С), взвешенного с точностью до 0,0002 г, в 100 см3 воды, не содержащей углекислого газа.
Допускается готовить раствор бифталата калия по ГОСТ 4919.2, таблица 2.
5.11.2. Молярную концентрацию раствора гидроокиси калия (с3), моль/дм3, определяют по ГОСТ 25794.1.
За результат определения принимают среднее арифметическое значение не менее трех определений, отличающихся не более чем на 0,0005 моль/дм3.
Молярную концентрацию раствора гидроокиси калия проверяют не реже одного раза в две недели.
5.12. Гидроокись калия, спиртовый раствор с (KOH) = 0,2 моль/дм3. Готовят, хранят и устанавливают молярную концентрацию по 5.11, при этом берут 12 - 13 г гидроокиси калия и 0,2 - 0,3 г бифталата калия.
5.12.1. Гидроокись калия, спиртовый раствор с (KOH) = 0,05 моль/дм3.
Готовят, хранят и устанавливают молярную концентрацию по 5.11, при этом берут (3 + 0,1) г гидроокиси калия и 0,05 - 0,07 г бифталата калий.
5.13. Растворитель для определения кислотных и щелочных чисел.
Смешивают 500 см3 толуола, 5 см3 воды и 495 см3 безводного пропан-2-ола (5.9) или 700 см3 толуола, или 300 см3 этилового спирта.
Растворитель для титрования приготавливают в больших количествах, но ежедневно проводят контрольные испытания перед применением.
Примечание - Для полного растворения тяжелых остатков асфальтовых веществ готовят растворитель для титрования, в котором толуол заменен хлороформом.
5.14. Растворитель для определения кислотности.
Смешивают 300 си3 этилового спирта и 700 см3 хлороформа.
5.15. Гидроокись бария по ГОСТ 4107.
5.16. Хлороформ по соответствующей нормативной документации.
5.17. Известь натронная или аскарит по соответствующей нормативной документации.
5.18. Хромовая смесь: калий двухромовокислый по ГОСТ 4220, кислота серная по ГОСТ 4204, 5 %-ный раствор.
5.19. Сита Линде или цеолит типа NaX uлu CdA по соответствующей нормативной документации.
6. АППАРАТУРА
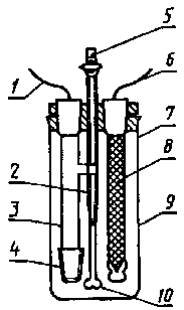
Устройство для потенциометрического титрования представлено на рисунке 1.
6.1. Аппарат для титрования вручную
6.1.1. Измерительный прибор, вольтметр или потенциометр с точностью показаний ± 0,005 B и чувствительностью ± 0,002 B, диапазоном измерения не менее ± 0,5 B в случае использования электродов по 6.1.2 и 6.1.3, когда сопротивление между ними от 0,2 до 20 МОм. Заземляют измерительный прибор и исключают влияние постороннего электрического поля на любую часть поверхности стеклянного электрода, провода стеклянного электрода, титровального стенда или измерительного прибора.
1 - провод для сравнительного электрода; 2 - удлиненный конец бюретки (перед мешалкой); 3 - электрод сравнения; 4 - трубка со стеклянным шлифом у основания; 5 - бюретка; 6 - экранированный провод для стеклянного электрода; 7 - бакелитовая основа; 8 - стеклянный электрод (защищен внутри); 9 - стакан; 10 - пропеллерная мешалка
Рисунок 1 - Устройство для потенциометрического титрования
Примечание - Аппарат может состоять из электронного вольтметра с силой тока на входе менее 5´10-12А, сопротивлением электродов 1000 МОм, соединенных с измерительным прибором, снабженным заземленным металлическим экраном, так, чтобы исключить влияние внешнего электростатического поля.
Конец электрода, погруженный в раствор, должен быть закрыт стеклом (в виде полушария) с радиусом приблизительно 7 мм, припаянным к трубке электрода. Толщина стекла в полушарии должна быть такой, чтобы сопротивление полушария составляло 100 - 1000 МОм при 25 °С.
Электрод должен содержать воспроизводимую, герметично запаянную жидкостную ячейку для электросоединения с внутренней поверхностью полушария.
Электросоединение от запаянной контактной ячейки к проводу измерительного прибора должно быть окружено электрическим заземленным экраном.
Экран должен быть изолирован от электросоединения изоляционным материалом самого высокого качества, таким как резина или стекло, чтобы сопротивление между экраном и всей длиной электросоединения было более 50000 МОм.
Этот электрод должен изготовляться из стекла и снабжаться наружной съемной стеклянной трубкой с запаянным концом, погружаемым в раствор для титрования.
Стеклянная трубка длиной от 8 до 25 мм служит основанием для электрода и должна быть слегка заужена на конус. Запаянный конец электрода должен выступать из трубки на 2 - 20 мм.
Поверхность основания должна быть непрерывной и шероховатой.
Посередине на поверхности основания электрода должно находиться одно или несколько отверстий диаметром 1 мм. Электрод должен содержать необходимое количество ртути, каломель и электрическое соединение с ртутью.
Сравнительный хлорсеребряный электрод ЭВЛ-1М1 или ЭВЛ-1М3.
Сравнительные электроды следует почти полностью наполнить электролитом, насыщенным раствором KCl (5.10), который можно пополнять через отверстие электрода, закрываемое пробкой.
Электроды не должны давать утечки электролита более 1 капли за 10 мин (проверка электродов).
Примечание - В этом методе нежелательно применять комбинированные электроды вследствие их плохой чувствительности.
6.1.4. Механическая мешалка со стеклянными лопатками длиной 6 мм в виде пропеллера (рисунок 1), установленными под углом 30 - 45°, или магнитная мешалка.
Корпус двигателя мешалки должен быть заземлен. Работа мешалки не должна вызывать никаких электрических помех.
6.1.5. Бюретка вместимостью 10 см3 с ценой деления 0,05 см3 и калиброванная с точностью ± 0,02 см3 со стеклянным краном на расстоянии 100 - 130 мм от конца бюретки. Допускается использовать бюретки типов 6-2-5 и 7-2-10 по ГОСТ 29252. Бюретка для гидроокиси калия должна иметь предохранительную трубку, содержащую натронную известь или другое абсорбирующее CO2 вещество.
Допускается использовать стаканы типа Н-2-250 ТС по ГОСТ 25336.
6.1.7. Титровальный стенд для поддержки электродов, мешалки и бюретки.
Примечание - Целесообразно иметь устройство, позволяющее удалять стакан, не нарушая положения электродов, бюретки и мешалки.
6.2. Аппарат для автоматического титрования
Системы автоматического титрования должны соответствовать 6.1 и техническим характеристикам, указанным в 6.2.1 - 6.2.3.
6.2.2. Бюретки, работающие от двигателя, с точностью подачи титранта ± 0,01 см3.
6.3. Колбы мерные вместимостью 1000 см3 по ГОСТ 1770.
6.4. Цилиндры измерительные вместимостью 50, 100 и 1000 см3 по ГОСТ 1770.
6.5. Пипетки вместимостью 10 см3 по ГОСТ 29228.
6.6. Колбы круглодонные типа КГУ-2-2-1000-34 ТХС по ГОСТ25336.
6.7. Дефлегматор елочный или шариковый по ГОСТ 25336.
6.8. Холодильник типа ХПТ исполнений 1, 2, 3 по ГОСТ 25336.
6.9. Весы аналитические с погрешностью взвешивания не более 0,0002 г.
6.10. Секундомер.
7. ПОДГОТОВКА ПРОБЫ
7.1. Отбор проб производят по ГОСТ 2517.
7.1.1. Пробу анализируемого продукта перемешивают 5 мин стеклянной палочкой или встряхиванием в склянке, заполненной не более 2/3 ее объема.
7.2. Подготовка пробы отработанного масла
7.2.1. Необходимо строго соблюдать метод отбора проб, так как сам осадок состоит из компонентов кислотного характера или абсорбирует кислотные компоненты из образца. Нарушение метода отбора проб влияет на результат определения.
Так как во время хранения в отработанном масле происходят качественные изменения, образцы после отбора пробы из системы смазки следует испытывать как можно быстрее, с обязательной записью даты отбора проб и испытания.
7.2.2. Пробу отработанных масел нагревают до (60 ± 5) °С в контейнере до тех пор, пока осадок в масле не станет однородной взвесью. Если контейнер изготовлен из жести или стекла и заполнен более чем на 3/4 объема, переносят весь образец в чистую стеклянную бутылку вместимостью не менее чем на 1/3 больше объема образца. Переносят весь осадок из контейнера в бутылку, энергично взбалтывая содержимое контейнера.
Примечание - Если образцы не содержат осадка, заметного невооруженным глазом, указанную процедуру можно исключить.
7.2.3. После тщательного перемешивания взвесь или часть ее фильтруют через сито с размером ячеек 100 меш для удаления механических примесей.
8. ПОДГОТОВКА СИСТЕМЫ ЭЛЕКТРОДОВ
8.1. Хранение электродов
8.1.1. Стеклянный электрод (6.1.2) (не реже одного раза в неделю при постоянном применении) промывают, погружая в холодный раствор хромовой смеси на 15 - 30 с. Вместо хромовой смеси можно применять моющий раствор.
Примечание -Электроды не следует оставлять погруженными в хромовую смесь более чем на несколько минут, чтобы избежать их повреждения.
8.1.2. Раствор хлорида калия в каломельном или хлорсеребряном электродах (6.1.3) меняют не реже одного раза в неделю. Следует убедиться в присутствии кристаллического хлористого калия. Уровень электролита в электродах должен быть всегда выше уровня жидкости в стакане для титрования.
8.1.3. Если электроды не используют, их погружают в воду. Электроды нельзя оставлять в титрующем растворе на длительное время между титрованиями. Электроды не очень хрупкие, но обращаться с ними следует осторожно.
8.2.1. Стеклянный электрод до и после каждого употребления тщательно вытирают чистой мягкой тканью и ополаскивают водой.
8.2.2. Каломельный и хлорсеребряный сравнительные электроды вытирают тканью, осторожно снимают стеклянную трубку у основания и обе поверхности тщательно вытирают.
Вновь свободно надевают трубку и дают стечь нескольким каплям электролита, чтобы смочить стеклянное соединение у основания. Тщательно смачивают поверхности у основания электролитом, плотно устанавливают трубку и ополаскивают электрод водой.
8.2.3. Перед каждым титрованием погружают подготовленные электроды в воду не менее чем на 5 мин и протирают концы электродов сухой тканью, чтобы удалить избыток воды.
8.3. Проверка чувствительности электродов
8.3.1. Систему «измерительный прибор - электрод» испытывают при введении в действие нового прибора, при установлении новых электродов, поочередно погружая электроды в хорошо перемешанную смесь, состоящую из 100 см3 растворителя для титрования и 1,0 - 1,5 см3 0,1 моль/дм3 спиртового раствора гидроокиси калия (5.11).
8.3.2. Систему «измерительный прибор - электрод» считают пригодной для применения, если расхождение в потенциале между одними и теми же электродами, погруженными в неводный кислый буферный раствор (5.5) и растворитель для титрования с раствором гидроокиси калия (5.11), составляет более 480 мВ.
Примечание - Для получения воспроизводимых значений потенциалов необходимо тщательно промывать электроды, особенно стеклянное соединение у основания, и регулярно испытывать электроды, так как загрязнение может вызнать ненадежные неустойчивые значения потенциалов при титровании. Конечные точки могут быть выбраны как по точкам изгиба на кривой титрования, так и по произвольно установленным потенциалам ячейки.
9. ГРАДУИРОВКА АППАРАТУРЫ
9.1. Ежедневно для каждой пары электродов определяют показания измерительного прибора в неводном кислом (5.1) и щелочном (5.2) буферных растворах. Это необходимо для выбора конечной точки титрования в том случае, когда на кривой титрования отсутствуют четкие точки перегиба.
9.2. Готовят электроды, как указано в 8.2, затем погружают их в соответствующие неводные буферные растворы и перемешивают в течение 5 мин, поддерживая температуру в пределах 2 °С от температуры, при которой проводят титрование. Регистрируют значение потенциала электродов. Эти показания берут как конечные точки на кривых титрования, не имеющих точек перегиба.
10. ПРОВЕДЕНИЕ АНАЛИЗА
10.1. В стакан для титрования (6.1.6) вместимостью 250 см3 отбирают массу образца согласно таблице 1 и растворяют в 125 см3 растворителя для титрования (5.13). Электроды готовят в соответствии с 8.2. Стакан помещают на титровальный стенд (6.1.7), регулируя его положение так, чтобы электроды наполовину были погружены в испытуемый раствор. Включают мешалку (6.1.4) и регулируют обороты так, чтобы, несмотря на энергичное перемешивание, раствор не разбрызгивался и в нем не образовывались воздушные пузырьки.
Таблица 1 - Масса пробы для испытания
|
Масса пробы для испытания, г |
Погрешность взвешивания, г |
|
|
0,05 - 1,0 |
20,0 ± 2,0 |
0,10 |
|
1,0 - 5,0 |
5,0 ± 0,5 |
0,02 |
|
5 - 20 |
1,0 ± 0,1 |
0,005 |
|
20 - 100 |
0,25 ± 0,02 |
0,001 |
|
100 - 250 |
0,1 ± 0,01 |
0,0005 |
Примечание - Для загущенных масел масса пробы для титрования (0,7 ± 0,2) г.
Кислотность определяют в светлых нефтепродуктах, при определении кислотности на анализ берут 100 см3 нефтепродукта.
10.2. Определение кислотного числа
Заполняют бюретку 0,1 моль/дм3 спиртовым раствором гидроокиси калия (при кислотном числе до 1 мг/г - 0,05 моль/дм3 спиртовым раствором гидроокиси калия) (5.11) и помещают в штатив так, чтобы конец бюретки был погружен на 25 мм в жидкость в стакане.
Записывают начальный объем раствора в бюретке и показание измерительного прибора (потенциал электродов).
10.3. Метод титрования вручную
Примечание - За показания измерительного прибора принимают потенциал, не изменяющийся в течение 1 мин более чем на 5 мВ. Это означает, что необходимо 1 - 2 мин для изменения потенциала на 100 мВ при добавлении 0,05 см раствора. Добавление 0,1 см3 требует 3 - 5 мин.
10.3.2. В начале титрования, а также в точках перегиба кривой титрования, когда добавление 0,1 см3 0,1 моль/дм3 раствора гидроокиси калия вызывает изменение потенциала более чем на 30 мВ, добавляют порции раствора по 0,05 см3.
10.3.3. На промежуточных участках, когда добавление 0,1 см3 0,1 моль/дм3 спиртового раствора гидроокиси калия вызывает изменение потенциала менее чем на 30 мВ, объем титранта увеличивают так, чтобы однократно введенная порция раствора вызывала изменение потенциала не более чем на 30 мВ.
10.3.4. Титрование заканчивают, когда потенциал после добавления 0,1 см3 раствора гидроокиси калия изменится менее чем на 5 мВ, а определяемый потенциал системы указывает на то, что титруемый раствор является более щелочным, чем неводный щелочной буферный раствор.
10.3.5. Удаляют титруемый раствор, промывают электроды и конец бюретки растворителем для титрования, затем пропан-2-олом или этанолом в зависимости от применяемого растворителя и заканчивают промывку дистиллированной водой. Погружают электроды в дистиллированную воду не менее чем на 5 мин перед следующим титрованием для восстановления водного гелевого слоя стеклянного электрода.
Хранят электроды в дистиллированной воде. Если обнаруживается, что электроды загрязнены, их очистку проводят согласно рисунку 2.
10.4. Метод автоматического титрования
10.4.1. Регулируют аппарат в соответствии с инструкциями изготовителя, чтобы установить потенциал при титровании вручную, как указано в примечании к 10.3.1, и (или) обеспечить непрерывную скорость подачи титранта менее чем 0,2 см3/мин во время титрования и 0,05 см3/мин в точках перегиба и в конечной точке, соответствующей точке при титровании свежеприготовленного стандартного неводного щелочного буферного раствора.
10.4.2. Проводят титрование с автоматической регистрацией кривой титрования.
Титруют 0,1 моль/дм3 спиртовым раствором гидроокиси калия до получения постоянного потенциала (например, изменение потенциала менее 5 мВ при добавлении 0,1 см3 раствора гидроокиси калия (автоматическая конечная точка) или до тех пор, пока изменение потенциала щелочного буферного раствора не покажет, что раствор более щелочной, чем свежеприготовленный неводный щелочной буферный раствор (конечная точка выбрана предварительно).
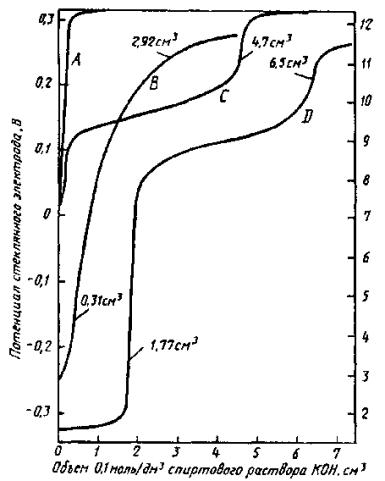
А - контрольное определение на 125 см3 растворителя для титрования;
В - 10,00 г отработанного картерного масла и 125 см3 растворителя для титрования.
Так как четких точек перегиба не видно, конечные точки выбирают по показаниям измерительного прибора, полученным на двух неводных буферных растворах;
С - 10,00 г масла, содержащего слабую кислоту и 125 см3 растворителя для титрования. Конечную точку выбирают в наиболее вертикальной части перегиба;
Д - 10,00 г масла, содержащего слабые и сильные кислоты и 125 см3 растворителя для титрования. Конечные точки выбирают в наиболее вертикальных частях двух точек перегиба
Примечания.
1. На некоторых измерительных приборах знак напряжения противоположный
2. Представленные на рисунке кривые даны для приблизительной оценки, так как в зависимости от типа прибора абсолютные значения потенциала могут меняться.
Рисунок 2 - Кривые титрования
10.4.3. После окончания титрования промывают электроды и конец бюретки растворителем для титрования, затем пропан-2-олом или этанолом и водой. Погружают электроды в воду не менее чем на 5 мин перед следующим применением, чтобы произошло насыщение водой гелевого слоя стеклянного электрода.
Если электроды загрязнены, их следует обработать согласно разделу 8.
Хранят электроды в дистиллированной воде.
10.5. Контрольное испытание
Для каждой серии образцов проводят контрольный опыт, титруя 125 см3 растворителя для титрования без анализируемого продукта.
При титровании вручную добавляют 0,1 или 0,05 моль/дм2 спиртового раствора гидроокиси калия по 0,05 см3 и записывают показания измерительного прибора и объема раствора из бюретки.
Титрование с автоматической регистрацией кривой титрования проводят по 10.4.
10.6. Определение щелочного числа
10.6.1. Определение проводят, как указано в 10.3, употребляя для титрования спиртовый раствор соляной кислоты 0,1 моль/дм3.
10.6.2. Для каждой серии образцов проводят контрольный опыт, титруя 125 см3 растворителя порциями по 0,05 см3 спиртового раствора соляной кислоты 0,1 моль/дм3.
10.6.3. При обратном титровании после проведения титрования по 10.6.1 продолжают добавлять из бюретки 0,1 моль/дм3 раствор соляной кислоты до потенциала на 115 мВ выше установленного для кислого буферного раствора (до pH 2). После того, как потенциал остается постоянным в течение 1 мин, избыток соляной кислоты титруют раствором гидроокиси калия 0,1 моль/дм3, добавляя в один прием по 0,01 - 0,02 см3, до потенциала, установленного в кислом буферном растворе (до pH 4), или скачка потенциала в этой области.
10.7. Определение кислотности
10.7.1. Для определения кислотности в стаканчик для титрования наливают 100 см3 растворителя и титруют его 0,05 моль/дм3 раствором гидроокиси калия, добавляя по 0,03 см3 и менее титранта. Титрование ведут до потенциала, установленного в щелочном буферном растворе. Затем в стаканчик наливают 100 см3 анализируемого продукта и вновь титруют 0,05 моль/дм3 раствором гидроокиси калия до того же потенциала. Вблизи потенциала буферного раствора после каждого добавления очередной порции титранта ожидают, пока потенциал установится, то есть изменение его будет составлять не более 5 мВ (около 0,1 pH) в течение 30 - 60 с.
11. ОБРАБОТКА РЕЗУЛЬТАТОВ АНАЛИЗА
11.1. Метод титрования вручную
Наносят на график объемы добавляемого 0,1 моль/дм3 спиртового раствора гидроокиси калия или 0,1 моль/дм3 раствора соляной кислоты соответственно показаниям измерительного прибора (рисунок 2).
Как конечную точку отмечают четкую точку перегиба кривой, которая находится вблизи потенциала свежеприготовленных неводных кислотных и щелочных буферных растворов. В случае кривых* не имеющих четких точек перегиба (см. рисунок 2, кривая В), за конечные точки принимают потенциал для соответствующих неводных буферных растворов. При титровании отработанных масел за конечную точку принимают точку на кривой, соответствующую показанию измерительного прибора, полученному на свежеприготовленном неводном кислотном буферном растворе.
Примечания
1. В точках перегиба кривой титрования добавление порций раствора по 0,05 см вызывает изменение потенциала более чем на 15 мВ и не менее чем на 30 больше значения, полученного при добавлении предыдущих и последующих одинаковых порций. Определенные точки перегиба можно различить только в областях с одинаковыми добавлениями.
2. Совместная работа, проводимая по определению кислотного числа товарных масел, присадок и отработанных масел, показала четкие точки перегиба для свежих масел, присадок и отсутствие или нечеткие точки перегиба для отработанных масел.
11.2. Метод автоматического титрования
Отмечают конечные точки на кривых титрования, полученных в 10.4, как и в методе титрования вручную.
11.3. Расчет кислотного, щелочного чисел и кислотности применим к методу титрования вручную и методу автоматического титрования.
11.3.1. Общее кислотное число К1 в миллиграммах гидроокиси калия на 1 г продукта вычисляют по формуле
![]()
где Vo - объем 0,1 моль/дм3 раствора гидроокиси калия, израсходованный на титрование контрольного опыта до значения ЭДС в щелочном буферном растворе или до скачка потенциала в этой области, см;
V1 - объем 0,1 или 0,05 моль/дм3 раствора гидроокиси калия, израсходованный на титрование образца до значения ЭДС в щелочном буферном растворе или до скачка потенциала в этой области, см;
m1 - масса анализируемого продукта, г;
с3 - концентрация раствора гидроокиси калия, определенная по 5.11.2, моль/дм,
56,1 - эквивалентная масса гидроокиси калия, г.
11.3.2. Кислотное число сильных кислот K2 в миллиграммах гидроокиси калия на 1 г продукта вычисляют по формуле
![]()
где V2 - объем 0,1 или 0,05 моль/дм3 раствора соляной кислоты, израсходованный на титрование контрольного опыта до значения ЭДС в кислом неводном буферном растворе или до скачка потенциала в этой области, см;
V3 - объем 0,1 или 0,05 моль/дм3 раствора гидроокиси калия, израсходованный на титрование образца до значения ЭДС в кислом неводном буферном растворе или до скачка потенциала в этой области, см;
с4 - концентрация раствора соляной кислоты, определенная по 5.7.2, моль/дм.
11.3.3. Щелочное число сильных оснований Щ1 в миллиграммах гидроокиси калия на 1 г продукта вычисляют по формуле
![]()
где V4 - объем 0,1 моль/дм раствора соляной кислоты, израсходованный на титрование образца до значения ЭДС в щелочном буферном растворе или до скачка потенциала в этой области, см3;
т2 - масса анализируемого продукта, г.
11.3.4. Общее щелочное число Щ2 в миллиграммах гидроокиси калия на 1 г продукта, определенное прямым титрованием, вычисляют по формуле
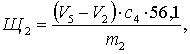
где V5 - объем 0,1 моль/дм3 раствора соляной кислоты, израсходованный на титрование образца до значения ЭДС в кислом буферном растворе или до скачка потенциала в этой области, см.
11.3.5. Общее щелочное число Щ3 в миллиграммах гидроокиси калия на 1 г продукта, определенное обратным титрованием, вычисляют по формуле
![]()
где V6 - объем 0,1 моль/дм3 раствора соляной кислоты, добавляемый к раствору анализируемого продукта, см;
V7 - объем 0,1 моль/дм3 раствора гидроокиси калия, израсходованный на титрование избытка соляной кислоты до значения ЭДС в кислом буферном растворе или до скачка потенциала в этой области, см3.
11.3.6. Кислотность К3 в миллиграммах гидроокиси калия на 100 см3 нефтепродукта вычисляют по формуле
![]()
где V8 - объем 0,05 моль/дм3 раствора гидроокиси калия, израсходованный на титрование до значения ЭДС в щелочном буферном растворе, см.
11.3.7. За результат анализа принимают среднее арифметическое результатов не менее двух последовательных определений, расхождения между которыми не превышают значений, указанных в таблицах 2 - 5.
12. ТОЧНОСТЬ МЕТОДА
12.1. Кислотное число
12.1.1. Сходимость
Расхождения между последовательными результатами испытания, полученными одним и тем же оператором на одной и той же аппаратуре при постоянно действующих условиях на идентичном исследуемом материале при нормальной и правильной эксплуатации, не должны превышать средних значений, приведенных в таблице 2, более одного случая из двадцати.
Таблица 2- Сходимость при определении кислотного числа, %
|
Товарные масла и концентраты присадки в точках перегиба |
Отработанные масла в конечных точках буферных растворов |
|||
|
Тип титрования |
Ручное |
Автоматическое |
Ручное |
Автоматическое |
|
Процент средних значений |
7 |
6 |
5 |
12 |
12.1.2. Воспроизводимость
Расхождения между двумя единственными и независимыми результатами, полученными разными операторами, работающими в разных лабораториях на идентичном исследуемом материале при нормальной и правильной эксплуатации, не должны превышать средних значений, приведенных в таблице 3, более одного случая из двадцати.
Таблица 3- Воспроизводимость при определении кислотного числа, %
|
Товарные масла и концентраты присадки в точках перегиба |
Отработанные масла в конечных точках буферных растворов |
|||
|
Тип титрования |
Ручное |
Автоматическое |
Ручное |
Автоматическое |
|
Процент средних значений |
20 |
28 |
39 |
44 |
12.2. Кислотное число сильных кислот
Данные точности для кислотного числа сильных кислот не разработаны ввиду редкого обнаружения (появления) его при анализе образцов.
12.3. Щелочное число и кислотность
12.3.1. Сходимость
Результаты двух последовательных определений, полученные одним лаборантом на одной и той же аппаратуре и пробе продукта в одинаковых условиях, признаются достоверными (с 95 %-ной доверительной вероятностью), если расхождения между ними не превышают значений, указанных в таблицах 4 и 5.
12.3.2. Воспроизводимость
Результаты испытаний, полученные разными лаборантами в разных лабораториях на одной и той же пробе продукта, признаются достоверными (с 95 %-ной доверительной вероятностью), если расхождения между ними не превышают значений, указанных в таблицах 4 и 5.
Таблица 4 - Сходимость и воспроизводимость при определении щелочного числа
|
Сходимость, мг КОН/г |
Воспроизводимость, мг КОН/г |
|
|
От 0,05 до 1,0 |
0,02 |
0,04 |
|
Св. 1,0 » 5,0 |
0,1 |
0,2 |
|
» 5,0 » 20,0 |
0,5 |
1,0 |
|
» 20,0 » 100 |
2,0 |
4,0 |
|
» 100 » 250 |
5,0 |
10,0 |
Таблица 5 - Сходимость и воспроизводимость при определении кислотности
|
Сходимость, мг КОН/100 см3 |
Воспроизводимость, мг КОН/100 см3 |
|
|
До 0,5 |
0,10 |
0,6 |
|
Св. 0,5 до 1,0 |
0,15 |
0,7 |
|
» 1,0 » 2,0 |
0,20 |
0,8 |
|
» 2,0 » 5,0 |
0,20 |
1,5 |
13. ПРОТОКОЛ ИСПЫТАНИЯ
Протокол испытания должен содержать следующее:
а) тип и идентификацию испытуемого продукта;
б) ссылку на данный международный стандарт или национальный стандарт;
в) результат испытания (см. 11);
г) любое отклонение по соглашению или другим документам от установленной методики;
д) дату испытания.
ПРИЛОЖЕНИЕ А
(обязательное)
ОПРЕДЕЛЕНИЕ ЩЕЛОЧНЫХ ЧИСЕЛ ОСНОВАНИЙ И СОЛЕЙ, ВХОДЯЩИХ В СОСТАВ СУЛЬФОНА ТНЫХ И АЛКИЛСАЛИЦИЛА ТНЫХ ПРИСАДОК
Для анализа присадок 0,1 - 0,2 г присадки (m3) взвешивают с погрешностью не более 0,0002 г и растворяют ее в растворителе, приготовленном по 5.13, взятом в объеме по 10.1.
А.1. ОПРЕДЕЛЕНИЕ ЩЕЛОЧНОГО ЧИСЛА, ОБУСЛОВЛЕННОГО НАЛИЧИЕМ ГИДРООКИСИ КАЛЬЦИЯ И УГЛЕКИСЛОГО КАЛЬЦИЯ В КАЛЬЦИЕВЫХ СУЛЬФОНА ТНЫХ ПРИСАДКАХ
А.1.1. Раствор присадки титруют 0,1 моль/дм3 раствором соляной кислоты по 5.7 до скачка потенциала, прибавляя в один прием по 0,1 см3, а после изменения потенциала более чем на 15 мВ (pH 0,25) - по 0,05 см3. Наличие скачка потенциала примерно на 100 - 130 мВ больше потенциала щелочного буферного раствора (в области примерно 9,3 - 8,8 pH) указывает на присутствие в присадке гидроокиси кальция.
А.1.2. Если при прямом титровании не наблюдается скачка потенциала или он получается недостаточно четким, массу уменьшают до 0,07 - 0,09 г. Если и в этом случае скачок потенциала отсутствует, то гидроокись кальция отсутствует.
А.1.3. Общее щелочное число определяют обратным титрованием по 10.6.3.
А.1.4. Обработка результатов
А.1.4.1. Щелочное число, обусловленное наличием гидроокиси кальция, Щ4, в миллиграммах КОН на 1 г присадки, вычисляют по формуле
![]()
где V9 - объем 0,1 моль/дм раствора соляной кислоты, израсходованный на титрование до скачка потенциала, см.
А.1.4.2. Пересчет щелочного числа Щ4 на массовую долю окиси кальция Щ5 в процентах производят по формуле
![]()
где 0,50 - отношение эквивалента окиси кальция к эквиваленту гидроокиси калия.
А.1.4.3. Общее щелочное число Щ3 вычисляют по 11.3.3.
А.1.4.4. Щелочное число, обусловленное наличием углекислого кальция, Щ6, в миллиграммах КОН на 1 г присадки, вычисляют по формуле
Щ6 = Щ3 - Щ4.
А.1.4.5. Пересчет щелочного числа Щ6 массовую долю окиси кальция Щ7 в процентах производят по формуле
![]()
А.2. ОПРЕДЕЛЕНИЕ ЩЕЛОЧНОГО ЧИСЛА, ОБУСЛОВЛЕННОГО НАЛИЧИЕМ ГИДРООКИСИ БАРИЯ И УГЛЕКИСЛОГО БАРИЯ В БАРИЕВЫХ СУЛЬФОНАТНЫХ ПРИСАДКАХ
А.2.1. Если начальная ЭДС меньше ЭДС, установленной в щелочном буферном растворе, в присадке присутствует гидроокись бария.
А.2.2. Если начальная ЭДС равна или больше ЭДС, установленной в щелочном буферном растворе, гидроокись бария в присадке отсутствует.
А.2.3. Общее щелочное число определяют обратным титрованием по 10.6.3.
А.2.4. Обработка результатов
А.2.4.1. Щелочное число, обусловленное наличием гидроокиси бария, Щ1, в миллиграммах КОН на 1 г присадки, вычисляют по 11.3.3.
А.2.4.2. Пересчет щелочного числа Щ1 на массовую долю окиси бария Щ8 в процентах производят по формуле
![]()
где 1,37 - соотношение эквивалентов окиси бария и гидроокиси калия.
Примечание - Если в присадке содержатся примеси в виде гидроокиси калия или едкого натра, то их определяют вместе с гидроокисью бария.
А.2.4.3. Общее щелочное число Щ3 вычисляют по 11.3.5.
А.2.4.4. Щелочное число, обусловленное наличием углекислого бария, Щ9, вычисляют по формуле
Щ9 = Щ3 - Щ1.
А.2.4.5. Пересчет щелочного числа Щ9 на массовую долю окиси бария Щ10 в процентах производят по формуле
![]()
А.3. ОПРЕДЕЛЕНИЕ ЩЕЛОЧНОГО ЧИСЛА, ОБУСЛОВЛЕННОГО НАЛИЧИЕМ АЛКИЛСАЛИЦИЛАТА КАЛЬЦИЯ, ГИДРООКИСИ КАЛЬЦИЯ И УГЛЕКИСЛОГО КАЛЬЦИЯ В КАЛЬЦИЕВЫХ АЛКИЛСАЛИЦИЛАТНЫХ ПРИСАДКАХ
А.3.1. Содержание в присадке гидроокиси кальция определяют так же, как и для сульфонатных кальциевых присадок.
А.3.2. Общее щелочное число определяют обратным титрованием по первому скачку потенциала. После достижения первого скачка потенциала продолжают титрование до второго скачка потенциала для определения содержания алкилсалициловой кислоты, образовавшейся при разложении соляной кислотой алкилсалицилата кальция.
А.3.3. Обработка результатов
А.3.3.1. Щелочное число, обусловленное наличием гидроокиси кальция, Щ< , в миллиграммах КОН на 1 г присадки, и массовую долю окиси кальция Щ5 в процентах вычисляют так же, как для сульфатных присадок.
А.3.3.2. Общее щелочное число Щ3 вычисляют по 11.3.5.
А.3.3.3. Щелочное число, обусловленное наличием алкилсалицилата кальция, Щ11, выраженное в миллиграммах КОН на 1 г присадки, вычисляют по формуле
![]()
где V10 - объем 0,1 моль/дм3 раствора гидроокиси калия, израсходованный на
титрование до второго скачка потенциала, см3;
V11 - объем 0,1 моль/дм3 раствора гидроокиси калия, израсходованный на
титрование до первого скачка потенциала, см3.
A3.3.4. Пересчет щелочного числа Щ11 на массовую долю окиси кальция Щ12 в процентах производят по формуле
![]()
А.3.3.5. Щелочное число, обусловленное наличием углекислого кальция. Щ13 вычисляют по разности общего щелочного числа и суммы щелочных чисел, обусловленных наличием алкилсалицшата кальция
Щ13 = Щ3 - (Щ4 + Щ11).
А.3.3.6. Пересчет щелочного числа Щ13 на массовую долю окиси кальция Щ14 в процентах производят по формуле
![]()
|
Ключевые слова: нефтепродукты, смазочные материалы, химический анализ, определение содержания кислоты, кислотное число, кислотность, общее щелочное число, щелочное число сильных оснований, число нейтрализации, титрование |
СОДЕРЖАНИЕ
|
1. Назначение и область применения. 1 8. Подготовка системы электродов. 8 |