Государственное санитарно-эпидемиологическое нормирование Российской Федерации
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ.
ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств
изопропилфенацина в воде
методом высокоэффективной
жидкостной хроматографии
Методические указания
МУК
4.1.2292-07
1. Разработаны Федеральным научным центром гигиены им. Ф.Ф. Эрисмана (Т.В. Юдина, Н.Е. Федорова, В.Н. Волкова).
2. Рекомендованы к утверждению Комиссией по санитарно-эпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 21.06.2007 № 2).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г.Г. Онищенко 10 октября 2007 г.
4. Введены в действие с 25 декабря 2007 г.
5. Введены впервые.
Содержание
УТВЕРЖДАЮ
Руководитель Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный санитарный
врач Российской Федерации
Г.Г. Онищенко
10 октября 2007 г.
Дата введения: 25 декабря 2007 г.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение
остаточных количеств изопропилфенацина в воде
методом
высокоэффективной жидкостной хроматографии
Методические
указания
МУК 4.1.2292-07
Настоящие методические указания устанавливают метод высокоэффективной жидкостной хроматографии для определения в воде массовой концентрации изопропилфенацина в диапазоне 0,0002-0,004 мг/дм3.
2-(α-фенил-изопропилфенил)-ацетил)-индан-1,3-дион
(IUРАС)
С3Н7
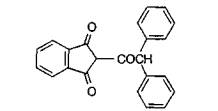
С26Н22О3
Мол. масса 382,15
Твердое вещество желто-оранжевого цвета. Температура плавления 148°С, кипения - более 350°С. Плотность 1,21 г/см3. Хорошо растворим в большинстве органических растворителей (ацетоне, этаноле, диэтиловом эфире и др.). Практически не растворим в воде - 0,3 мг/дм3.
Агрегатное состояние в воздушной среде - аэрозоль и пары.
Острая пероральная токсичность (LD50) для крыс - более 1,6±0,2 мг/кг, мышей - 3,4±0,5 мг/кг.
Область применения
Изопропилфенацин - ротентицид класса индандионов, обладающий антикоагулянтной активностью, рекомендуется для борьбы с грызунами в открытом грунте (осень, зима, весна) на зимующих культурах (зерновые, пастбищные травы, древесные, кустарниковые насаждения и др.), в защищенном грунте на всех культурах независимо от сезона. Применяется в виде приманки.
ОДУ изопропилфенацина в воде водоемов - 0,0008 мг/дм3.
1. Метрологические характеристики
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и её составляющие) результатов измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1, для соответствующих диапазонов концентраций.
Таблица 1
Метрологические параметры
|
Анализируемый объект |
Диапазон определяемых концентраций, мг/кг (дм3) |
Показатель точности (граница относительной погрешности) ±δ, %Р=0,95 |
Стандартное отклонение повторяемости, σr % |
Предел повторяемости, r, % |
Предел воспроизводимости, R, % |
|
Вода |
от 0,004 до 0,001 вкл. |
100 |
4,2 |
12 |
15 |
|
менее 0,001 до 0,0002 |
150 |
5,4 |
15 |
19 |
Полнота извлечения вещества, стандартное отклонение, доверительный интервал среднего результата для полного диапазона концентраций (n=20) приведены в табл. 2.
Таблица 2
Полнота извлечения вещества, стандартное отклонение, доверительный интервал среднего результата
|
Анализируемый объект |
Метрологические параметры, Р=0,95, n=20 |
||||
|
предел обнаружения, мг/дм3 |
диапазон определяемых концентраций, мг/дм3 |
среднее значение определения, % |
стандартное отклонение, S, % |
доверительный интервал среднего результата, ±, % |
|
|
Вода |
0,0002 |
0,0002-0,004 |
91,3 |
3,8 |
2,7 |
2. Метод измерений
Методика основана на определении вещества с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) с ультрафиолетовым детектором после экстракции из анализируемой пробы воды дихлорметаном и последующей очистки экстракта на патроне для твердофазной экстракции Sep Pak Silica.
3. Средства измерений, вспомогательные устройства, реактивы и материалы
3.1. Средства измерений
|
Жидкостный хроматограф с ультрафиолетовым детектором с переменной длиной волны (фирмы Waters, США) 15311-02 |
Номер в Государственном реестре средств измерений |
|
Весы аналитические ВЛА-200 |
|
|
Колбы мерные 2-50-2, 2-100-2 и 2-1000-2 |
|
|
Меры массы |
|
|
Пипетки градуированные 2 класса точности вместимостью 1,0; 2,0; 5,0; 10 см3 |
ГОСТ 29227 |
|
Пробирки градуированные вместимостью 5 или 10 см5 |
|
|
Цилиндры мерные 2 класса точности вместимостью 10, 50, 100 и 1000 см3 |
Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Изопропилфенацин, аналитический стандарт с содержанием основного вещества (сумма изомеров) 94,6% (ЗАО «Щелково Агрохим») |
|
|
Ацетонитрил для хроматографии, хч |
ТУ 6-09-4326-76 |
|
Вода бидистиллированная, деионизованная или перегнанная над КМnО4 |
|
|
н-Гексан, хч |
ТУ 6-09-33-75 |
|
Натрий серно-кислый безводный, хч |
ГОСТ 4166 |
|
Кислота орто-фосфорная, хч, 85% |
ГОСТ 6552 |
|
Метилен хлористый (дихлорметан), хч |
ГОСТ 12794 |
|
Этиловый эфир уксусной кислоты (этилацетат) эталонный |
ГОСТ 4166 |
Допускается использование реактивов иных производителей с аналогичной или более высокой квалификацией.
3.3. Вспомогательные устройства, материалы
|
Аллонж прямой с отводом для вакуума (для работы с концентрирующими патронами) |
|
|
Баня ультразвуковая фирмы Донау (Швейцария) |
|
|
Бумажные фильтры «красная лента», обеззоленные |
ТУ 6-09-2678-77 |
|
Воронки делительные вместимостью 1000 см3 |
ГОСТ 25336 |
|
Воронки конусные диаметром 30-37 и 60 мм |
ГОСТ 25336 |
|
Груша резиновая |
|
|
Колбы плоскодонные вместимостью 200-250 см3 |
ГОСТ 9737 |
|
Колбы круглодонные на шлифе, вместимостью 10, 100 и 250 см3 |
ГОСТ 9737 |
|
Мембранные фильтры капроновые, диаметром 47 мм |
|
|
Насос водоструйный |
ГОСТ 10696 |
|
Патроны для твердофазной экстракции типа Sep-Pak Plus Silica Cartridges (масса сорбента 690 г) |
|
|
Пробирки центрифужные |
ГОСТ 25336 |
|
Ротационный вакуумный испаритель В-169 фирмы Buchi, Швейцария |
ТУ 25-11-917-74 |
|
Стаканы химические, вместимостью 50 и 100 см3 |
ГОСТ 25336 |
|
Стекловата |
|
|
Стеклянные палочки |
|
|
Установка для перегонки растворителей через мембрану |
|
|
Хроматографическая колонка стальная, длиной 250 мм, внутренним диаметром 4,6 мм, содержащая Symmetry® С18, зернением 5 мкм |
|
|
Шприц для ввода образцов для жидкостного хроматографа вместимостью 50-100 мм3 |
|
|
Шприц медицинский с разъемом Льюера |
ГОСТ 22090 |
Допускается применение хроматографических колонок и другого оборудования с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007, требования электробезопасности при работе с электроустановками по ГОСТ 12.1.019, а также требования, изложенные в технической документации на жидкостный хроматограф.
4.2. Помещение должно соответствовать требованиям пожаробезопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009. Содержание вредных веществ в воздухе не должно превышать норм, установленных ГН 2.2.5.1313-03 «Предельно-допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны». Организация обучения работников безопасности труда - по ГОСТ 12.0.004.
5. Требования к квалификации операторов
К выполнению измерений допускают специалистов, имеющих квалификацию не ниже лаборанта-исследователя, с опытом работы на жидкостном хроматографе.
К проведению пробоподготовки допускают оператора с квалификацией «лаборант», имеющего опыт работы в химической лаборатории.
6. Условия измерений
При выполнении измерений соблюдают следующие условия:
- процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20±5)°С и относительной влажности не более 80%.
- выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к выполнению измерений
Выполнению измерений предшествуют следующие операции: очистка органических растворителей (при необходимости), подготовка подвижной фазы для ВЭЖХ, кондиционирование хроматографической колонки, приготовление растворов для градуировки и внесения, установление градуировочной характеристики, подготовка патронов для твердофазной экстракции, проверка хроматографического поведения вещества на них, отбор проб.
7.1. Подготовка органических растворителей
7.1.1. Очистка ацетонитрила
Ацетонитрил кипятят с обратным холодильником над пентоксидом фосфора не менее 1 часа, после чего перегоняют, непосредственно перед употреблением ацетонитрил повторно перегоняют над прокаленным карбонатом калия.
7.1.2. Очистка этилацетата
Этилацетат промывают последовательно 5% водным раствором карбоната натрия, насыщенным раствором хлористого кальция, сушат над безводным карбонатом калия и перегоняют или подвергают ректификационной перегонке на колонне с числом теоретических тарелок не менее 50.
7.1.3. Очистка н-гексана
Растворитель последовательно промывают порциями концентрированной серной кислоты, до тех пор, пока она не перестанет окрашиваться в желтый цвет, водой до нейтральной реакции промывных вод, перегоняют над поташом.
7.2. Подготовка подвижной фазы для ВЭЖХ
В мерную колбу вместимостью 1000 см3 помещают 890 см3 ацетонитрила, 110 см3 бидистиллированной или деионизованной воды и 1 см3 ортофосфорной кислоты, перемешивают, фильтруют и дегазируют.
7.3. Кондиционирование хроматографической колонки
Промывают колонку подвижной фазой (приготовленной по п. 7.2) при скорости подачи растворителя 1,0 см3/мин до установления стабильной базовой линии.
7.4. Приготовление градуировочных растворов и растворов внесения
7.4.1. Исходный раствор изопропилфенацина для градуировки (концентрация 100 мкг/см3)
В мерную колбу вместимостью 100 см3 вносят 0,01 г изопропилфенацина, добавляют 50-70 см3 ацетонитрила, перемешивают, доводят ацетонитрилом до метки, вновь перемешивают. Раствор хранится в холодильнике в течение месяца.
Растворы № 1-5 готовят объемным методом путем последовательного разбавления исходного раствора для градуировки.
7.4.2. Раствор № 1 изопропилфенацина для градуировки и внесения (концентрация 10 мкг/см3)
В мерную колбу вместимостью 100 см3 помещают 10 см3 исходного раствора изопропилфенацина с концентрацией 100 мкг/см3 (п. 7.4.1), разбавляют ацетонитрилом до метки, перемешивают. Раствор хранится в холодильнике в течение месяца.
Этот раствор используют для приготовления проб с внесением при оценке полноты извлечения действующего вещества методом «внесено-найдено».
7.4.3. Рабочие растворы № 2-5 изопропилфенацина для градуировки (концентрация 0,05-1,0 мкг/см3)
В 4 мерные колбы вместимостью 100 см3 помещают по 0,5; 1,0; 5,0 и 10,0 см3 градуировочного раствора № 1 с концентрацией 10 мкг/см3 (п. 7.4.2), доводят до метки подвижной фазой, приготовленной по п. 7.2, тщательно перемешивают, получают рабочие растворы №№ 2-5 с концентрацией изопропилфенацина 0,05; 0,1; 0,5 и 1,0 мкг/см3, соответственно.
Растворы хранятся в холодильнике в течение недели.
7.5. Установление градуировочной характеристики
Градуировочную характеристику, выражающую линейную (с угловым коэффициентом) зависимость суммы площадей 2 пиков орто- и параизомеров изопропилфенацина (мкВ·с) от концентрации вещества в растворе (мкг/см3), устанавливают методом абсолютной калибровки по 4-м растворам для градуировки №№ 2-5.
В инжектор хроматографа вводят по 20 мм3 каждого градуировочного раствора и анализируют в условиях хроматографирования по п. 7.5.1. Осуществляют не менее 3 параллельных измерений. Устанавливают площади пиков изомеров действующего вещества, рассчитывают сумму площадей орто- и параизомеров изопропилфенацина.
Градуировочный график проверяют ежедневно по анализу 2 растворов для градуировки различной концентрации. Если значения площадей отличаются более чем на 10% от данных, заложенных в градуировочную характеристику, ее строят заново, используя свежеприготовленные рабочие растворы для градуировки.
7.6. Приготовление 2% раствора уксусной кислоты в этилацетате
В мерную колбу вместимостью 100 см3 помещают 50-70 см3 этилацетата, вносят 2 см ледяной уксусной кислоты, доводят до метки этилацетатом, тщательно перемешивают.
7.7. Подготовка концентрирующего патрона Sep-Pak Plus Silica для очистки экстракта
Патрон Sep-Pak Plus Silica устанавливают на аллонж с прямым отводом для вакуума, сверху в патрон вставляют шприц с разъемом Льюера объемом не менее 10 см3, используемый в качестве емкости для элюента.
Концентрирующий патрон промывают последовательно 5 см3 этилацетата, затем 5 см3 смеси гексан-этилацетат (1:1, по объему). Процедуру проводят с использованием вакуума, скорость потока растворов через патрон не должна превышать 5 см3/мин, при этом нельзя допускать высыхания поверхности патрона.
Примечание: В отсутствии специального аллонжа, жидкость продавливают через патрон с помощью шприца, скорость продавливания раствора не должна превышать 1-2 капли в сек.
7.8. Проверка хроматографического поведения изопропилфенацина
на концентрирующем
патроне Sep-Pak Plus Silica
В круглодонную колбу вместимостью 10 см3 помещают 0,2 см3 градуировочного раствора №1 изопропилфенацина (п. 7.4.2), растворитель упаривают досуха при температуре не выше 35°С, остаток растворяют в 2 см3 этилацетата, помещают на 30 с в ультразвуковую баню. Затем в колбу добавляют 2 см3 гексана, смесь тщательно перемешивают и вносят на концентрирующий патрон, подготовленный по п. 7.7. Колбу обмывают 5 см3 смеси гексан-этилацетат (1:1, по объему) и также вносят на патрон. Патрон дополнительно промывают 15 см3 смеси гексан-этилацетат (1:1, по объему), 20 см3 смеси этих же растворителей в объемном соотношении 3:7, затем 20 см3 этилацетата. Скорость прохождения раствора через патрон не должна превышать 1-2 капли в сек. Элюат отбрасывают.
Изопропилфенацин элюируют с патрона 25 см3 2% уксусной кислоты в этилацетате (п. 7.6), собирая 5 порций элюата по 5 см3 каждая непосредственно в круглодонные колбы. Растворы в колбах упаривают досуха при температуре не выше 35°С. Остаток в каждой колбе растворяют в 2 см3 подвижной фазы (приготовленной по п. 7.2) и анализируют содержание изопропилфенацина по п. 9.3. Фракции, содержащие изопропилфенацин, объединяют и вновь анализируют. Рассчитывают уровень вещества в элюате, определяют полноту смывания с патрона и необходимый для очистки объем элюента.
Примечание: Проверку хроматографического поведения изопропилфенацина следует проводить обязательно, поскольку профиль вымывания может изменяться при использовании новой партии патронов и растворителей.
8. Отбор проб
Отбор проб производится в соответствии с ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб», «Унифицированными правилами отбора проб сельскохозяйственной продукции, пищевых продуктов и объектов окружающей среды для определения микроколичеств пестицидов» (№ 2051-79 от 21.08.79).
Пробы воды анализируют в день отбора, при необходимости хранят в холодильнике при температуре 4-6°С в течение 10 недель. Для длительного хранения пробы замораживают и хранят в полиэтиленовой таре в морозильной камере при температуре -18°С.
Перед анализом образцы воды фильтруют через неплотный бумажный фильтр.
9. Выполнение определения
9.1. Экстракция
Образец анализируемой воды объемом 500 см3 помещают в делительную воронку, вместимостью 1000 см3, добавляют 75 см3 хлористого метилена, интенсивно встряхивают делительную воронку в течение 2 мин. После полного разделения фаз нижний органический слой переносят в круглодонную колбу, вместимостью 250 см3, фильтруя его через 2 см слой безводного сульфата натрия, помещенный в конусную химическую воронку диаметром 60 мм, снабженную бумажным фильтром «красная лента». Операцию экстракции водной фазы повторяют, еще дважды порциями этилацетата по 50 см3. Отстоявшийся слой хлористого метилена (нижняя фаза) фильтруют в колбу с ранее полученным экстрактом.
Объединенный экстракт упаривают на ротационном вакуумном испарителе при температуре не выше 40°С, подвергают очистке в соответствии с п. 9.2.
9.2. Очистка экстракта
Сухой остаток в колбе, полученный по п. 9.1, растворяют в 2 см3 этилацетата, помещают на 30с в ультразвуковую баню. Затем в колбу добавляют 2 см3 гексана, смесь тщательно перемешивают и вносят на концентрирующий патрон Sep-Pak Plus Silica, подготовленный по п. 7.7. Колбу обмывают 5 см3 смеси гексан-этилацетат (1:1, по объему) и также вносят на патрон. Патрон дополнительно промывают 15 см3 смеси гексан-этилацетат (1:1, по объему), 20 см3 смеси этих же растворителей в объемном соотношении 3:7, затем 20 см3 этилацетата. Скорость прохождения раствора через патрон не должна превышать 1-2 капли в сек. Элюат отбрасывают.
Изопропилфенацин элюируют с патрона 20 см3 2% уксусной кислоты в этилацетате (п. 7.6), собирая элюат непосредственно в круглодонную колбу. Раствор упаривают досуха при температуре не выше 35°С. Остаток в колбе растворяют в 2 см3 подвижной фазы (приготовленной по п. 7.2) и анализируют содержание изопропилфенацина по п. 9.3.
9.3. Условия хроматографирования
Измерения выполняют при следующих режимных параметрах.
Жидкостной хроматограф «Breeze» с ультрафиолетовым детектором (фирма Waters, США).
Хроматографическая колонка стальная, длиной 250 мм, внутренним диаметром 4,6 мм, содержащая Symmetry® С18, зернением 5 мкм.
Температура колонки: комнатная.
Подвижная фаза: ацетонитрил-вода-орто-фосфорная кислота (89:11:0,1, по объему).
Скорость потока элюента: 1,0 см3/мин.
Рабочая длина волны: 312 нм.
Чувствительность: 0,005 ед. абсорбции на шкалу.
Объем вводимой пробы: 20 мм3.
Ориентировочное время выхода изопропилфенацина:
- орто-изомер: 7,72-8,01 мин
- пара-изомер: 9,14-9,45 мин.
Линейный диапазон детектирования: 1-20 нг.
Образцы, дающие пики, большие, чем градуировочный раствор изопропилфенацина с концентрацией 1 мкг/см3, разбавляют (не более чем в 50 раз) подвижной фазой для ВЭЖХ (подготовленной по п. 7.2).
10. Обработка результатов анализа
Содержание изопропилфенацина в пробе рассчитывают по формуле:
где Х - содержание изопропилфенацина в пробе, мг/дм3;
A - концентрация изопропилфенацина, найденная по градуировочному графику, в соответствии с величиной суммы площадей хроматографических пиков орто- и параизомеров, мкг/см3;
W - объем экстракта, подготовленного для хроматографирования, см3;
V - объем анализируемого образца воды, см3.
11. Проверка приемлемости результатов параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости (1):
![]() (1)
(1)
где X1, X2 - результаты параллельных определений, мг/дм3;
r - значение предела повторяемости (табл. 1), при этом r=2,8 σr. При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
![]() мг/дм3 при вероятности Р=0,95, где
мг/дм3 при вероятности Р=0,95, где![]()
![]() - среднее арифметическое результатов определений, признанных приемлемыми,
мг/дм3;
- среднее арифметическое результатов определений, признанных приемлемыми,
мг/дм3;
Δ - граница абсолютной погрешности, мг/дм3;
![]()
где δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций, табл. 1), %.
В случае если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание вещества в пробе менее 0,0002 мг/дм3»*
__________________
*0,0002 мг/дм3 - предел обнаружения.
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-2002 «Точность (правильность и прецинзионность) методов и результатов измерений».
13.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится методом добавок.
Величина добавки Сд должна удовлетворять условию:
![]()
где ![]() - характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой соответственно) мг/дм3, при этом:
- характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой соответственно) мг/дм3, при этом:
Dл = ± 0,84D,
где D - граница абсолютной погрешности, мг/дм3;
![]()
где δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций, табл. 1), %.
Результат контроля процедуры Кк рассчитывают по формуле:
где ![]() - среднее арифметическое
результатов параллельных определений (признанных приемлемыми по п. 11)
содержания компонента в образце с добавкой, испытуемом образце, концентрация
добавки, соответственно, мг/дм3.
- среднее арифметическое
результатов параллельных определений (признанных приемлемыми по п. 11)
содержания компонента в образце с добавкой, испытуемом образце, концентрация
добавки, соответственно, мг/дм3.
Норматив контроля К рассчитывают по формуле
![]() ,
,
Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
|Кк| ≤ К, (2)
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости:
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости (R)
![]() (3)
(3)
где X1, Х2 - результаты измерений в двух разных лабораториях, мг/дм3;
R - предел воспроизводимости (в соответствии с диапазоном концентраций, табл. 1), %.