ГОСТ Р 50595-93
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ВЕЩЕСТВА ПОВЕРХНОСТНО-АКТИВНЫЕ
МЕТОД ОПРЕДЕЛЕНИЯ БИОРАЗЛАГАЕМОСТИ В ВОДНОЙ СРЕДЕ
ГОССТАНДАРТ РОССИИ
Москва
Предисловие
1. РАЗРАБОТАН И ВНЕСЕН Техническим комитетом ТК 193 "Кислоты жирные синтетические, высшие жирные спирты, поверхностно-активные вещества"
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Госстандарта России от 28.09.93 № 216
3. ВВЕДЕН ВПЕРВЫЕ
СОДЕРЖАНИЕ
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ВЕЩЕСТВА ПОВЕРХНОСТНО-АКТИВНЫЕ
Метод определения биоразлагаемости в водной среде
Surface active agents.
Method for determination of
biodegrxdability in aqueous medium
Дата введения 1995-01-01
1 ОБЛАСТЬ ПРИМЕНЕНИЯ
Настоящий стандарт распространяется на метод определения биоразлагаемости поверхностно-активных веществ (далее - ПАВ) и устанавливает условия, приемы и метод определения их биоразлагаемости как таковых, так и в составах бытовых и технических препаратов.
Стандарт распространяется на анионные, неионогенные, катионные (кроме четвертичных солей аммония) и амфолитные ПАВ, а также их композиции.
Стандарт не распространяется на методы оценки токсичности ПАВ по отношению к водным микроорганизмам.
Поверхностно-активные вещества при попадании в водную среду разлагаются с различной скоростью под воздействием физико-химических и биохимических факторов в зависимости от условий среды и вида ПАВ.
Метод позволяет устанавливать кинетические характеристики процессов биоразложения ПАВ в аэробных условиях в водной среде, а также ориентировочно-допустимый уровень содержания ПАВ в сточных водах, подаваемых в аэротенки.
Показатели биоразлагаемости ПАВ, определяемые по настоящему стандарту, учитываются при санкционировании ассортимента, объемов производства и применения ПАВ, а также при выборе условий и способов очистки сточных вод.
2 НОРМАТИВНЫЕ ССЫЛКИ
В настоящем стандарте использованы ссылки на следующие стандарты и технические условия:
|
ГОСТ 61-75 |
Кислота уксусная |
|
|
ГОСТ 83-79 |
Натрий углекислый |
|
|
ГОСТ 84-76 |
Натрий углекислый 10-водный |
|
|
ГОСТ 1770-74 |
Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки |
|
|
ГОСТ 199-78 |
Натрий уксусно-кислый 3-водный |
|
|
ГОСТ 450-77 |
Кальций хлористый технический |
|
|
ГОСТ 3118-77 |
Кислота соляная |
|
|
ГОСТ 3760-79 |
Аммиак водный |
|
|
ГОСТ 3772-74 |
Аммоний фосфорно-кислый двузамещенный |
|
|
ГОСТ 3773-72 |
Аммоний хлористый |
|
|
ГОСТ 4108-72 |
Барий хлористый 2-водный |
|
|
ГОСТ 4148-78 |
Железо (II) серно-кислое 7-водное |
|
|
ГОСТ 4197-74 |
Натрий азотисто-кислый |
|
|
ГОСТ 4198-75 |
Калий фосфорно-кислый однозамещенный |
|
|
ГОСТ 4204-77 |
Кислота серная |
|
|
ГОСТ 4208-72 |
Соль закиси железа и аммония двойная серно-кислая (соль Мора) |
|
|
ГОСТ 4217-77 |
Реактивы. Калий азотно-кислый |
|
|
ГОСТ 4220-75 |
Реактивы. Калий двухромово-кислый |
|
|
ГОСТ 43 28-77 |
Натрия гидроокись |
|
|
ГОСТ 4517-87 |
Реактивы. Метод приготовления вспомогательных реактивов и растворов, применяемых при анализе |
|
|
ГОСТ 4523-77 |
Реактивы. Магний серно-кислый 7-водный |
|
|
ГОСТ 58 21-78 |
Реактивы. Кислота сульфаниловая |
|
|
ГОСТ 5845-79 |
Реактивы. Калий-натрий винно-кислый 4-водный |
|
|
ГОСТ 6709-72 |
Вода дистиллированная |
|
|
ГОСТ 9147-80 |
Посуда и аппаратура лабораторная фарфоровые |
|
|
ГОСТ 9871-75 |
Термометры стеклянные ртутные электроконтактные и терморегуляторы |
|
|
ГОСТ 11773-76 |
Реактивы. Натрий фосфорно-кислый двузамещенный |
|
|
ГОСТ 13045-81 |
Ротаметры |
|
|
ГОСТ 13805-76 |
Пептон сухой ферментативный для бактериологических целей |
|
|
ГОСТ 19627-74 |
Гидрохинон |
|
|
ГОСТ 20015-91 |
Хлороформ |
|
|
ГОСТ 23519-79 |
Фенол синтетический технический |
|
|
ГОСТ 25336-82 |
Посуда и оборудование лабораторные стеклянные |
|
|
ГОСТ 25794.2-83 |
Методы приготовления титрованных растворов для окислительно-восстановительного титрования |
|
|
ГОСТ 27025-86 |
Реактивы. Общие указания по проведению испытаний |
|
|
Качество воды. Термины и определения |
||
|
ГОСТ 29232-91 |
Анионные и неионогенные поверхностно-активные вещества. Определение критической концентрации мицеллообразования. Метод определения поверхностного натяжения с помощью пластины, скобы или кольца |
|
|
ТУ 6-09-01-744-88 |
Фосфорно-12-вольфрамовая (7) кислота водная (фосфорно-вольфрамовая кислота) |
|
|
ТУ 6-09-07-1703-90 |
1-Нафтиламин |
|
3 ОПРЕДЕЛЕНИЯ, ОБОЗНАЧЕНИЯ И СОКРАЩЕНИЯ
Таблица 1
|
Термин |
Определение |
Условные обозначения |
|
1 Поверхностно-активные вещества (Tenside, Surfactant) |
Вещества с асимметричной молекулярной структурой, молекулы которых содержат один или несколько гидрофобных радикалов и одну или несколько гидрофильных групп Примечания 1. Такая структура обуславливает поверхностную активность молекул поверхностно-активных веществ, т.е. способность концентрироваться на межфазных поверхностях раздела, тем самым изменяя свойства системы. 2 Детергенты (моющие средства) включают поверхностно-активные вещества (10-20%) и полезные добавки (до 80%) |
ПАВ |
|
2 Биоразлагаемость поверхностно-активных веществ |
Способность молекул подвергаться деструкции (вплоть до углекислого газа, минеральных солей и воды) под воздействием микрофлоры, присутствующей в биологических очистных сооружениях и водоемах |
|
|
- первичная |
Стадия разложения молекул, соответствующая нарушению их первичной структуры и обусловленной этим потере ими поверхностно-активных свойств |
|
|
-показатель |
Кинетические критерии оценки функционирования биотической системы "активный ил - ПАВ", характеризующие способность молекул ПАВ разлагаться, а активного ила адаптироваться |
|
|
3 Режим процесса биоразложения: |
|
|
|
- квазистационарный |
Режим после завершения переходного периода, обусловленного введением в систему ПАВ, лимитируемый скоростями ферментативных реакций разложения ПАВ неадаптированным активным илом и отображаемый на зависимости Свых=f(t) с выходом на плато А (рисунок 1 а, б, в) |
|
|
- стационарный |
Режим, который достигается после завершения адаптации активного ила и отображается на зависимости Свых=f(t) выходом на плато Б (рисунок 1 а, в) |
|
|
4 Активный ил |
|
|
|
- неадаптированный |
Культивируемый на синтетической сточной воде, содержащей набор минеральных солей и пептон |
|
|
- адаптированный к ПАВ |
Культивируемый на синтетической сточной воде, содержащей испытуемое ПАВ в течение времени, равного (или большего) продолжительности индукционного периода |
|
|
5. Критическая концентрация мицеллообразования |
Характерная для поверхностно-активных веществ в водном растворе концентрация (на практике - узкий интервал концентрации), при превышении которой в растворе появляются и развиваются ассоциаты молекул поверхностно-активных веществ - мицеллы, что приводит к резкому изменению зависимости ряда физико-химических свойств раствора от концентрации |
ККМ |
|
6 Химическое потребление кислорода |
Потребление кислорода, определяемое методом бихроматной окисляемости |
ХПК |
4 ПРИНЦИП МЕТОДА
Метод основан на определении способности молекул ПАВ подвергаться биоразложению в аэробных условиях биологических очистных сооружений и водных объектов.
Определение проводят с использованием двух аэротенков (контрольного и опытного) при режимах, моделирующих нормальные условия работы биологических очистных сооружений. При этом в контрольный аэротенк непрерывно подают синтетическую сточную воду, а в опытный (после завершения подготовительного периода) - синтетическую сточную воду с добавлением испытуемого ПАВ, концентрация которого постоянна на весь период опыта и равна половине критической концентрации мицеллообразования.
В качестве показателей биоразлагаемости приняты кинетические характеристики процесса биоразложения ПАВ, рассчитанные из кинетических кривых остаточного содержания ПАВ в очищенной сточной воде, поступающей из опытного аэротенка:
- тип кинетической зависимости процесса биоразложения;
- продолжительность индукционного периода;
- период полуразложения поверхностно-активного вещества адаптированным (или неадаптированным) илом.
5 СРЕДСТВА ИЗМЕРЕНИЙ. ВСПОМОГАТЕЛЬНЫЕ УСТРОЙСТВА, РЕАКТИВЫ И МАТЕРИАЛЫ
Аэротенки объемом 6 дм3 конструкции АКХ им. К.Д Памфилова (приложения А и Б) или любой другой конструкции с известными характеристиками (рабочий объем, период аэрации).
Дозатор синтетической сточной воды любого типа, обеспечивающий ее непрерывную подачу в аэротенк с заданной скоростью, предпочтительно 1 дм3/ч.
Индикатор расхода воздуха ротаметрический типа РМА-1 по ГОСТ 13045.
Терморегулятор ТПК-М-5П.О.50.201 по ГОСТ 9871 (или любой другой аналогичного типа).
Натрий углекислый по ГОСТ 83, ч.
Натрий уксусно-кислый 3-водный по ГОСТ 199, ч.
Калий фосфорно-кислый однозамещенный по ГОСТ 4198, ч. д. а.
Аммоний фосфорно-кислый двузамещенный по ГОСТ 3772, ч. д. а.
Кальций хлористый технический по ГОСТ 450.
Магний серно-кислый 7-водный по ГОСТ 4523, ч. д. а.
Пептон сухой ферментативный по ГОСТ 13805.
Ил активный неадаптированный, культивированный на синтетической сточной воде, содержащей набор минеральных солей и пептон в концентрациях, приведенных в таблице 2, по режимам, указанным в 6.2.
Примечание - Допускается использовать в опытах активный ил из регенераторов городских сооружений биологической очистки. При этом он должен быть отмыт от взвешенных веществ и других посторонних примесей культивированием на синтетической сточной воде в течение не менее 20 сут.
6 ОПРЕДЕЛЕНИЕ БИОРАЗЛАГАЕМОСТИ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ
Определение биоразлагаемости ПАВ включает следующие этапы;
- условия проведения определения;
- подготовка к определению;
- выполнение определения;
- обработка результатов определения.
6.1 Условиями определения биоразлагаемости являются:
- расход синтетической сточной воды, подаваемой в аэротенк, - 1 дм3/ч температурой (20±5) °С;
- расход воздуха ~ 2 дм3 /мин;
- концентрация поверхностно-активного вещества в синтетической сточной воде, подаваемой в аэротенк, постоянная и равная половине критической концентрации мицеллообразования.
6.2 Подготовка к определению включает следующие этапы:
- загрузку суспензии неадаптированного активного ила в контрольный и опытный аэротенки;
- подачу синтетической сточной воды (без ПАВ) в оба аэротенка;
- проверку режимов работы аэротенков;
- проверку надежности работы аэротенков (при освоении методики или обучении).
6.2.1. Загрузку суспензии неадаптированного активного ила в аэротенки проводят до концентрации (2,5 ±0,2) г/дм3 по сухому веществу, концентрацию ила корректируют по результатам ежедневных анализов, избыточный ил из аэротенков удаляют.
6.2.2. Синтетическую сточную воду готовят растворением минеральных солей и пептона в водопроводной дехлорированной воде. Состав приведен в таблице 2.
Таблица 2 Состав синтетической сточной воды
|
Компонент сточной воды |
Массовая концентрация, мг/дм3 |
|
Натрий углекислый |
50,0 |
|
Натрий уксусно-кислый |
50,0* |
|
Калий фосфорно-кислый однозамещенный |
25,0 |
|
Аммоний фосфорно-кислый двузамещенный |
25.0 |
|
Кальций хлористый |
7,5 |
|
Магний серно-кислый |
5,0* |
|
Пептон |
100-150 (до ХПК= 220±20 мгО2/дм3) |
* В пересчете на безводные соли
6.2.3. Проверку режимов работы аэротенков осуществляют путем периодического отбора и анализа очищенной сточной воды и активного ила.
Значения показателей нормального режима работы аэротенка (при подаче синтетической сточной воды состава, соответствующего таблице 2) приведены в таблице 3, в графе "Значения показателей контрольного аэротенка".
6.2.4. Проверку надежности работы аэротенков проводят в период их освоения и при обучении методике определения биоразлагаемости, определяя биоразлагаемость ПАВ известного состава по описанной методике. Полученные при этом показатели биоразлагаемости должны соответствовать данным, представленным в таблице 4.
Таблица 3 - Показатели работы аэротенков
|
Наименование показателясм |
||
|
контрольного аэротенка |
опытного аэротенка при нарушенном режиме работы, вызванном испытуемым ПАВ |
|
|
1 Иловый индекс, см3/г |
От 40 до 60 |
Свыше 100 |
|
2 Концентрация аммонийного азота (N) в очищенной воде, мг/дм3 |
" 0,4 " 0,6 |
Более 1,0 |
|
3 Концентрация азота нитратов (N) в очищенной воде, мг/дм3 |
" 0,7 " 10,0 |
Менее 3,0 |
|
4 Хлопок активного ила |
Компактный |
Измельчение (диспергирование) |
|
5 Наличие гидробионтов, например: |
Philodina roseola
|
Полное отсутствие указанных видов или наличие "плохих" форм: Paramaecium caudatum, |
Примечание - Режим работы опытного аэротенка, в который подается синтетическая сточная вода с ПАВ, считается нарушенным, если его работа отличается от режима контрольного аэротенка хотя бы по одному из приведенных в таблице показателей
6.3 Выполнение определения биоразлагаемости
Определение биоразлагаемости ПАВ включает два этапа:
- введение в состав синтетической сточной воды, подаваемой в опытный аэротенк, испытуемого ПАВ;
- периодический отбор проб очищенной сточной воды и активного ила из опытного и контрольного аэротенка с последующим их анализом.
6.3.1 Определение проводят при постоянной концентрации ПАВ, равной половине критической концентрации мицеллообразования, значение которой должно быть указано в нормативном документе на испытуемое вещество или определено предварительно любым способом, например, из изотермы поверхностного натяжения водных растворов поверхностно-активного вещества по ГОСТ 29232.
Примечание - Для подавляющего большинства ПАВ критическая концентрация мицеллообразования совпадает с токсикологическим показателем - эффективной концентрацией (ЕС100), при которой нарушается нормальное функционирование биоценоза активного ила. Поэтому определение показателей биоразлагаемости рекомендуется проводить при равных нагрузках по концентрации поверхностно-активного вещества обычно 0,5 ЕС100 (0,5 критической концентрации мицеллобразования). В этих условиях токсическое влияние поверхностно-активных веществ на биоценоз активного ила находится на подпороговом уровне.
Таблица 4 - Поверхностно-активные вещества, используемые для проверки надежности работы аэротенков, и показатели их биоразлагаемости
|
Наименование ПАВ |
Массовая концентрация ПАВ на входе аэротенка, Свх, мг/дм3 |
Продолжительность индукционного периода, сут |
Тип кинетической зависимости процесса биоразложения |
Период полуразложения поверхностно-активного вещества активным илом |
|
|
неадаптированным Тн1/2, ч |
адаптированным Тн1/2, ч |
||||
|
н-Алкил сульфаты натрия фракции С12 - С14 |
100 |
1,5±0.5 |
1 |
0,17±0,05 |
0,033±0,006 |
|
Алкилбензол-сульфонаты натрия на н-парафинах |
50 |
6,5±0,5 |
1 |
1,0±0,2 |
0,04±0,01 |
|
р-Изононилфенилполиоксиэтилен-гликолевые эфиры (неонол АФ9-10) |
30 |
6,5±0,5 |
1 |
12,8±2,2 |
0,07±0,02 |
Если же при концентрации, равной половине критической концентрации мицеллообразования, не достигается стационарный режим или обнаружится нарушение режимов работы аэротенка, то опыт прекращают, активный ил выливают, аэротенк заполняют новым неадаптированным активным илом, подготавливают его к работе в соответствии с 6.2 и повторно проводят определение показателей биоразлагаемости при концентрации испытуемого ПАВ меньше половины критической концентрации мицеллообразования. Об этом обязательно указывают в отчете.
6.3.2 Объекты анализа:
- очищенная сточная вода;
- суспензия активного ила.
6.3.3 Перечень анализируемых, показателей очищенной сточной воды, активного ила и состояния аэротенка приведен в таблице 5.
Отбор проб очищенной сточной воды и активного ила для анализов осуществляют через каждые (24±0,5) ч. Периодичность анализов приведена в таблице 5.
Расчет трех показателей биоразлагаемости ПАВ проводят по кинетическим зависимостям изменений остаточных концентраций ПАВ (ХПК) в очищенной сточной воде.
Таблица 5 - Форма таблицы, составленная по результатам анализов очищенной сточной воды и активного ила*
|
Продолжительность испытаний (включая подготовительный период), сут |
Показатели очищенной сточной воды в аэротенке |
Показатели активного ила в аэротенке |
Высота столба пены в опытном аэротенке, см |
Видовой состав активного ила (наличие индикаторных микроорганизмов) |
|||||||||||||
|
Массовая концентрация ПАВ в опытном аэротенке,** мг/дм3 |
ХПК, мг О2/дм3 |
Массовая концентрация азота, мг/дм3 |
Иловый индекс, см3/г |
Зольность, % |
Массовая концентрация, мг/дм3 |
||||||||||||
|
нитритного |
нитратного |
аммонийного |
|||||||||||||||
|
контрольном |
опытном |
контрольном |
опытном |
контрольном |
опытном |
контрольном |
опытном |
контрольном |
опытном |
контрольном |
опытном |
контрольном |
опытном |
||||
|
|
Ежедневно*** |
Ежедневно |
1 раз в 3-4 дня |
|
|
Ежедневно |
1 раз в 3-4 дня |
Ежедневно |
Ежедневно |
1 раз в 3-4 дня |
|||||||
*Методы анализа – см. приложение Е
**Массовую концентрацию ПАВ в синтетической сточной воде, подаваемой в аэротенк, указывают дополнительно для каждой серии опытов
***Периодичность отбора проб и анализа очищенной сточной воды
6.4. Обработка результатов определения биоразлагаемости
Результатами определения биоразлагаемости являются показатели:
- тип кинетической зависимости процесса биоразложения;
- продолжительность индукционного периода;
- период полуразложения поверхностно-активного вещества адаптированным (или неадаптированным) активным илом.
6.4.1 Определение типа кинетической зависимости
Строят графические зависимости Свых = f(t).
Типичные виды кинетических зависимостей Свых = f(t), характерных для процесса биоразложения, приведены на рисунке 1.
Тип I - характерен для большинства ПАВ, биоразложение которых протекает с активацией процесса (рисунок 1а).
Тип II - частный случай типа I с продолжительностью индукционного периода более 25 сут (рисунок 1 б).
Тип III - характерен для некоторых ПАВ, процесс биоразложения которых протекает с самоингибированием (рисунок 1 в).
6.4.2 Определение продолжительности индукционного периода
По окончании тридцатисуточного эксперимента проводят графическое или аналитическое (на ЭВМ) определение продолжительности индукционного периода (tинд).
6.4.2.1 Графическое определение
Определение значения tинд ПАВ с кинетическими зависимостями I и III типов сводится к нахождению той области (Свых, t), в которой зависимость Свых = f(t) выходит на плато (Б).
Примечание - В случае, если отсутствуют методики прямого химического определения остаточной концентрации поверхностно-активного вещества, продолжительности индукционного периода находят из зависимостей ХПК = f(t).
6.4.2.2. Достоверность результатов определения продолжительности индукционного периода
Достоверность определения продолжительности индукционного периода (tинд), установленная на одном ПАВ по внутрилабораторной сходимости результатов, составляет ±10%.
6.4.3 Определение периодов полуразложения
6.4.3.1 Периоды полуразложения адаптированным (Ta1/2) и неадаптированным (Тн1/2) активным илом рассчитывают по формулам:
- для адаптированного активного ила (стационарный режим, рис. 1 а, в - Б)
![]() , (1)
, (1)
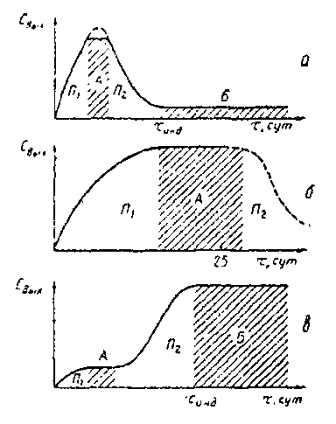
А - квазистационарный режим; Б - стационарный режим биоразложения ПАВ; П1 и П2 - переходные режимы; типы кинетических зависимостей: а - I, б - II, в - III.
Рисунок 1 - Концентрация пав на выходе (Свых) аэротенка в зависимости от характера течения процесса, вида ПАВ и продолжительности испытаний
- для неадаптированного активного ила (квазистационарный режим, рис. 1 б - А)
где Cвх, ![]() и
и ![]() - массовая
концентрация поверхностно-активного вещества на входе аэротенка и в очищенной
сточной воде в квазистационарном и стационарном режимах биоразложения, мг/дм3;
- массовая
концентрация поверхностно-активного вещества на входе аэротенка и в очищенной
сточной воде в квазистационарном и стационарном режимах биоразложения, мг/дм3;
V - объем аэротенка, дм3;
q - скорость потока, дм3/ч;
Примечание - В случае отсутствия специфических аналитических методик определения остаточной концентрации поверхностно-активного вещества в очищенной сточной воде биоразлагаемость оценивают из кинетики изменения ХПК очищенной сточной воды по формулам 3, 4):
- для адаптированного активного ила (стационарный режим, рис. 1 а, в - Б)
![]() , (3)
, (3)
- для неадаптированного активного ила (квазистационарный режим, рис. 1 б - А)
где ![]() . - химическое потребление кислорода синтетической
сточной воды на входе аэротенка и очищенной сточной воды; в квазистационарном и
стационарном режимах биоразложения, мг О2/дм3.
. - химическое потребление кислорода синтетической
сточной воды на входе аэротенка и очищенной сточной воды; в квазистационарном и
стационарном режимах биоразложения, мг О2/дм3.
6.4.3.2 Оценка достоверности определения периодов полуразложения
Достоверность определения периодов полуразложения определяется точностью определения концентрации ПАВ в очищенной сточной воде:
а) анионных - фотометрическим методом с метиленовым синим при массовой концентрации 0,1 мг/дм3; относительное стандартное отклонение ±19%;
б) неионогенных - фотометрическим методом с фосфорно-вольфрамовой кислотой при массовой концентрации (0,5-10,0) мг/дм3; относительное стандартное отклонение ±10 %.
В соответствии с указанным выше относительная ошибка при определении периодов полуразложения составляет:
- для анионных ПАВ ±24%;
- для неионогенных ПАВ ± 12 %.
Примечание - Оценка достоверности определения показателей биоразлагаемости по данным ХПК: стандартное отклонение при определении ХПК в интервале 50-140 мг/дм3 составляет ± 20 %. Соответственно ошибка при определении периодов полного биоразложения ПАВ (по ХПК) составляет ±30 %.
6.4.4 Определение продолжительности индукционного периода и периодов полуразложения с использованием ЭВМ
Алгоритм программы определения продолжительности индукционного периода и периодов полуразложения приведен в приложении В.
Программа написана на языке TURBOBASIC для персональных ЭВМ типа IBM PC/XT/AT.
6.5 Обработка результатов определения
На основе полученных согласно 6.3 результатов проводят отнесение ПАВ к классу биоразлагаемости в соответствии с классификацией, приведенной в таблице 6.
Таблица 6 - Классификация поверхностно-активных веществ по биоразлагаемости
|
Класс биоразлагаемости |
Лимитирующий показатель при отнесении к классу биоразлагаемости дли типов кинетической зависимости процесса биоразложения |
||
|
I |
II |
III |
|
|
Продолжительность индукционного периода tинд, сут |
Период полуразложения активным илом, ч |
||
|
неадаптированным |
адаптированным Та 1/2 |
||
|
1 Быстроразлагаемые |
Менее 3 |
Менее 0,22 |
|
|
2 Умеренноразлагаемые |
От 3 до 10 включ. |
От 0,22 до 1,05 включ. |
|
|
3 Медленноразлагаемые |
От 11 до 25 включ. |
" 1,06 " 4,33 " |
|
|
4 Чрезвычайно медленно разлагаемые |
Более 25 |
Более 4,33 |
|
Пример определения биоразлагаемости поверхностно-активных веществ приведен в приложении Д.
6.6 Определение ориентировочно-допустимых уровней содержания ПАВ в стоках, подаваемых в аэротенки (ОДУА) и водоемах (ОДУВ)
Концентрацию ПАВ, при которой аэротенк работает в течение не менее 20 сут после достижения адаптации устойчиво, без нарушений режимов, указанных в таблице 3, принимают в качестве ориентировочно допустимого уровня (ОДУА) при сбросе на биологические очистные сооружения.
Концентрацию ПАВ, при которой достигается предельная адсорбция на границе вода - воздух, принимают в качестве ориентировочно-допустимого уровня для воды водоемов (ОДУВ).
6.7 Составление заключения и выдача рекомендаций по способам переработки сточных вод
6.7.1 По результатам определения показателей биоразлагаемости составляют заключение по форме, приведенной в приложении Г.
6.7.2 Для предупреждения негативного влияния ПАВ, попадающих со сточными водами в водные системы, рекомендуется следующие методы очистки сточных вод (по классам) (таблица 7).
Таблица 7 - Рекомендуемые приемы очистки стоков
|
Приемы, рекомендуемые для очистки сточных вод, содержащих ПАВ |
Класс по биоразлагаемости |
|||
|
1* |
2 |
3 |
4** |
|
|
Биологические методы очистки |
+ |
+ |
+ |
- |
|
Локальные физико-химические методы очистки |
- |
- |
+ |
+ |
*В порядке исключения допускается сброс в водные объекты после соответствующего разбавления до ПДК
**Без локальной очистки стоков физико-химическими методами сбросы на биологические очистные сооружения не рекомендуются
ПРИЛОЖЕНИЕ А
(обязательное)
Модель аэротека-отстойника
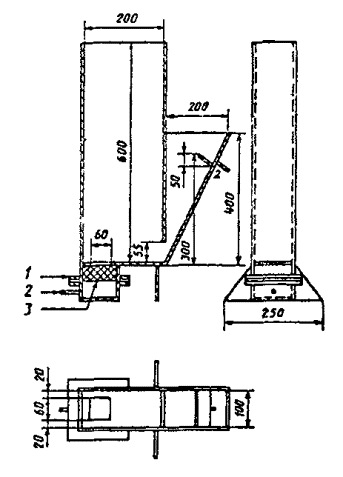
1 - фланцевое соединение 2 - штуцер; 3 - фильтросная пластина.
Рисунок А.1
ПРИЛОЖЕНИЕ Б
(обязательное)
Схема установки для определения биоразлагаемости поверхностно-активных веществ непрерывным методом
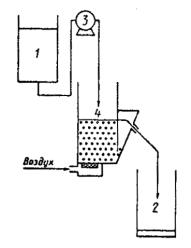
1-2 - емкости для загрязненной сточной воды; 3 - дозатор; 4 - аэротенк-отстойник
Рисунок Б.1
ПРИЛОЖЕНИЕ В
ПРОГРАММА РАСЧЕТА ПОКАЗАТЕЛЕЙ БИОРАЗЛАГАЕМОСТИ ПАВ
color 8,7
defdbl a-z
dim x(300), y(300)
dim z(200, 10), c(200, 10)
dim xx(300), уу(300)
open "PRN" for output as#l
open "SCRN:" for output as#2
n=362
co=50
m=14
data 1, 2, 3, 4, 5, 7, 8, 9, 10, 11, 12, 15, 16, 17
for i = I to m
read x(i)
next
data 4.1, 2.3, 3.6, 2.3, 2.1, 1.3, 1.1, 3.1, 1.1, 1.0, 0.8, 0.7, 0.7, 0.6
for i = 1 to m
read y(i)
next
‘***нахождение макс. и мин. значений х,у***
xmax=x(l)
xmin=x(l)
ymax=y(l)
ymin=y(l)
for i=l to m
if xmax<x(i) then xmax=x(i)
if xmin>x(i) then xmin=x(i)
if ymax<y(i) then ymax=y(i)
if ymin>y(i) then ymin=y(i),
next
screen 2
‘***построение осей координат***
line (40, 180)-(570,180), 3
line (40, 180)-(40, 20), 3
‘***построение сетки***
for i=l80 to 20 step-16
for j=40 to 570 step 10
pset(j,i)
next j,i
for i=40 to 570 step 53
for j=180 to20 step -4
pset (i.j)
next j,i
‘***преобразование значений х и у в графические координаты***
for i=1 to m
xg = (х(i)-xmin)*530/(xmax-xmin)+40
yg = 180-(у(i)-ymin)*160/(ymax-ymin)
pset (xg,yg), 3
line((xg-3).(yg-2))-((xg+3).(yg+2)).7.b
next
4444 a$=inkey$ if a$=” ” then 4444
screen 0
n2=m
n1=m-l
98 y8=0
for l=n1 to n2
y8=y8+y(l)
next l
y9=y8/(n2-n1+1)
y91=y9
ep=0.2*y9
for l=nl to n2
if abs(y9-y(l)) >ep then 187
next l
lf n1>1 then 198
‘на построение
goto 1189
198 n1=n1-1
goto 98
187 n4=n1-1
‘наклон участок
n3=n4-1
122 n5=n3
n6=n4
99 a1=a
b1=b
gosub 1000
Ta=(y91-a)/b
Ka=(co-y91)/y91/6
pr=(co-y91)/(co*100
for l=n3 to n4
y9=a+b*x(l)
ep=0.2*y9
if abs (y9-y(l))> ep then 88
next 1
a1=a
b1=b
n31=n3
if n3>1 then 118
‘построить угол
goto 1189
118 n3=n3-1
goto 99
88 a=a1
b=b1
n3=n31
y8=0
y7=y(1)
for l=1 to n3+1
y8=y8+y(l)
if y7<y(l) then
y7=y(l)
x7=x(l)
end if
next l
print y7, x7
555 a$=inkey$: if a=" " then 555
y9=y8/n3
ep=0.2*y9
for i=l to n3
if abs(y9-y(l))>ep then 186
next l
‘построение
1189 screen 0
x9=(y9-a)/b
n1=n3
n2=n4
goto 3333
186 y9=y7
x9=x7
goto 1189
‘***расчет ур и d***
3333 syу=0
for i =n1 to n2
yp=a+b*x(i)
syy=syy+(y(i)-ур)^2/ур^2
next
d=sqr(syy/(n2-n1))
sl=0
for i=n2+l to m
sl=sl+y(i)
next
f1=s1/(m-n2)
xmaxl=(fl-a)/b
screen 2
‘***построение осей координат***
line (40, 180)-(570, 180), 3
line (40, 180)-(40 ,20), 3
‘***построение сетки***
for i=180 to 20 step -16
for j=40 to 570 step 10
pset (j, i)
next j,i
for i=40 to 570 step 53
for j=180 to 20 step -4
pset (i, j)
next j, i
‘***преобразование значений х и у в графические координаты***
for i=l to m
xg=(x(i)-xmin)*530/(xmax-xmin)+40
yg=l80-(y(i)-ymin)*160/(ymax-ymin)
pset(xg, yg), 3
line ((xg-3), (yg-2))-((xg+3), (yg+2)),7,b
next
‘***построение расчетных прямых***
if nl=l then
for x=xmax1 to xmax step (xmax-xmin)/530
y=f1
xg=(x-xmin)*530/(xmax-xmin)+40
yg=180-(y-ymin)*160/(ymax-ymin)
pset(xg, yg)
next
else if n3=l then
for х=x9 to xmax1 step (xmax-xmin)/530
yp=a+b*x
xg=(x-xmin)*530/(xmax-xmin) +40
yg=180-(yp-ymin)*160/ (ymax-ymin)
pset (xg, yg)
next
for x=xmaxl to xmax step (xmax-xmin)/530
y=f1
xg=(x-xmin)*530/(xmax-xmin)+40
yg=180-(y-ymin)*160/(ymax-ymin)
pset (xg, yg)
next
else
for x=x9 to xmax1 step (xmax-xmin)/530
yp=a+b*x
xg=(x-xmin)*530/(xmax-xmin)+40
yg=180-(yp-ymin)*160/(ymax-ymin)
pset (xg, yg) : next
for x=xmax1 to xmax step (xmax-xmin)/530
y=f1
xg=(x-xmin)*530/(xmax-xmin)+40
yg=l80-(y-ymin)*160/(ymax-ymin)
pset (xg, yg)
next
for x=x(l) to x9 step (xmax-xmin)/530
yp=y9
xg=(x-xmin)*530/(xmax-xmin)+40
yg=180-(yp-ymin)*160/(ymax-ymin)
pset (xg, yg)
next
end if
2222 as=inkeys: if as=” “then 2222
for k=1 to 35
next
screen 0
print ”ВВЕДИТЕ ВЫБОР ВЫВОДА ДАННЫХ:”
print ”1 - ВЫВОД НА ПЕЧАТЬ”
print ”2 - ВЫВОД НА ЭКРАН”
input k
cls
print #k,” Tm”;” Km”;” Та”=” Ка”;” %”
for l=1 to n3
if abs(y9-y(l))<ep then Km=(co-y9)/y9/6
goto 1001
km=(со-у7)/у7/6
goto 1001
next
1001 print #k, using”####,##”; x9, Km, Та, Ка, pr, y9, x7
print #k, “КОЭФФИЦИЕНТЫ В ПОРЯДКЕ СЛЕДОВАНИЯ РАВНЫ:”
print #k, using “###.##”; a, b
print #k, “АППРОКСИМАЦИЯ ВИДА у=А+Вх”
print #k,” x”;” у”;” ур”
for i=nl to n2
yp=a+b*x(i)
print #k, using “###.##”; x(i), y(i), ур
next
print #k, using “###.##”; d
print #k, using “Y=###.## X=###.##”;f1, xmax1
stop
1000 rem print “***ПОДПРОГРАММА APR***”
sx=0
sxx=0
sy=
sxy=0
for i=n5 to n6
sx=sx+x(i)
sy=sy+y(i)
sxx=sxx+x(i)
sxy=sxy+x(i)*y(i)
next
а=(sx*sxy-sy*sxx)/(sx^2-(n6-n5+1) sхх)
b=(sx*sy-(n6-n5+1)*sxy)/(sx^2-(n6-n5+1)*sxx)
return
123 print ”неверно заданы нач. или кон.”
stop
goto 122
ПРИЛОЖЕНИЕ Г
(обязательное)
ФОРМА ЗАКЛЮЧЕНИЯ ПО РЕЗУЛЬТАТАМ ОПРЕДЕЛЕНИЯ ПОКАЗАТЕЛЕЙ БИОРАЗЛАГАЕМОСТИ ПАВ В ВОДНОЙ СРЕДЕ
а) Химическое и товарное наименование.
б) Нормативный документ.
в) Химический состав препарата и сведения о его компонентах или примесях (токсичность, биоразлагаемость, санитарно-гигиенические нормативы).
г) Физико-химические свойства.
Коллоидно-химические характеристики (концентрация достижения предельной адсорбции на границе вода - воздух, критическая концентрация мицеллообразования).
д) Результаты экспериментальных исследований биоразлагаемости ПАВ в аэротенках (форма - таблица 5) с определением кинетических характеристик процесса биоразложения:
- тип кинетической зависимости;
- продолжительность индукционного периода;
- периоды полураэложения ПАВ адаптированным и (или) неадаптированным активным илом;
- ориентировочно-допустимый уровень содержания ПАВ в сточных водах, подаваемых на аэротенк (ОДУА), и в водоемах (ОДУВ).
е) Класса биоразлагаемости.
ж) Общие выводы.
з) Ответственный исполнитель организации, проводивший исследования биоразлагаемости ПАВ. Подпись, печать, дата.
ПРИЛОЖЕНИЕ Д
(рекомендуемое)
ПРИМЕРЫ ОПРЕДЕЛЕНИЯ БИОРАЗЛАГАЕМОСТИ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ
1 ПАВ с кинетическими зависимостями типа 1 (алкилбензолсульфонат натрия)
В соответствии с 6.2 подготавливают к работе два аэротенка - контрольный и опытный.
Устанавливают концентрацию н-алкилбензолсульфоната в синтетической сточной воде на входе аэротенка: Свх = 0,5 ККМ = 50 мг/дм3.
Проводят определение показателей очищенной сточной воды. Результаты сводят в таблицу по форме таблицы 5.
Строят графическую зависимость Свых = f(t). Результаты приведены на рисунке Д.1. По кинетической зависимости процесса биоразложения указанное вещество относится к типу 1. Из рисунка Д.1 определяют продолжительность индукционного периода: tинд = (6,5 ± 0.5) сут.
В соответствии с 6.4.3 определяют периоды полуразложения вещества в часах:
- неадаптированным активным илом по формуле (2)
![]() ;
;
- адаптированным активным илом по формуле (1)
![]() .
.
Отнесение н-алкилбензолсульфоната натрия к классу по биоразлагаемости проводят в соответствии с таблицей 6.
Поскольку указанное вещество относится по кинетике процесса биоразложения к типу I, лимитирующий показатель - продолжительность индукционного периода. Её значение (6,5 ± 0,5) сут, т.е. указанное вещество следует отнести ко 2-му классу - "умеренно разлагаемые" вещества.
2 ПАВ с кинетическими зависимостями типа II
В соответствии с классификацией к данному типу относятся ПАВ, у которых продолжительность индукционного периода превышает 25 сут. Например, оксиэтилированные на 40 молей окиси этилена р-изононилфенолы (неонолы АФ9-40) имеют следующие показатели: tинд = (31,5 ± 0,5) сут, Тн1/2 =(19 ± 3) ч, а Та1/2 =(0,22 ± 0,55) ч. Указанный продукт по значению tинд относится к 4 классу, по значению Та1/2 - ко 2-му классу, по значению Тн1/2 - к 4-му классу. Окончательно указанное пав относится к 4-му классу биоразлагаемости.
3 ПАВ с кинетическими зависимостями типа III
В соответствии с классификацией к данному типу относятся ПАВ, у которых процесс биоразложения самоингибируется. Например, цианметилированные оксиэтилированные на 10 молей окиси этилена р-изононилфенолы (неонол АФ9-9Ц) имеют следующие показатели: tинд = (13 ± 1) сут, Тн1/2 =(0,46 ± 0,10) ч, а Та1/2 =(10 ± 3) ч. Указанный продукт по значению tинд относится к 3-му классу, по значению Тн1/2 - к 4-му классу, по значению Та1/2 - ко 2-му классу. Окончательно указанное ПАВ относят к 4-му классу биоразлагаемости.
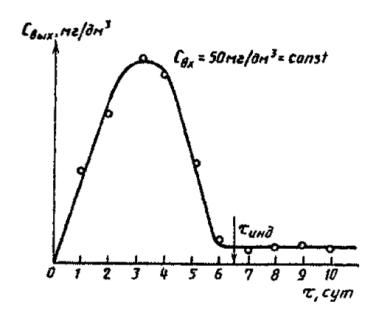
Рисунок Д.1 - Концентрация алкилбензолсульфоната на основе н-парафинов в очищенной сточной воде в зависимости от продолжительности испытаний
ПРИЛОЖЕНИЕ Е
(рекомендуемое)
Методы анализа, используемые при определении показателей биоразлагаемости ПАВ
1 ОБЩИЕ ТРЕБОВАНИЯ К МЕТОДАМ АНАЛИЗА
1.1 Общие указания по проведению анализа - по ГОСТ 27025.
1.2 Допускается применение других средств измерения с метрологическими характеристиками и оборудования с техническими характеристиками не хуже, а реактивов по качеству не ниже указанных и настоящем стандарте.
1.3 Допускается применение других методов анализа, точность которых не ниже указанной в настоящем стандарте.
2 КОЛОРИМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ АНИОНАКТИВНЫХ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ (АПАВ)
Метод основан на образовании ассоциатов анионактивных ПАВ с красителем метиленовым синим, растворимых в хлороформе и практически нерастворимых воде. Экстракцию комплексного соединения хлороформом проводят сначала щелочной среде, а затем в кислой, что позволяет устранять мешающее влияние ионов минеральных солей (хлоридов, нитратов и др.).
Определению мешают сульфиды, их влияние устраняют добавлением пероксида водорода.
2.1 Средства измерений, вспомогательные устройства и реактивы
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г.
Фотоэлектроколориметр.
Воронки ПД-1-250 ХС по ГОСТ 25336.
Воронка В-36-80 ХС по ГОСТ 25336.
Колбы 2-50-2, 2-100-2 и 2-1000-2 по ГОСТ 1770.
Пипетки вместимостью 2, 5, 10 и 50 см3.
Вода дистиллированная по ГОСТ 6709.
Кислота серная по ГОСТ 4204.
Метиленовый синий.
Натрий фосфорно-кислый двузамещенный по ГОСТ 11733.
Натрия гидроокись по ГОСТ 4329.
Хлороформ по ГОСТ 20015.
2.2 Подготовка к анализу
2.2.1 Приготовление образцов сравнения анионактивного ПАВ
Образцы сравнения готовят из стандартного образца АПАВ массовой концентрации 0,1 кг/см3 АПАВ.
2.2.2 Приготовление фосфатного буферного раствора
10,0 г двузамещенного фосфорно-кислого натрия помещают мерную колбу, растворяют в дистиллированной воде, добавляют раствор гидроокиси натрия до рН = 10 и разбавляют водой до объема 1 дм3.
2.2.3 Приготовление нейтрального раствора метиленового синего
0?35 г метиленового синего помещают мерную колбу, растворяют в воде и доводят объем до 1 дм3.
2.2.4 Приготовление кислого раствора метиленового синего
0,35 г метиленового синего помещают в мерную колбу, растворяют в 500 см3 воды, добавляют 6,5 см3 концентрированной серной кислоты и доводят объем до 1 дм3 водой.
2.3 Построение градуировочного графика
Готовят растворы сравнения. Для этого в делительные воронки помещают по 1, 2, 3, 4 или 5 см3 раствора сравнения, содержащего 0,1 мг/см3 АПАВ, разбавляют дистиллированной водой до 100 см3, приливают 10 см3 фосфатного буферного раствора, 5 см3 нейтрального раствора метиленового синего, 15 см3 хлороформа. Осторожно встряхивают в течение 1 мин и после отстаивания хлороформный слой сливают в другую делительную воронку, в которую налито 110 см3 дистиллированной воды и 5 см3 кислого раствора метиленового синего. Взбалтывают осторожно в течение 1 мин, дают отстояться и сливают слой хлороформа в мерную колбу вместимостью 50 см3 через небольшую воронку с вложенным в нее тампоном ваты, предварительно смоченным хлороформом.
Экстрагирование проводят три раза, дважды наливая в первую делительную воронку по 15 см3 хлороформа и один раз 10 см3 и повторяя описанные операции. Собранные в мерной колбе вместимостью 50 см3 экстракты разбавляют хлороформом, доводя объем до метки.
Оптическую плотность растворов сравнения измеряют на фотоэлектроколориметре по отношению к контрольному раствору при длине волны 650 нм (красный светофильтр).
По полученным данным строят градуировочный график, откладывая на оси абсцисс введенные в дистиллированную воду массы АПАВ в миллиграммах, а на оси ординат - соответствующие им значения оптических плотностей.
2.4 Проведение анализа
Объем воды, отбираемой для анализа, при концентрации АПАВ до 5 мг/дм3 составляет от 50 до 20 см3, до 10 мг/дм3 - 10 см3, до 30 мг/дм - 5 см3, до 70 мг/дм3 - 2 см3.
Аликвоту анализируемой воды помещают в делительную воронку, разбавляют дистиллированной водой до 100 см и далее анализ проводят, как указано в 2.3 данного приложения.
По полученному значению оптической плотности, пользуясь градуировочным графиком, находят массу АПАВ в анализируемой воде миллиграммах.
2.5 Обработка результатов
Массовую концентрацию анионных ПАВ в воде X1 миллиграммах на кубический дециметр рассчитывают по формуле
![]() , (Е.1)
, (Е.1)
где m - найденная по градуировочному графику масса АПАВ, мг, V - объем анализируемой пробы, см3
3 КОЛОРИМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ НЕИОНОГЕННЫХ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ (НПАВ)
Определение основано на осаждении НПАВ в виде комплексного соединения с фосфорновольфрамовой кислотой и хлористым барием, которое при растворении в концентрированной серной кислоте даст с гидрохиноном красно-коричневую окраску.
Определению мешают сульфаты при массовой концентрации их более 200 мг/дм3, влияние которых устраняют путем разбавление пробы, а также белки, которые удаляют с помощью гидроокиси цинка.
3.1 Средства измерений, вспомогательные устройства, реактивы и растворы
Фотоэлектроколориметр.
Центрифуга.
Баня водяная.
Колба 2-100-2 и 2-1000-2 по ГОСТ 1770.
Пипетки вместимостью 1, 2, 5 и 10 см3.
Пробирка ПЗ-25 ХС по ГОСТ 25336.
Барий хлористый 2-водный по ГОСТ 4108, раствор с массовой долей 10%.
Вода дистиллированная по ГОСТ 6709.
Гидрохинон по ГОСТ 19627, раствор в серной кислоте с массовой долей 5%.
Кислота серная по ГОСТ 4204.
Кислота соляная по ГОСТ 3118 разбавленная 1:1.
Фосфорно-12-вольфрамовая (7) кислота водная (фосфорно-вольфрамовая кислота) по ТУ 6-09-01-744-88, раствор с массовой долей 2%.
3.2 Подготовка к анализу
Готовят стандартный раствор неионогенного ПАВ массовой концентрации 0,1 кг/см3 НПАВ.
3.3 Построение градуировочного графика
Готовят растворы сравнения. Для этого в мерные колбы вместимостью 100 см3 помещают по 0, 1, 2, 3, 4 и 5 см3 раствора сравнения, содержащего 0,1 мг/см3 НПАВ, и доводят объем до метки дистиллированной водой, получая растворы сравнения НПАВ с массовой концентрацией 0, 1, 2, 3, 4 и 5 мг/дм3. Затем по 10 см3 полученных растворов пипеткой помещают в пробирки, добавляют 2 капли раствора соляной кислоты, 1 см3 раствора хлористого бария и 1 см3 раствора фосфорновольфрамовой кислоты и перемешивают тонкой стеклянной палочкой, пользуясь ей и дальше в ходе анализа.
Далее пробирки помещают в кипящую водяную баню, выдерживают в течение 15 минут. Затем пробирки вынимают, центрифугируют 5 мин со скоростью 2500 об/мин и сливают раствор, находящийся над осадком (очень осторожно, лучше отсосать через тонкий капилляр с помощью вакуум-насоса). Оставшийся осадок дважды промывают, наливая в пробирку по 5 см3 горячей дистиллированной воды, и дважды центрифугируют. Подсушенный в сушильном шкафу при 105°С осадок растворяют в 3 см3 концентрированной серной кислоты. После растворения осадка добавляют 1 см3 раствора гидрохинона, перемешивают тщательно палочкой и добавляют еще 6 см3 концентрированной серной кислоты.
Оптическую плотность растворов сравнения измеряют на фотоэлектроколориметре по отношению к контрольному раствору при длине волны 500 нм (зеленый светофильтр).
По полученным данным строят градуировочный график, используя на оси абсцисс введенные в дистиллированную воду массы НПАВ в миллиграммах, а на оси ординат - соответствующие им значения оптических плотностей.
3.4 Проведение анализа
В пробирку помещают 10 см3 анализируемой пробы воды исходной или разбавленной так, чтобы массовая концентрация НПАП в пробе была в пределах 2-6 мг/дм3, и далее анализ проводят, как указано в 3.3 данного приложения.
По полученному значению оптической плотности, пользуясь градуировочным графиком, находят массу НПАВ анализируемой воде в миллиграммах.
3.5 Обработка результатов
Массовую концентрацию НПАВ воде X2 в миллиграммах на кубический дециметр рассчитывает по формуле:
![]() , (Е.2)
, (Е.2)
где m- найденная по градуировочному графику масса НПАВ, мг; V - объем анализируемой пробы, см3.
4 ХИМИЧЕСКОЕ ПОТРЕБЛЕНИЕ КИСЛОРОДА (ХПК)
Метод основан на практически полном окислении органических веществ, содержащихся в воде, двухромово-кислым калием в кислой среде до двуокиси углерода и воды. Избыток двухромово-кислого калия оттитровывают раствором соли Мора в присутствии индикатора (фенилантраниловой кислоты или ферроина) и катализатора (серно-кислое серебро).
4.1 Средства измерений, вспомогательные устройства, реактивы и растворы
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г.
Бюретка вместимостью 25 см3 с ценой деления 0,1 см3.
Колба 2-100-2 по ГОСТ 1770.
Колба П-1-250-29/32 ТС по ГОСТ 25336.
Пипетка вместимостью 20 см3.
Стаканчик для взвешивания типа СВ по ГОСТ 25336.
Вода дистиллированная по ГОСТ 6709.
Железо (II) серно-кислое 7-водное по ГОСТ 4148
Калий двухромово-кислый по ГОСТ 4220, раствор молярной концентрации c(1/6K2Cr2O7) = 0,1 моль/дм3, готовят по ГОСТ 25794.2.
Кислота серная по ГОСТ 4204, х.ч.
Серебро серно-кислое.
Соль закиси железа и аммония двойная серно-кислая (соль Мора) по ГОСТ 4208, раствор молярной концентрации c(NH4)2SO4FeSO4×6 Н2О) = 0,05 моль/дм3, готовят по ГОСТ 25794.2.
1,10-Фенантролин, ч.
Раствор ферроина; готовят следующим образом: 1,415 г 1,10-фенантролина и 0,695 г 7-водного серо-кислого железа (II) помещают в мерную колбу вместимостью 100 см3, растворяют в воде, разбавляют водой до метки и перемешивают.
4.2 Проведение анализа
20 см3 сточной воды или другой анализируемой жидкости * помещают в колбу, добавляют 10 см3 раствора двухромово-кислого калия и малыми порциями приливают 30 см3 концентрированной серной кислоты. Затем добавляют 200 мг серно-кислого серебра, содержимое тщательно перемешивают и после присоединения обратного холодильника, смесь равномерно кипятят течение 2 ч. Затем колбу охлаждают, обмывая стенки холодильника 50 см3 дистиллированной воды, добавляют 2-3 капли раствора ферроина и титруют избыток двухромово-кислого калия раствором соли Мора.
Одновременно проводят контрольный опыт с 20 см3 дистиллированной воды.
*Объем пробы для анализа подбирают таким образом, чтобы на ее окисление расходовалось не более 8 см3 титрованного раствора двухромово-кислого калия. При этом надо соблюдать условие, при котором сумма объемов анализов анализируемой жидкости и двухромово-кислого калия относилось бы к объему серной кислоты как 1:1
4.3 Обработка результатов
Химическое потребление кислорода ХПК в миллиграммах кислорода на кубический дециметр анализируемой воды (мг О2/дм3) вычисляют по формуле
![]() , (Е.3)
, (Е.3)
где V1 - объем раствора соли Мора, израсходованный на титрование контрольного раствора, см3; V2 - объем раствора соли Мора, израсходованный на титрование анализируемой пробы, см3; N - молярная концентрация применяемого раствора соли Мора, моль/дм3; К - поправочный коэффициент раствора соли Мора; 8 - грамм-эквивалент кислорода, мг; V0 - объем анализируемой воды, взятой для анализа, см3.
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, относительное расхождение между которыми не превышает допускаемое расхождение, равное 10 % при доверительной вероятности Р = 0,95.
5 ОПРЕДЕЛЕНИЕ АЗОТА НИТРИТОВ
Метод определения азота нитритов основан на образовании диазосоединений при реакции нитритов с сульфаниловой кислотой. Полученное диазосоединение реагирует с 1-нафтиламином, образуя окрашенное в ярко-красный цвет азосоединение. Интенсивность окраски пропорциональна концентрации нитритов.
Чувствительность метода - 0,005 мг/дм3.
5.1 Средства измерений, вспомогательные устройства, реактивы и растворы
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г.
Фотоэлектроколориметр.
Баня водяная.
Термостат лабораторный.
Колбы мерные по ГОСТ 1770 вместимостью 100 и 1000 см3.
Пипетки вместимостью 1, 2, 5 и 10 см3.
Кислота уксусная по ГОСТ 61, концентрированная и раствор концентрации 4 моль/дм3.
Натрий азотисто-кислый по ГОСТ 4197, х. ч.
1-Нафтиламин по ТУ 6-09-07-1703.
Кислота сульфаниловая по ГОСТ 5821.
5.2 Подготовка к анализу
5.2.1 Приготовление раствора сульфаниловой кислоты
8,000 г сульфаниловой кислоты при нагревании на водяной бане растворяют в 300 см3 дистиллированной воды, раствор перемешивают, охлаждают и добавляют 290 см3 концентрированной уксусной кислоты. Объем полученного раствора доводят до 1 дм3 дистиллированной водой.
5.2.2 Приготовление раствора 1-нафтиламина
5,000 г 1-нафтиламина растворяют в 1 дм3 уксусной кислоты концентрации 5 моль/дм3, затем раствор фильтруют через фильтр, хорошо промытый горячей дистиллированной водой, и хранят в склянке из темного стекла.
Для приготовления раствора уксусной кислоты концентрации 5 моль/дм 290 см3 концентрированной уксусной кислоты разбавляют до объема 1 дм3 дистиллированной водой.
5.2.3 Приготовление реактива Грисса
Смешивают равные объемы раствора сульфаниловой кислоты и раствора 1-нафтиламина в склянке из темного стекла с пришлифованной стеклянной пробкой. Реактив готовят в день определения.
5.2.4 Приготовление раствора, содержащего нитритный азот
0,492 г азотисто-кислого натрия переносят колбу, растворяют в дистиллированной воде и доводят до метки водой в мерной колбе вместимостью 1 дм3 (раствор А).
10 см3 раствора А помещают в мерную колбу вместимостью 1 дм3 и доводят объем до метки водой. 1 см3 раствора содержит 0,001 мг нитритного азота (раствор Б).
5.3 Построение градуировочного графика
Готовят серию растворов сравнения, помещая в мерные колбы вместимостью 100 см3 по 0; 0,5; 1,0; 2,0; 3,0. 4.0; 5,0 и 6,0 см3 раствора Б. Прибавляют по 2 см3 реактива Грисса, доводят объем раствора до метки дистиллированной водой, перемешивают и выдерживают 20 мин при 30°С в термостате, после чего измеряют оптическую плотность по отношению к контрольному раствору на фотоэлектроколориметре в кюветах с толщиной поглощающего свет слоя 50 мм при длине волны 520-550 нм (зеленый светофильтр).
По полученным данным строят градуировочный график, откладывая на оси абсцисс введенные массы азота нитритов в миллиграммах, а на оси ординат - соответствующие им значения оптических плотностей.
5.4 Проведение анализа
В мерную колбу вместимостью 100 см3 вносят навеску анализируемой воды, содержащую не более 0,005 мг азота нитритов. В колбу прибавляют 2 см3 реактива Грисса, доводят объем раствора до метки дистиллированной водой и далее анализ проводят, как описано в 5.3 данного приложения.
По полученному значению оптической плотности, пользуясь градуировочным графиком, находят массу нитритного азота в анализируемой воде миллиграммах.
5.5 Обработка результатов
Массовую концентрацию нитритного азота Х3 в миллиграммах на кубический дециметр рассчитывают по формуле
![]() , (Е.4)
, (Е.4)
где т - масса нитриного азота, найденная по градуировочному графику, мг, V - объем анализируемой воды, см3.
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, относительное расхождение между которыми не превышает допускаемое расхождение, равное 5 % при доверительной вероятности Р = 0,95.
6 ОПРЕДЕЛЕНИЕ НИТРАТНОГО АЗОТА
Колориметрическое определение нитратного азота основано на реакции нитратов с 1, 2, 4-фенолдисульфокислотой в результате которой образуются окрашенные желтый цвет нитропроизводные. Этим способом можно определять от 0,01 до 4 мг нитратного азота в 1 дм3 воды.
6.1 Средства измерений, вспомогательные устройства, реактивы и растворы
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г.
Фотоэлектроколориметр.
Баня водяная.
Колба Кн-1-250-29/32ТС по ГОСТ 25336.
Колбы 2-100-2 и 2-1000-2 по ГОСТ 1770.
Пипетки градуированные вместимостью 1, 2, 5 и 10 см3.
Цилиндр 1-50 по ГОСТ 1770.
Чашка выпарительная по ГОСТ 9147.
Холодильник воздушный длиной 1100 мм и диаметром 8-10 мм.
Аммиак водный по ГОСТ 3760, раствор молярной концентрации 4 моль/дм3.
Вода дистиллированная по ГОСТ 6709.
Калий азотно-кислый по ГОСТ 4217.
Кислого серная по ГОСТ 4204, х. ч.
Фенол по ГОСТ 23519.
Хлороформ по ГОСТ 20015.
6.2 Подготовка к анализу
6.2.1 Приготовление раствора, содержащего азотно-кислый калий
0,721 г азотно-кислого калия, высушенного при 105°С, переносят в мерную колбу вместимостью 1 дм3, растворяют в дистиллированной воде, добавляют 1 см3 хлороформа и доводят объем раствора водой до метки. 1 см3 этого раствора содержит 0,01 нитратного азота (раствор А).
10 см раствора А разбавляют в мерной колбе вместимостью 100 см3 водой до метки и перемешивают (раствор Б). Раствор Б применяют свежеприготовленным. 1 см3 раствора Б содержит 0,01 мг нитратного азота.
6.2.2 Приготовление сульфофенолового реактива
3 г фенола смешивают с 20,1 см3 серной кислоты и нагревают 6 ч на кипящей водяной бане в колбе с пробкой, в которую вставлен воздушный холодильник.
6.3. Построение градуировочного графика
Готовят серию растворов сравнения, помещая пипетками в выпарительные чашки по 0; 0,5; 1.0; 2,0, 5,0 и 10,0 см3 раствора Б и добавляют дистиллированную воду до 10 см3. Анализируемые растворы в чашках досуха выпаривают на водяной бане, охлаждают и прибавляют по 2 см3 сульфофенолового реактива, быстро смачивая при этом весь сухой остаток, дают постоять 10 мин, приливают 15 см3 воды и перемешивают до растворения. Затем количественно переносят в мерные колбы вместимостью 300 см3, добавляют 10 см3 раствора аммиака, доводят объем раствора до метки и тщательно перемешивают.
Оптическую плотность растворов сравнения измеряют по отношению к контрольному раствору на фотоэлектроколориметре при длине волны 410 нм (фиолетовый светофильтр) в кювете с толщиной поглощающего свет слоя 50 мм.
По полученным данным строят градуировочный график, откладывая на оси абсцисс введенные массы нитратного азота в миллиграммах, а на оси ординат - соответствующие значения оптических плотностей.
6.4 Проведение анализа
10 см3 анализируемой воды помещают выпарительную чашку и досуха выпаривают водяной бане. После охлаждения сухой остаток смачивают 2 см3 сульфофенолового раствора, дают постоять 10 мин, приливают 15 cм3 воды и перемешивают до растворения. Затем количественно переносят в мерную колбу вместимостью 100 см3, добавляют 10 см3 раствора аммиака и далее анализ проводят, как описано в 6.3 данного приложения.
По полученному значению оптической плотности, пользуясь градуировочным графиком, находят массу нитратного азота в анализируемой воде в миллиграммах.
6.5 Обработка результатов
Массовую концентрацию нитратного азота X4 в миллиграммах на кубический дециметр рассчитывают по формуле
![]() , (Е.5)
, (Е.5)
где m - масса нитратного азота, найденная по градуировочному графику, мг; V - объем анализируемой воды, см3.
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, относительное расхождение между которыми не превышает допускаемое расхождение, равное 10 % при доверительной вероятности Р = 0,95.
7 ОПРЕДЕЛЕНИЕ АММОНИЙНОГО АЗОТА
Метод определение аммонийного азота основан на образовании окрашенного соединения - йодистого меркураммония - при взаимодействии иона NH4 с реактивом: Несслера.
Чувствительность метола - 0,005 мг/дм3.
Определению аммонийного азота с реактивом Несслера мешают соединения с несколькими амидными группами, алифатические и ароматические амины, спирты, альдегиды, ацетон, органические хлорамины и другие органические соединения, реагирующие с реактивом Несслера. В их присутствии аммонийный азот отгоняют из анализируемой воды и определяют его в полученном дистилляте.
Определению мешают соли жесткости, железо, сульфиды, свободный хлор, мутность воды.
7.1 Средства измерений, вспомогательные устройства, реактивы и растворы
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г.
Фотоэлектроколориметр
Колба Кн 1 - 100 -29/32 по ГОСТ 25336.
Колба 2-1000-2 по ГОСТ 1770
Пипетки вместимостью 1, 2 и 50 см3.
Аммоний хлористый по ГОСТ 3773, х. ч.
Вода дистиллированная по ГОСТ 6709.
Калий-натрий винно-кислый 4-водный (Сегнетова соль) по ГОСТ 5845.
Натрий углекислый 10-водный по ГОСТ 84, х.ч.
Реактив Несслера, готовят по ГОСТ 4517.
7.2 Подготовка к анализу
7.2.1 Приготовление безаммиачной дистиллированной воды
К 2 дм3 дистиллированной воды прибавляют 10-годный углекислый натрий до слабощелочной реакции и упаривают раствор на 1/4 объема. Воду хранят в бутыли с нижним тубусом. В пробку бутыли вставляют хлоркальциевую трубку.
7.2.2 Приготовление раствора сегнетовой соли
50 г сегнетовой соли растворяют в 100 см3 безаммиачной дистиллированной воды. Раствор хранят в склянке из темного стекла в темном месте.
7.2.3 Приготовление раствора, содержащего аммонийный азот
0,383 г перекристаллизованного и высушенного при 100-105°С хлористого аммония помещают в мерную колбу вместимостью 1 дм3, растворяют в безаммиачной дистиллированной воде и доводят объем раствора этой же водой до метки (раствор А).
1 см раствора А содержит 0,1 мг аммонийного азота.
7.3 Построение градуировочного графика
Готовят серию растворов сравнения, помещая пипетками в мерные колбы вместимостью 100 см3 по 0; 0,5; 1,0; 2,0; 2.5, и 3,0 см раствора А. доводят объемы раствора безаммиачной дистиллированной водой до метки и тщательно перемешивают. По 50 см3 полученных растворов сравнения помещают пипеткой в конические колбы вместимостью 100 см3, добавляют 2 см3 раствора ceгнетовой соли и 1 см3 реактива Несслера, перемешивают и точно через 10 мин измеряют оптическую плотность растворов сравнения по отношению к контрольному раствору на фотоэлектроколориметре при длине волны 425 нм (синий светофильтр) в кювете с толщиной поглощающего свет слоя 50 мм.
По полученным значениям оптических плотностей строят градуировочный график, откладывая на оси абсцисс введенные массы аммонийного азота в миллиграммах, а на оси ординат - соответствующие им значения оптических плотностей.
7.4 Проведение анализа
В коническую колбу вместимостью 100 см3 отбирают пипеткой 50 см3 профильтрованной анализируемой воды, содержащей 0.02-0,08 мг аммонийного азота (при большем содержании азота пробу предварительно разбавляют). К пробе добавляют 2 см3 раствора сегнетовой соли и 1 см3 реактива Несслера и далее анализ проводят, как описано в 7.3 данного приложения.
По полученному значению оптической плотности, пользуясь градуировочным графиком, находят массу аммонийного азота в анализируемой воде в миллиграммах.
7.5 Обработка результатов
Массовую концентрацию аммонийного азота X5 в миллиграммах на кубический дециметр рассчитывают по формуле
![]() , (Е.6)
, (Е.6)
где m - масса аммонийного азота, найденная по градуировочному графику, мг; V - объем анализируемой воды, см3.
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, относительное расхождение между которыми не превышает допускаемое расхождение, равное 5 % при доверительной вероятности Р = 0,95.
8 ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИ АКТИВНОГО ИЛА
Определенное количество иловой смеси из аэротенка фильтруют через предварительно высушенный и взвешенный фильтр, затем высушивают при 105°С. Концентрацию ила определяют гравиметрическим методом.
8.1 Средства измерений, вспомогательные устройства и материалы
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г.
Шкаф сушильный лабораторный.
Воронка В-56-80 ХС по ГОСТ 25336.
Стаканчик СВ-14/8 по ГОСТ 25336.
Цилиндр 1-100-2 по ГОСТ 1770.
Эксикатор по ГОСТ 25336.
Фильтр обеззоленный "белая лента".
8.2 Подготовка к анализу
Обеззоленный фильтр "белая лента" помещают в стаканчик и сушат сушильном шкафу при 105°С до постоянной массы.
8.3 Проведение анализа
Активный ил в аэротенке хорошо перемешивают и отбирают в цилиндр иловую смесь, которую затем фильтруют через обеззоленный фильтр, предварительно доведенный до постоянной массы и вложенный в воронку. Остатки ила со стенок цилиндра смывают дистиллированной водой. Воронку с фильтром подсушивают в сушильном шкафу.
Подсушенный фильтр осторожно складывают и помещают в стаканчик (не закрывая его крышкой), в котором доводился до постоянной массы пустой фильтр, а затем в сушильном шкафу высушивают в течение часа. Стаканчик закрывают крышкой, охлаждают в эксикаторе и взвешивают. Эти операции повторяют до получения постоянной массы, причем продолжительность просушиваний сокращают до 30 мин.
Результаты всех взвешиваний в граммах записывают с точностью до третьего десятичного знака.
Сухой остаток сохраняют для определения зольности по 9.2. данного приложения.
8.4 Обработка результатов
Массовую концентрацию активного ила X6 в граммах на кубический дециметр вычисляют по формуле
![]() , (Е.7)
, (Е.7)
где m1 - масса высушенного фильтра с активным илом, г; т2. - масса высушенного фильтра без активного ила, г; V - объем профильтрованной иловой смеси, см3.
9 ОПРЕДЕЛЕНИЕ ЗОЛЬНОСТИ АКТИВНОГО ИЛА
Зольность активного ила определяют гравиметрическим методом после прокаливания сухого осадка, полученного при определении концентрации активного ила.
9.1 Средства измерений и вспомогательные устройства
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200г.
Печь муфельная.
Тигель фарфоровый по ГОСТ 9147.
Эксикатор по ГОСТ 25336.
9.2 Проведение анализа
Взвешенный обеззоленный фильтр с высушенным активным илом, полученным по 8.3 данного приложения, помещают в предварительно прокаленный при температуре 600°С и доведенный до постоянной массы фарфоровый тигель и осторожно поджигают спичкой. Затем фарфоровый тигель с озоленным фильтром 60 мин прокаливают в муфельной печи при температуре 600°С. Тигель охлаждают, выдерживают в эксикаторе 30 мин и взвешивают. Прокаливание и взвешивание повторяют до получения постоянной массы, причем продолжительность повторных прокаливаний сокращают до 30 мин. Результаты всех взвешиваний в граммах записывают с точностью до четвертого десятичного знака.
9.3 Обработка результатов
Зольность сухого вещества активного ила X в процентах рассчитывают по формуле
![]() , (Е.8)
, (Е.8)
где m1 - масса тигля с остатком после прокаливания, г; m2 - масса пустого тигля, г; m0 - масса остатка после высушивания, полученная по 8.3 данного приложения, г.
10 ОПРЕДЕЛЕНИЕ ИЛОВОГО ИНДЕКСА
Иловый индекс равен объему, занимаемому 1 г сухого вещества активного ила через 30 мин отстаивания в цилиндре.
10.1 Средство измерений
Цилиндр 1-100-2 по ГОСТ 1770.
10.2 Проведение анализа
Пробу иловой смеси взбалтывают, наливают 100 см цилиндр и отстаивают течение 30 мин, затем измеряют объем, занимаемый активным илом.
10.3 Обработка результатов
Иловый индекс Ии в кубических сантиметрах на грамм рассчитывают по формуле
![]() , (Е.9)
, (Е.9)
где V - объем активного ила в цилиндре после 30-минутного отстаивания, см3; X - массовая концентрация активного ила, определенная по 8.4 данного приложения, г/см3.
11 ГИДРОБИОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ АКТИВНОГО ИЛА
Гидробиологическое исследование активного ила проводят микроскопированием с целью контроля за его качеством, а также за работой биологических очистных сооружений (аэротенков).
11.1 Средства измерений, вспомогательные устройства
Микроскоп МБИ-6 или аналогичный.
Предметные и покровные стекла.
11.2 Подготовка к исследованию
10 см3 активного ила отбирают непосредственно из аэротенка. Затем на предметное стекло пипеткой наносят небольшую каплю суспензии активного ила, накрывают покровным стеклом и укрепляют на предметном столике микроскопа.
11.3 Проведение измерения
Проводят микроскопирование, для чего пробу просматривают вначале при малом увеличении (окуляр 10х или 15х, объектив 8х), затем при большом (окуляр 10х или 15х, объектив 40х). Просматривают не менее 3 проб.
11.4 Обработка результатов
Количество организмов учитывают по пятибалльной системе: один - единично, два - мало, три - порядочно, четыре - много, пять - масса. Отмечают также состояние организмов, их подвижность, работу реснитчатого аппарата.
Проводят определение видов организмов по определителям (например Атлас "Фауна аэротенков", Л.6 "Наука, 1984, 264 с).
12 ОПРЕДЕЛЕНИЕ ПЕНООБРАЗОВАНИЯ
Метод основан на измерении высоты столба пены над уровнем аэрируемой жидкости в аэротенке.
12.1 Средство измерения
Линейка, градуированная в сантиметрах и миллиметрах.
12.2 Проведение измерения
С помощью линейки измеряют среднюю высоту столба пены над уровнем аэрируемой жидкости, прикладывая линейку к аэротенку.
За результат измерения принимают среднее арифметическое результатов пяти измерений, проведенных в течение 30 мин.
Ключевые слова: поверхностно-активные вещества, биоразлагаемость, иловый индекс, кинетические характеристики, концентрация, период полуразложения критическая концентрация мицеллообразования