ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ПРИРОДОПОЛЬЗОВАНИЯ
|
УТВЕРЖДАЮ И.о. директора ФГУ «Федеральный центр анализа и оценки техногенного воздействия ______________О.А. Хахалин «19»апреля 2011 |
ТОКСИКОЛОГИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
МЕТОДИКА
ОПРЕДЕЛЕНИЯ ОСТРОЙ ТОКСИЧНОСТИ
ПИТЬЕВЫХ, ПРЕСНЫХ ПРИРОДНЫХ И СТОЧНЫХ ВОД,
ВОДНЫХ ВЫТЯЖЕК ИЗ ПОЧВ, ОСАДКОВ СТОЧНЫХ ВОД И
ОТХОДОВ ПО СМЕРТНОСТИ ДАФНИЙ (Daphnia magna Straus)
ПНД Ф Т 14.1:2:4.12-06 Т 16.1:2.3:3.9-06
МОСКВА
2006 г.
(издание 2011 г.)
СОДЕРЖАНИЕ
НАЗНАЧЕНИЕ И ОБЛАСТЬ ПРИМЕНЕНИЯ МЕТОДИКИ
Настоящий документ устанавливает методику определения острой токсичности питьевых, пресных природных и сточных вод, водных вытяжек из почв, осадков сточных вод, отходов производства и потребления в лабораторных условиях с использованием в качестве тест-объекта низших ракообразных дафний.
1. ПРИНЦИП МЕТОДИКИ
Методика основана на определении смертности дафний (Daphnia magna Straus) при воздействии токсических веществ, присутствующих в исследуемой водной среде, по сравнению с контрольной культурой в пробах, не содержащих токсических веществ (контроль). Количество живых и мертвых дафний определяется методом прямого счета.
Острое токсическое действие исследуемой воды или водной вытяжки из почв, осадков сточных вод и отходов на дафний устанавливается по их смертности (летальности) за определенный период экспозиции. Критерием острой токсичности служит гибель 50 % и более дафний за 48 часов в исследуемой пробе при условии, что в контрольном эксперименте все рачки сохраняют свою жизнеспособность.
В экспериментах по определению острого токсического действия устанавливают:
· среднюю летальную концентрацию отдельных веществ (кратность разбавления вод или водной вытяжки из почв, осадков сточных вод и отходов, содержащих смеси веществ), вызывающую гибель 50 % и более тест-организмов (ЛК50-48, ЛКР50-48);
· безвредную кратность разбавления вод, водных вытяжек, вызывающую гибель не более 10 % тест-объектов за 48-часовую экспозицию (БКР10-48)
2. МЕТРОЛОГИЧЕСКИЕ ХАРАКТЕРИСТИКИ МЕТОДИКИ
Настоящая методика обеспечивает получение результатов анализов с погрешностями, не превышающими значений, приведенных в таблице 1.
Таблица 1
Результаты метрологической аттестации методики
|
Диапазон измерений, шт. |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), sr,. % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), sR. % |
Предел повторяемости (относительное значение допускаемого расхождения между тремя результатами параллельных определений), r, % |
Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами, полученными в двух лабораториях), R, % |
|
От 0 до 10 вкл. |
8.0 |
13.0 |
26 |
36 |
3. ОБОРУДОВАНИЕ, МАТЕРИАЛЫ, РЕАКТИВЫ
Для проведения исследований по данной методике необходимы следующие средства измерений, материалы и реактивы:
3.1. Средства измерений
· весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г (ГОСТ Р 53228-2008);
· весы лабораторные общего назначения с наибольшим пределом взвешивания 1000 г (ГОСТ Р 53228-2008);
· гири (ГОСТ 7328-2001);
· рН-метр электронный РН-009(II)А (ГОСТ 25.7416.01-71);
· люксметр цифровой ТЮ 1403 (ТУ 4485-0152-05764771-96);
· фотоэлектроколориметр ИПС-03 (ТУ 4437-003-26218570-2006);
· термометр лабораторный шкальный с диапазоном измерения от 0 до 50 °С с ценой деления шкалы 0,5 °С (ГОСТ 28498-90);
· цилиндры вместимостью 25. 50. 100, 1000 см3 второго класса точности (ГОСТ 1770-74)
· колбы мерные 2-25-2.2-50-2, 2-100-2 (ГОСТ 1770-74);
· пипетки вместимостью 1, 2. 5, 10 см3 с ценой деления 0,1 см3 (ГОСТ 29227- 91);
· микропипетки 0,1 см3; 0,2 см3 с ценой деления 0,01 см3 (ГОСТ 29227-91);
3.2. Вспомогательное оборудование
· климатостат Р-2 (бокс для культивирования дафний) ТУ 4211-004-26218570- 2006 или климатостат В3 ТУ 4211-008-26218570-2009, позволяющие поддерживать освещение лампами дневного света 1200 - 2500 лк, фотопериод (12 + 12) часов и температуру окружающего воздуха (20 ± 1) °С;
· устройство для экспонирования рачков УЭР-03 ТУ 3615-006-26218570-2007 в комплекте со стеклянными пробирками объемом 100 см3;
· культиватор КВ-05 для культивирования водорослей, ТУ 3615-006- 26218570-2007;
· центрифуга лабораторная медицинская ЦЛН-1 с комплектом пробирок (ТУ 5-375-4261-76, ТУ 5-4260);
· холодильник бытовой, обеспечивающий замораживание (-20 ± 1 °С) и хранение проб (от +2 до +4 °С);
· пипетки автоматические дозаторы (любого типа) объемом 0,1 см3 и 0,2 см3;
· пипетки стеклянные объемом 2 см3 с отрезанным и оплавленным концом для пересадки рачков (ГОСТ 29227-91);
· воронки лабораторные (ГОСТ 25336-82);
· стаканы стеклянные лабораторные вместимостью 150, 200, 250, 1000 см3 (ГОСТ 25336-82Е);
3.3. Реактивы и материалы
· вода дистиллированная (ГОСТ 6709-72);
· вода питьевая (ГОСТ Р 51232-98);
· калий двухромовокислый стандарт-титр (ТУ 6-09-2540-87);
калий азотнокислый х.ч. (ГОСТ 4217-77);
· калий фосфорнокислый однозамещенный 3-водный (ГОСТ 4198-75);
· магний сернокислый 7-водный (ГОСТ 4523-77);
· кадмий сернокислый 8-водный (ГОСТ 4456-75);
· цитрат железа;
· культура зеленой водоросли Сhlогеllа vulgaris Beijer
· дрожжи хлебопекарные (ГОСТ 171-81);
· культура тест-организмов - Daphnia magna Straus с характеристиками по «Определителю пресноводных беспозвоночных Европейской части СССР» (планктон и бентос). - Л.: Гидрометеоиздат, 1977 (Кутикова, Старобогатов);
· ткани шелковые (для муки и крахмала - мельничный газ) № 25-43. (ОСТ 4403-67);
· сачки диаметром 1 - 2 см из мельничного газа (изготавливаются кустарно);
Примечание. Допускается использование средств измерений, вспомогательных устройств и материалов другого типа, имеющих аналогичные характеристики
4. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
4.1. При работе с химическими веществами, загрязненными почвами, осадками сточных вод, отходами и сточными водами необходимо соблюдать требования техники безопасности по ГОСТ 12.1.007-76 «ССБ. Вредные вещества. Классификация и обшие требования безопасности».
4.2. При подготовке проб загрязненных почв, осадков сточных вод и отходов необходимо пользоваться средствами индивидуальной защиты: специальной одеждой по ГОСТ 12.4.103-83, респираторами, очками защитными по ГОСТ Р 12.4.013-97, резиновыми перчатками по ГОСТ 20010-93.
4.3. К воздуху производственных помещений предъявляются санитарно- гигиенические требования по ГОСТ 12.1.005-88.
4.4. Безопасность при работе с электроустановками обеспечивается по ГОСТ Р 12.1.019-2009 и в соответствии с требованиями инструкций к оборудованию.
4.5. Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83.
4.6. Рабочие столы и поверхности должны содержаться в чистоте. В конце дня проводится влажная уборка рабочих поверхностей.
4.7. Необходимо организовать обучение работающих безопасности труда по ГОСТ 12.0.004-90.
5. ТРЕБОВАНИЕ К КВАЛИФИКАЦИИ ЛИЦ, ПРОВОДЯЩИХ БИОТЕСТИРОВАНИЕ
К биотестированию допускаются специалисты с квалификацией «техник», «лаборант», освоившие методические приемы водной токсикологии и уложившиеся в нормативы контроля при освоении методики.
6. УСЛОВИЯ ПРОВЕДЕНИЯ БИОТЕСТИРОВАНИЯ
Биотестирование проводится в лабораторных условиях в соответствии с ГОСТ 15150, помещение не должно содержать токсичных паров и газов.
Температура окружающего воздуха в лаборатории (17 - 27) °С. Атмосферное давление (84 - 106) кПа (630 - 800) мм рт.ст. Освещение помещения может быть естественным или искусственным и не ограничено особыми требованиями.
Температура в климатостате Р2 (В3) для биотестирования (20 ± 1) °С.
Освещение в климатостате Р2 (В3) обеспечивается лампами дневного света. Освещенность для дафний (1200 - 2500) лк при фотопериоде (день/ночь) 12 + 12 часов.
7. ПОДГОТОВКА К ПРОВЕДЕНИЮ БИОТЕСТИРОВАНИЯ
Для проведения биотестирования предварительно разрабатывают программу отбора проб, готовят посуду, оборудование, вспомогательные материалы для отбора проб и проведения биотестирования, пробоотборники, места хранения отобранных проб, а также рабочие места для обработки доставленных в лабораторию проб и исследования их на токсичность. Все процедуры предварительной подготовки должны исключать попадание токсичных, органических и каких-либо других веществ из окружающих предметов или среды в исследуемую воду или в водные вытяжки из почв, осадков сточных вод и отходов.
7.1. Подготовка посуды для отбора, хранения проб и биотестирования
Подготовка производится согласно «Методике определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222. Для отбора проб воды используют посуду из полиэтилена или политетрафторэтана, а при наличии в воде нефтепродуктов, моющих средств и пестицидов - банки из темного стекла.
Для отбора проб почв, осадков сточных вод и отходов используют банки из темного стекла или посуду из нержавеющей стали. Для отбора проб, исследуемых на токсичность, нельзя использовать посуду с хромовым покрытием.
Посуда из полиэтилена и стекла для отбора проб и биотестирования должна быть химически чистой. Посуду промывают раствором азотной кислоты с массовой долей 10 %. Стенки посуды осторожно смачивают этим раствором, после чего на 2- 3 часа посуду оставляют, затем тщательно промывают водопроводной водой, нейтрализуют раствором пищевой соды и промывают 3 - 4 раза дистиллированной водой. При сильном загрязнении посуды, а также новую посуду промывают водой, заполняют раствором азотной кислоты с массовой долей 10 % и выдерживают не менее суток, затем тщательно промывают водопроводной и не менее 3 - 4 раз дистиллированной водой. Посуду для отбора проб почв, осадков сточных вод и отходов, изготовленную из нержавеющей стали, тщательно моют, очищают пищевой содой, промывают водопроводной водой и ополаскивают 3 - 4 раза дистиллированной водой. Для мытья посуды не разрешается пользоваться хромовой смесью (смесью бихромата калия и серной кислоты), синтетическими поверхностно-активными веществами и органическими растворителями.
Химически чистую посуду для биотестирования хранят с закрытыми стеклянными притертыми пробками или завинчивающимися крышками в защищенных от пыли ящиках лабораторного стола или на закрытых полках, стеллажах и т.п.
7.2. Подготовка «щыпивационной воды
Выполняется согласно «Методике определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222. Культивационная вода используется для культивирования дафний: в качестве контрольной при биотестировании; для разбавления исследуемых вод.
Для подготовки культивационной воды питьевую воду отстаивают в течение 3 - 7 суток (до полного дехлорирования) в бутылях из бесцветного стекла. При отсутствии питьевой воды удовлетворительного качества допускается использование бутилированной негазированной питьевой воды или поверхностной пресной или грунтовой воды, отобранной вне зоны влияния источниковзагрязнения и профильтрованной через мембранный фильтр с размером пор 3,5 мкм. Мембранные фильтры перед употреблением тщательно промывают и кипятят в дистиллированной воде не менее 10 мин.
Культивационная вода должна удовлетворять следующим требованиям:
· отсутствие органических загрязняющих веществ, хлора, токсических веществ, антагонистических для дафний организмов (сине-зеленых водорослей) и пищевых конкурентов (простейших, многоклеточных);
· pH 7,0 - 8,5;
· жесткость общая от 80 до 250 мг/дм3 (выраженная в СаСО3);
· температура от +19 °С до +25 °С.
В культивационной воде требуемого качества выживаемость тест-культуры рачков дафний за 48-часовой период биотестирования должна быть не ниже 100 %. При этом 50 % гибель рачков в конце первых суток экспонирования должна наступать при внесении в нее бихромата калия в диапазоне концентрации 0,9 - 2,0 мг/дм3. Более низкая чувствительность к данному модельному токсиканту может быть вызвана присутствием в культивационной воде повышенного количества примесей, способных вступать с ним во взаимодействие. В результате этого токсикант становится менее доступным для тест-организма. Для повышения чувствительности биотеста можно разбавить культивационную воду дистиллированной водой в 1,5 - 3,0 раза. После разбавления культивационная вода должна быть нетоксичной для рачков и обеспечивать их хорошую плодовитость в маточной и синхронной культуре.
При исследовании вод с повышенным солесодержанием (содержание сухого остатка выше 1 г/дм3) проводят предварительную постепенную адаптацию культуры тест-обьектов, добавляя небольшими порциями хлористый натрий в культивационную воду (содержание солей по сухому остатку не должно превышать 6 г/дм3).
При использовании в силу необходимости культивационной воды, не отвечающей требованиям установленного качества, все отклонения отмечают в протоколе испытаний.
7.3. Получение исходного материала, транспортировка, содержание и кормление дафний, выращивание культуры
Исходный материал для культивирования водорослей, дафний можно получить в лабораториях, занимающихся биотестированием, имеющих культуру требуемой видовой принадлежности, чувствительность которой к модельному токсиканту укладывается в установленный диапазон по п. 10, а измеряемые с помощью этой культуры тест-параметры соответствуют установленным характеристикам погрешности (см. п. 2).
7.3.1. Транспортировка дафний
Производится согласно «Методике определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222. Дафний транспортируют в стеклянной емкости с крышкой (в термосе, если температура окружающей среды выходит за пределы 20 ± 2 °С). Емкость заполняется местной культивационной водой на 2/3 объема, и в нее сачком переносятся дафнии. Плотность посадки приблизительно 25 особей на 1 дм3 воды; для кормления добавляется 3 см3 водорослевой суспензии на 1 дм3 воды. В лаборатории воду с дафниями по стенке сосуда переливают в емкость для культивирования, объем которой должен в 2 - 3 раза превышать количество воды с рачками. Культиватор с дафниями помещают в климатостат или бокс и в течение 1 - 2 дней небольшими порциями приливают приготовленную культивационную воду (см. п. 7.2) для адаптации дафний к новой воде.
В лаборатории содержат два вида культуры дафний: маточную (массовую), используемую как источник для возобновления в периоды потери культуры синхронизированной и синхронизированную, используемую непосредственно для биотестирования.
7.3.2. Выращивание и содержание маточной культуры дафний
Культуру дафний выращивают в климатостате Р-2 или эквивалентном приспособлении, обеспечивающем поддержание искусственного освещения лампами дневного света с интенсивностью света от 1200 до 2500 лк, 12-часовой световой и ночной (без освещения) периоды; температуру (20 ± 2) °С.
Выращивание культуры производится согласно «Методике определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222. В качестве культиваторов используют чашки кристаллизационные толстостенные или батарейные стаканы объемом 2 - 5 дм3, которые наполняют на 3/4 объема культивационной водой, сажают туда самок дафний среднего размера с выводковыми камерами, заполненными эмбрионами, и неплотно прикрывают культиваторы (от попадания пыли и для уменьшения испарения) пластинами из стекла или оргстекла толщиной не менее 6 мм. Для пересадки в культиваторы можно отобрать взрослых самок с помощью фильтрования культуры через крупное сито (размер ячеек 1800 - 2200 мкм). Маточная культура дафний поддерживается в одном или двух сосудах. Ежедневно утром с поверхности воды в сосудах, в которых культивируются рачки, стерильной марлевой салфеткой снимается дрожжевая и бактериальная пленка. Кормление дафний осуществляют в соответствии с требованиями пункта 7.4. Содержание растворенного кислорода в культиваторах должно быть не менее 6 мг/дм3, что достигается регулярной пересадкой дафний в свежую культивационную воду. Аэрирование воды в культиваторах с дафниями не допускается.
Один или два раза в неделю осуществляется пересадка культуры в свежую культивационную воду (частота пересадки определяется содержанием растворенного кислорода в культиваторах). Для этого вода вместе с рачками осторожно переливается в чистый культиватор так, чтобы накопившийся осадок остался на дне. В чистый культиватор добавляется свежая порция культивационной воды. Плотность маточной культуры не должна превышать 20 - 25 особей на 1 дм3 культивационной воды.
Не допускается использование молоди маточной культуры для биотестирования.
7.3.3. Выращивание синхронизированной культуры
Биотестирование воды и водных вытяжек проводят только на синхронизированной культуре дафний. Синхронизированной является одновозрастная культура, полученная от одной самки путем ациклического партеногенеза в третьем поколении. Такая культура генетически однородна. Рачки, ее составляющие, обладают близкими уровнями устойчивости к токсическим веществам, одновременно созревают и в одно время дают генетически однородное потомство. Получение синхронизированной культуры производится в климатостате согласно «Методике определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222. Для этого отбирают одну самку средних размеров с выводковой камерой, заполненной эмбрионами, и помещают в химический стакан объемом 250 см3, заполненный культивационной водой на 200 см3. Появившаяся молодь переносится в кристаллизатор (25 особей на 1 дм3 воды) и культивируется указанным способом. Полученная третья генерация является синхронизированной культурой и может быть использована для биотестирования в возрасте 6 - 24 часов.
Чтобы отобрать для опытов одновозрастную культуру, дафний фильтруют с помощью комплекта сит. Взрослые дафнии задерживаются на крупном сите (размер ячеек 1000 - 2200 мкм), а молодые, в возрасте от 6 до 24 часов, на самом мелком (размер ячеек 450 - 560 мкм).
Для непрерывного осуществления массовых анализов на токсичность различных сред при большом количестве проб необходимо культивирование 4 - 5 генетически однородных синхронизированных культур, отличающихся друг от друга по возрасту. Таким образом, обеспечивается постоянный приток тестовых организмов. Синхронизированную культуру выдерживают в условиях по п. 7.3.2; кормление осуществляется по п. 7.4.
Пересадка плодоносящих самок в свежую культивационную воду осуществляется один раз в неделю. Родившуюся молодь ежедневно отсаживают и используют для биотестирования.
7.4. Подготовка корма и кормление
Дафниям необходимо обеспечить комбинированное дрожже-водорослевое питание. В качестве водорослевого корма используется культура зеленой водоросли Chlorella vulgaris Beijer. Культура водоросли выращивается в культиваторе КВ-05 в течение 24 часов на 5 % среде Тамия (см. Приложение 5). Клетки водоросли отделяют центрифугированием. Осадок разбавляют культивационной водой до концентрации 0,5 - 0,6 ед. оптической плотности (прибор ИПС-03). Данный способ подготовки корма допускает использование культуры водоросли хлорелла, выращенной на 50 % среде Тамия. Водорослевое кормление маточной и синхронизированной культур дафний производится через каждые 1 - 2 суток путем добавления в емкости с рачками указанной выше суспензии хлореллы. Количество добавляемой суспензии должно составлять около 1/20-той части объема маточной и синхронизированной культуры дафний. При этом концентрация клеток водоросли после добавления в среду с рачками должна быть эквивалентна оптической плотности суспензии 0,02 - 0,03.
Для дрожжевого питания культуры рачков готовится суспензия из 1 г свежих или 0,5 г сухих хлебопекарных дрожжей в 100 см3 дистиллированной воды. После набухания суспензию тщательно перемешивают. Допускается хранить дрожжевую суспензию в холодильнике 1 - 2 суток. Кормление дрожжами производится 1 раз в неделю путем добавления по 3 см3 тщательно перемешанной дрожжевой суспензии на 1 дм3 культуры рачков. Водорослевый корм в этот день дается в количестве в три раза меньше.
7.4.1. Кормление дафний в эксперименте
Кормление дафний производят до проведения токсикологического эксперимента. Дафний в опыте не кормят.
7.5. Отбор, транспортировка, хранение и подготовка проб
7.5.1. Отбор, транспортировка, хранение и подготовка проб воды
7.5.1.1. Отбор, транспортировка и хранение проб воды
Для проведения анализа на острую токсичность необходимо отобрать не менее 1000 см3 пробы воды. Отбираемый объем должен быть в два раза больше требуемого для хранения дубликата пробы до конца биотестирования.
Методы отбора, транспортировки, хранения, подготовки к выполнению биотестирования должны обеспечить неизменность состава проб в интервале времени между отбором проб и их анализом.
Общие процедуры отбора проб определены в ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб», ГОСТ Р. 51593-2000 «Вода питьевая. Отбор проб».
Отбор проб в поверхностных проточных и непроточных водоемах осуществляется в соответствии с ГОСТ 17.1.5.05-85 «Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков».
Для отбора проб используют устройства в соответствии с требованиями ГОСТ 17.1.5.04-81 «Охрана природы. Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Общие технические условия».
Остальные условия отбора, транспортировки и хранения проб воды должны соответствовать «Методике определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222. Пробы отбирают вручную специальными приспособлениями или с применением автоматических пробоотборников, при этом емкости для проб должны быть изготовлены из нетоксичного материала, легко выниматься из пробоотборника для очистки и мытья.
Для отбора глубинных проб воды из озер, водохранилищ, прудов и рек следует использовать батометры системы Молчанова, Рутнера или Скадовского- Зернова.
Для отбора проб с глубины 0.5 м и более используется бутыль с привязанной пробкой, которую помещают в футляр, или пробоотборник с грузом. Футляр снабжен петлей, к которой привязывают веревку с размеченными отрезками, указывающими глубину погружения. На требуемой глубине с помощью привязанной к пробке веревки выдергивают пробку из горла бутыли. После заполнения бутыли водой (на поверхности воды не появляются пузырьки воздуха) ее поднимают на поверхность.
Отбор проб питьевых вод осуществляется в соответствии с ГОСТ Р 51592-2000 «Вода питьевая. Отбор проб».
Отбор питьевых вод перед поступлением в распределительную сеть производят из кранов на водоводах, расположенных на входе в установку обеззараживания.
Пробы питьевой воды в источнике водоснабжения и сточной воды с глубины менее 0,5 м отбираются пробоотборником любого типа объемом 500 - 700 см3.
Водопроводную воду отбирают из-под крана, многократно ополоснув его отбираемой водой, после 10-минутного слива при полностью открытом кране. Кран антисептической обработке не подвергается.
Отбор сточных вод осуществляется в соответствии с требованиями НВН 33-5.3.01-85 «Инструкция по отбору проб для анализа сточных вод».
Отбор природных и сточных вод следует производить в местах наибольшего перемешивания. Сточные воды отбираются на средней глубине потока, где твердые частицы равномерно распределены.
Очищенные сточные, а также питьевые воды на стадии водоподготовки следует отбирать до системы хлорирования.
При исследовании сточных вод на токсичность не допускается отбор разовой пробы. Количество необходимых порций выбирают на основе опыта проведения анализа. Предпочтительно отбирать среднесуточную пробу каждый час в течение часов. После тщательного перемешивания всего объема отобранной пробы для исследования берется необходимое количество воды.
Допустимое минимальное количество отбираемых единичных проб для последующего смешения - три, с интервалом между отборами не менее часа.
При взятии проб измеряют температуру воды. Для этого используют термометры с ценой деления 0,5 °С. Для определения температуры на месте взятия пробы 1 дм3 воды наливают в склянку, нижнюю часть термометра погружают в воду и через 5 мин отсчитывают показания, держа его вместе со склянкой на уровне глаз. Точность определения ±0,5 °С.
Не допускается консервирование проб, предназначенных для исследования на токсичность.
Отобранные пробы наливают, предварительно дважды ополаскивая отбираемой водой, в банки или флаконы, заполняя их до краев и закрыв без пузырьков воздуха пришлифованными стеклянными пробками или полиэтиленовыми крышками. Под полиэтиленовые крышки подкладывают стерильные тефлоновые прокладки или прокладки из алюминиевой фольги. Пробы упаковывают в деревянные ящики для переноски проб и прокладывают бумагой или ветошью. Для лучшей сохранности в жаркую погоду пробы транспортируют в контейнерах-холодильниках при температуре от +4 до +10 °С. В холодный период года контейнеры должны быть снабжены термоизолируюшими прокладками, обеспечивающими предохранение проб от промерзания. При транспортировке не следует держать пробы на свету.
При отборе пробы составляют протокол по утвержденной форме (см. Приложение 1), в котором указывают цель пробоотбора, число, время, место отбора пробы, температуру воды (или результаты других произведенных измерений), номер пробы, ставят подпись и расшифровывают подпись отбиравшего пробы. На бутыль наклеивают этикетку с указанием номера пробы, места, даты и времени ее отбора.
При отборе проб необходимо соблюдать технику безопасности. На крупных водотоках и водоемах следует соблюдать навигационные правила и правила эксплуатации используемого судна. Постоянные точки контроля следует выбирать в местах, которые были бы доступны в любое время года и где отсутствуют какие- либо природные опасности. На очистных сооружениях отбор проб осуществляется в специально предназначенных местах, маркированных и освещаемых в темное время суток. Отбор проб воды производится бригадой, состоящей минимум из двух человек. Перед работой бригада должна быть проинструктирована о мерах предосторожности при выполнении программы работ в зависимости от места отбора, климатических условий и т.д. Пробы, поступающие в лабораторию для исследования, должны быть зарегистрированы в журнале учета с обязательным указанием числа емкостей и номера протокола отбора проб для каждой пробы.
Биотестирование проб воды проводят не позднее 6 часов после их отбора. При невозможности проведения анализа в указанный срок пробы воды охлаждают (+2 - +4 °С). Хранить пробы следует не более 24 часов после отбора. О продолжительности хранения проб воды делают отметку в протоколе биотестирования. В исключительных случаях при отсутствии летучих органических веществ допускается замораживание проб (-20 °С) и их хранение до двух недель, однако следует помнить, что после размораживания токсичность воды может измениться. В случае предполагаемого замораживания пробы при ее отборе не следует заполнять сосуды полностью, чтобы избежать их разрыва. Если пробы требуется отстаивать или фильтровать, то фильтрация и отстаивание должны предшествовать замораживанию.
7.5.1.2. Подготовка проб воды к биотестированию
Подготовка производится согласно рекомендациям «Методики определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222.
Перед биотестированием предварительно охлажденные или замороженные пробы доводят до температуры 20 ± 2 °С. При наличии в сточных водах крупнодисперсных включений (с диаметром частиц более 3,3 мкм) необходима фильтрация пробы через наиболее пористые обеззоленные фильтры «белая лента» (недопустимо использовать «синюю ленту», так как она задерживает коллоидные вещества, что занижает результаты биотестирования).
Природные воды фильтруют через мембранные фильтры с диаметром пор 3,5 мкм (фильтр перед применением должен быть промыт и простерилизован кипячением в дистиллированной воде не менее 10 мин) или через обеззоленные фильтры «белая лента». Активный хлор, используемый для обеззараживания питьевых и сточных вод, является токсическим веществом, поэтому перед биотестированием питьевых вод, а также при необходимости анализа сточных вод после системы хлорирования хлор следует удалить из исследуемой воды отстаиванием пробы с открытой крышкой при температуре от +2 до +4 °С не менее 24 часов.
Проба воды, подлежащая биотестированию, должна иметь pH 7,0 - 8,2, если pH пробы выходит за указанные пределы, в отдельном эксперименте устанавливается токсичность, вызываемая водородным показателем. Затем определяется токсичность воды после нейтрализации пробы. Подкисление осуществляют 10 %-ным раствором НСl, подщелачивание - 10 %-ным раствором NaOH. После нейтрализации пробы аэрируют 10 - 20 мин для стабилизации pH. Регулирование pH не должно вызывать химической реакции с веществами, присутствующими в пробе (выпадение осадка, комплексообразование) и не должно более чем на 5 % изменять концентрацию исследуемых вод.
При исследовании грунтовых или других вод с содержанием железа двухвалентного более 1 мг/дм3 (валовая форма) необходимо предварительное отстаивание проб не менее 24 часов при температуре от +2 до +4 °С. Осветленная вода сифонируется и анализируется на токсичность.
7.5.1.3. Приготовление разбавлений исследуемых вод для биотестирования
Приготовление производится согласно рекомендациям «Методики определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222.
Для приготовления разбавлений исследуемых вод используется культивационная вода. Предварительно перед приготовлением необходимых разбавлений воды для исследования подготавливают соответствующей емкости посуду, в которой будут готовить растворы. Объем используемой посуды должен на 1/3 превышать необходимый объем приготавливаемого разбавления исследуемых вод.
Перед приготовлением разбавлений нужно подготовить по возможности два одинаковых сосуда: один для разбавления, а другой для хранения раствора (может случиться, что в ближайшие часы процедуру биотестирования в определенном разбавлении необходимо будет повторить). Как во время приготовления разбавлений, так и при их хранении бутыли или другая посуда обязательно должны быть закрыты предварительно подобранными пробками и снабжены надписями о приготовленной концентрации исследуемых вод. Приготовление растворов, разбавлений, проведение биотестирования выполняются при комнатной температуре. Температура культивационной и исследуемой воды должна быть также доведена до комнатной температуры перед приготовлением разбавлений.
Для приготовления разбавлений берут определенные, отмеренные мерной посудой, объемы исследуемой и разбавляющей (культивационной) воды. В качестве мерной посуды для объемов меньше 10 см3 используются мерные пипетки. Для объемов более 10 см3 - мерные цилиндры. Поверхностные, пресные, грунтовые и сточные воды с неизвестной степенью токсичности анализируются в 100, 30, 9, 3 и 1 %-ной концентрациях. Сточные и очищенные сточные воды (отобранные до системы хлорирования), если не известны их токсические свойства, тестируются в первичном испытании в большем наборе разведении. Если предварительно известно, что сточные воды обладают гипертоксичностью, а также если это можно предположить по данным гидрохимического исследования, исследуемые концентрации уменьшаются и составляют 10; 3; 1,0; 0,3; 0,1 %. Возможен произвольный выбор разведений. Чем выше предполагаемая токсичность, тем большей должна быть кратность разбавлений исходной пробы.
После получения предварительных результатов биотестирования при необходимости готовятся и анализируются дополнительные разбавления.
Если при первичном токсикологическом испытании разбавление сточных вод делается в стандартных (предложенных выше) концентрациях или наугад, то при повторном исследовании разбавления готовят, исходя из полученных результатов проведенных исследований. При этом для более точного определения степени токсичности тестируемых вод кратность разбавления лучше брать равной двум, т.е. 100; 50; 25; 12,5; 6,25 %. В процессе приготовления разбавлений пробы тщательно перемешивают.
При выполнении практического биотестирования используют в основном два (наиболее важных) показателя, характеризующих содержание исследуемой воды в разбавленном (культивационной водой) растворе: во сколько раз исследуемая вода разбавлена и каково ее процентное содержание в разбавлении. Данные показатели заносят в рабочий журнал (см. Приложение 2).
Пример. Как путем разбавления получить х %-ный раствор
сточной воды и рассчитать, во сколько раз она разбавлена. Величину х будем
измерять в долях. Тогда единица соответствует раствору, в котором х - доля
исследуемой воды и (1 - х) - доля чистой культивационной воды. Культивационной
воды в растворе больше, чем сточной в ![]() раз. Степенью разбавления называется
величина
раз. Степенью разбавления называется
величина ![]()
Если х измеряется в процентах, то эта величина запишется в виде:
![]()
Итак, если к одной доле сточной воды добавить (100-х) % долей культивационной воды, мы получим х %-ный раствор. Например, для получения 5 %-ного раствора сточных вод вычислим степень разбавления
![]()
и получим, что 1 доля сточных вод и 19 долей культивационной воды составят при смешении 5 %-ный раствор сточных вод, т.е. 5 %-ный раствор сточных вод получится при их 20-кратном разбавлении.
7.5.2. Отбор, транспортировка, хранение и подготовка проб почвы
7.5.2.1. Отбор, транспортировка, хранение проб
Методы отбора, транспортировки, хранения, подготовки к выполнению биотестирования должны обеспечить неизменность состава проб почвы в интервале времени между отбором и их анализом.
Отбор проб грунта, транспортировка и хранение осуществляется в соответствии с ГОСТ 12071-84 «Грунты. Отбор, упаковка, транспортирование и хранение образцов», ГОСТ 27753.1-88 «Грунты тепличные. Методы отбора проб».
Отбор проб почвы, их транспортировка и хранение осуществляется в соответствии с ГОСТ 17.4.3.01-83 «Охрана природы. Почвы. Общие требования к отбору проб», ГОСТ 17.4.4.02-84 «Почвы. Методы отбора и подготовки проб для химического, бактериологического, гельминтологического анализа», ГОСТ 28168-89 «Почвы. Отбор проб», а таюке согласно рекомендациям «Методики определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222.
При отборе проб почвы должна быть определена протяженность и топография зон загрязнения. Участки для отбора проб почвы должны хорошо отражать структуру района исследования: почвенный покров, материнскую породу, рельеф, геологические и гидрологические характеристики.
Необходимым условием отбора проб почвы является предохранение их от вторичного загрязнения (в том числе атмосферных осадков) на всех этапах отбора и подготовки проб к биотестированию. Для сравнимости результатов необходимо, чтобы приемы выбора пунктов и способ отбора проб почвы были идентичны при каждом исследовании почвы на токсичность.
Дня характеристики загрязнения почвы на определенной площади отбираются объединенные пробы почвы. Объединенную пробу составляют путем смешивания единичных проб почвы, отобранных в разных точках данной пробной площадки размером не менее 10×10 м (100 м2), которая располагается в типичном для данной территории месте. На каждые 20 га площади закладывается не менее одной пробной площадки. При обследовании площади менее 0,5 га размер площадки уменьшается и составляет 5×5 м.
Объединенную пробу составляют из 5 - 10 или 15 - 20 единичных проб (в зависимости от однородности исследуемого участка), равномерно размещенных на пробной площадке. Объем единичных проб почвы должен быть одинаков, поэтому для пробоотбора лучше использовать почвенный щуп. Щуп - это узкий металлический желоб, заостренный с одного конца и имеющий рукоятку для удобства пользования. Примерные размеры щупа: длина 1,25 - 1,5 м; диаметр 15 - 20 мм. Желоб в щупе составляет 3/4 его общей длины.
Взятие смешанного образца проводится следующим образом: лопатой делается прикопка на глубину до 30 - 40 см, отмечается мощность и цвет верхнего горизонта или слоя и изменения в цвете и состоянии от поверхности вглубь, после чего со стенки берется образец на полную глубину горизонта (слоя) массой 1 - 2 кг после предварительной очистки поверхности почвы от растений. Отбирается также образец поверхностной пробы до глубины 5 - 10 см той же массы.
Единичные пробы ссыпают на крафт-бумагу или клеенку, тщательно перемешивают, квартуют (сокращают) в 3 - 4 раза (почву разравнивают на бумаге в виде квадрата, делят на четыре части, две противоположные части отбрасывают, две оставшиеся части перемешивают). Оставшуюся после квартования почву делят на 6 - 9 квадратов, из центра которых отбирают примерно одинаковое количество почвы, обеспечивая захват всей толщины слоя, переносят в банки из стекла с герметичной крышкой. Таким образом получают объединенную пробу, масса которой приблизительно 2 кг (1 кг на анализ и 1 кг для хранения дубликата). При отборе проб почвы составляют протокол по утвержденной форме (см. Приложение 1), в котором указывают цель пробоотбора, число, время, место отбора пробы, номер пробы, ставят подпись и расшифровывают подпись отбиравшего. На банку, контейнер наклеивают этикетку с указанием номера пробы, места, даты и времени ее отбора. Транспортируют пробы при температуре окружающего воздуха от +4 до +28° С.
Пробы, поступающие в лабораторию, должны быть зарегистрированы в журнале учета с обязательным указанием числа емкостей и номера протокола отбора проб для каждой пробы.
Пробы почв должны быть подвергнуты анализу не позднее 12 ч от момента отбора. При невозможности обеспечения данного условия объединенные пробы в естественно влажном состоянии хранят в холодильнике (в банках с притертой или плотно завинченной крышкой) не более одной недели при температуре от +2 до +4°С. Пробы почв не консервируют.
Для проведения контрольных измерений токсичности фоновых образцов почвы проводят отбор почвы на фоновых (незагрязненных) участках обследуемых областей.
При отборе проб почвы для приготовления фоновых образцов используют типичные для данного региона почвы, характерные по агрохимическим свойствам.
7.5.2.2. Приготовление водной вытяжки из почв
Приготовление производится согласно рекомендациям «Методики определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний», ФР.1.39.2007.03222. В лаборатории отобранные на токсикологический анализ почвы сначала разрыхляют вручную металлическим шпателем и освобождают от материала, заведомо относящегося к инородным (случайным) механическим включениям (возможные промышленные, строительные бытовые отходы и т.п.), а также галечника, обломков камней, корневищ, веток. Решение об изъятии таких включений из подготавливаемой пробы принимают на основе изучения полевого описания конкретного места ее отбора; эти сведения должны являться обязательной частью сопроводительной документации к пробам, направленным на токсикологический анализ.
Перед биотестированием пробы просеивают сквозь сито с размером ячей 1 мм и доводят до воздушно-сухого состояния. Для этого пробу подсушивают в вытяжном шкафу или в хорошо проветриваемом помещении, размещая ее (в зависимости от массы и естественной влажности) в стеклянных кристаллизаторах подходящей вместимости, на стекле или на чистых листах плотной бумаги.
Размещенные таким образом пробы почвы выдерживают открытыми не менее 2-х часов при комнатной температуре и влажности воздуха (ГОСТ 5180-84 «Грунты. Методы лабораторного определения физических характеристик»). Подготовленную пробу распределяют на ровной поверхности слоем толщиной не более 1 см и отбирают ложкой или шпателем из 5-ти точек методом конверта. Не допускается предназначенные для исследования на токсичность пробы почв подвергать тепловой обработке, поэтому гигроскопическая влажность почвы определяется в отдельном образце.
Проба с массой приблизительно 300 г делится на две равные части: для биотестирования и для определения гигроскопической влажности после высушивания до постоянной массы, что необходимо для пересчета воздушносухой пробы на массу абсолютно-сухой по формуле:
![]()
где ∆Мабс.сух - масса абсолютно-сухого образца г; ∆Мвозд.сух. - масса воздушносухого образца почвы, г; Кср - коэффициент пересчета массы воздушно-сухой пробы на массу абсолютно-сухой (среднее расчетное значение из трех измерений).
Для определения массовой доли почвы в воздушно-сухой пробе необходимо:
1. Взвесить три пустых высушенных бюкса с крышками и зафиксировать их массы (Moi), затем взвесить эти же бюксы с навесками воздушно-сухой пробы (около 1 г) и зафиксировать их массы (Мвозд.сух.i).
2. Установить открытые бюксы с воздушно-сухими пробами в сушильный шкаф. Пробы выдержать в сушильном шкафу в течение 3 ч при температуре от 105 до 115 °С. Закрыть бюксы притертыми крышками, перенести их в эксикатор и выдержать там до полного остывания (около 40 мин). Взвесить бюксы с навесками абсолютно-сухой пробы и зафиксировать их массы (Мабс.сух..i)- После взвешивания пробы почвы следует повторно высушить в течение 2 ч, затем охладить в эксикаторе и снова взвесить. После первого и второго высушивания допустимое расхождение в массе не должно превышать 0.005 г. В противном случае высушивание следует повторить. Точность взвешивания для всех экспериментов должна составлять 0,001 г.
3. Рассчитать значения коэффициента пересчета Ki для каждого эксперимента по формуле:
![]()
где Ki - коэффициент пересчета в i-том измерении; Мабс.сух.i - масса бюксы с абсолютно-сухим образцом в i-м измерении, г; Mвозд.cyx.i - масса бюксы с воздушно-сухим образцом в i-м измерении, г; Мoi - масса пустой бюксы в i-м измерении, г.
4. Так как по результатам измерений получено три значения коэффициента, производят расчет его среднего значения (Кср) по формуле:
![]()
Далее среди трех величин Кi рассчитывают размах (R) полученных значений с учетом максимальной (Кmax) и минимальной (Kmin) величин по формуле:
![]()
Если полученное значение R > 10 %, то эксперимент повторяют, устранив причину неудовлетворительных результатов.
Водную вытяжку из почвы для биотестирования готовят в соотношении: 1 часть почвы (с учетом гигроскопической влажности) и 4 части культивационной воды (допускается использование дистиллированной воды). Вода не должна содержать СО2, так как в его присутствии растворяются карбонаты кальция и магния по причине образования растворимых бикарбонатов, которые увеличивают сухой остаток и общую щелочность водной вытяжки и тем самым искажают результаты биотестирования.
Для удаления углекислого газа из культивационной или дистиллированной воды ее предварительно обрабатывают по п. 7.2.
Для приготовления водной вытяжки из почвы отвешивают 100 - 200 г пробы почвы в воздушно-сухом состоянии, пересчитав ее массу на массу абсолютносухой. Масса пробы на стадии перед приготовлением водной вытяжки должна быть достаточной для получения необходимого объема экстракта при проведении биотестирования во всех предполагаемых разведениях с учетом контрольных испытаний. Навеску почвы помещают в колбу емкостью 1000 см3 и приливают 4- кратное количество культивационной воды.
Далее на аппарате для встряхивания жидкости полученную смесь в течение 2-х часов встряхивают, после чего отстаивают в течение 30 мин. Надосадочная жидкость сифонируется, а затем профильтровывается через бумажные обеззоленные фильтры «белая лента» или через мембранные фильтры с диаметром пор 3,5 мкм (фильтры предварительно промывают и кипятят в дистиллированной воде не менее 10 мин). Бумажный фильтр помещают в воронку Бюхнера диаметром 15 - 20 см.
Перед тем как вылить вытяжку на фильтр содержимое склянки или колбы встряхивают, чтобы взмутить присутствующие взвешенные частицы почвы. На фильтр стараются перенести всю взвесь. При выливании струю суспензий направляют на боковую двойную стенку бумажного фильтра, но не на дно фильтра, так как при выливании на дно бумага может легко порваться. Фильтрация осуществляется с помощью вакуумного водяного или электрического насоса. Для фильтрации применяется слабый вакуум (не более 20 мм рт.ст.). Первые порции фильтрата часто бывают мутными и их нужно несколько раз перефильтровать до прозрачного раствора.
При повышенной мутности водной вытяжки из почв допускается отстаивание в холодильнике до 5 суток. Затем жидкость над осадком сифонируется. При устойчивом появлении окраски и высокой мутности водной вытяжки, получаемой из некоторых типов почв (например, гумусированные, дерново-подзолистые, торфяные и др. почвы) водную вытяжку из них готовят в соотношении 1 часть почвы (с учетом гигроскопической влажности) и 10 частей дистиллированной воды.
Вытяжка из почв должна иметь величину pH в диапазоне 7,0 - 8.2. При необходимости вытяжку перед серийным разбавлением предварительно нейтрализуют. После нейтрализации пробы аэрируют 10 - 20 мин для стабилизации pH. Непосредственно перед началом биотестирования пробы доводят до температуры 20 ± 2 °С. Биотестируемая проба водной вытяжки из почв должна иметь концентрацию растворенного кислорода не ниже 6 мг/дм3, в противном случае пробу аэрируют.
Приготовление разведений водной вытяжки для биотестирования проводят по п. 7.5.1.3.
7.5.3. Отбор, транспортировка, хранение и подготовка проб осадков сточных вод, отходов
7.5.3.1. Отбор, транспортировка и хранение проб
Методы отбора, транспортировки, хранения, подготовки к выполнению биотестирования должны обеспечить неизменность состава проб осадков, отходов в интервале времени между отбором и их анализом.
Отбор проб осадков сточных вод на Песковых, шламовых, иловых площадках производится согласно рекомендациям «Методики определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний»; ФР.1.39.2007.03222.
Если осадок на площадке представлен однородной массой, площадку следует разделить на 4 равные части. Отобрать 4 пробы из центра каждого квадрата лопатой послойно с глубины 0 - 5 см, 5 - 10 см и до конечной глубины площадки (до песка или бетонного покрытия) не менее 1000 г каждой пробы.
Если осадок на площадке находится в твердом и жидком состоянии, отбор осуществляется из разных участков с разделением их на квадраты и отбором из центра каждого квадрата твердых осадков, как описано ранее, а жидких - пробоотборником с разной глубины заполненной жидкими осадками площадки из 3 горизонтов: с поверхности, середины и со дна заполнения. Жидкие и твердые осадки отбираются в разные емкости. Жидких осадков отбирают 2 дм3 (1 дм для анализа и 1 дм3 для хранения дубликата).
Пробы твердых осадков тщательно перемешивают и 3 - 4 раза квартуют как указано для почв. Вес объединенной пробы должен быть 2 кг (1 кг для анализа и 1 кг для хранения дубликата).
Пробы осадков сточных вод не подлежат консервированию.
Пробы осадков сточных вод, поступившие в лабораторию на исследование, должны быть документально оформлены и маркированы. Необходимыми сопроводительными документами являются бланк описания осадка и протокол пробоотбора (см. Приложение 1).
Пробы, поступающие в лабораторию для исследования на токсичность, должны быть зарегистрированы в журнале учета с обязательным указанием числа емкостей и номера протокола отбора проб для каждой пробы.
Хранить пробу можно в холодильнике не более одной недели в стеклянной банке с притертой или плотно завинченной крышкой.
Пробоотбор отходов может быть связан с отбором следующих групп отходов, классифицируемых: а) по типу образования: отходы производства (промышленные/производственные отходы (ПО)), отходы потребления (твердые бытовые отходы (ТБО)), смешанные отходы (смесь ПО и ТБО); б) по агрегатному состоянию: твердые (пылеобразные, порошкообразные, зернистые, шлаки, гранулированные, кусковые), пасто-, смоло- и студнеобразные (текучие, пластичные, вязкие), полужидкие (шламообразные), эмульсии, суспензии, пульпы жидкие; в) по степени однородности: гомогенные и гетерогенные.
Время взятия и периодичность пробоотбора отходов имеет существенное значение для производств, использующих сырье переменного состава или перешедших на иной вид сырья, изменяющих технологический режим процесса или его технологическую (конструкционную) схему, а также для органических ПО и ТБО. При осуществлении производственного экологического контроля за отходами частота отбора проб определяется планом-графиком, согласованным с территориальными органами государственного контроля.
Отбор проб ПО производят не реже 1 раза в год при условии неизменности технологического процесса и используемого сырья, а также в любое другое время для осуществления контрольных проверок возможных технологических сбоев. При переходе на иные сырьевые ресурсы или при изменении технологии вновь образующиеся отходы нуждаются в установлении нового класса токсичности (опасности) по результатам нового пробоотбора.
Отбор проб ТБО, а также отходов, образующихся при их сжигании (инсинерации, пиролизе) и компостировании, необходимо проводить на предприятии не реже 4 раз в год (1 раз в квартал).
Отбор проб ПО может осуществляться периодически и непрерывно. Выбираемый способ пробоотбора зависит от количества образующегося отхода в единицу времени (за один производственный цикл, сутки, год), аппаратурного оформления технологического процесса, методов сбора и накопления отхода, предполагаемой токсичности (на основании сопоставления с изученными отходами аналогичных производств).
При периодическом пробоотборе объединенная проба образуется из нескольких точечных проб, отобранных в одно и то же время из одного и того же источника образования или накопления отходов (из бункера, хвостохранилища, ковша, шламонакопителя, отвала, свалки, карьера и др.). Единичные пробы отбираются в местах хранения или захоронения отходов по равномерной сети опробования.
Отбор проб производят из горных выработок (расчисток, закопушек, канав, шурфов) или скважин, пройденных с помощью буровых станков, установок или приспособлений различных конструкций. Кроме того, в местах хранения отходов, являющихся источником образования пыли, проводят измерения загрязнения воздушной среды.
В зависимости от целей исследования различают периодический пространственный, периодический глубинный и периодический смешанный пробоотбор. При периодическом пробоотборе, как правило, имеют дело с большим исходным объемом отхода (более 1 т).
Для осуществления пространственного пробоотбора намечают пробную площадку в виде квадрата со сторонами не менее 10 м. Затем отбирают с поверхности по схеме конверта 5 единичных проб (ГОСТ 17.4.4.02-84). На каждые 20 га накопителя (хранилища, свалки) закладывают не менее одной пробной площадки. Если территория накопителя составляет менее 0,5 га, размер пробной площадки должен быть не менее 5×5 м. Из единичных проб, отобранных с одной пробной площадки, приготавливают одну объединенную промежуточную пробу. Смесь объединенных промежуточных проб образует объединенную пробу, направляемую на исследование.
Осуществляя глубинный пробоотбор. руководствуются ориентировочной глубиной хранилища и количеством одноразово загружаемых в него отходов.
Смешанный пробоотбор заключается в отборе проб из кучи. При отборе проб из кучи рекомендуется отбирать одну единичную пробу с ее вершины (если это возможно осуществить), не менее четырех единичных проб из равноудаленных друг от друга точек основания кучи и произвольное количество точечных проб с ее боковой поверхности. Общее число проб, отбираемое из кучи высотой до 2 м, должно быть не менее 9. При увеличении высоты кучи на 1 м минимально необходимое число проб увеличивается на 4.
При непрерывном пробоотборе объединенная проба отхода образуется из нескольких (не менее 2-х) единичных проб, отобранных в одном и том же месте через одинаковые промежутки времени (час, сутки, месяц).
Количество отбираемых отходов может выражаться в единицах массы (грамм, килограмм) или в единицах объема (литры). Единицы массы используются для характеристики количества твердых сыпучих отходов. Единицы объема наиболее применимы для выражения количеств жидких и полужидких отходов. Количество пастообразных отходов может быть охарактеризовано как единицами массы, так и единицами объема.
Количество и необходимый объем отбираемой пробы отхода зависит от его агрегатного состояния, влажности, степени однородности и его зернистости (для сыпучих отходов).
Объединенная проба отхода может быть приготовлена из М-го количества единичных проб или из М-го количества объединенных промежуточных проб (в случае закладки нескольких пробных площадок на территории протяженных хранилищ). Недопустимо образование объединенной пробы одновременно из единичных и объединенных промежуточных проб.
Объединенная проба отхода может быть приготовлена по принципу средневзвешенности или среднепропорциональности.
По принципу средневзвешенности объединенная проба отхода образуется путем смешения одинакового массового количества вещества. Обычно так поступают, имея дело с сыпучими твердыми и пастообразными отходами с влажностью от 30 до 70 %.
По принципу среднепропорциональности объединенная проба приготавливается из одинаковых объемов отходов. Наиболее часто таким образом готовят пробу полужидких отходов и паст с высокой влажностью (> 70 %).
Единичные пробы отходов перед объединением тщательно гомогенизируют. Обращаясь с твердыми сыпучими и пастообразными отходами, используют металлические шпатели. Полужидкие отходы гомогенизируют встряхиванием.
Для механизированной проходки скважин применяют буровые станки и установки различных способов бурения (вращательного, ударно-канатного, пневмоударного, шнекового) и самых различных конструкций, обеспечивающих представительный отбор проб. Шурфы также могут проходиться механизированным способом.
Для ручной проходки скважин применяют буры и щупы различных конструкций.
Отбор единичных проб проводят по равномерной сетке, размер которой выбирают в соответствии с нормативными документами, действующими на предприятии, на котором образуется отход, или определяется необходимым числом единичных проб. Число единичных проб рассчитывается, исходя из степени изменчивости нормируемых компонентов в данных отходах и заданной погрешности их определения.
Иногда, для подтверждения представительности выбранных точек пробоотбора, производят выборочное обследование точек пробоотбора.
Отбор сыпучих отходов из тары (вагон, кузов автомобиля, контейнер и др.) производят с помощью щупа. Отбор единичных проб производится погружением щупа в опробуемую массу до середины или на всю высоту тары.
Масса единичных проб устанавливается в зависимости от состава опробуемого отхода и размера максимальных частиц (кусков). Расхождение по массе отдельных единичных проб не должно превышать 20 %.
Отобранные единичные пробы соединяют в объединенную пробу или сразу после пробоотбора, или после отдельной их подготовки до определенного этапа квартования, а затем объединяют в нужных пропорциях.
Сокращение пробы в зависимости от исходной массы объединенной пробы и размера частиц (кусков) проводят строго по выбранной схеме сокращения.
Для сокращения объединенной пробы применяют метод квартования с предварительным сбрасыванием на конус. Объединенная проба отхода (при отсутствии специальных требований) должна составлять не менее 5 кг (2,5 кг для анализа и 2,5 кг для хранения дубликата).
Пробы отходов не подлежат консервированию. Пробы отходов хранят в холодильнике (в банках с притертой или плотно закрытой крышкой) не более одной недели.
Пробы отходов, поступившие в лабораторию на исследование, должны быть документально оформлены и маркированы. Необходимыми сопроводительными документами являются бланк описания отхода и протокол пробоотбора (см. Приложение 1). Маркировка отходов осуществляется произвольной форме, но с обязательным занесением обозначений в лабораторный журнал.
При проведении отбора проб отходов должны соблюдаться меры, исключающие загрязнение окружающей среды от применения бурового оборудования. Контроль за содержанием вредных веществ в воздухе рабочей зоны осуществляется в соответствии с требованиями ГОСТ 12.1.005-88. При подготовке проб должны соблюдаться меры, исключающие запыление окружающей среды, и правила захоронения (складирования) материала пробы, полученного в результате сокращения объединенной пробы.
7.5.3.2. Приготовление водной вытяжки из почв, осадков сточных вод, отходов
Водная вытяжка из осадков сточных вод и отходов готовится из соотношения «твердая фаза : жидкость» как «1:10» в соответствии с «Методикой определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний»; ФР.139.2001.00283. В качестве жидкости используется культивационная вода (допускается использование дистиллированной воды).
Твердые отходы и осадки сточных вод. Проба тщательно перемешивается сначала перекатыванием на гладкой, гибкой и плотной подстилке, затем - совком. Для пробоподготовки пробы отходов требуется 2,5 кг, пробы осадков сточных вод-1 кг. Общий объем отобранной пробы (5 кг отходов или 2 кг осадков) делится на представительные половины, одна из частей возвращается в сосуд для хранения, оставшаяся часть разрыхляется и тщательно просматривается. В случае обнаружения частиц более 10 мм их осторожно измельчают с помощью металлического шпателя до размера менее 10 мм. Недопустимо механически размалывать смесь. Затем проба высушивается до воздушно-сухого состояния, как указано в п. 7.5.2.2. При плохом высыхании отхода экспозицию высушивания допускается увеличивать до 24 часов.
После этого проба сокращается 3 - 4 раза методом квадратирования. Тщательно перемешанную пробу разравнивают на гладкой ровной поверхности на крафт-бумаге, клеенке или полиэтиленовой пленке и с помощью линейки или специальной решетки делят на равные квадраты. Затем из квадратов в шахматном порядке отбирают порции, обеспечивая захват всей толщины слоя, и объединяя порции в пробу с минимальной абсолютно-сухой массой 200 г представительной пробы, которая делится на две части и предназначается для биотестирования и определения влажности.
Влажность осадков и отходов определяется по п. 7.5.2.2. Измеренная характеристика влажности используется для расчета массы воздушно-сухой пробы, предназначенной для приготовления водной вытяжки. Обычно требуется 120 - 200 г воздушно-сухой массы пробы. После выщелачивания 100 г абсолютносухой массы пробы будет получено приблизительно 900 см3 водной вытяжки. Учитывая это, следует рассчитать общее необходимое минимальное количество отбираемой порции с учетом процедуры сокращения пробы. Масса пробы на стадии перед приготовлением водной вытяжки должна быть достаточной для получения необходимого объема экстракта для проведения биотестирования во всех предполагаемых разведениях. Проба осадков, отходов в воздушно-сухом состоянии взвешивается так, чтобы абсолютно сухая масса была 100 ± 1 г. Массу и содержание влаги записывают, проба помещается в сосуд для выщелачивания.
Шламы. Шламы с большим содержанием твердой фазы, не разделяющиеся самостоятельно, обрабатываются так же, как твердые отходы. Отдельно определяется содержание влаги. Масса шлама, эквивалентная 100 ± 1 г абсолютно-сухой массы используется для приготовления водной вытяжки.
Шламы с большим содержанием жидкости (влажность более 70 %) обрабатываются следующим образом. Жидкость фильтруется через вакуумный фильтр (0,45 мкм), собирается 300 г влажно-твердого материала. Если такого количества пробы недостаточно для получения 200 г абсолютно сухого вещества, собирается столько, сколько необходимо. Пробы высушиваются до воздушносухого состояния по п. 7.5.2.2. При плохом высушивании экспозицию допускается увеличить до 24 ч.
Проба делится на две части, в одной определяется содержание влаги, а другая часть, составляющая 100 ± 1 г абсолютно-сухой массы, переносится в сосуд для выщелачивания. В рабочем журнале регистрируется масса остатка и содержание влаги в нем. Твердые шламы выщелачиваются культивационной водой в пропорции 1:10.
Жидкие отходы. Жидкие и содержащие менее 1 % взвешенного материала отходы и осадки сточных вод не подвергаются выщелачиванию, а испытываютсяпрямо на экотоксичность методами биотестирования после фильтрации через фильтр «белая лента».
Выполнение процедуры подготовки экстракта выщелачивания. В сосуд для выщелачивания, где находится взвешенная воздушно-сухая масса отхода или осадка сточных вод с абсолютно-сухой массой 100 ± 1 г, добавляется вода, используемая для культивирования (или дистиллированная вода). Вода добавляется в сосуд для выщелачивания в соотношении «сухая масса: жидкость» - «1:10». Обычно это 1000 см3 воды на 100 г абсолютно-сухой массы. Если используется меньшее количество пробы, уменьшается количество жидкости. Нельзя использовать для выщелачивания менее чем 20 г твердого вещества и 200 см3 воды. Объемы воды более 10 см3 измеряются мерным цилиндром, объемы меньше 10 см3 - мерной пипеткой.
Смесь должна перемешиваться слабо на мешалке в течение 7 - 8 часов таким образом, чтобы твердое вещество находилось во взвешенном состоянии. Недопустимо измельчение частиц отходов или осадков при перемешивании. Используется большая лопасть механической мешалки или магнитная мешалка, а скорость перемешивания должна быть наименьшей, при которой материал поддерживается во взвешенном состоянии (не более 70 об/мин).
После окончания перемешивания раствор с осадком оставляют на ночь (12 - 18 ч) для отстаивания. Затем жидкость над осадком сифонируется.
Если после отстаивания жидкость становится прозрачной, фильтрование не требуется; если же имеется какой-либо видимый взвешенный материал, то жидкость должна быть профильтрована. В случае применения фильтрования это отмечается в рабочем журнале. Фильтрация осуществляется через фильтр «белая лента» на воронке Бюхнера. Для фильтрации применяется слабый вакуум (не более 20 мм рт.ст.) с помощью водяного или электрического насоса такой же мощности. Вакуум должен быть выключен немедленно после прохождения всей жидкости через фильтр во избежание дегазации фильтрата. В исключительных случаях при повышенной мутности водной вытяжки из отхода после фильтрации допускается ее отстаивание в холодильнике до 5 суток. Затем жидкость над осадком сифонируется.
Полученный экстракт выщелачивания исследуют на токсичность. Процедуру биотестирования необходимо начать не позднее, чем через 6 ч после приготовления вытяжки из осадка, отхода. Если это невозможно, допускается хранение экстракта в холодильнике не более 48 ч при температуре 4 °С. Перед биотестированием необходимо измерить pH, температуру и содержание 02 в полученном экстракте.
Водная вытяжка из осадков сточных вод или отходов должна иметь pH = 7,0 - 8,2. При необходимости пробы нейтрализуют. После нейтрализации пробы аэрируют 10 - 20 мин для стабилизации pH. Перед биотестированием температуру пробы доводят до 20 ± 2 °С. Биотестируемая проба водной вытяжки из осадков и отходов должна иметь концентрацию растворенного кислорода не ниже 6 мг/дм3, в противном случае пробу аэрируют. Данные регистрируют в журнале. Приготовление разведений водной вытяжки для биотестирования проводят по п. 7.5.1.3.
Если осадки сгонных вод или отходы были разделены на жидкую и твердую фракции, результаты исследования жидкой фракции и экстракта выщелачивания из твердой фракции должны быть указаны в отчете отдельно. Если одна из этих частей была признана токсичной, токсичным признается весь отход.
8. ПРОЦЕДУРА БИОТЕСТИРОВАНИЯ
Для определения острого токсического действия проводится биотестирование исходной исследуемой воды или водной вытяжки из почв, осадков сточных вод. отходов и нескольких их разбавлений, приготовленных по п. 7.5.1.2.
Определение токсичности каждой пробы без разбавления и каждого разбавления проводится в трех параллельных сериях. В качестве контроля используется три параллельные серии с культивационной водой. Биотестирование проводится с соблюдением требований к температуре, продолжительности фотопериода и качеству культивационной воды по пунктам 7.2.
Биотестирование проводится в пробирках объемом 100 см3, которые заполняются 50 см3 исследуемой воды. В пробирки помещают по десять дафний в возрасте 6 - 24 ч. Чувствительность дафний к токсикантам зависит от возраста рачков, поэтому в протоколе отмечают возраст используемой молоди. Возраст определяется по размеру рачков. Дафний отлавливают из емкостей, в которых выращивается синхронизированная культура. В отдельный химический стакан отсаживают одновозрастных рачков, а затем отлавливают по одному пипеткой (с отпиленным и оплавленным концом) объемом 2 см3 с резиновой грушей. Помещают рачков по одному на сачок, через который вода сливается в отдельный химический стакан, после чего дафний сачком вносят в пробирки с исследуемой водой.
Посадку рачков начинают с контрольной серии. В исследуемые растворы дафний помещают, начиная с больших разбавлений (меньших концентраций загрязняющих веществ) к меньшим разбавлениям. После каждой посадки в исследуемые растворы сачок тщательно промывается в сосуде объемом 2 дм3 с культивационной водой. Для работы с серией контроля должен быть отдельный сачок.
Для каждой серии исследуемой воды используется 3 пробирки. Общее количество пробирок, используемых в опытах, равно утроенной сумме всех разбавлений плюс 3 для исходной воды и 3 для контроля.
В экспериментах по определению острой токсичности дафний кормят только перед началом эксперимента до отсадки рачков в пробирки с тестируемой водой. Во время опыта корм в пробирки с тестируемой водой не добавляют.
Пробирки с пробами воды и тест-организмами помещаются во вращающуюся кассету устройства для экспонирования рачков УЭР-02 (03). Благодаря вращению кассеты происходит непрерывная и одинаковая аэрация всех тестируемых проб. При этом выбранная скорость вращения (6 - 8 оборотов в минуту) не создает стрессовой ситуации для самих рачков.
Учет смертности дафний в опыте и контроле проводят каждые 24 часа. Опыт прекращается, если в течение 24 часов во всех вариантах (разбавлениях тестируемой воды) наблюдается гибель более 50 % рачков. Неподвижные особи считаются погибшими, если не начинают двигаться в течение 15 секунд после легкого покачивания пробирки.
В экспериментах по определению острой токсичности растворы не меняют. Результаты наблюдений заносят в рабочий журнал (см. Приложение 2). Если наблюдается гибель дафний в контроле, результаты опыта не учитывают, и он должен быть повторен.
После того, как результаты эксперимента учтены, в каждой пробирке проводят измерения pH. Температура в пробирках должна соответствовать (20 ± 2)°С, а pH 7,0 - 8,2. Все отклонения от установленных норм, а также данные по каждой серии разбавлений, исходной воды и контролю также заносят в рабочий журнал и протокол результатов эксперимента.
9. ОЦЕНКА РЕЗУЛЬТАТОВ ТОКСИКОЛОГИЧЕСКОГО АНАЛИЗА
9.1. При определении острой токсичности питьевых, сточных, поверхностных, грунтовых вод, а также водных вытяжек из почв, осадков сточных вод, отходов и их разбавлений устанавливают:
• среднюю летальную кратность разбавления вод. водных вытяжек,
вызывающую гибель 50 % тест-объектов за 48-часовую экспозицию (ЛКР50-48);
• безвредную кратность разбавления вод, водных вытяжек, вызывающую гибель не более 10 % тест-объектов за 48-часовую экспозицию (БКР10-48).
9.2. Для определения острой токсичности исследуемых вод, водной вытяжки рассчитывается процент погибших в тестируемой воде дафний (А. %) по сравнению с контролем:
|
|
(2) |
где ХК - количество выживших дафний в контроле; ХТ - количество выживших дафний в тестируемой воде.
При А ≤ 10 % тестируемая вода или водная вытяжка не оказывает острого токсического действия. Этот % погибших рачков используется для расчета безвредной кратности разбавления тестируемых вод. При А ³ 50 % проба воды, водная вытяжка оказывает острое токсическое действие. Этой величиной руководствуются при определении средней летальной кратности разбавления тестируемых вод, например, при установлении класса опасности отходов.
9.3. Если экспериментально не удалось получить точного значения кратности разбавления, вызывающей 50 %-ную гибель дафний за 48 часов экспозиции, то для получения значения ЛКР50-48 без выполнения дополнительных экспериментов используется графический метод определения.
9.3.1. Графический метод определения ЛКР50-48
Чтобы получить на графике линейную зависимость, используется пробит- анализ. Результаты экспериментов по установлению острого токсического действия из рабочего журнала (см. Приложение 2) заносят в табл. 2. Значения пробитов устанавливают по табл. 3. В табл. 4 вносят значения пробитов для экспериментально установленного процента гибели дафний (см. табл. 2, 3) и значения десятичных логарифмов для исследованных концентраций сточных вод, водных вытяжек из почв, осадков сточных вод, отходов.
По значениям пробитов (см. табл. 3) и десятичных логарифмов от экспериментально полученных данных (табл. 2) строится график (рис. 1). По оси абсцисс откладываются значения логарифмов процентных концентраций исследуемых вод, по оси ординат - пробиты от значений процента гибели дафний. Экспериментально полученные значения вносятся в систему координат и через точки проводится прямая.
Таблица 2
Форма записи результатов определения острой токсичности сточной воды
Таблица 3
Значения пробитов для экспериментально устанавливаемой гибели дафний от 0 до 99 %
|
Гибель, % |
0 |
1 |
2 |
4 |
5 |
6 |
7 |
8 |
9 |
|
|
0 |
- |
2,67 |
2,95 |
3,12 |
3,25 |
3,35 |
3,45 |
3,52 |
3,59 |
3,66 |
|
10 |
3,72 |
3,77 |
3,82 |
3,83 |
3,92 |
3,96 |
4,01 |
4,05 |
4,08 |
4,12 |
|
20 |
4,16 |
4,19 |
4,23 |
4,26 |
4,29 |
4,33 |
4,36 |
4,39 |
4,42 |
4,45 |
|
30 |
4,48 |
4,50 |
4,53 |
4,56 |
4,59 |
4,61 |
4,64 |
4,67 |
4,69 |
4,72 |
|
40 |
4,75 |
4,77 |
4,80 |
4,82 |
4,85 |
4,87 |
4,90 |
4,92 |
4,95 |
4,97 |
|
50 |
5,00 |
5,03 |
5,05 |
5,08 |
5,10 |
5,13 |
5,15 |
5,18 |
5,20 |
5,23 |
|
60 |
5,25 |
5,28 |
5,31 |
5,33 |
5,36 |
5,39 |
5,40 |
5,44 |
5,47 |
5,50 |
|
70 |
5,52 |
5,55 |
5,58 |
5,61 |
5,64 |
5,67 |
5,71 |
5,74 |
5,77 |
5,81 |
|
80 |
5,84 |
5,88 |
5,92 |
5,95 |
5,99 |
6,04 |
6,08 |
6,13 |
6,18 |
6,23 |
|
90 |
6,28 |
6,34 |
6,41 |
6,48 |
6,55 |
6,64 |
6,75 |
6,88 |
7,05 |
7,33 |
Таблица 4
Значения десятичных логарифмов для исследованных концентраций сточных вод и пробитное значение от экспериментально установленного процента гибели дафний
|
Концентрация сточных вод (С), % |
Количество погибших дафний, % |
Пробитное значения для % гибели дафний |
|
|
6,25 |
0,7959 |
0 |
- |
|
12,5 |
1,0969 |
10 |
3,72 |
|
25 |
1,3980 |
60 |
5,25 |
|
50 |
1,6990 |
80 |
5,84 |
|
100 |
2,0000 |
93 |
6,48 |
По значениям пробитов и логарифмам чисел, взятых из табл. 4, строится график (рис. 1).
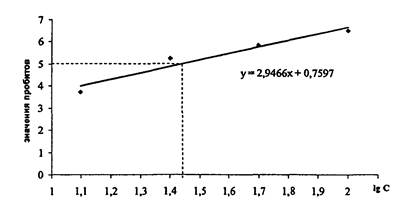
Рис. 1. Линейная зависимость пробигного значения гибели дафний от логарифма концентраций исследуемых сточных вод
На графике параллельно оси логарифмов концентраций (lgC) проводится прямая из точки, соответствующей пробитому значению 5, что соответствует 50 %-ной гибели дафний (см. табл. 3). Из точки пересечения прямых с графиком зависимости пробитного значения ингибирования тест-параметра от логарифма концентраций опускают перпендикуляр на ось логарифма концентраций и получают значение логарифма концентрации исследуемых вод, водных вытяжек, соответствующей JIKP50-48. Далее логарифм концентрации переводят в процентную концентрацию.
Для нахождения точных значений величин логарифмов концентраций, соответствующих 50 %-ному ингибированию тест-параметра, график строят в программе Excel (пакет Microsoft Office). Для этого после запуска данной программы ввести из таблицы 4 в двух отдельных колонках значения логарифма % разбавления тестируемой воды и соответствующие им значения пробитов. Затем включить «мастер диаграмм», указав в опции «тип диаграммы» параметр «точечная». В строке «диапазон» внести значения колонки с пробитами, выделив саму колонку. В ряд х аналогичным образом вносятся значения логарифма % концентрации. Уравнение прямой, описывающее взаимосвязь между этими величинами, получают следующим образом: в параметре «диаграмма» указывается команда «добавить линию тренда». В опции «линия тренда», «тип» указывается «линейная», в опции «линия тренда», «параметры» помечается галочкой окошко «уравнение на диаграмме».
Из уравнения линии тренда (у = kх+b) получаем значения величин х = (у - b)/k = lgC, соответствующие величинам у (значениям пробитов). Так, для приведенного примера логарифм концентрации исследуемой воды, вызывающей 50 % -ное ингибирование тест-параметра за 48 часов экспозиции (у = 5,0), рассчитывается как:
х = (5,0 - 0,7597)/2,9466 = 1,439.
Отсюда, С50-48 = 101,439 = 27,54 %. Таким образом, устанавливается, что 27,54 %-ная концентрация исследуемой сточной воды или ее разбавление в 3,63 раза (100 %/27,54 %) вызывает 50 %-ную гибель тест-объектов за 48 часов (ЛКP50-48 = 3,63).
Аналогичным образом рассчитывается безвредная кратность разбавления (БКР10-48). вызывающая 10 %-ное ингибирование тесг-параметра за 48 часов экспозиции (у = 3,72):
х = (3,72 - 0.7597)/2,9466 = 1,005.
Отсюда, С10-48 = 101,005= 10,11 %., т.е. эта концентрация исследуемой сточной воды или ее разбавление в 9,9 раза (100 %/10, 11 %) вызывает 10 %-ную гибель тест-объектов за 48 часов (БКР10-48 = 9,9).
Все полученные расчеты, график по результатам острого эксперимента вносят в рабочий журнал и заполняются графы 12, 13 в Приложении 2.
10. КОНТРОЛЬ ЧУВСТВИТЕЛЬНОСТИ ТЕСТ-ОРГАНИЗМОВ К МОДЕЛЬНОМУ ТОКСИКАНТУ
Контроль определения токсичности воды проводится один раз в квартал по модельному токсиканту - калию двухромовокислому (К2Сr2О7). Диапазон концентраций модельного токсиканта, при действии которого в течение 24 часов гибнет 50 % дафний, составляет 0,9 - 2,0 мг/дм3. Удовлетворительные результаты, полученные при проверке диапазона реагирования тест-организмов на модельный токсикант, не обеспечивают гарантии адекватного реагирования организмов на другие токсиканты и тем более их смеси, однако регулярно проводимая проверка позволяет выявить ошибки при приготовлении исследуемых смесей и растворов, нарушения, допускаемые в процессе культивирования организмов и условий проведения опытов.
Процедура определения диапазона реагирования тест-организмов на модельный токсикант. Определяют ту концентрацию модельного токсиканта, при которой за 24 часа гибнет 50 % подопытных организмов. Для этого на основании стандарт-титра методом последовательных разбавлений готовят серию растворов двухромовокислого калия в культивационной воде с концентрациями 0,5; 1,0; 1,5; 2,0; 2,5 мг/дм3. Испытания на дафниях проводят в соответствии с прописью методики.
Если концентрация двухромовокислого калия, вызвавшая острую токсичность за 24 часа, находится в интервале 0,9 - 2,0 мг/дм3, то чувствительность культуры дафний соответствует необходимым требованиям, и она может быть использована в биотестировании.
Если концентрация модельного токсиканта, вызвавшая острую токсичность, не находится в данном интервале, то следует проверить точность приготовления исследуемых растворов и условия проведения опытов. Если ошибки при проведении опытов исключены, необходимо сменить культуру тест-организмов, т.е. взять новую культуру в учреждениях, где она имеется.
В тех случаях, когда чувствительность дафний не укладывается в установленный диапазон по причине ухудшения качества водопроводной воды, используемой для приготовления культивационной воды, например, в период весенних паводков, то культура дафний не меняется. Проводятся мероприятия по улучшению качества культивационной воды, включая разбавление культивационной воды в 1.5 - 3 раза дистиллированной водой (п. 7.2).
11. ОБРАБОТКА И ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ ТОКСИКОЛОГИЧЕСКОГО АНАЛИЗА
За результат токсикологического анализа принимают среднее арифметическое значение трех результатов параллельных определений, расхождение между наибольшим и наименьшим значениями из которых, выраженное в процентах по отношению к среднему значению, не должно превышать предела повторяемости. Значения предела повторяемости (r) для трех результатов параллельных определений приведены в таблице 6. Если размах (Xmax - Xmin) больше (r), выясняют причины появления неприемлемых результатов параллельных определений.
Расхождение между минимальными и максимальными значениями измерений, выраженное в процентах по отношению к среднему значению данных, полученных в двух лабораториях для одной пробы воды, не должно превышать предела воспроизводимости (R). При выполнении этого условия приемлемы оба результата измерений, и в качестве окончательного результата может быть использовано их общее среднее значение. Величины предела воспроизводимости приведены в таблице 6.
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости согласно разделу 5 ГОСТ Р ИСО 5725-2002, часть 6.
Таблица 6
Примечание: при представлении результата токсикологического анализа в документах, выдаваемых лабораторией, указывают:
- количество результатов параллельных определений, использованных для расчета результата анализа;
способ определения результата токсикологического анализа (среднее арифметическое значение или медиана параллельных определений).
БИБЛИОГРАФИЯ
ГОСТ 24481-80 Вода питьевая. Отбор проб.
ГОСТ 17.1.5.04-81 Охрана природы. Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Обшие технические условия.
ГОСТ 17.4.3.01-83 Охрана природы. Почвы. Общие требования к отбору проб.
ГОСТ 17.4.4.02-84 Почвы. Методы отбора и подготовки проб для химического, бактериологического, гельминтологического анализа.
ГОСТ 12071-84 Грунты, Отбор, упаковка, транспортирование и хранение образцов.
ГОСТ 5180-84 Грунты. Методы лабораторного определения физических характеристик.
ГОСТ 2517-85 Нефть и нефтепродукты. Методы отбора проб.
ГОСТ 17.4.3.03-85 (СТ СЭВ 4469-84) Почвы. Общие требования к методам определения загрязняющих веществ.
ГОСТ 26423-85 - ГОСТ 26428-85 Почвы. Методы определения катионноанионного состава водной вытяжки.
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков.
ГОСТ 27753.1-88 Грунты тепличные. Методы отбора проб.
ГОСТ 28168-89 Почвы. Отбор проб.
ГОСТ Р 52029-2003 Вода. Единица жесткости.
ГОСТ Р 8.563-96 ГСИ. Методики выполнения измерений.
ГОСТ Р 50.2.008-2001 ГСОЕИ Методики количественного химического анализа. Содержание и порядок проведения метрологической экспертизы.
МУ 2.1.7.730-99 Гигиеническая оценка качества почвы населенных мест. - Минздрав России, М.,1999.
НВН 33-5.3.01-85 Инструкция по отбору проб для анализа сточных вод.
СТ СЭВ 4710-84 Воды подземные. Общие требования к отбору проб.
Аринушкина Е.В. Руководство по химическому анализу почв. - М.: Изд-во МГУ, 1970.-488с.
Жмур Н.С. Методика определения токсичности воды и водных вытяжек из почв, осадков сточных вод, отходов по смертности и изменению плодовитости дафний. -ФР.1.39.2001.00283. М.: АКВАРОС, 2001. - 48 с.
Исакова Е.Ф., Колосова Л.В. Метод биотестирования с использованием дафний // Методы биотестирования вод: Сб. ст. / АН СССР. - Черноголовка, 1988.-С. 50-57.
Плохинский Н.А. Математические методы в биологии. Учебно-методическое пособие. - М.: Изд-во МГУ, 1978. - 340 с.
Приложение 1
(рекомендуемое)
Протокол отбора проб №_____
|
1 |
Дата и время отбора |
|
||||||||||
|
2 |
Цель пробоотбора |
|
||||||||||
|
3 |
Место отбора (наименование точки отбора) |
|
||||||||||
|
4 |
Анализируемый объект |
Вода, почва, осадки сточных вод, отходы (нужное подчеркнуть) |
||||||||||
|
5 |
Вид пробы |
Разовая, среднесуточная, точечная, объединенная (нужное подчеркнуть) |
||||||||||
|
6 |
Вид отбора пробы |
Параллельный, последовательный (нужное подчеркнуть) |
||||||||||
|
7 |
Используемый пробоотборник |
Стеклянный, эмалированный, нержавеющая сталь, бур почвенный, щуп, лопата (нужное подчеркнуть) |
||||||||||
|
8 |
Номер на емкости |
|
||||||||||
|
9 |
Материал емкости |
Полиэтилен, стекло, нержавеющая сталь (нужное подчеркнуть) |
||||||||||
|
10 |
Наличие и способ опломбирования емкости |
|
||||||||||
|
11 |
Проба отобрана для проведения анализа |
На токсичность методом биотестирования |
||||||||||
|
12 |
Условия отбора |
t, ℃ |
pH |
O2 |
||||||||
|
Примечание |
||||||||||||
|
||||||||||||
Приложение 2
(рекомендуемое)
Форма регистрации условий и результатов биотестирования в рабочем журнале
|
1 |
Дата, время отбора проб |
1130 ч, 10 февраля 2011 г. |
|
2 |
Место отбора |
Очистные сооружения г. Красноярска. Очищенная сточная вода, выходящая из вторичного отстойника |
|
3 |
Используемые тест-организмы, возраст |
Дафнии возраст 6 - 24 ч. |
|
4 |
Оборудование и условия биотестирования |
Климатостат Р2, t = 20 ± 1 °С, фотопериод: 12 ч. - световой, 12 ч. - ночной, освещенность искусственная (1400 лк) |
|
5 |
Время хранения пробы от отбора до начала биотестирования |
4 ч |
|
6 |
Режим кормления |
10 см3 суспензии водорослей хлорелла на 200 см3 синхронной культуры |
|
7 |
Повторности для каждого разбавления воды |
Три |
|
8 |
Исследуемые концентрации сточных вод |
6,25; 12,5; 25; 50; 100 % |
|
9 |
Соответствующая степень разбавления сточных вод |
Разбавления в 16; 8; 4; 2; 1 (без разбавления) раз |
|
10 |
t, pH исследуемой воды |
Измерения перед началом биотестирования и при завершении экспериментов- все показатели в пределах установленных в методике оптимальных значений |
|
11 |
Средняя летальная кратность разбавления в остром опыте ЛКР5СМ8. |
27, 54 %-ная концентрация сточных вод или кратность разбавления в 3,63 раз |
|
12 |
Безвредное разбавление в остром опыте БКР КМ8 |
10, 11 %-ная концентрация сточных вод или кратность разбавления в 9,9 раз |
|
13 |
Данные гидрохимических анализов исследуемой воды |
В приложении к акту проверки |
Приложение 3
(рекомендуемое)
Наименование организации_________________________________________________
Наименование объекта_____________________________________________________
Биотестируемая среда______________________________________________________
Условия отбора и транспортировки проб______________________________________
Пробы отобраны (Ф. И. О., должность)_______________________________________
Дата отбора проб__________________________________________________________
Дата доставки проб________________________________________________________
Используемая МВИ________________________________________________________
РЕЗУЛЬТАТЫ БИОТЕСТИРОВАНИЯ
|
№ п/п |
Дата биотестирования |
Место отбора проб |
Тестируемая проба |
Тест-объект |
Продолжительность наблюдения (ч, суг) |
Оценка тестируемой пробы |
|
|
Дафния |
Оказывает (не оказывает) острое токсическое действие. Безвредная кратность разбавления |
||||||
|
Биотестирование проводил________ _______________________________________ |
|||||||
|
подпись |
расшифровка подписи |
||||||
|
Заключение_____________________________________________________________ ________________________________________________________________________ ________________________________________________________________________ ________________________________________________________________________ ____________________________________________ |
|||||||
|
Начальник организации___________ _______________________________________ |
|||||||
|
подпись |
расшифровка подписи |
||||||
Приложение 4
(справочное)
В качестве тест-объекта используется Daphnia magna Straus. Относится к низшим ракообразным, отряду ветвистоусых. Дафнии обитают в планктоне стоячих и слабопроточных пресноводных водоемов, широко распространены на территории России.
Морфология. Тело дафний овальной формы, сжато с боков, заключено в прозрачный панцирь. Тело нечетко сегментировано на головной, грудной и брюшной отделы (рис. 2). Голова покрыта щитом, передний край которого вытянут, образуя рострум. Под рострумом расположены две пары конечностей: антеннулы и антенны, последние сильно развиты, служат для скачкообразного перемещения в толще воды. Пять пар грудных конечностей сильно расчленены, снабжены щетинками, служат для фильтрации воды, питания, дыхания. Брюшной (абдоминальный) отдел туловища заканчивается постабдоменом, дорсальный край которого имеет выемку, характерную для дафний данного вида. Расположение внутренних органов представлено на рис. 2. В головном отделе, не покрытом раковиной, расположена пара глаз: большой - сложный, маленький - простой. Под панцирем дафний легко различимы сердце, кишечник, выводковая камера, которая находится в спинной части туловища. В выводковой камере протекает эмбриональное развитие дафний.
Рост, развитие и размножение. Наиболее интенсивно дафния растет первые дни после рождения, при каждой линьке сбрасывая старый панцирь. Оптимальное питание обеспечивает удвоение размеров рачков в промежутке между линьками. После наступления половой зрелости рост дафний замедляется, снижается и частота линек. Всего в течение жизни дафния может линять до 24 раз. Выметанная молодь имеет в длину 0,7 - 0,9 мм, половозрелые самки - 2,2 - 2,4 мм, самцы - 2,0 - 2,1 мм. Максимальные размеры самок - 6,0 мм при сыром весе 7 - 10 мг. В природе в летнее время, а в лаборатории при оптимальных условиях культивирования круглый год дафнии размножаются без оплодотворения - партеногенетически (рождаются только самки). При резком изменении условий существования или культивирования (похолодание, голод, перенаселенность и т.п.) в культуре появляются самцы. Самцы отличаются от самок меньшими размерами, видоизмененной формой тела, антеннул, постабдомена. Резкое изменение условий существования вызывает переход к половому размножению, дафнии откладывают «зимние яйца», размещающиеся в эффипиуме, образованном из часта створок панциря. При очередной линьке эффипиум отделяется (в природе- осенью), падает на дно водоема, где яйца проходят стадию зимнего покоя. Весной из них появляются самки, снова переходящие к партеногенетическому размножению.
Период созревания рачков при оптимальной температуре (+20 ± 2 °С) и хорошем питании - 5 - 8 суток, длительность эмбрионального развития - 3 - 4 суток, а при повышении температуры до 25 °С - 46 часов. Затем происходит вымет молоди (партеногенетических самок) каждые 3 - 4 суток. Количество молоди у молодых самок - 10 - 15, у зрелых - 30 - 40 особей. В природе дафнии живут в среднем 20 - 25 суток, а в лаборатории при оптимальном режиме 3 - 4 месяца и более. При температуре свыше 25 °С продолжительность жизни дафний может сокращаться до 25 суток. Голодание увеличивает продолжительность жизни, но задерживает рост и наступление линек.
Питание и отношение к содержанию кислорода. По характеру питания относятся к фильтраторам, в природе дафнии питаются взвешенными в воде бактериями, одноклеточными водорослями, детритом, растворенными органическими веществами. Пища поступает с потоком воды, направленным грудными конечностями, через выросты - в брюшной желоб вдоль основания конечностей и ко рту рачка. Оптимальное для жизнедеятельности дафний содержание растворенного в воде кислорода - 6 - 7 мг/дм3. Однако дафния достаточно устойчива к изменению кислородного режима и снижению растворенного в воде кислорода до 2 мг/дм3 и ниже, что связано с ее способностью синтезировать гемоглобин. Повышенное содержание гемоглобина в крови дафний при ухудшении кислородного режима сопровождается окрашиванием рачков в красный цвет.
Рис. 2. Строение Daphnia magna Straus: а - самка: 1 - антенна, 2 - сложный глаз, 3 - антеннула, 4 - грудные ножки, 5 - яичник, б - створки панциря, 7 - каудальные когти, 8 - постабдомен, 9 - хвостовые щетинки, 10 - выводковая камера, 11 - сердце, 12 - кишечник, 13 - печеночные выросты; б - самец; в - внешний вид эффипиума
Приложение 5
(обязательное)
Выращивание культуры водорослей
Выращивание культуры водоросли хлорелла (Chlorella vulgaris Beijer) производится в разработанном в Сибирском федеральном университете культиваторе КВ-05. В качестве реактора используется прозрачная бутыль из бесцветного стекла емкостью 400 см3, широко используемая в медицине при переливании препаратов. В реактор заливается суспензия водоросли в объеме (125 ± 10) см3. Для обеспечения углекислым газом емкость с суспензией непрерывно вращается вокруг своей продольной оси. Благодаря этому поддерживается близкое к равновесному содержание СО2 в культуральной среде за счет активного растворения содержащейся в воздухе углекислоты.
В процессе культивирования суспензия водоросли облучается светом лампы накаливания 40 Вт, 220В, установленной в приборе над реактором. Постоянная температура среды, равная (36,0 ± 0,5) °С, поддерживается автоматическим включением и выключением встроенного вентилятора по команде блока термостабилизации прибора.
Питательная среда Тамия для культивирования водоросли хлорелла
Растворы А и Б готовятся отдельно, раствор А (Н3ВО3 - 2,86 г/дм3; MnСl2×4Н2О - 1,81 г/дм3; ZnSO4×5Н20 - 0,222 г/дм3) и раствор Б (МоО3 - 17,64 мг/дм3; NH4VO3, - 22,96 мг/дм3). Затем отдельно стерилизуют каждый раствор 30 мин кипячением, охлаждают, плотно закрывают притертой пробкой и хранят в холодильнике при температуре от +2 до +4 °С до трех месяцев.
Культура водоросли для кормления дафний выращивается на 5 % питательной среде Тамия*, состав которой представлен в таблице. Питательная среда и растворы всех солей готовятся на дистиллированной воде. Для избежания образования осадка навеску каждого вещества сначала растворяют в небольшом количестве воды (50 - 100) см3, а затем растворы сливают вместе в указанной последовательности и доливают воду до объема 1 дм3.
___________________
*Допустимо использовать для кормления дафний культуру водоросли хлорелла, выращенную на более концентрированной среде Тамия (напимер., 50 %). В этом случае клетки водоросли должны быть отделены от питательной среды центрифугированием и ресуспензированы в небольшом количестве культивационной воды.
При систематическом потреблении культуры водоросли питательную среду удобнее готовить не из навесок солей, а из их концентрированных растворов (см. табл.). При приготовлении 1 дм3 5 % питательной среды Тамия эти растворы последовательно вносятся в указанном объеме в 0,5 дм3 дистиллированной воды. Затем добавляются заранее приготовленные растворы микроэлементов и лимоннокислого железа, а общий объем среды доводится дистиллированной водой до 1 дм3. Растворы солей и микроэлементов, а также приготовленная питательная среда хранятся в холодильнике при 2 - 4 °С не более 3 месяцев.
Засев водоросли в культиватор КВ-05 производится-с начальной оптической плотностью 0,010 ± 0,002 (кювета 2 см, l = 560 нм, прибор ИПС-03). Для этого в (110 ± 10) см3 5 % питательной среды вносится (5 ± 1) см3 суспензии водоросли с оптической плотностью 0,210 ± 0,020, профильтрованной через 3 - 4 слоя марли или вату. Культура выращивается в полустационарном режиме, который достигается ее ежедневным пересевом в свежую среду. Такой режим культивирования позволяет без соблюдения условий стерильности поддерживать альгологически чистую культуру водоросли. При перерывах в работе свежевыращенную культуру водоросли можно хранить в холодильнике при температуре (2 - 4) °С в течение 2 - 4 месяцев.