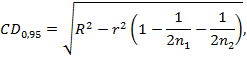ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ
В СФЕРЕ ПРИРОДОПОЛЬЗОВАНИЯ
|
УТВЕРЖДАЮ |
|
Директор ФБУ «Федеральный центр |
|
анализа и оценки техногенного воздействия» |
|
________________ В.В. Новиков |
|
17 июня 2014 г. |
КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ ВОД
МЕТОДИКА ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ
ПОЛИХЛОРИРОВАННЫХ ДИБЕНЗО-п-ДИОКСИНОВ
И ДИБЕНЗОФУРАНОВ В ПРОБАХ ПИТЬЕВЫХ, ПОВЕРХНОСТНЫХ
ПРИРОДНЫХ И ОЧИЩЕННЫХ СТОЧНЫХ ВОД МЕТОДОМ
ХРОМАТО-МАСС-СПЕКТРОМЕТРИИ
ПНДФ
14.1:2:4.251-08
(ФР.1.31.2014.17406)
Методика
допущена для целей государственного
экологического контроля
МОСКВА
(издание 2014 г.)
Методика рассмотрена и одобрена федеральным бюджетным учреждением «Федеральный центр анализа и оценки техногенного воздействия» (ФБУ «ФЦАО»).
Настоящее издание методики действует до выхода нового издания.
Главный инженер ФБУ «ФЦАО» ____________ Е.Е. Троицкая.
Разработчики:
Федеральное государственное бюджетное учреждение науки Институт проблем экологии и эволюции им. А.Н. Северцова Российской академии наук (ИПЭЭРАН).
Адрес: 119071, г. Москва, В-71, Ленинский пр., д. 33.
Телефон: (499) 135 13 80.
ФГУП Научно-технический центр радиационно-химической безопасности и гигиены ФМБА России.
Адрес: 123182, г. Москва, ул. Щукинская, д. 40.
Телефон: (499) 720 43 24.
ФГБУ «Научно-производственное объединение «Тайфун», Федеральная служба по гидрометеорологии и мониторингу окружающей среды.
Адрес: 243020, Калужская область, г. Обнинск, ул. Победы, д. 4.
Телефон: (48439) 4 39 20.
Разработчик: Федеральное государственное бюджетное учреждение науки Институт проблем экологии и эволюции им. А.Н. Северцова Российской академии наук (ИПЭЭ РАН).
Адрес: 119071, г. Москва, В-71, Ленинский пр., д. 33.
Телефон: (499) 135 13 80.
Разработчик: ФГУП Научно-технический центр радиационно-химической безопасности и гигиены ФМБА России (правопреемник Российского научно-исследовательского центра чрезвычайных ситуаций).
Адрес: 123182, г. Москва, ул. Щукинская, д. 40.
Телефон: (499) 720 43 24.
Разработчик: ФГБУ «Научно-производственное объединение «Тайфун», Федеральная служба по гидрометеорологии и мониторингу окружающей среды.
Адрес: 243020, г. Обнинск, ул. Победы, д. 4.
Телефон: (48439) 4 39 20.
Методика измерений аттестована Федеральным Государственным унитарным предприятием «Всероссийский научно-исследовательский институт метрологической службы» (ФГУП «ВНИИМС»), Свидетельство об аттестации № № 01.00225/205-3-14 от 19 Февраля 2014 г., порядковый номер регистрации в Федеральном информационном фонде по обеспечению единства измерений.
Содержание
1 Назначение и область применения
Настоящий документ устанавливает методику измерений массовых концентраций (далее концентраций) 17 высокотоксичных полихлорированных дибензо-п-диоксинов (ПХДД) и дибензофуранов (ПХДФ): 2,3,7,8-ТетраХДД; 1,2,3,7,8-ПентаХДД; 1,2,3,4,7,8-ГексаХДД; 1,2,3,6,7,8-ГексаХДД; 1,2,3,7,8,9-ГексаХДД; 1,2,3,4,6,7,8-ГептаХДД; ОктаХДД; 2,3,7,8-ТетраХДФ; 1,2,3,7,8-ПентаХДФ; 2,3,4,7,8-ПентаХДФ; 1,2,3,4,7,8-ГексаХДФ; 1,2,3,6,7,8-ГексаХДФ; 2,3,4,6,7,8-ГексаХДФ; 1,2,3,7,8,9-ГексаХДФ; 1,2,3,4,6,7,8-ГептаХДФ; 1,2,3,4,7,8,9-ГептаХДФ; ОктаХДФ в пробах питьевой воды, поверхностных природных и очищенных сточных вод методом хромато-масс-спектрометрии и расчета на их основе содержания токсичных полихлорированных дибензо-п-диоксинов и дибензофуранов с помощью установленных диоксиновых эквивалентов токсичности. Методика позволяет определять и другие изомеры ПХДД и ПХДФ, а также суммарные концентрации ПХДД и ПХДФ со степенью хлорирования от четырёх до восьми.
Всего существуют 75 различных ПХДД и 135 ПХДФ, отличающихся количеством и местом присоединения атомов хлора. Наиболее токсичными являются перечисленные выше 17 изомеров ПХДД и ПХДФ, имеющие атомы хлора, в том числе и в 2,3,7,8-положениях. Самым токсичным является 2,3,7,8-тетрахлордибензо-п-диоксин (2,3,7,8-ТХДД). Токсичность других ПХДД и ПХДФ выражается в коэффициентах токсичности (диоксиновых эквивалентах токсичности, ДЭ) - долях от токсичности 2,3,7,8-ТХДД, принятой за единицу (таблицы 2, 3 приложения 3).
Диапазон измерений массовой концентрации ПХДД и ПХДФ составляет от 0,50 до 100 пг/дм3 при объёме анализируемой пробы воды 1 - 20 дм3. Предельно допустимая концентрация 2,3,7,8-ТетраХДД в воде составляет 1 пг/дм3.
Влияние возможных мешающих соединений устраняется в процессе подготовки пробы к анализу.
2 Требования к показателям точности измерений
При соблюдении всех регламентированных условий и проведении анализа в точном соответствии с данной методикой значения погрешности (и её составляющих) результатов измерений не превышают значений, приведённых в таблице 1.
|
Диапазон измерений массовой концентрации полихлорированных дибензо-п-диоксинов и дибензофуранов, пг/дм3 |
Показатель точности (границы относительной погрешности), ±δ, % при Р = 0,95 |
Показатель повторяемости (относительное стандартное отклонение повторяемости), σr, % |
Показатель воспроизводимости (относительное стандартное отклонение воспроизводимости), σR, % |
Предел повторяемости, r, %, Р = 0,95, n = 2 |
Предел воспроизводимости, R, %, Р = 0,95, n = 2 |
|
от 0,50 до 20,0 включ. |
72 |
18 |
36 |
50 |
100 |
|
св. 20,0 до 100 включ. |
40 |
10 |
20 |
28 |
55 |
3 Требования к средствам измерений, вспомогательным устройствам, материалам, реактивам
При выполнении измерений применяют следующие средства измерений, вспомогательные устройства, материалы и реактивы.
3.1 Средства измерений
3.1.1 Хромато-масс-спектрометрическая система, включающая:
- газовый хроматограф со следующими характеристиками: температура термостата до 400 °С, скорость программирования температуры от 1 до 50 °С/мин, температура инжектора до 350 °С, температура интерфейса до 350 °С, работа с колонками диаметром от 0,1 до 0,53 мм, детектор split-splitless и/или on-column
- масс-спектрометр высокого или низкого разрешения, с диапазоном масс 50 - 600 а.е.м. электронной или химической ионизацией с детектированием отрицательных ионов, позволяющий регистрировать ионные масс-хроматограммы по номинальным (в случае низкого разрешения) или точным (до 10-3 Да в случае высокого разрешения) массам
- капиллярные хроматографические колонки длиной 25 - 60 м, и внутренним диаметром 0,15 - 0,32 мм с неполярной или слабополярной неподвижной фазой типа DB-5ms, SGE ВРХ5, Ultra-2 и др. или высокополярной неподвижной фазой типа SP 2331, CP Sil 88, DB-DIOXIN, (допускается использование и других колонок с неподвижными фазами, обеспечивающими разделение определяемых компонентов)
- компьютерную систему управления и обработки данных.
Чувствительность должна обеспечивать регистрацию не менее 0,2 пг 2,3,7,8 ТХДД при отношении сигнал/шум равном 3.
3.1.2 Весы лабораторные специального или высокого класса точности с ценой деления не более 0,1 мг, наибольшим пределом взвешивания не более 210 г по ГОСТ Р 53228-2008.
3.1.3 Микрошприцы вместимостью 10 мм3, с ценой деления 0,1 мм3 фирмы «Hamilton».
3.1.4 Термометр лабораторный с диапазоном измеряемой температуры от 0 °С до 100 °С и ценой деления 1 °С по ТУ 25-2022.0006.90.
3.1.5 Термометр лабораторный с диапазоном измеряемой температуры от 0 °С до 500 °С и ценой деления 2 °С по ТУ 25-2022.0006.90.
3.1.6 Автоматические дозаторы вместимостью от 100 до 1000 мм3, приведённая погрешность ±0,8 %.
3.1.7 Автоматические дозаторы вместимостью от 10 до 100 мм3, приведённая погрешность ±0,6 %.
3.1.8 Цилиндры мерные исполнения 3 вместимостью 25 см3, 50 см3, 100 см3, 1000 см3 по ГОСТ 1770-74.
3.1.9 Колбы мерные наливные 2-25-2, 2-50-2 по ГОСТ 1770-74.
3.1.10 Пипетки мерные 1-2-1, 2-2-5 по ГОСТ 29227-91.
3.1.11 ГСО 9631-2010 состава раствора полихлорированных дибензофуранов в нонане (ДФ-2), с погрешностью содержания каждого компонента не более ±10 % (стандартный раствор изотопно-меченых ПХДД и ПХДФ - стандарт-имитатор (СИ), используется как дополнительный стандарт на любой стадии подготовки проб); состав приведён в таблице 2.
Таблица 2. Состав стандарта-имитатора ДФ-2
|
Конгенеры ПХДФ |
Концентрация, нг/см3 |
|
2,3,4,7,8-Пентахлордибензофуран-13С12 (2,3,4,7,8-ПеХДФ-13С12) |
1000 |
|
1,2,3,4,7,8-Гексахлордибензофуран-13С12 (1,2,3,4,7,8-ГкХДФ-13С12) |
1000 |
|
1,2,3,4,7,8,9-Гептахлордибензофуран-13С12 (1,2,3,4,6,7,8-ГпХДФ-13С12) |
1000 |
3.1.12 ГСО 9630-2010 состава раствора полихлорированных дибензо-п-диоксинов и дибензофуранов в нонане (ДФ-1) или ГСО 9632-2010 состава раствора полихлорированных дибензо-п-диоксинов и дибензофуранов в нонане (ДФ-3) с погрешностью содержания каждого компонента не более ±10 %, (стандартный раствор изотопно-меченых ПХДД и ПХДФ - внутренний стандарт-имитатор (ВСИ), вводится на стадии подготовки проб к анализу); состав приведён в таблицах 3, 4.
Таблица 3. Состав внутреннего стандарта-имитатора ДФ-1
|
Конгенеры ПХДД/ПХДФ |
Концентрация, нг/см3 |
|
2,3,7,8-тетрахлордибензодиоксин-13С12 (2,3,7,8-ТХДД-13С12) |
1000 |
|
1,2,3,7,8-пентахлордибензо-п-диоксин-13С12 (1,2,3,7,8-ПеХДД-13С12) |
1000 |
|
1,2,3,6,7,8-гексахлордибензо-п-диоксин-13С12 (1,2,3,6,7,8-ГкХДД-13С12) |
1000 |
|
1,2,3,4,7,8-гексахлордибензо-п-диоксин-13С12 (1,2,3,4,7,8-ГкХДД-13С12) |
1000 |
|
1,2,3,4,6,7,8-гептахлордибензо-п-диоксин-13С12 (1,2,3,4,6,7,8-ГпХДД-13С12) |
1000 |
|
Октахлордибензо-п-диоксин-13С12 (ОХДД-13С12) |
2000 |
|
2,3,7,8-тетрахлордибензофуран-13C12 (2,3,7,8-ТХДФ-13С12) |
1000 |
|
1,2,3,7,8-пентахлордибензофуран-13С12 (1,2,3,7,8-ПеХДФ-13С12) |
1000 |
|
2,3,4,7,8-пентахлордибензофуран-13C12 (2,3,4,7,8-ПеХДФ-13С12) |
1000 |
|
1,2,3,4,7,8-гексахлордибензофуран-13С12 (1,2,3,4,7,8-ГкХДФ-13С12) |
1000 |
|
1,2,3,6,7,8-гексахлордибензофуран-13С12 (1,2,3,6,7,8-ГкХДФ-13С12) |
1000 |
|
1,2,3,7,8,9-гексахлордибензофуран-13С12 (1,2,3,7,8,9-ГкХДФ-13С12) |
1000 |
|
2,3,4,6,7,8-гексахлордибензофуран-13С12 (2,3,4,6,7,8-ГкХДФ-13С12) |
1000 |
|
1,2,3,4,6,7,8-гептахлордибензофуран-13С12 (1,2,3,4,6,7,8-ГпХДФ-13C12) |
1000 |
|
1,2,3,4,7,8,9-гептахлордибензофуран-13С12 (1,2,3,4,7,8,9-ГпХДФ-13C12) |
1000 |
Таблица 4. Состав внутреннего стандарта-имитатора ДФ-3
|
Конгенеры ПХДД/ПХДФ |
Концентрация, нг/см3 |
|
2,3,7,8-Teтpaxлopдибензодиоксин-13C12 (2,3,7,8-ТХДД-13С12) |
1000 |
|
1,2,3,7,8-Пентахлордибензо-п-диоксин-13С12 (1,2,3,7,8-ПеХДД-13С12) |
1000 |
|
1,2,3,6,7,8-Гексахлордибензо-п-диоксин-13С12 (1,2,3,6,7,8-ГкХДД-13С12) |
1000 |
|
l,2,3,4,7,8-Гeкcaхлopдибензо-п-диоксин-13С12 (1,2,3,4,7,8-ГкХДД-13С12) |
1000 |
|
1,2,3,4,6,7,8-Гептахлордибензо-п-диоксин-13С12 (1,2,3,4,6,7,8-ГпХДД-13С12) |
1000 |
|
Октахлордибензо-п-диоксин-13C12 (ОХДД-13С12) |
2000 |
|
2,3,7,8-Тетрахлордибензофуран-13C12 (2,3,7,8-ТХДФ-13С12) |
1000 |
|
1,2,3,7,8-Пентахлордибензофуран-13C12 (1,2,3,7,8-ПеХДФ-13С12) |
1000 |
|
1,2,3,6,7,8-Гексахлордибензофуран-13С12 (1,2,3,6,7,8-ГкХДФ-13С12) |
1000 |
|
1,2,3,4,6,7,8-Гептахлордибензофуран-13С12 (1,2,3,4,6,7,8-ГпХДФ-13С12) |
1000 |
3.1.13 ГСО 9633-2010 состава раствора полихлорированных дибензо-п-диоксинов и дибензофуранов в нонане (ДФ-4) с погрешностью содержания каждого компонента не более ±10 %, (стандартный раствор изотопно-меченых ПХДД и ПХДФ - инструментальный внутренний стандарт (ИВС), вводится в подготовленный очищенный экстракт непосредственно перед измерением); состав приведён в таблице 5.
Таблица 5. Состав стандартного раствора ДФ-4
|
Конгенеры ПХДД |
Концентрация, нг/см3 |
|
1,2,3,4-Тетрахлордибензо-п-диоксин-13С12 (1,2,3,4-ТХДД-13С12) |
500 |
|
1,2,3,7,8,9-Гексахлордибензо-п-диоксин-13С12 (1,2,3,7,8,9-ГкХДД-13С12) |
500 |
3.1.14 ГСО 9634-2010 состава раствора полихлорированных дибензо-п-диоксинов и дибензофуранов в нонане (ДФ-5) с погрешностью содержания каждого компонента не более ±10 % (стандартный раствор используется для приготовления градуировочных растворов); состав приведён в таблице 6.
Таблица 6. Состав стандартного раствора ДФ-5
|
Конгенеры ПХДД/ПХДФ |
Концентрация, нг/см3 |
|
2,3,7,8-Тетрахлордибензодиоксин (2,3,7,8-ТХДД) |
400 |
|
1,2,3,7,8-пентахлордибензо-п-диоксин (1,2,3,7,8-ПеХДД) |
2000 |
|
1,2,3,6,7,8-гексахлордибензо-п-диоксин (1,2,3,6,7,8-ГкХДД) |
2000 |
|
1,2,3,7,8,9-гексахлордибензо-п-диоксин (1,2,3,7,8,9-ГкХДД) |
2000 |
|
1,2,3,4,7,8-гексахлордибензо-п-диоксин (1,2,3,4,7,8-ГкХДД) |
2000 |
|
1,2,3,4,6,7,8-гептахлордибензо-п-диоксин (1,2,3,4,6,7,8-ГпХДД) |
2000 |
|
Октахлордибензо-п-диоксин (ОХДД) |
2000 |
|
2,3,7,8-тетрахлордибензофуран (2,3,7,8-ТХДФ) |
400 |
|
1,2,3,7,8-пентахлордибензофуран (1,2,3,7,8-ПеХДФ) |
2000 |
|
2,3,4,7,8-пентахлордибензофуран (2,3,4,7,8-ПеХДФ) |
2000 |
|
1,2,3,4,7,8-гексахлордибензофуран (1,2,3,4,7,8-ГкХДФ) |
2000 |
|
1,2,3,6,7,8-гексахлордибензофуран (1,2,3,6,7,8-ГкХДФ) |
2000 |
|
1,2,3,7,8,9-гексахлордибензофуран (1,2,3,7,8,9-ГкХДФ) |
2000 |
|
2,3,4,6,7,8-гексахлордибензофуран (2,3,4,6,7,8-ГкХДФ) |
2000 |
|
1,2,3,4,6,7,8-гептахлордибензофуран (1,2,3,4,6,7,8-ГпХДФ) |
2000 |
|
1,2,3,4,7,8,9-гептахлордибензофуран (1,2,3,4,7,8,9-ГпХДФ) |
2000 |
|
Октахлордибензофуран (ОХДФ) |
2000 |
Допускается использование других средств измерений, изотопно-меченых веществ, а также чистых веществ, произведенных другими фирмами, с содержанием основного компонента не менее 98 % и метрологическими и техническими характеристиками не хуже приведенных выше.
3.2 Вспомогательные устройства
3.2.1 Ротационный испаритель типа ИР-1 М2 по ТУ 25-1173.102-84.
3.2.2 Сушильный шкаф типа 2В-151 по МРТУ 42-1411-61.
3.2.3 Плитка электрическая с закрытой спиралью мощностью 800 Вт типа ЭПШ-1-0,8/200 по ГОСТ 14919-83.
3.2.4 Устройство для встряхивания жидкостей любого типа.
3.2.5 Концентратор Кудерна-Даниша с испарительной колбой вместимостью 50 см3, концентрирующей пробиркой вместимостью 10 см3 и трехшариковой колонкой Снайдера фирмы Supelco.
3.2.6 Эксикатор 2-250 по ГОСТ 25336-82.
3.2.7 Аппарат Сокслета 45/40 250.
3.2.8 Колонка стеклянная длиной 500 мм и внутренним диаметром 25 мм.
3.2.9 Колонка стеклянная длиной 200 мм и внутренним диаметром 14 мм.
3.2.10 Колонка стеклянная длиной 150 мм и внутренним диаметром 10 мм.
3.2.11 Флаконы для образцов с коническим дном и герметичной пробкой типа Wheaton Mini-Vials вместимостью 1, 3, 5 и 10 см3.
3.2.12 Флаконы для образцов с герметичной пробкой вместимостью 1, 3, 5 ,10 и 30 см3.
3.2.13 Пробирки кварцевые 10×100 мм по ГОСТ 19908-90.
3.2.14 Посуда и оборудование лабораторные стеклянные по ГОСТ 25336-82:
воронки лабораторные В-36-50, В-100-150
насадки для экстрагирования (аппарат Сокслета) НЭТ-500ТС
дефлегматор 250-14/23-29/32-ТС
колбы конические Кн-1-100-14/23 ТС, Кн-1-250-24/29 ТС
колбы круглодонные К-1-500-29/32 ТС, К-1-1000-29/32 ТС, К-1-2000-29/32 ТС
колбы грушевидные К-1-50-14/23, К-1-100-14/23, К-1-250-29/32
насос водоструйный
стаканы В-1-50 ТС, В-1-100 ТС
холодильник ХПТ-1-300-14/23 ХС
3.2.15 Трубки полиэтиленовые с внешним диаметром 2 мм.
3.2.16 Трубки силиконовые.
3.2.17 Резистор ПЭВ-15 8200 Ом по ОЖО467546 ТУ.
3.2.18 Воздух сжатый кл. 1 по ГОСТ 17433-80.
3.2.19 Редуктор кислородный по ГОСТ 5.1381-72.
3.2.20 Электропечь муфельная (tмакс 800 °С) по ТУ 79-337-72.
3.2.21 Флаконы для образцов с коническим дном и герметичной тефлонированной пробкой типа Waters Allince Total Recovery вместимостью 1 см3.
3.2.22 Трубка стеклянная длиной 100 мм, внешним диаметром 7 мм, внутренним диаметром 3,5 мм (для колонки с активированным углем).
3.2.23 Фильтры из стекловолокна, марки GF/D производства фирмы «Whatman Ltd».
3.2.24 Специализированная посуда и оборудование. Методика предусматривает использование для очистки проб специально изготавливаемой посуды и оборудования:
- колонка внутренним диаметром 18 мм, длиной 250 мм с шлифовым соединением 14/23 сверху с сужением снизу,
- колонка внутренним диаметром 18 мм, длиной 300 мм с шлифовым соединением 14/23 сверху с сужением снизу,
- колонка внутренним диаметром 10 мм, длиной 100 мм с шлифовым соединением 14/23 сверху с сужением снизу,
- резервуар вместимостью около 100 см3 с шлифовыми соединениями 14/23 снизу (керн) и сверху (муфта),
- нагреватель для стеклянных трубок диаметром до 9 мм и температурой нагревания до 110 °С, изготовленный на базе резистора ПЭВ-15, 8200 ом, по ТУ ОЖО467546.
3.3 Реактивы и материалы
3.3.1 Ацетон, квалификация «ос.ч.» по ТУ-6-09-3513-86.
3.3.2 Толуол, квалификация «х.ч.» по ТУ 2631-002-29483781-2005.
3.3.3 Метанол, квалификация «х.ч.» по ГОСТ 6995-77.
3.3.4 н-Гексан производства фирмы НПК «Криохром», по ТУ-2631-001-04715285-2012.
3.3.5 Метилен хлористый, квалификация «ос.ч.» по ТУ 6-09-06-856-71.
3.3.6 Спирт этиловый по ГОСТ 18300-87.
3.3.7 н-Тридекан, квалификация «ч.» по ТУ 6-09-3732-74.
3.3.8 н-Гептан квалификация «эталонный» по ТУ 2631-023-44493179-98.
3.3.9 Кислота серная, квалификация «х.ч.» по ГОСТ 4204-77.
3.3.10 Натрий сернокислый безводный, квалификация «х.ч.» по ГОСТ 4166-76.
3.3.11 Натрий хлористый, квалификация «х.ч.» по ГОСТ 4233-77.
3.3.12 Кальций хлористый безводный, квалификация «ч.» по ТУ 6-09-4711-81
3.3.13 Калия гидроокись, квалификация «х.ч.» по ГОСТ 24363-80.
3.3.14 Кислота соляная квалификация «ос.ч» по ГОСТ 14261-77.
3.3.15 Алюминия оксид для хроматографии, активированный основной по Брокманну 1 производства фирмы «Sigma-Aldrich».
3.3.16 Уголь АХ-21 производства фирмы «Anderson Development».
3.3.17 Гелий газообразный, марка «А» по ТУ 0271-135-31323949.
3.3.18 Азот сжатый высокой чистоты по ТУ 2114-009-45905715-2011.
3.3.19 Целит 545 производства фирмы «Alltech».
3.3.20 Силикагель Kieseigel 60, 70 - 230 мкм производства фирмы «Merck».
3.3.21 Вата медицинская гигроскопическая по ГОСТ 5556-81.
3.3.22 Вода дистиллированная по ГОСТ 6709-72.
3.3.23 н-Декан, для следового анализа, производства фирмы «Merck», № 803405.0250 по нормативным документам.
3.3.24 Мембранные фильтры с размером пор 0,45 мкм (Durapore membrane filters) фирмы «MerkMillipore».
3.3.25 Волокнистый кварцевый материал по ТУ 6-11-15-191-81.
Примечание - Допускается применение других вспомогательных устройств, материалов и реактивов с метрологическими и техническими характеристиками не хуже приведённых выше.
4 Метод измерений
Метод основан на экстракции ПХДД/ПХДФ из пробы, в которую предварительно внесен изотопно-меченый внутренний стандарт-имитатор ПХДД/ПХДФ (ВСИ-1) (таблицы 6, 7), органическим растворителем, очистке экстракта от сопутствующих соединений, мешающих определению ПХДД/ПХДФ, внесении инструментального изотопно-меченого внутреннего стандарта (ИВС-1) (таблица 8), концентрировании экстракта и последующем его анализе с помощью сочетания высокоэффективной капиллярной газовой хроматографии и масс-спектрометрии (ГХ-МС) высокого или низкого разрешения.
Идентификацию конгенеров ПХДД/ПХДФ осуществляют по хроматографическим временам удерживания, наличию характеристических ионов в масс-спектрах хроматографически выделенного конгенера и соотношению интенсивностей (площадей) пиков, отвечающих характеристическим ионам идентифицируемых компонентов и стандартов-имитаторов, на регистрируемых ионных масс-хроматограммах.
Концентрации конгенеров ПХДД/ПХДФ определяют по площадям соответствующих хроматографических пиков на ионных масс-хроматограммах по методу изотопного разбавления и внутреннего стандарта.
5 Требования безопасности, охраны окружающей среды
5.1 При выполнении измерений с использованием хромато-масс-спектрометра соблюдают правила электробезопасности в соответствии с ГОСТ 12.1.019-2009 и инструкцией по эксплуатации хромато-масс-спектрометра.
5.2 При выполнении измерений соблюдают требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76.
5.3 При работе с диоксинами соблюдают правила техники безопасности в соответствии со специальными инструкциями по работе с диоксином («Инструкция по технике безопасности по работе с 2,3,7,8-ТХДД», утверждена 3ГУ при МЗ СССР от 02.12.1986 г.).
5.4 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и оснащено средства пожаротушения по ГОСТ 12.4.009-83.
5.5 Помещения, в которых проводится подготовка проб, должны быть оборудованы приточно-вытяжной вентиляцией с кратностью обмена воздуха не менее 1C час-1. Реактивы для приготовления градуировочных и рабочих растворов должны храниться в морозильной камере при температуре не выше минус 18 °С.
5.6 Все операции по приготовлению аттестованных смесей, градуировочных растворов, подготовке образца к анализу следует проводить в вытяжном шкафу.
5.7 Пробы, подготовленные к анализу, градуировочные и контрольные растворы, аттестованные смеси хранят в ампулах, закрытых завинчивающейся или запрессованной крышкой с тефлонированной резиновой прокладкой, прокалываемой микрошприцом.
5.8 Меры по оказанию первой помощи при попадании ПХДД/ПХДФ и их растворов на кожу, в глаза и желудок проводят в соответствии с «Временной инструкцией по лечению отравлений диоксином», утверждённой заместителем Министра здравоохранения СССР от 10 сентября 1986 г.
5.9 Организацию обучения работников технике безопасности труда проводят по ГОСТ 12.0.004-90.
6 Требования к квалификации операторов
К работам по подготовке проб допускают специалистов с образованием не ниже среднего, прошедших соответствующую подготовку и имеющих навыки работы в химической лаборатории. К проведению анализов допускают специалистов с образованием не ниже среднего, имеющих опыт работы на газовом хроматографе и масс-спектрометре. Все работающие должны быть проинструктированы о правилах работы с веществами 1 - 2 класса опасности, органическими растворителями, правилах работы в химической лаборатории, со сжатыми газами и с электроустановками.
7 Требования к условиям измерений
При выполнении измерений соблюдают следующие условия:
|
- температура окружающего воздуха |
(20 ± 5) °С |
|
- атмосферное давление |
от 84 до 106 кПа |
|
- относительная влажность |
от 40 % до 75 % |
|
- напряжение в сети |
(220 ± 22) В |
8 Отбор, хранение и транспортировка проб
Отбор проб воды проводят согласно ГОСТ Р 51593-2000 «Вода питьевая. Отбор проб», ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб», а также «Методике отбора проб воды для определения полихлорированных дибензо-п-диоксинов», утвержденной Госстандартом РФ 11.12.92 г. Пробы отбирают в количестве от 1 до 20 дм3 в стеклянные бутыли темного стекла (или защищенные от попадания света) с притертой пробкой или с пробкой, снабженной тефлоновой прокладкой. Объем пробы, необходимый для анализа, зависит от реальной чувствительности хромато-масс-спектрометра. Если чувствительность равна 0,1 пг, то при инжектировании 0,2 частей экстракта для достижения чувствительности детектирования 0,1 пг/дм3 необходим объем пробы 5 дм3. Если чувствительность равна 1 пг, то при инжектировании 0,5 частей экстракта для достижения чувствительности детектирования 0,1 пг/дм3 необходим объем пробы 20 дм3.
Если период от отбора пробы до экстракции составляет более 4 часов, то пробу необходимо законсервировать добавлением 0,5 - 1 см3 бензола или 0,2 - 0,5 г азида натрия в зависимости от объема пробы. Законсервированные пробы, защищенные от попадания света, могут храниться до семи суток при комнатной температуре. Пробы без консервации могут храниться до 30 суток при температуре не выше 4 °С.
При отборе проб составляют акт отбора, который представляют в лабораторию.
В акте указывают:
- наименование пробы,
- место, дату и время отбора проб,
- наименование Заказчика,
а также все условия и обстоятельства, которые могли повлиять на отбор проб.
Акт должен быть подписан специалистом, отбиравшим пробу, и представителями заинтересованных сторон, если они при этом присутствовали.
9 Подготовка к выполнению измерений
При подготовке к выполнению измерений проводят следующие работы.
9.1 Подготовка растворителей и сорбентов
9.1.1 Органические растворители перегоняют в стеклянной посуде с ректификационной колонкой длиной 50 см, отбрасывая предгон (~ 5 %) и кубовый остаток (~ 10 %). Растворители с маркой «pesticide grade» (для анализа пестицидов) могут использоваться без дополнительной очистки.
9.1.2 Активирование силикагеля
Силикагель активируют в сушильном шкафу при 150 °С в течение 16 ч.
9.1.3 Подготовка силикагеля, импрегнированного серной кислотой (40 %)
Взвешивают 1,00 кг (результат взвешивания записывают с точностью до второго десятичного знака) активированного силикагеля в стеклянной банке вместимостью около 3 дм3, добавляют 362 см3 концентрированной серной кислоты (ρ = 1,84 г/см3), закрывают крышкой и перемешивают содержимое до полной гомогенизации содержимого. Для приготовления силикагеля, содержащего 30 и 44 % серной кислоты, используют 233 и 427 см3 концентрированной серной кислоты, соответственно. Приготовленный сорбент хранят до использования в герметично закрытой ёмкости.
9.1.4 Активирование оксида алюминия
Оксид алюминия активируют при 550 - 600 °С в течение 16 ч в кварцевых пробирках по 4,00 г (результат взвешивания записывают с точностью до второго десятичного знака) в каждой, затем охлаждают до 100 °С и пробирки помещают в герметично закрытую стеклянную банку или эксикатор, содержащие безводный хлорид кальция. После активирования сорбент необходимо использовать в течение 5 суток, по истечении которых процедуру активации следует повторить.
В стеклянный цилиндр диаметром 6 см вносят 100 см3 метанола и 10,00 г угля АХ-21 (результат взвешивания записывают с точностью до второго десятичного знака), смесь встряхивают и оставляют на 10 мин, затем жидкость с не осевшей на дно фракцией угля декантируют, осадок высушивают при 80 °С и активируют при 150 °С в течение 12 часов.
9.1.6 Подготовка силикагеля, импрегнированного гидроксидом калия
В 2 дм3 метанола растворяют 300,0 г гидроксида калия (результат взвешивания записывают с точностью до первого десятичного знака), затем при непрерывном перемешивании добавляют 1,0 кг силикагеля (результат взвешивания записывают с точностью до первого десятичного знака). Смесь перемешивают до гомогенного состояния. Реакционную смесь оставляют в герметичной ёмкости на сутки. Полученный продукт помещают в стеклянную колонку и промывают смесью метанола и метилена хлористого (1:1). Остаток растворителей вытесняют сжатым воздухом, полученный силикат калия активируют при 200 - 250 °С в течение 17 часов.
9.1.7 Подготовка сульфата натрия
Сульфат натрия прокаливают при температуре 500 - 550 °С в течение 16 часов. После охлаждения до температуры 60 - 70 °С его переносят в банку с герметичной крышкой и хранят до использования.
9.2 Приготовление рабочих растворов
9.2.1. Приготовление рабочего раствора изотопно-меченого стандарта-имитатора (СИ-1).
В мерную колбу вместимостью 20 см3 вносят с помощью автоматического дозатора 0,1 см3 стандартного раствора ДФ-2 (3.1.11) и доводят объем раствора в колбе до метки н-деканом. Массовые концентрации конгенеров-имитаторов в рабочем растворе (в нг/см3) приведены в таблице 7.
Таблица 7. Массовые концентрации конгенеров-имитаторов в рабочем растворе СИ-1 (в нг/см3)
|
Конгенеры ПХДФ |
СИ |
СИ-1 |
|
2,3,4,7,8-Пентахлордибензофуран-13С12 (2,3,4,7,8-ПеХДФ-13С12) |
1000 |
5 |
|
1,2,3,4,7,8-Гексахлордибензофуран-13С12 (1,2,3,4,7,8-ГкХДФ-13С12) |
1000 |
5 |
|
1,2,3,4,7,8,9-Гептахлордибензофуран-13С12 (1,2,3,4,6,7,8-ГпХДФ-13С12) |
1000 |
5 |
9.2.2 Приготовление рабочего раствора изотопно-меченого стандарта-имитатора (ВСИ-1, ВСИ-1а).
В мерную колбу вместимостью 50 см3 вносят с помощью автоматического дозатора 0,1 см3 стандартного раствора ДФ-1 или ДФ-3 (3.1.11) и доводят объем раствора в колбе до метки н-деканом. Массовые концентрации конгенеров-имитаторов в рабочем растворе (в нг/см3) приведены в таблицах 8, 9 соответственно.
Таблица 8. Массовые концентрации конгенеров-имитаторов в рабочем растворе ВСИ-1 (в нг/см3)
|
Конгенеры ПХДД/ПХДФ |
ВСИ |
ВСИ-1 |
|
2,3,7,8-ТХДД-13C12 |
1000 |
2 |
|
1,2,3,7,8-ПеХДД-13С12 |
1000 |
2 |
|
1,2,3,6,7,8-ГкХДД-13С12 |
1000 |
2 |
|
1,2,3,4,7,8-ГкХДД-13С12 |
1000 |
2 |
|
1,2,3,4,6,7,8-ГпХДД-13C12 |
1000 |
2 |
|
ОХДД-13С12 |
2000 |
4 |
|
2,3,7,8-ТХДФ-13C12 |
1000 |
2 |
|
1,2,3,7,8-ПеХДФ-13С12 |
1000 |
2 |
|
2,3,4,7,8-ПеХДФ-13С12 |
1000 |
2 |
|
1,2,3,4,7,8-ГкХДФ-13С12 |
1000 |
2 |
|
1,2,3,6,7,8-ГкХДФ-13C12 |
1000 |
2 |
|
1,2,3,7,8,9-ГкХДФ-13С12 |
1000 |
2 |
|
2,3,4,6,7,8-ГкХДФ-13С12 |
1000 |
2 |
|
1,2,3,4,6,7,8-ГпХДФ-13С12 |
1000 |
2 |
|
1,2,3,4,7,8,9-ГпХДФ-13С12 |
1000 |
2 |
Таблица 9. Массовые концентрации конгенеров-имитаторов в рабочем растворе ВСИ-la (в нг/см3)
|
Конгенер ПХДД/ПХДФ |
ВСИ |
ВСИ-1а |
|
2,3,7,8-ТХДД (13C12 99 %) |
1000 |
2 |
|
1,2,3,7,8-ПеХДД (13С12 99 %) |
1000 |
2 |
|
1,2,3,6,7,8-ГхХДД (13С12 99 %) |
1000 |
2 |
|
1,2,3,4,6,7,8-ГпХДД (13С12 99 %) |
1000 |
2 |
|
ОХДД (13С12 99 %) |
2000 |
4 |
|
2,3,7,8-ТХДФ (13С12 99 %) |
1000 |
2 |
|
1,2,3,7,8-ПеХДФ (13C12 99 %) |
1000 |
2 |
|
1,2,3,6,7,8-ГхХДФ (13C12 99 %) |
1000 |
2 |
|
1,2,3,4,6,7,8-ГпХДФ (13С12 99 %) |
1000 |
2 |
Приготовленный раствор перемешивают в ультразвуковой бане в течение 10 мин, расфасовывают в стеклянные ампулы вместимостью 1 см3. Ампулы запаивают и хранят до использования, избегая попадания солнечного света, не более 2 лет.
9.2.3 Приготовление рабочего раствора инструментального внутреннего стандарта (ИВС-1).
В мерную колбу вместимостью 10 см3 с помощью автоматического дозатора вносят 1000 мм3 стандартного раствора изотопно-меченого инструментального внутреннего стандарта (3.3.1.4) и доводят объем раствора в колбе до метки н-тридеканом. Массовые концентрации конгенеров в рабочем растворе внутреннего стандарта ИВС-1 (в нг/см3) приведены в таблице 10.
Таблица 10. Массовые концентрации конгенеров в рабочем растворе ИВС-1 (в нг/см3)
|
Конгенер ПХДД/ПХДФ |
ИВС |
ИВС-1 |
|
1,2,3,4-ТХДД (13C12 99 %) |
500 |
50 |
|
2,3,7,8,9-ГхХДД (13C12 99 %) |
500 |
50 |
Приготовленный раствор перемешивают в ультразвуковой бане в течение 10 мин, расфасовывают в стеклянные ампулы вместимостью 1 см3. Ампулы запаивают и хранят до использования, избегая попадания солнечного света не более 2 лет.
9.2.4 Приготовление контрольного раствора ПХДД/ПХДФ (С-1).
С помощью автоматических дозаторов вместимостью от 100 до 1000 мм3 и от 10 до 100 мм3 последовательно вносят во флакон вместимостью 4 см3 1950 мм3 н-декана, 50 мм3 стандартного раствора ДФ-5 (3.1.14). Полученный раствор содержит 10 нг/см3, 2,3,7,8-ТХДД, по 100 нг/см3 ОХДД и ОХДФ и по 50 нг/см3 остальных конгенеров ПХДД/ПХДФ.
Приготовленный раствор перемешивают в ультразвуковой бане в течение 10 мин, расфасовывают в стеклянные ампулы вместимостью 1 см3. Раствор используют для приготовления контрольных проб.
9.2.4 Приготовление градуировочных растворов.
9.2.4.1 Приготовление раствора CS1.
С помощью автоматических дозаторов вместимостью от 100 до 1000 мм3 и от 10 до 100 мм3 последовательно вносят во флакон вместимостью 4 см3 3830 мм3 н-декана, 10 мм3 стандартного раствора ДФ-5 (3.1.14) и 160 мм3 стандартного раствора ДФ-3 (3.1.12).
9.2.4.2 Приготовление раствора CS2.
С помощью автоматических дозаторов вместимостью от 100 до 1000 мм3 и от 10 до 100 мм3 последовательно вносят во флакон вместимостью 4 см3 1870 мм3 н-декана, 50 мм3 стандартного раствора ДФ-5 (3.1.14) и 80 мм3 стандартного раствора ДФ-3 (3.1.12).
9.2.4.3 Приготовление раствора CS3.
С помощью автоматических дозаторов вместимостью от 100 до 1000 мм3 и от 10 до 100 мм3 последовательно вносят во флакон вместимостью 2 см3 910 мм3 н-декана, 50 мм3 стандартного раствора ДФ-5 (3.1.14) и 40 мм3 стандартного раствора ДФ-3 (3.1.12).
9.2.4.4 Приготовление раствора CS4.
С помощью автоматических дозаторов вместимостью от 100 до 1000 мм3 и от 10 до 100 мм3 последовательно вносят во флакон вместимостью 2 см3 860 мм3 н-декана, 100 мм3 стандартного раствора ДФ-5 (3.1.14) и 40 мм3 стандартного раствора ДФ-3 (3.1.12).
9.2.4.5 Приготовление раствора CS5.
С помощью автоматических дозаторов вместимостью от 100 до 1000 мм3 и от 10 до 100 мм3 последовательно вносят во флакон вместимостью 2 см3 760 мм3 н-декана, 200 мм3 стандартного раствора ДФ-5 (3.1.14) и 40 мм3 стандартного раствора ДФ-3 (3.1.12).
Концентрации определяемых веществ в полученных растворах (в нг/см3) приведены в таблице 11.
Хранят растворы в герметично закрытых флаконах при температуре не выше минус 10 °С, избегая попадания солнечного света, не более 6 месяцев, а в стеклянных запаянных ампулах не более 2 лет.
Таблица 11. Массовые концентрации диоксинов в градуировочных растворах (в нг/см3)
|
Конгенер ПХДД/ПХДФ |
CS1 |
CS2 |
CS3 |
CS4 |
CS5 |
|
2,3,7,8-ТХДД |
1 |
10 |
20 |
40 |
80 |
|
1,2,3,7,8-ПеХДД |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,4,7,8-ГкХДД |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,6,7,8-ГкХДД |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,7,8,9-ГкХДД |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,4,6,7,8-ГпХДД |
5 |
50 |
100 |
200 |
400 |
|
ОХДД |
10 |
100 |
200 |
400 |
800 |
|
2,3,7,8-ТХДФ |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,7,8-ПеХДФ |
5 |
50 |
100 |
200 |
400 |
|
2,3,4,7,8-ПеХДФ |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,4,7,8-ГкХДФ |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,6,7,8-ГкХДФ |
5 |
50 |
100 |
200 |
400 |
|
2,3,4,6,7,8-ГкХДФ |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,6,7,8-ГкХДФ |
5 |
50 |
100 |
200 |
400 |
|
2,3,4,6,7,8-ГкХДФ |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,7,8,9-ГкХДФ |
5 |
50 |
100 |
200 |
400 |
|
1,2,3,4,6,7,8-ГпХДФ |
5 |
50 |
100 |
200 |
400 |
|
ОХДФ |
10 |
100 |
200 |
400 |
800 |
|
2,3,7,8-ТХДД (13С12 99 %) |
40 |
40 |
40 |
40 |
40 |
|
1,2,3,7,8-ПеХДД (13С12 99 %) |
40 |
40 |
40 |
40 |
40 |
|
1,2,3,6,7,8-ГхХДД (13С12 99 %) |
40 |
40 |
40 |
40 |
40 |
|
1,2,3,4,6,7,8-ГпХДД (13С12 99 %) |
40 |
40 |
40 |
40 |
40 |
|
ОХДД (13С12 99 %) |
80 |
80 |
80 |
80 |
80 |
|
2,3,7,8-ТХДФ (13С12 99 %) |
40 |
40 |
40 |
40 |
40 |
|
1,2,3,7,8-ПеХДФ (13С12 99 %) |
40 |
40 |
40 |
40 |
40 |
|
1,2,3,6,7,8-ГхХДФ (13С12 99 %) |
40 |
40 |
40 |
40 |
40 |
|
1,2,3,4,6,7,8-ГпХДФ (13С12 99 %) |
40 |
40 |
40 |
40 |
40 |
9.3 Подготовка проб
9.3.1 Объем анализируемой пробы должен быть не менее 1 дм3.
9.3.2 Перед экстракцией в пробу должны быть внесены изотопно-меченые внутренние стандарты-имитаторы (СИ-1 и ВСИ-1а или ВСИ-1) (таблицы 7, 8, 9).
9.3.3 Количество добавляемых внутренних стандартов (ориентировочно 100 - 200 пг) должно быть таким, чтобы отношение сигнал/шум соответствующих им пиков на масс-хроматограммах было не менее 250:1 по всем веществам.
9.3.4 Смеси внутренних стандартов разбавляют ацетоном в день использования таким образом, чтобы в каждую пробу было внесено не менее 1 см3 раствора с объёмной долей ацетона не менее 95 %.
9.3.5 Пробы воды, содержащие более 1 % взвешенных частиц, фильтруют через стекловолокнистый фильтр с размером пор 0,45 мм. Перед фильтрацией к пробе добавляют смесь изотопно-меченых стандартов. Фильтрат экстрагируют в соответствии с 9.4.2, а фильтр с остатком - в аппарате Сокслета в соответствии с 9.4.3.
9.3.6 Часть пробы, достаточная для проведения повторного анализа, должна храниться при температуре не выше 10 °С.
9.4 Экстракция
В пробу воды объёмом 1 дм3 с помощью дозатора, пипетки или микрошприца вводят 0,05 см3 рабочего раствора стандарта-имитатора СИ-1 и ВСИ-la или ВСИ-1 (таблицы 7, 8, 9) и встряхивают для уравновешивания в течение часа.
Экстракцию проб воды проводят последовательно тремя порциями метилена хлористого в делительной воронке достаточной вместимости. Объем метилена хлористого должен составлять не менее 10 % от объёма пробы для первой экстракции и не менее 5 % для последующих. Экстракт осушают безводным сульфатом натрия.
Фильтр с остатком помещают в аппарат Сокслета и экстрагируют толуолом 18 - 20 часов.
Смесь двух экстрактов упаривают на роторном испарителе до ~ 5 см3 и очищают в соответствии с 9.5.
9.5 Очистка экстрактов и подготовка к анализу
9.5.1 Очистка экстракта на «многослойной» колонке.
В стеклянную колонку длиной 250 мм и внутренним диаметром 18 мм помещают подложку из стеклянной ваты, затем последовательно слой нейтрального силикагеля - 1 см3, силикагеля, импрегнированного гидроксидом цезия (калия) - 1 см3, сульфата натрия - 1 см3, силикагеля, импрегнированного серной кислотой, - 1 см3, сульфата натрия - 1 см3, силикагеля, импрегнированного серной кислотой, - 1 см3, сульфата натрия - 1 см3 и нейтрального силикагеля - 1 см3. Экстракт пропускают через колонку, смывают остатки из колбы или концентрирующей пробирки двумя порциями гексана (5 см3) и также переносят в колонку. После прохождения раствора колонку промывают 50 см3 гексана, выдувая остаток растворителя током воздуха. Экстракты объединяют и далее счищают на угольной колонке.
9.5.2 Очистка экстракта на угольной колонке
20 мг угля АХ-21 (результат взвешивания записывают с точностью до первого десятичного знака), подготовленного согласно 9.1.5, и 180 мг целлита (результат взвешивания записывают с точностью до первого десятичного знака) перемешивают в ступке до однородного состояния и помещают в стеклянную трубку (3.2.22) между двумя тампонами из стеклянной ваты. Колонку присоединяют тефлоновым капилляром к резервуару, из которого колонку последовательно промывают 5 см3 толуола, 2 см3 ацетона, 2 см3 метилена хлористого и 5 см3 гексана со скоростью около 2 см3/мин, не допуская высыхания колонки. Через подготовленную колонку пропускают экстракт и промывают последовательно порциями по 10 см3 метилена хлористого, ацетона и гексана. Затем колонку переворачивают, помещают в печь, нагретую до 110 °С и элюируют планарные соединения 10 см3 толуола в обратном направлении (планарная фракция). Элюат упаривают на ротационном испарителе до «капли», добавляют 2 см3 смеси гексана и метилена хлористого (75:25 по объему) и очищают на «многослойной» колонке в соответствии с 9.4.1. После чего экстракт очищают на колонке с оксидом алюминия.
9.5.3 Очистка экстракта на колонке с оксидом алюминия.
В стеклянную колонку длиной 150 мм и внутренним диаметром 10 мм помещают подложку из волокнистого кварцевого материала и 4 г оксида алюминия, а сверху - 2 см3 сернокислого натрия. Колонку промывают 10 см3 гексана и вносят пробу до того, как мениск растворителя достигнет сорбента. Колонку промывают 20 см3 гексана и последовательно элюируют 20 см3 смеси гексана и метилена хлористого (95:5 по объёму) и 50 см3 смеси гексана и метилена хлористого (50:50 по объёму).
Экстракт упаривают до объёма около 2 см3 на ротационном испарителе, переносят во флакон Mini-Vial вместимостью 5 см3, добавляют 0,01 см3 рабочего раствора инструментального внутреннего стандарта (ИВС-1) (9.2.3) и 10 мм3 тридекана. Образец упаривают в токе азота до полного испарения растворителя (кроме тридекана). Возможно использование других алифатических углеводородов (нонан, декан), не мешающих проведению анализа.
Подготовленные для анализа пробы могут храниться до 40 суток при температуре не выше 4 °С.
9.5.4 Разбавление конечного экстракта (не более чем в 10 раз).
Операцию проводят только в тех случаях, когда сигналы тех или иных определяемых конгенеров превышают их сигналы, полученные для наиболее концентрированного из градуировочных растворов (CS5). Объем добавляемого растворителя рассчитывается исходя из того, чтобы сигнал после разбавления составлял приблизительно половину сигнала этого же конгенера в растворе CS5. Растворитель добавляют с помощью шприца соответствующего объёма.
9.6 Подготовка прибора
Хромато-масс-спектрометрическую систему готовят к работе в соответствии с инструкцией по её эксплуатации. Проверяют функционирование системы, вводя в инжектор хроматографа растворитель и контрольный образец, и оценивают общую чувствительность прибора, фон, наличие эффектов «памяти» и артефактов.
Система ГХ-МС должна обеспечивать отношение сигнал : шум не менее 3:1 для каждого компонента контрольного раствора. В связи с тем, что в настоящее время не существует капиллярных колонок, способных разделить все изомеры, в ряде случаев анализ проводят в два этапа. Сначала, применяют неполярную колонку типа DB-5ms. Если обнаруживают 1,2,3,7,8,9-ГкХДД, 2,3,7,8-ТХДФ, 2,3,4,7,8-ПеХДФ, 1,2,3,4,7,8-ГкХДФ, то ту же пробу анализируют на полярной колонке, например, SP2331, для определения именно этих изомеров.
Примерная температурная программа для разделения конгенеров ПХДД и ПХДФ на колонке DB-5ms:
|
Режим инжектора |
без деления потока (splitless) |
|
Задержка продувки инжектора |
1 мин |
|
Время сброса растворителя |
5 мин |
|
Длина колонки |
30 м |
|
Диаметр колонки |
0,25 мм |
|
Толщина плёнки фазы |
0,25µ |
|
Программирование температуры: |
|
|
Начальная температура колонки |
160 °С |
|
Начальное время задержки |
1 мин |
|
Скорость нагрева колонки |
10 °С/мин до 220 °С, 3 °С/мин до 300 °С |
|
Температура инжектора |
290 °С |
|
Скорость потока гелия через колонку |
1 см3/мин |
|
Температура интерфейса |
290 °С |
|
Температура ионного источника |
250 °С |
|
Селективное сканирование |
массы ионов в табл. 12 |
|
Энергия ионизирующих электронов |
50 - 70 эВ |
|
Инжектируемый объём |
1 мм3 |
Устанавливают программу работы масс-спектрометра для селективного детектирования характеристических ионов аналитов с массами, указанными в таблице 12.
Таблица 12. Массы регистрируемых ионов и соотношение площадей их пиков на масс-хроматограммах
|
Конгенер |
M1 |
М2 |
Соотношение площадей пиков |
|
ТХДД |
319,897 |
321,894 |
0,77 |
|
ТХДФ |
303,902 |
305,899 |
0,77 |
|
ПеХДД |
355,855 |
357,852 |
1,32 |
|
ПеХДФ |
339,860 |
341,857 |
1,32 |
|
ГкХДД |
389,816 |
391,813 |
1,24 |
|
ГкХДФ |
373,821 |
375,818 |
1,24 |
|
ГпХДД |
423,777 |
425,774 |
1,05 |
|
ГпХДФ |
407,782 |
409,779 |
1,05 |
|
ОХДД |
557,738 |
559,735 |
0,89 |
|
ОХДФ |
441,743 |
443,740 |
0,89 |
|
13C12-ТХДД |
331,937 |
333,934 |
0,77 |
|
13С12-ТХДФ |
315,942 |
317,939 |
0,77 |
|
13C12-ПеХДД |
367,895 |
369,892 |
1,32 |
|
13C12-ПеХДФ |
351,900 |
353,897 |
1,32 |
|
13С12-ГкХДД |
401,856 |
403,853 |
1,24 |
|
13С12-ГкХДФ |
383,864 |
385,861 |
1,24 |
|
13С12-ГпХДД |
435,817 |
437,814 |
1,05 |
|
13C12-ГпХДФ |
417,825 |
419,822 |
1,05 |
|
13С12-ОХДД |
469,778 |
471,775 |
0,89 |
Примечания к таблице 12:
1 При использовании масс-спектрометра низкого разрешения регистрируют ионы с соответствующими номинальными массами, напр. вместо 319,897 - 320 и т.д.
2 Для обеспечения большей достоверности результатов можно регистрировать три иона молекулярного кластера каждого аналита, например для ТХДД, ионы - (М)+, (М+2)+, (М+4)+, м/z 320, 322, 324 а.е.м. соответственно.
3 При использовании масс-спектрометра низкого разрешения в режиме ХИ ОИ детектируют ионы, массы которых приведены в таблице 12а.
4 При использовании других изотопно-меченых стандартов в таблицу масс регистрируемых ионов включают массы их молекулярных ионов.
|
Анализируемая группа конгенеров ПХДД/ДФ |
Тип иона |
Характеристические ионы, m/е, а.е.м. |
Соотношение площадей пиков |
|
ТХДД |
M-, (М + 2)-, (М + 4)- |
320; 322; 324 |
0,8:1:0,5 |
|
[13С12]-2,3,7,8-ТХДД |
(М + 2)-, (М + 4)- |
334; 336 |
1:0,5 |
|
ПеХДД |
М-, (М + 2)-, (М + 4)- |
354; 356; 358 |
0,7:1:0,5 |
|
[13С12]-1,2,3,7,8-ПеХДД |
М-, (М + 2)- |
366; 368 |
0,7:1 |
|
ГхХДД |
(М - Сl)-, (М - Сl + 2)-, (М - Сl + 4)- |
353; 355; 357 |
0,6:1:0,6 |
|
[13C12]-1,2,3,6,7,8-ГхХДД |
(М - Сl + 2)-, (М - Сl + 4)- |
367; 369 |
1:0,6 |
|
[13C12]-1,2,3,7,8,9-ГхХДД |
(М - Cl + 2)-, (М - Сl + 4)- |
367; 369 |
1:0,6 |
|
ГпХДД |
(М - Сl)-, (М - Сl + 2)-, (М - Сl + 4)- |
387; 389; 391 |
0,3:1:0,7 |
|
[13Cl2]-l,2,3,4,6,7,8-ГпХДД |
(М - Cl + 2)-, (М - Сl + 4)- |
401; 403 |
1:0,7 |
|
ОХДД |
(М - Сl + 2)-, (М - Сl + 4)-, (М - Сl + 6)- |
423; 425; 427 |
0,4:1:0,3 |
|
[13С12]-ОХДД |
(М - Сl + 2)-, (М - Сl + 4)- |
435; 437 |
0,4:1 |
|
ТХДФ |
М-, (М + 2)-, (М + 4)- |
304; 306; 308 |
0,7:1:0,5 |
|
[13С12]-2,3,7,8-ТХДФ |
(М + 2)-, (М + 4)- |
316; 318 |
0,7:1 |
|
ПХДФ |
М-, (М + 2)-, (М + 4)- |
338; 340; 342 |
0,6:1:0,7 |
|
[13C12]-1,2,3,7,8-ПеХДФ |
(М + 2)-, (М + 4)- |
352; 354 |
1:0,7 |
|
ГхДФ |
М-, (М + 2)-, (М + 4)- |
372; 374; 376 |
0,5:1:0,8 |
|
[13C12]-1,2,3,6,7,8-ГхХДФ |
(М + 2)-, (М + 4)- |
386; 388 |
1:0,8 |
|
ГпХДФ |
М-, (М + 2)-, (М + 4)- |
406; 408; 410 |
0,4:1:0,9 |
|
[13C12]-1,2,3,4,6,7,8-ГпХДФ |
(М + 2)-, (М + 4)- |
420; 422 |
1:0,9 |
|
ОХДФ |
М-, (М + 2)-, (М + 4)- |
442; 444; 446 |
0,9:1:0,7 |
Эффективность разделения и абсолютные времена для всех токсичных ПХДД, ПХДФ проверяют перед каждой серией вводом в хромато-масс-спектрометр градуировочного раствора CS4. Времена удерживания зависят от типа колонки и условий работы.
Относительные времена удерживания некоторых ПХДД/ПХДФ на двух разных неподвижных фазах (неполярной и полярной) приведены в таблице 13.
Таблица 13. Относительные времена удерживания некоторых ПХДД/ПХДФ
|
Конгенер |
Неподвижная фаза |
|
|
Неполярная DB-5MS |
Полярная SP-2331 |
|
|
1,2,3,4-ТХДД |
0,99 |
1,02 |
|
2,3,7,8-ТХДД |
1,00 |
1,00 |
|
1,2,3,7,8-ПеХДД |
1,23 |
1,40 |
|
1,2,3,4,7,8-ГкХДД |
1,46 |
2,08 |
|
1,2,3,6,7,8-ГкХДД |
1.47 |
1,94 |
|
1,2,3,7,8,9-ГкХДД |
1,50 |
2,15 |
|
1,2,3,4,6,7,8-ГпХДД |
1,76 |
2,98 |
|
ОХДД |
2,17 |
4,50 |
|
2,3,7,8-ТХДФ |
0,96 |
0,96 |
|
1,2,3,7,8-ПеХДФ |
1,18 |
1,31 |
|
2,3,4,7,8-ПеХДФ |
1,22 |
1,35 |
|
1,2,3,4,7,8-ГкХДФ |
1,39 |
2,01 |
|
1,2,3,6,7,8-ГкХДФ |
1,39 |
2,03 |
|
2,3,4,6,7,8-ГкХДФ |
1,43 |
2,07 |
|
1,2,3,7,8,9-ГкХДФ |
1,48 |
2,09 |
|
1,2,3,4,6,7,8-ГпХДФ |
1,61 |
2,83 |
|
1,2,3,4,7,8,9-ГпХДФ |
1,74 |
2,96 |
|
ОХДФ |
2,12 |
4,45 |
Чувствительность прибора определяют один раз в день (или после настройки прибора) путём анализа градуировочного раствора ПХДД/ПХДФ. Приемлемый критерий качества - соотношение сигнал-шум больше 3:1 при инжекции 0,2 пг 2,3,7,8-ТХДД.
9.7 Установление градуировочной характеристики
Для установления градуировочной характеристики последовательно анализируют градуировочные растворы CS1 - CS5, инжектируя по 0,001 см3 каждого раствора.
Проверку чистоты прибора на содержание анализируемых компонентов проводят после измерений каждого градуировочного раствора путём инжекции декана. Приемлемый критерий - величина вносимой ошибки за счёт фона прибора не должна превышать 1 % от среднего значения определяемых концентраций.
Градуировочную зависимость отношения площадей хроматографического пика каждого определяемого компонента и пика иона внутреннего стандарта от массовой концентрации устанавливают с помощью программного обеспечения, при этом коэффициент корреляции должен быть не менее 0,99.
Поскольку осуществляется регистрация двух ионов каждого определяемого компонента и стандарта, для построения градуировочной зависимости могут использоваться:
один из регистрируемых ионов каждого определяемого компонента и стандарта, сумма пиков двух ионов или среднее значение пиков двух ионов.
Градуировочный коэффициент Ki определяют по формуле (1)
|
|
(1) |
где Ai, As - площади пиков определяемого компонента в образце и во внутреннем стандарте, соответственно, в единицах счета,
Pi, Ps - количество определяемого компонента в образце и во внутреннем стандарте (в пг), соответственно.
Зависимость считается линейной, если среднеквадратическое отклонение значения градуировочного коэффициента Ki в каждой точке не превышает 20 %.
Рассчитывают средние значения относительных коэффициентов чувствительности для каждого индивидуального конгенера ПХДД/ПХДФ для всех градуировочных растворов.
10 Порядок выполнения измерений
Хроматографическое разрешение подтверждают анализом градуировочного раствора, проводимым до и после анализа аналитической серии. Приемлемое значение - разделение пиков 1,2,3,4,7,8-ГхДФ и 1,2,3,6,7,8-ГхДФ соответствует условию (2)
|
2h/(H1 + H2) < 0,7, |
(2) |
где Н1 и Н2 - высоты пиков конгенеров, h - высота долины между ними.
Отбирают с помощью микрошприца 0,001 см3 анализируемого раствора и вводят в инжектор газового хроматографа в режиме splitless или on-column. Регистрируют ионные масс-хроматограммы для ионов, соответствующих определяемым конгенерам и используемым стандартам-имитаторам (СИ) и внутренним стандартам (ИВС).
Определяют времена удерживания определяемых соединений и внутренних стандартов.
Времена удерживания ПХДД/ПХДФ (по отношению к внутреннему стандарту) не должны отличаться от измеренных для стандартных образцов ПХДД/ПХДФ более чем на 0,01 %, а в случае использования соответствующего изотопно-меченого внутреннего стандарта - не более чем на 1 с или на 1 - 2 скана от времени удерживания внутреннего стандарта.
Отношение площадей хроматографических пиков на парных масс-хроматограммах ионов M1 и М2, регистрируемых для каждого определяемого компонента и внутреннего стандарта, должно быть в пределах ±15 % от теоретического, приведенного в таблице 12, 12а.
Стабильность работы прибора проверяют путем анализа градуировочного раствора CS2 до и после анализа серии образцов. Критерием стабильной работы прибора является то, что различие значений градуировочного коэффициента Ki, рассчитанных до и после анализа серии образцов с помощью системы обработки данных, не должно превышать ±15 %.
11 Обработка результатов измерений
По окончании измерений с помощью системы обработки данных фиксируют на масс-хроматограммах пики в области времен удерживания, соответствующих определяемым компонентам и внутренним стандартам.
Идентификацию определяемых компонентов проводят, вычисляя отношение площадей хроматографических пиков на масс-хроматограммах ионов M1 и М2, регистрируемых для каждого определяемого соединения и внутреннего стандарта, и сравнивают его с теоретическим значением, приведенным в табл. 12, 12а. Это отношение должно иметь расхождение с теоретическим в пределах не более 15 %, например, для ТХДД - от 0,65 до 0,89 (теоретическое отношение равно 0,77).
Компонент в данной пробе считается идентифицированным, если выполняется приведенное выше условие и если его время удерживания совпадает с временем удерживания соответствующего изотопно-меченого внутреннего стандарта (отличается от него не более чем на 1 с или на 1 - 2 скана) или отличается от времени удерживания, установленного при градуировке, не более, чем на 0,01 %.
Если хроматографические пики в указанной области времен удерживания имеются, но отношение площадей пиков выходит за эти пределы, то говорить о положительной идентификации по этим пикам в данной пробе нельзя, и требуется дополнительная очистка или использование других условий анализа (использование хроматографической колонки с другой неподвижной фазой или техники получения масс-спектра).
Массовую концентрацию обнаруженных компонентов Xi рассчитывают по формуле (3)
|
|
(3) |
где Xi - массовая концентрация i-го компонента, пг/дм3,
Ai - площадь пика (в единицах счета) на масс-хроматограмме иона, регистрируемого для определения данного соединения,
Аs - площадь пика на масс-хроматограмме внутреннего стандарта (в единицах счета),
Rs - количество добавленного к пробе стандарта-имитатора, пг,
В - объем анализируемой пробы, дм3,
Ki - градуировочный коэффициент.
Для проведения расчетов выбирают для каждого определяемого компонента и изотопно-меченого стандарта (таблицы 12, 12а) на масс-хроматограммах либо по одному из двух ионов M1 или М2, указанных в таблице 12 (или любых ионов из таблицы 12а), либо сумму площадей соответствующих пиков для ионов M1 и М2, либо среднее значение площадей пиков для ионов M1 и М2.
Определяют эффективность извлечения Ri i-го внутреннего стандарта-имитатора по формуле (4)
|
|
(4) |
где Аsi, Ask - площади пиков на масс-хроматограммах i-го стандарта-имитатора и инструментального стандарта;
Рsi, Рsk - масса стандарта-имитатора и инструментального стандарта, соответственно, пг.
Эффективность извлечения Ri должна быть в пределах 50 - 110 %. Значения степени извлечения, не укладывающиеся в этот интервал, допускаются для гепта- и октахлорзамещенных ПХДД/ПХДФ при условии, что их вклад в общий эквивалент токсичности не превышает 10 %.
12 Оформление результатов измерений
Результат анализа в документах, предусматривающих его использование, представляют в виде
Xi ± ∆i, пг/дм3 при Р = 0,95,
где Xi - результат определения массовой концентрации i-го компонента, пг/дм3,
∆i - абсолютная погрешность измерений i-го компонента: ∆i = 0,01 × δ × Xi,
где δ - относительная погрешность, % (табл. 1).
Эквивалент токсичности TEQ рассчитывается путём суммирования произведений массовой концентрации каждого конгенера на соответствующий коэффициент токсичности (приложение 3).
TEQ = ∑Xi × ДЭi
Форма протокола приведена в приложении 4.
13 Оценка приемлемости результатов измерений, получаемых в условиях воспроизводимости
Приемлемость результатов измерений, полученных в двух лабораториях, оценивают сравнением разности этих результатов с критической разностью CD0,95 по формуле (5)
|
|
(5) |
где ![]() - больший результат измерений (среднее
арифметическое значение двух параллельных определений), пг/дм3,
- больший результат измерений (среднее
арифметическое значение двух параллельных определений), пг/дм3,
![]() - меньший результат измерений (среднее
арифметическое значение двух параллельных определений), пг/дм3,
- меньший результат измерений (среднее
арифметическое значение двух параллельных определений), пг/дм3,
![]() - среднее арифметическое результатов
измерений для двух лабораторий, пг/дм3,
- среднее арифметическое результатов
измерений для двух лабораторий, пг/дм3,
CD0,95 - значение критической разности, рассчитывается по формуле (6), где n1, n2 - число параллельных определений в первой и второй лаборатории.
|
|
(6) |
где R - предел воспроизводимости, % (таблица 1),
r - предел повторяемости, % (таблица 1).
Если критическая разность не превышена, то приемлемы оба результата измерений, приводимых двумя лабораториями, и в качестве окончательного результата используют их общее среднее значение. Если критическая разность превышена, выполняют процедуры, изложенные в 5.3.3 ГОСТ Р ИСО 5725-6-2002. При разногласиях руководствуются 5.3.4 ГОСТ Р ИСО 5725-6-2002.
14 Контроль качества результатов измерений при реализации методики в лаборатории
Контроль качества результатов измерений в лаборатории при реализации методики осуществляют по ГОСТ Р ИСО 5725-6-2002, используя контроль стабильности среднеквадратического отклонения промежуточной прецизионности по 6.2.3 и показателя правильности по 6.2.4. Проверку стабильности осуществляют с применением контрольных карт Шухарта.
Периодичность контроля стабильности результатов выполняемых измерений регламентируют в Руководстве по качеству лаборатории.
Рекомендуется устанавливать контролируемый период так, чтобы количество результатов контрольных измерений было от 20 до 30.
При неудовлетворительных результатах контроля, например, при превышении предела действия или регулярном превышении предела предупреждения, выясняют причины этих отклонений, в том числе проводят смену реактивов, проверяют работу оператора.
Приложение 1 (справочное)
Конгенер ПХДД/ПХДФ - любой из индивидуальных дибензо-п-диоксинов и дибензофуранов с содержанием хлора от 1 до 8 атомов в молекуле. Порядок замещения для конкретного изомера указывается цифровым индексом, согласно правилам IUPAC, например, 1,2,3,4,5-пентахлордибензо-п-диоксин.
Стандарт-имитатор (СИ) - смесь конгенеров ПХДД/ПХДФ, изотопно-меченных углеродом 13С12, водимая в пробу на стадии обработки для контроля полноты извлечения.
Инструментальный внутренний стандарт (ИВС) - изотопно-меченые углеродом 13С12 конгенеры ПХДД/ПХДФ, не входящие в состав СИ, вводимые в подготовленный к анализу экстракт для контроля эффективности экстракции конгенеров, входящих в состав ИВС, проверки стабильности работы масс-спектрометра и оперативного контроля эффективности хроматографического разделения изомеров.
Дополнительный внутренний стандарт - изотопно-меченые углеродом 13С12 конгенеры ПХДД/ПХДФ, не входящие в состав СИ и ИВС, вводимые в пробу или экстракт на любой выбранной стадии подготовки к анализу для контроля этой стадии.
Холостой опыт - аналитическая процедура, включающая экстракцию, очистку, количественное определение, со всеми реактивами и материалами и с холостой пробой (ГОСТ Р 52361-2005).
Холостая проба - проба вещества (материала) объекта аналитического контроля, аналогичная аналитической пробе, но не содержащая аналита - (ГОСТ Р 52361-2005).
Предел определения - количество вещества, которое обеспечивает отклик, отношение которого к фону составляет не менее 3:1 для каждого регистрируемого иона при условии выполнения основных требований к хромато-масс-спектрометрической идентификации: правильные время удерживания и изотопное соотношение. Расчет предела определения проводится для каждого из 17-ти индивидуальных ПХДД/ПХДФ, для которых предусмотрены коэффициенты токсичности (далее - токсичных ПХДД/ПХДФ).
Коэффициенты токсичности - токсичность конгенеров ПХДД и ПХДФ по отношению к 2,3,7,8-тетрахлордибензо-п-диоксину, токсичность которого принята за 1. При вычислении суммарной и максимально возможной концентраций могут использоваться различные системы коэффициентов токсичности. Если не указано иного, то считается, что в данной методике используется система коэффициентов токсичности (WHO-TEF, табл. 2 приложение 1), введённых Всемирной организацией здравоохранения в 1998 г. и в 2005 г.
Эквивалент токсичности - значение содержания конгенера ПХДД и ПХДД, умноженное на соответствующий коэффициент токсичности.
Суммарная концентрация ПХДД и ПХДФ - сумма концентраций индивидуальных ПХДД и ПХДФ, выраженных в единицах эквивалента токсичности. Концентрации компонентов, содержание которых ниже предела определения, принимаются равными нулю.
Приложение 2 (справочное)
Условные обозначения и сокращения
|
I-TEF |
International toxicity equivalency factor - международный коэффициент токсичности |
|
I-TEQ |
International toxicity equivalent - диоксиновый эквивалент в системе международных коэффициентов токсичности |
|
EPA US |
Environmental Protection Agency - Агентство по охране окружающей среды (США) |
|
WHO |
World Health Organization - Всемирная Организация Здравоохранения (ВОЗ) |
|
WHO-TEF |
Коэффициент токсичности, введённый ВОЗ для человека в 1998 и 2005 гг. |
|
WHO-TEQ (TEQWHO, ДЭWHO) |
Диоксиновый эквивалент в системе коэффициентов токсичности ВОЗ для человека |
|
ПХДД |
Полихлорированные дибензо-п-диоксины |
|
ПХДФ |
Полихлорированные дибензофураны |
|
ТХДД |
Тетрахлордибензо-и-диоксины |
|
ТХДФ |
Тетрахлордибензофураны |
|
ПеХДД |
Пентахлордибензо-п-диоксины |
|
ПеХДФ |
Пентахлордибензофураны |
|
ГкХДД |
Гексахлордибензо-п-диоксины |
|
ГкХДФ |
Гексахлордибензофураны |
|
ГпХДД |
Гептахлордибензо-п-диоксины |
|
ГпХДФ |
Гептахлордибензофураны |
|
ОХДФ |
Октахлордибензо-п-диоксины |
|
ОХДФ |
Октахлордибензофураны |
|
мг |
миллиграмм (1 мг = 10-3 г) |
|
мкг |
микрограмм (1 мкг = 10-6 г) |
|
нг |
нанограмм (1 нг = 10-9 г) |
|
пг |
пикограмм (1 пг = 10-12 г) |
|
ХИ ОИ |
химическая ионизация с регистрацией отрицательных ионов |
Приложение 3 (обязательное)
|
Вещество |
Номер CAS |
Изотопно-меченый аналог |
Номер CAS |
|
2,3,7,8-ТХДД |
1746-01-6 |
13С12-2,3,7,8-ТХДД |
76523-40-5 |
|
37Сl4-2,3,7,8-ТХДД |
85508-50-5 |
||
|
Сумма ТХДД |
41903-57-5 |
|
|
|
2,3,7,8-ТХДФ |
51207-31-9 |
13С12-2,3,7,8-ТХДФ |
89059-46-1 |
|
Сумма-ТХДФ |
55722-27-5 |
|
|
|
1,2,3,7,8-ПеХДД |
40321-76-4 |
13C12-1,2,3,7,8-ПеХДД |
109719-79-1 |
|
Сумма-ПеХДД |
36088-22-9 |
|
|
|
1,2,3,7,8-ПеХДФ |
57117-41-6 |
13C12-1,2,3,7,8-ПеХДФ |
109719-77-9 |
|
2,3,4,7,8-ПеХДФ |
57117-31-4 |
13С12-2,3,4,7,8-ПеХДФ |
116843-02-8 |
|
Сумма-ПеХДФ |
30402-15-4 |
|
|
|
1,2,3,4,7,8-ГкХДД |
39227-28-6 |
13C12-1,2,3,4,7,8-ГкХДД |
109719-80-4 |
|
1,2,3,6,7,8-ГкХДД |
57653-85-7 |
13C12-1,2,3,6,7,8-ГкХДД |
109719-81-5 |
|
1,2,3,7,8,9-ГкХДД |
19408-74-3 |
13C12-l,2,3,7,8,9-ГкХДД |
109719-82-6 |
|
Сумма-ГкХДД |
34465-46-8 |
|
|
|
1,2,3,4,7,8-ГкХДФ |
70648-26-9 |
13C12-l,2,3,4,7,8-ГкХДФ |
114423-98-2 |
|
1,2,3,6,7,8-ГкХДФ |
57117-44-9 |
13C12-1,2,3,6,7,8-ГкХДФ |
116843-03-9 |
|
1,2,3,7,8,9-ГкХДФ |
72918-21-9 |
13C12-1,2,3,7,8,9-ГкХДФ |
116843-04-0 |
|
2,3,4,6,7,8-ГкХДФ |
60851-34-5 |
13С12-2,3,4,6,7,8-ГкХДФ |
116843-05-1 |
|
Сумма-ГкХДФ |
55684-94-1 |
|
|
|
1,2,3,4,6,7,8-ГпХДД |
35822-46-9 |
13C12-1,2,3,4,6,7,8-ГпХДД |
109719-83-7 |
|
Сумма-ГпХДД |
37871-00-4 |
|
|
|
1,2,3,4,6,7,8-ГпХДФ |
67562-39-4 |
13C12-l,2,3,4,6,7,8-ГпХДФ |
109719-84-8 |
|
1,2,3,4,7,8,9-ГпХДФ |
55673-89-7 |
13С12-1,2,3,4,7,8,9-ГпХДФ |
109719-94-0 |
|
Сумма-ГпХДФ |
38998-75-3 |
|
|
|
ОХДД |
3268-87-9 |
13С12-ОХДД |
114423-97-1 |
|
ОХДФ |
39001-02-0 |
|
|
Таблица 2. Коэффициенты токсичности ПХДД и ПХДФ Всемирной организации здравоохранения
|
Вещество |
Коэффициент токсичности, WHO-TEF |
|
|
система 1998 г. |
система 2005 г. |
|
|
полихлорированные дибензо-п-диоксины |
||
|
2,3,7,8-ТХДД |
1 |
1 |
|
1,2,3,7,8-ПеХДД |
1 |
1 |
|
1,2,3,4,7,8-ГкХДД |
0,1 |
0,1 |
|
1,2,3,6,7,8-ГкХДД |
0,1 |
0,1 |
|
1,2,3,7,8,9-ГкХДД |
0,1 |
0,1 |
|
1,2,3,4,6,7,8-ГпХДД |
0,01 |
0,01 |
|
ОХДД |
0,0001 |
0,0003 |
|
полихлорированные дибензофураны |
||
|
2,3,7,8-ТХДФ |
0,1 |
0,1 |
|
1,2,3,7,8-ПеХДФ |
0,05 |
0,03 |
|
2,3,4,7,8-ПеХДФ |
0,5 |
0,3 |
|
1,2,3,4,7,8-ГкХДФ |
0,1 |
0,1 |
|
1,2,3,6,7,8-ГкХДФ |
0,1 |
0,1 |
|
1,2,3,7,8,9-ГкХДФ |
0,1 |
0,1 |
|
2,3,4,6,7,8-ГкХДФ |
0,1 |
0,1 |
|
1,2,3,4,6,7,8-ГпХДФ |
0,01 |
0,01 |
|
1,2,3,4,7,8,9-ГпХДФ |
0,01 |
0,01 |
|
ОХДФ |
0,0001 |
0,0003 |
Таблица 3. Международная система коэффициентов токсичности ПХДД и ПХДФ
|
Вещество |
Коэффициент токсичности, I-TEF |
|
полихлорированные дибензо-п-диоксины |
|
|
2,3,7,8-ТХДД |
1 |
|
1,2,3,7,8-ПеХДД |
0,5 |
|
1,2,3,4,7,8-ГкХДД |
0,1 |
|
1,2,3,6,7,8-ГкХДД |
0,1 |
|
1,2,3,7,8,9-ГкХДД |
0,1 |
|
1,2,3,4,6,7,8-ГпХДД |
0,01 |
|
ОХДД |
0,001 |
|
полихлорированные дибензофураны |
|
|
2,3,7,8-ТХДФ |
0,1 |
|
1,2,3,7,8-ПеХДФ |
0,05 |
|
2,3,4,7,8-ПеХДФ |
0,5 |
|
1,2,3,4,7,8-ГкХДФ |
0,1 |
|
1,2,3,6,7,8-ГкХДФ |
0,1 |
|
1,2,3,7,8,9-ГкХДФ |
0,1 |
|
2,3,4,6,7,8-ГкХДФ |
0,1 |
|
1,2,3,4,6,7,8-ГпХДФ |
0,01 |
|
1,2,3,4,7,8,9-ГпХДФ |
0,01 |
|
ОХДФ |
0,001 |
Приложение 4 (рекомендуемое)
Форма представления результатов анализа
ПРОТОКОЛ № _____ от «___» _____________________________________________ количественного химического анализа пробы _____________________________________________________________________
Подпись ответственного исполнителя ______________ Примечание: допустимо представление дополнительной информации по характеристикам проб, отбору проб и результатам анализа.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||