ЦЕНТР ИССЛЕДОВАНИЯ И КОНТРОЛЯ ВОДЫ
|
|
УТВЕРЖДАЮ Главный инженер Центра исследования контроля воды ____________ Г.Ф. Глущенкова 02.11.2005 г. |
КАЧЕСТВО ВОДЫ.
Методика выполнения измерений содержания
свободной углекислоты в пробах питьевых и природных вод.
Титриметрический метод.
ЦВ 1.01.17-2004
ФР.1.31.2005.01580
Санкт-Петербург
2005
|
КАЧЕСТВО ВОДЫ. Методика
выполнения измерений |
1 Область применения
Настоящий документ устанавливает титриметрический метод определения содержания свободной углекислоты в пробах питьевых и природных вод в диапазоне измерений от 5,0 до 300 мг/дм3.
Метод определения содержания свободной углекислоты включает три этапа:
1) определение общей кислотности;
2) определение свободной кислотности;
3) определение кислотности, обусловленной слабыми нелетучими кислотами.
Содержание свободной углекислоты определяют по общей кислотности за вычетом свободной кислотности и кислотности, обусловленной слабыми нелетучими кислотами. Соотношение форм углекислоты от рН воды приведено в Приложении А.
2 Нормативные ссылки
В настоящем документе использованы ссылки на следующие стандарты:
ГОСТ 12.0.004-90 ССБТ. Организация обучения безопасности труда. Общие положения.
ГОСТ 12.1.004-91 ССБТ. Пожарная безопасность. Общие требования.
ГОСТ 12.1.007-76 ССБТ. Вредные вещества. Классификация и общие требования безопасности.
ГОСТ 12.4.009-83 ССБТ. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание.
ГОСТ 12.1.019-79 ССБТ. Электробезопасность. Общие требования и номенклатура видов защиты.
ГОСТ 12.4.021-75 ССБТ. Системы вентиляционные. Общие требования.
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия.
ГОСТ 4328-77 Натрия гидроокись. Технические условия.
ГОСТ 6709-72. Вода дистиллированная. Технические условия.
ГОСТ 9147-80 Посуда и оборудование фарфоровые. Технические условия.
ГОСТ 10733-98 Часы наручные и карманные механические. Общие технические условия.
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия.
ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия.
ГОСТ 24104-2001 Весы лабораторные. Общие технические требования.
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры.
ГОСТ 27752-88 Часы электронно-механические кварцевые настольные, настенные и часы будильники. Общие технические условия.
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические условия. Методы испытания.
ГОСТ 29251-91 Посуда лабораторная стеклянная. Бюретки. Часть 1. Общие требования.
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб.
ГОСТ Р 51593-2000 Вода питьевая. Отбор проб.
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецезионность) методов и результатов измерений. Часть 6. Использование значений точности на практике.
3 Средства измерений, вспомогательное оборудование, реактивы, материалы
Весы лабораторные по ГОСТ 24104, с ценой деления не более 10 мг и наибольшим пределом взвешивания не менее 500 г.
Термометр стеклянный лабораторный по ГОСТ 28498 с ценой деления 2 °С, с диапазоном измерений от 0 до 150 °С.
РН-метр с погрешностью измерения не более ±0,1 ед. рН.
Бюретки по ГОСТ 29251, 2 класса точности, номинальной вместимостью 2, 5, 10, 25 см3.
Пипетки градуированные по ГОСТ 29227.
Колбы мерные по ГОСТ 1770, 2 класса точности.
Цилиндры с носиком 2 класса точности или мензурки по ГОСТ 1770.
Часы любого типа, например, по ГОСТ 10733 или ГОСТ 27752.
Шкаф сушильный общелабораторного назначения, обеспечивающий поддержание температуры (105 ± 5) °С.
Электроплитки с закрытой спиралью по ГОСТ 14919.
Колбы конические по ГОСТ 25336, вместимостью 250 см3.
Воронки стеклянные по ГОСТ 25336.
Стаканы химические по ГОСТ 25336.
Стаканчики для взвешивания по ГОСТ 25336.
Вода дистиллированная по ГОСТ 6709.
Натрия гидроокись по ГОСТ 4328, ч.д.а. или стандарт-титр, например, по ТУ-2642-001-0750062
Соляная кислота стандарт-титр, например, по ТУ 6-09-2540.
Метиловый оранжевый (индикатор), например, по ТУ- 6-09-5171.
Фенолфталеин (индикатор), например, по ТУ-6-09-5360.
Спирт этиловый по ГОСТ 18300.
Допускается использование средств измерений, вспомогательного оборудования и реактивов с метрологическими и техническими характеристиками не хуже указанных.
4 Отбор проб
Общие требования к отбору проб по ГОСТ Р 51592 и ГОС Р 51593.
Для измерения содержания свободной углекислоты пробы воды отбирают в посуду из стекла или полимерных материалов вместимостью не менее 500 см3 так, чтобы между слоем воды и пробкой не было воздушного пространства. Пробы не консервируют, к анализу приступают как можно быстрее, но не позднее, чем через 6 ч.
5 Подготовка к выполнению измерений
5.1 Приготовление растворов
5.1.1 Раствор гидроксида натрия молярной концентрации С (NaOH) = 15 моль/дм3
Растворяют 625 г гидроксида натрия в 800 см3 дистиллированной воды и оставляют раствор для осветления не менее, чем на 48 часов. Хранят раствор в плотно закрытом полиэтиленовом сосуде не более 6 мес.
5.1.2 Раствор гидроксида натрия молярной концентрации С (NaOH) = 0,1 моль/дм3
Для приготовления 1 дм3 раствора 6,6 см3 раствора гидроксида натрия, приготовленного по 5.1.1, вносят в мерную колбу вместимостью 1 дм3 и доводят до метки прокипяченной дистиллированной водой. Раствор хранят в сосуде с закрытой пробкой с хлор-кальциевой трубкой. Срок хранения - не более 1 мес. с еженедельным определением титра раствора.
В случае применения стандарт-титра (фиксанала) раствор готовят в соответствии с инструкцией по приготовлению. Раствор хранят в плотно закрытом полиэтиленовом сосуде. Срок хранения - не более 1 мес.
Поправочный коэффициент устанавливают по раствору соляной кислоты молярной концентрации С (НСl) = 0,1 моль/дм3.
5.1.3 Раствор гидроксида натрия молярной концентрации С (NaOH) = 0,01 моль/дм3
Для приготовления 1 дм3 раствора 100 см3 раствора гидроксида натрия, приготовленного по п. 5.1.2, вносят в мерную колбу вместимостью 1 дм3 и доводят до метки прокипяченной дистиллированной водой.
Поправочный коэффициент устанавливают по раствору соляной кислоты молярной концентрации С (НСl) = 0,01 моль/дм3.
Хранят раствор в плотно закрытом полиэтиленовом сосуде. Срок хранения - не более 7 сут.
5.1.4 Раствор соляной кислоты молярной концентрации С (НСl) = 0,1 моль/дм3
Раствор готовят из стандарт-титра (фиксанала) в соответствии с инструкцией по приготовлению. Раствор хранят в плотно закрытом стеклянном сосуде. Срок хранения - не более 6 мес.
5.1.5 Раствор соляной кислоты молярной концентрации С (НСl) = 0,01 моль/дм3
Для приготовления 1 дм3 раствора 100 см3 раствора соляной кислоты, приготовленного по п. 5.1.4, вносят в мерную колбу вместимостью 1 дм3 и доводят до метки прокипяченной дистиллированной водой. Срок хранения - не более 3 мес.
5.1.6 Раствор гидроксида натрия молярной концентрации С (NaOH) = 0,02 моль/дм3
Для приготовления 1 дм3 раствора 200 см3 раствора гидроксида натрия, приготовленного по п. 5.1.2, помещают в мерную колбу вместимостью 1 дм3 и доводят дистиллированной прокипяченной водой до метки. Хранят раствор в плотно закрытом полиэтиленовом сосуде. Срок хранения - не более 7 сут.
5.1.7 Приготовление индикаторов
5.1.7.1 Раствор метилового оранжевого
Для приготовления 1 дм3 раствора 0,5 г метилового оранжевого растворяют в небольшом количестве дистиллированной воды, количественно переносят в мерную колбу вместимостью 1 дм3 и доводят до метки дистиллированной водой. Срок хранения - не более 6 мес.
5.1.7.2 Раствор фенолфталеина
0,5 г фенолфталеина растворяют в 50 см3 96 % этилового спирта и добавляют 50 см3 дистиллированной воды. В раствор по каплям добавляют раствор гидрооксида натрия, приготовленный по 5.1.6, до появления слабой розовой окраски. Срок хранения - не более 1 года.
5.2 Установление поправочных коэффициентов растворов гидроксида натрия
В коническую колбу вместимостью 250 см3 наливают 70 ÷ 80 см3 прокипяченной дистиллированной воды, 10 см3 соляной кислоты (VHCL), см3, добавляют 3 - 5 капель раствора фенолфталеина и титруют раствором гидроксида натрия, (VNaOH), см3, до бледно-розового окрашивания, не исчезающего в течение 10 ÷ 30 с. Титрование повторяют 1 - 3 раза. Из полученных результатов берут среднее. Поправочный коэффициент раствора гидроксида натрия вычисляют по формуле:
K = VHCL/VNaOH
Значение поправочного коэффициента должно быть равным (1,00 ± 0,03). Если поправочный коэффициент выходит из указанных пределов, то раствор гидроксида натрия, соответственно, укрепляют или разбавляют. Поправочный коэффициент устанавливают при приготовлении растворов гидроксида натрия, но не реже 1 раза в неделю.
6 Выполнение измерений
6.1 Определение общей кислотности
В коническую колбу вместимостью 250 см3 помещают мензуркой или цилиндром 100 см3 исследуемой пробы, добавляют 5 ÷ 10 капель раствора фенолфталеина и титруют раствором гидроксида натрия, приготовленным по 5.1.2 или 5.1.3, до появления слаборозовой окраски, не исчезающей в течение 2 ÷ 3 мин.
Конечную точку титрования можно определить потенциометрически, проводя титрование до получения устойчивого значения рН = (8,3 ± 0,1).
Если при добавлении фенолфталеина к исследуемой пробе раствор сразу приобретает розовую окраску, отмечают, что углекислота отсутствует.
При необходимости определение общей кислотности повторяют следующим образом: в коническую колбу вместимостью 250 см3 помещают 5 ÷ 10 капель раствора фенолфталеина, почти весь объем титрованного раствора гидроксида натрия, затем 100 см3 исследуемой пробы, после чего дотитровывают по каплям до устойчивого розового окрашивания, либо до рН (8,3 ± 0,1) при потенциометрическом титровании.
6.2 Определение свободной кислотности
В коническую колбу вместимостью 250 см3 помещают мензуркой или цилиндром 100 см3 исследуемой воды, добавляют 3 капли раствора метилового оранжевого и титруют раствором гидроксида натрия, приготовленным по 5.1.2 или 5.1.3 до перехода окраски в золотисто-розовую.
Конечную точку титрования можно определить потенциометрически, проводя титрование до получения устойчивого значения рН = (4,5 ± 0,1).
Если при добавлении раствора метилового оранжевого к исследуемой пробе раствор становится желтым, отмечают, что свободная кислотность отсутствует (значение содержания свободной кислотности равно нулю).
6.3 Определение кислотности, обусловленной слабыми нелетучими кислотами
Оттитрованную по 6.2 пробу воды кипятят в течение 2 мин для удаления свободной двуокиси углерода, быстро охлаждают, добавляют 5 ÷ 10 капель раствора фенолфталеина и титруют раствором гидроксида натрия, приготовленным по 5.1.2 или 5.1.3, до появления устойчивого слабо-розового окрашивания. Конечную точку титрования можно определить потенциометрически, проводя титрование до получения устойчивого значения рН = (8,3 ± 0,1).
7 Вычисление результатов измерений
7.1 Значение общей кислотности, соб ммоль/дм3, вычисляют по формуле:
![]()
где С - молярная концентрация раствора гидроксида натрия, моль/дм3;
K - поправочный коэффициент раствора гидроксида натрия;
VToб - объем раствора гидроксида натрия, пошедшего на титрование, см3;
1000 - коэффициент массового пересчета;
V - объем пробы, взятой для определения, см3.
7.2 Значение свободной кислотности, ссв, ммоль/дм3, вычисляют по формуле:
![]()
где С - молярная концентрация раствора гидроксида натрия, моль/дм3;
K - поправочный коэффициент раствора гидроксида натрия;
VTcв - объем раствора гидроксида натрия, пошедшего на титрование, см3;
1000 - коэффициент массового пересчета;
V - объем пробы, взятой для определения, см3.
7.3 Значение кислотности, обусловленной слабыми нелетучими кислотами, сснк, ммоль/дм3, вычисляют по формуле:
![]()
где С - молярная концентрация раствора гидроксида натрия, моль/дм3;
K - поправочный коэффициент раствора гидроксида натрия;
VTснк - объем раствора гидроксида натрия, пошедшего на титрование, см3;
1000 - коэффициент массового пересчета;
V - объем пробы, взятой для определения, см3.
7.4 Значение содержания свободной углекислоты, у, мг/дм3, вычисляют по формуле:
у = 44∙(Соб - Ссв - Сснк),
где 44 - коэффициент пересчета.
7.5 При необходимости проверки приемлемости результатов измерения в условиях повторяемости (например, по требованию заказчика или в случае анализа сложных проб) получают два результата измерений содержания свободной углекислоты в пробах природных и питьевых вод по разделу 6 в условиях повторяемости.
Проверяют приемлемость результатов измерений, сравнивания расхождение между ними с пределом повторяемости (r для n = 2, таблица 2). Если полученное значение расхождения не превышает предела повторяемости, то за результат измерений содержания свободной углекислоты в пробе принимают среднее из двух полученных значений. В противном случае процедуру повторяют.
9 Оформление и представление результатов измерений
Результаты измерений содержания свободной углекислоты в анализируемой пробе в документах, предусматривающих их использование, представляют в виде:
у ± U, мг/дм3,
где U - расширенная неопределенность, вычисленная по формуле:
![]()
где ![]() -
значение расширенной неопределенности в относительных единицах из таблицы 1.
-
значение расширенной неопределенности в относительных единицах из таблицы 1.
10 Неопределенность измерений
Настоящая методика выполнения измерений обеспечивает получение результатов с расширенной неопределенностью, значения которой приведены в таблице 1.
|
Диапазон измерений содержания свободной углекислоты, у, мг/дм3 |
Суммарная стандартная неопределенность, |
Расширенная неопределенность, k
= 2, |
|
от 5 до 300 включ |
10 |
20 |
11 Контроль качества результатов измерений
Контроль стабильности результатов измерений в лаборатории осуществляют, используя методы контроля стабильности стандартного отклонения повторяемости. Для этого используют приведенные к среднему значению результатов анализа значения расхождений (w') полученных результатов единичных измерений с1 и с2, которые сравнивают с рассчитанными при построений контрольных карт пределами предупреждения и действия
w' ≤ UCL
w' = |c1 - с2|/y
у = 0,5 (c1 + с2),
где UCL - пределы действия, UCLд = 3,686σr или
предупреждения, UCLп = 2,834σr,
где σr - стандартное отклонение повторяемости результатов для значения у численно равного 1. Значение стандартного отклонения повторяемости приведено в таблице 2.
|
Диапазон измерений содержания свободной углекислоты, мг/дм3 |
Стандартное отклонение повторяемости, σr, % |
Предел повторяемости, r, % (n = 2) |
|
от 5 до 300 включ. |
9 |
25 |
Пример. За три дня получены результаты параллельных определений: 5,2 и 6,3 мг/дм3; 23 и 25 мг/дм3; 34 и 36 мг/дм3.
Рассчитывают расхождения:
w1' = |5,2 - 6,3|/0,5∙(5,2 + 6,3) = 0,19
w2' = |23 - 25|/0,5∙(23 + 25) = 0,08
w3' = |34 - 36|/0,5∙(34 + 36) = 0,19
Значения расхождений наносят на контрольную карту.
Для расчета UCLп и UCLд из таблицы 2 берут σr = 9 %.
Расчет UCLп = 2,834∙0,09 = 0,26; UCLд = 3,686∙0,09 = 0,33, где 0,09 - абсолютное значение σr = 9 % для у = 1.
При неудовлетворительных результатах контроля, например, превышение предела действия или регулярное превышение предела предупреждения, выясняют причины этих отклонений, в том числе проверяют работу оператора.
Периодичность проведения контроля стабильности результатов измерений устанавливают индивидуально для каждой лаборатории в соответствии с документами по внутрилабораторному контролю качества результатов анализа.
После внедрения МВИ в практику работы лаборатории при необходимости проверки приемлемости результатов измерений, полученных в условиях воспроизводимости, проводят межлабораторные сравнительные испытания с использованием данной методики для оценки стандартного отклонения воспроизводимости. Для расчета стандартного отклонения воспроизводимости используют ГОСТ Р ИСО 5725-2-2002, пункт 7.4. Проверку приемлемости результатов измерений в условиях воспроизводимости осуществляют по ГОСТ Р ИСО 5725-6-2002, пункт 5.3.
12 Требования безопасности
При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007 и ГОСТ 12.4.021.
При работе с электроустановками должны соблюдаться требования по электробезопасности по ГОСТ 12.1.019.
Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
Исполнители должны быть проинструктированы о мерах безопасности при работе с нагревательными приборами. Организация обучения работающих безопасности труда производится по ГОСТ 12.0.004.
13 Требования к квалификации оператора
Измерения по методике может выполнять лаборант, имеющий навыки работы в химической лаборатории и освоивший данную методику.
14 Условия выполнения измерений
При подготовке к выполнению измерений и при их проведении необходимо соблюдать условия, установленные в руководстве по эксплуатации или паспортах средств измерений и вспомогательных устройств. Измерение объема воды производится при температуре от 15 до 25 °С.
Приложение А
Соотношения форм производных угольной кислоты от рН воды
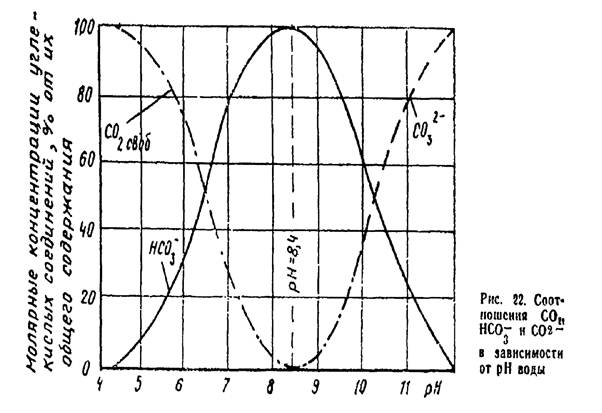
Рисунок 1А
Соотношения форм производных угольной кислоты от рН воды.
В зависимости от рН воды углекислота встречается в ней в свободном состоянии в виде углекислого газа СО2, в виде бикарбонат-ионов НСО-3 и карбонат-ионов СО2-3. При рН < 4,0 бикарбонат-ионы в воде отсутствуют и вся углекислота находится в виде углекислого газа. При рН 8,4 в воде содержатся почти одни ионы НСО-3 и при рН выше 10,5 - только ионы СО2-3.
Находящиеся в воде ионы НСО-3, СО2-3 и углекислый газ связаны углекислотным равновесием
СО2 + Н2О ↔ Н2СО3 ↔ Н+ + НСО-3 ↔ 2Н+ + СО2-3
Часть свободной углекислоты, находящаяся в равновесии с бикарбонатами, называется равновесной. Она как бы связана с бикарбонатами и поэтому не вступает в химические реакции. Избыточная свободная (или иначе агрессивная) углекислота в отличие от равновесной является очень активной и реакционно-способной.
В водах открытых водоемов вследствие низкого содержания углекислоты в воздухе наличие агрессивной углекислоты маловероятно. В подземных водах содержание агрессивной углекислоты иногда бывает довольно значительным.
СВИДЕТЕЛЬСТВО № 070094 о
метрологической аттестации ЦВ 1.01.17-2004 Методика выполнения измерений содержания свободной углекислоты в пробах питьевых и природных вод, разработанная Центром исследования и контроля воды, регламентированная в документе: «Качество воды. Методика выполнения измерений содержания свободной углекислоты в пробах питьевых и природных вод. Титриметрический метод. ЦВ 1.01.17-2004» аттестована в соответствии с ГОСТ Р 8.563-96. Аттестация осуществлена по результатам экспериментального исследования МВИ и метрологической экспертизы материалов по ее разработке. В результате аттестации установлено, что МВИ соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
Дата выдачи свидетельства 22 октября 2004 года
|
СОДЕРЖАНИЕ