Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств
пестицидов в пищевых продуктах,
сельскохозяйственном сырье и объектах
окружающей среды
Сборник
МУК 4.1.2859 - 4.1.2866-11
Москва 2011
1. Разработаны Российским государственным аграрным университетом - МСХА им. К.А. Тимирязева, Учебно-научный консультационный центр «Агроэкология пестицидов и агрохимикатов» Минсельхоза России (В.А. Калинин, профессор, канд. с-х. наук., Е.В. Довгилевич, ст.н.сотр., канд. биол. наук, А.В. Довгилевич, ст.н.сотр., канд. хим. наук, Н.В. Устименко, ст.н.сотр., канд. биол. наук, Е.Н. Щербинкина, инженер).
2. Рекомендованы к утверждению Комиссией по санитарно-эпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 28 12.2010 № 3).
3. Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г.Г. Онищенко 31 марта 2011 г.
4. Введены в действие с момента утверждения.
5. Введены впервые.
СОДЕРЖАНИЕ
|
|
УТВЕРЖДАЮ Руководитель
Федеральной службы Г.Г. Онищенко 31 марта 2011 г. Дата введения: с момента утверждения |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств Фенпропидина
в зеленой массе, зерне и соломе зерновых культур методом
высокоэффективной жидкостной хроматографии
Методические указания
МУК 4.1.2865-11
Общие положения и область применения
Свидетельство об аттестации методики от 25.06.2010 № 01.5.04.686.
Настоящий документ устанавливает метод высокоэффективной жидкостной хроматографии для определения массовой концентрации Фенпропидина в зеленой массе и зерне зерновых культур в диапазоне концентраций 0,01 - 0,1 мг/кг и в соломе в диапазоне 0,04 - 0,4 мг/кг.
Действующее вещество: Фенпропидин.
Структурная формула:
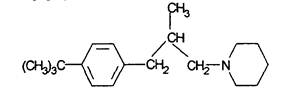
Название действующего вещества по ИЮПАК: (RS)-l-[3-(4-тpeтбутилфенил)-2-метилпропил]пиперидин.
Молекулярная масса: 273,5.
Эмпирическая формула: C19H31N.
Химически чистое вещество представляет собой бледно-желтую слегка вязкую жидкость без запаха.
Температура кипения > 250 °С, 70,2 °С/1,1 Ра.
Давление пара 17 мРа (25 °С).
Коэффициент распределения в системе н-октанол-вода: Kоw lgP = 2,9 (рН 7, 25 °С).
Растворимость в воде (мг/дм3, 25 °С): 530 (рН 7); 6,2 (рН 9).
Легко смешивается с ацетоном, этанолом, толуолом, н-октанолом и гексаном (25 °С). Стабилен при хранении в закрытом контейнере при комнатной температуре, по крайней мере, в течение 3 месяцев. Водные растворы устойчивы к воздействию УФ-света и гидролизу при 80 °С (рН 4,7 и 10). рКа 10,1 (сильное основание).
Краткая токсикологическая характеристика: у крыс острая оральная токсичность LD50 > 1447 мг/кг; при подкожном введении LD50 > 4000 мг/кг. Ингаляционная токсичность LD50 1220 мг в 1 м3 воздуха (Время экспозиции 4 ч). У кроликов вызывает раздражение кожи и глаз.
Не обладает мутагенным, канцерогенным и тератогенным действием.
Область применения: Фенпропидин - лиственный фунгицид системного действия с целебным защитным и искореняющим эффектом. Подавляет развитие таких заболеваний зерновых культур, как ложномучнистая роса, ржавчина и пятна на листьях, вызываемые, соответственно, фибами из родов Erysiphe graminis, Puccinia SPP и Rhynchosporium secalis.
Гигиенические нормативы в России для фенпропидина: МДУ в зерне хлебных злаков 0,25 мг/кг.
1. Метрологическая характеристика метода
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1 для соответствующих диапазонов концентраций.
Метрологические параметры
|
Объект анализа |
Диапазон определяемых концентраций, мг/кг |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr, % |
Показатель внутрилабораторной прецизионности, σRл, % |
Показатель воспроизводимости, σR, % |
Показатель точности* (границы относительной погрешности), ±δ, % |
|
Зеленая масса |
0,01 - 0,10 |
6 |
7 |
8 |
16 |
|
Зерно |
0,01 - 0,10 |
6 |
7 |
8 |
16 |
|
Солома |
0,04 - 0,10 |
5 |
6 |
8 |
16 |
|
0,10 - 0,40 |
3 |
4 |
5 |
10 |
|
|
* Соответствует расширенной неопределенности Uотн (в относительных единицах) при коэффициенте охвата k = 2. |
|||||
Полнота извлечения Фенпропидина, стандартное отклонение, доверительный интервал среднего результата для n = 20, Р = 0.95
|
Анализируемый объект |
Предел обнаружения, мг/кг |
Диапазон определяемых концентраций, мг/кг |
Среднее значение определения, % |
Стандартное отклонение, S |
Доверительный интервал среднего результата, ± % |
|
Зеленая масса |
0,01 |
0,01 - 0,1 |
87,3 |
5,15 |
2,4 |
|
Зерно |
0,01 |
0,01 - 0,1 |
90,4 |
5,8 |
2,7 |
|
Солома |
0,04 |
0,04 - 0,4 |
88,15 |
8,3 |
3,9 |
2. Метод измерения
Методика основана на определении Фенпропидина методом ВЭЖХ с использованием УФ-детектора после его экстракции из образцов смесью органического растворителя с водой и очистки экстракта путем перераспределения кислотно-основных форм Фенпропидина между двумя несмешивающимися фазами и методом твердофазной экстракции.
Идентификация Фенпропидина проводится по времени удерживания, количественное определение - методом абсолютной калибровки.
Избирательность метода обеспечивается сочетанием условий подготовки проб и хроматографирования.
3. Средства измерений, реактивы, вспомогательные устройства и материалы
3.1. Средства измерений
|
Жидкостный хроматограф «ACQUITY» фирмы «Waters» с быстросканирующим УФ-детектором, снабженным дегазатором, автоматическим пробоотборником и термостатом колонки |
|
|
Весы аналитические ВЛА-200 |
|
|
Весы технические BЛКT-500 |
|
|
рН-метр фирмы «Наnnа Instrument», мод. Р212 |
|
|
Колбы мерные на 10, 50, 100, 1000 см3 |
|
|
Микродозаторы Ленпипет переменного объема от 200 до 1000 мм3 и от 1 до 5 см3 |
|
|
Пипетки градуированные |
|
|
Цилиндры мерные на 50 и 100 см3 |
Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Ацетон, чда |
|
|
Ацетонитрил для ВЭЖХ, «В-230НМ» или хч |
ТУ 6-09-3534-87 |
|
Гексан, хч |
ТУ 2631-003-05807999-98 |
|
Вода бидистиллированная, деионизированная, Фенпропидин с содержанием основного вещества 97,7 %, Мактешим Аган |
ГОСТ 6709-79 |
|
Натрий сернокислый, безводный, хч |
|
|
Соляная кислота, 0,1М водный раствор |
|
|
Гидроксид натрия, 1М водный раствор |
|
|
Подвижная фаза для ВЭЖХ: смесь ацетонитрила и 0,005 М ортофосфорной кислоты в соотношении 40:60 |
|
Допускается использование реактивов квалификацией не ниже указанных.
3.3. Вспомогательные устройства и материалы
|
Аналитическая колонка ACQUITY UPLC ВЕН С18 (100×2,1) мм, 1,7 мкм (Waters) Ультразвуковая баня «Сапфир» |
|
|
Воронки лабораторные В-75-110 |
|
|
Бидистиллятор |
|
|
Ротационный вакуумный испаритель фирмы BUCHI, мод. R 205 |
|
|
Фильтры бумажные «красная лента» |
ТУ 6.091678-86 |
|
Патроны, заполненные силикагелем 60 (Merck), 0,5 г |
|
Допускается использование другого вспомогательного оборудования с техническими характеристиками не хуже указанных.
4. Требования безопасности
4.1. При работе необходимо соблюдать требования техники безопасности, установленные для работ с токсичными, едкими, легковоспламеняющимися веществами (ГОСТ 12.1.005, ГОСТ 12.1.007). Организация обучения работников безопасности труда - ГОСТ 12.0.004.
При выполнении измерений с использованием жидкостного хроматографа и работе с электроустановками соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019-79 и инструкциями по эксплуатации приборов.
4.2. Помещение лаборатории должно быть оборудовано приточно-вытяжной вентиляцией, соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009. Содержание вредных веществ в воздухе не должно превышать норм, установленных ГН 2.2.5.1313-03 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны».
5. Требования к квалификации операторов
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы методом высокоэффективной жидкостной хроматографии, ознакомленный с руководством по эксплуатации хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п. 13.
6. Условия измерений
При выполнении измерений выполняют следующие условия:
• процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха 20 ± 5 °С и относительной влажности не более 80 %.
• выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к определению
7.1. Кондиционирование колонки
Перед началом анализа колонку (Acquity ВЕН С18) кондиционируют в потоке подвижной фазы (0,1 - 0,2 см3/мин) до стабилизации нулевой линии.
7.2. Приготовление растворов
7.2.1. 0,005 М раствор ортофосфорной кислоты: 0,5 ± 0,01 г 98 % ортофосфорной кислоты помещают в мерную колбу объемом 1 дм3, растворяют в бидистиллированной воде и доводят объем до метки.
7.2.2. Для приготовления подвижной фазы смешивают ацетонитрил с 0,005 М раствором ортофосфорной кислоты в соотношении 40:60 по объему, используя мерные цилиндры.
7.2.3. Приготовление элюента для твердофазной экстракции. В мерную колбу вместимостью 100 см3 помещают 20 см3 ацетона и доводят объем до метки гексаном. Перемешивают. Элюент хранят в вытяжном шкафу и используют свежеприготовленным.
7.3. Приготовление основного и градуировочных растворов
7.3.1. Основной раствор с концентрацией 0,5 мг/см3: точную навеску Фенпропидина (50 ± 0,5 мг) помещают в мерную колбу вместимостью 100 см3, растворяют в ацетонитриле и доводят объем до метки тем же растворителем.
Градуировочные растворы с концентрациями 0,1, 0,2, 0,5, 0,75 и 1,0 мкг/см3 готовят методом последовательного разбавления основного раствора по объему, используя подвижную фазу.
7.3.2. Раствор № 1 с концентрацией 1,0 мкг/см3: в мерную колбу вместимостью 100 см3 вносят 0,2 см3 основного раствора и доводят объем до метки подвижной фазой.
7.3.3. Раствор № 2 с концентрацией 0,75 мкг/см3: в мерную колбу вместимостью 10 см3 вносят 7,5 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.3.4. Раствор № 3 с концентрацией 0,5 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 5 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.3.5 Раствор № 4 с концентрацией 0,2 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 2,0 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.3.6. Раствор № 5 с концентрацией 0,1 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 1 см3 раствора № 1 и доводят объем до метки подвижной фазой.
Основной раствор можно хранить в холодильнике при температуре 0 - 4 °С в течение 1 месяца, градуировочные растворы - в течение суток.
При изучении полноты определения Фенпропидина в зеленой массе, зерне и соломе пшеницы используют ацетонитрильные растворы вещества.
7.4. Построение градуировочного графика
Для установления градуировочной характеристики (площадь пика - концентрация Фенпропидина в растворе) в хроматограф вводят по 10 мм3 градуировочных растворов (не менее 3 параллельных измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых концентраций). Затем измеряют площади пиков и строят график зависимости среднего значения площади пика от концентрации Фенпропидина в градуировочном растворе.
Методом наименьших квадратов рассчитывают градуировочный коэффициент (К) в уравнении линейной регрессии:
С = KS, где
S - площадь пика градуировочного раствора.
Градуировку признают удовлетворительной, если значение коэффициента линейной корреляции оказывается не ниже 0,99.
Градуировочную характеристику необходимо проверять при замене реактивов, хроматографической колонки или элементов хроматографической системы, а также при отрицательном результате контроля градуировочного коэффициента.
Градуировочную зависимость признают стабильной при выполнении следующего условия:
![]()
С - аттестованное значение массовой концентрации Фенпропидина в градуировочном растворе;
Ск - результат контрольного измерения массовой концентрации Фенпропидина в градуировочном растворе;
λконтр - норматив контроля градуировочного коэффициента, % (λконтр = 10 % при Р = 0,95).
7.5. Подготовка патронов для твердофазной экстракции
Непосредственно перед употреблением через патрон, заполненный силикагелем, пропускают 2,5 см3 гексана.
8. Отбор проб и хранение
Отбор проб зерна производится в соответствии с ГОСТ Р 50436-92 (ИСО 950-79) «Зерновые. Отбор проб зерна». Пробы зерна и соломы для определения остатков в урожае хранят в бумажной или тканевой упаковке при комнатной температуре. Перед анализом зерно и солому измельчают на лабораторных мельницах.
9. Проведение определения
9.1. Определение Фенпропидина в зеленой массе, зерне и соломе пшеницы
20 г зерна или измельченной зеленой массы или 5 г соломы помешают в коническую колбу вместимостью 250 см3 и экстрагируют 75 см3 смеси ацетона и воды в соотношении 7:3 в ультразвуковой бане в течение 15 мин. Массу фильтруют на воронке Бюхнера через бумажный фильтр «красная лента». Экстракцию повторяют с тем же объемом экстрагента. Объединенный экстракт упаривают на вакуумном ротационном испарителе при температуре водяной бани не выше 40 °С до полного удаления ацетона. Объем водного остатка доводят до 80 см3, подкисляют 1М раствором хлористоводородной кислоты до рН 3,0 и промывают дважды по 25 см3 гексана. Гексановый экстракт отбрасывают. К отделенному водному слою прибавляют около 5 см3 1М раствора гидроксида натрия до рН 9,0 и экстрагируют фенпропидин трижды по 25 см3 гексана. Экстракт фильтруют через слой безводного сульфата натрия и упаривают досуха на вакуумном ротационном испарителе при температуре водяной бани не выше 40 °С. Сухой остаток растворяют в 2,0 см3 гсксана и вносят в откондиционированный патрон, заполненный силикагелем. Патрон промывают 2 см3 гексана. Промывку отбрасывают. Фенпропидин элюируют 2 см3 элюента, приготовленного по п. 7.2.3. Элюат упаривают досуха. Сухой остаток растворяют в 1 см3 подвижной фазы, 10 мм3 полученного раствора вводят в хроматограф.
9.2. Условия хроматографирования
Ультраэффективный жидкостной хроматограф «ACQUITY» фирмы «Waters» с быстросканирующим УФ-детектором, снабженный дегазатором, автоматическим пробоотборником и термостатом колонки. Аналитическая колонка ACQUITY UPLC ВЕН С18 (2,1×100) мм, 1,7 мкм (Waters). Температура колонки (30 ± 1) °С. Подвижная фаза: смесь ацетонитрила и 0,005 М ортофосфорной кислоты в соотношении 40:60. Скорость потока элюента: 0,2 см3/мин. Рабочая длина волны УФ-детектора 220 нм. Объем вводимой пробы 10 мм3.
Время удерживания Фенпропидина 4,7 ± 0,1 мин.
Линейный диапазон детектирования сохраняется в интервале концентраций 0,1 - 1,0 мкг/см3.
10. Обработка результатов анализа
Количественное определение проводят методом абсолютной калибровки. Содержание Фенпропидина в зеленой массе, зерне и соломе пшеницы (X, мг/кг) вычисляют по формуле:
![]()
Sx - площадь пика Фенпропидина на хроматограмме испытуемого образца, мм2 (AU);
К - градуировочный коэффициент, найденный на стадии построения соответствующей градуировочной зависимости;
V - объем пробы, подготовленной для хроматографического анализа, см3;
Р - навеска анализируемого образца, г;
f - полнота извлечения Фенпропидина, приведенная в табл. 2 (%).
Содержание остаточных количеств фенпропидина в образце вычисляют как среднее из двух параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор Фенпропидина с концентрацией 1,0 мкг/см3, разбавляют подвижной фазой для ВЭЖХ.
11. Проверка приемлемости результатов параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости (1):
![]()
Х1 и Х2 - результаты параллельных определений, мг/кг;
r - значение предела повторяемости (r = 2,8σr).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
(X ± Δ) мг/ кг при вероятности Р = 0,95, где
Х - среднее арифметическое результатов определений, признанных приемлемыми, мг/кг;
Δ - граница абсолютной погрешности, мг/кг.
![]()
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание вещества в пробе менее нижней границы определения» (например: менее 0,01 мг/кг*, где * - 0,01 мг/кг - предел обнаружения Фенпропидина в зеленой массе и зерне пшеницы).
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Сд должна удовлетворять условию:
Сд = ΔЛX' + ΔЛX', где
±ΔЛX' (±ΔЛX') - характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой, соответственно), мг/кг; при этом:
ΔЛ = ±0,84Δ, где
Δ - граница абсолютной погрешности, мг/кг:
![]()
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк рассчитывают по формуле:
Кк = X' - X - Сд, где
X', X, Сд - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п. 11) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию:
|
|Кк| ≤ К, |
(2) |
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости (R):
|
|
(3) |
X1 и Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций), %.
14. Разработчики
Долженко В.И., Цибульская И.А., Журкович И.К., Луговкина Н.В., Ковров Н.Г. (ГНУ Всероссийский научно-исследовательский институт защиты растений, г. Санкт-Петербург).
Методика прошла метрологическую экспертизу (Свидетельство об аттестации № 01.5.04.2.015.25.11.09 от 26.11.09).