Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение концентраций ипконазола
в воздухе рабочей зоны и смывах
с кожных покровов операторов
методом капиллярной
газожидкостной хроматографии
Методические указания
МУК 4.1.2379-08
Москва 2009
1 .Разработаны Федеральным научным центром гигиены им. Ф.Ф. Эрисмана (Юдина Т.В., Ларькина М.В., Рогачева С.К.)
2. Рекомендованы к утверждению Комиссией по санитарно-эпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 3 апреля 2008 г. № 1).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г.Г. Онищенко 16 июня 2008 г.
4. Введены в действие с 5 сентября 2008 г.
5. Введены впервые.
|
|
УТВЕРЖДАЮ Руководитель
Федеральной службы Г.Г. Онищенко 16 июня 2008 г. Дата введения: 5 сентября 2008 г. |
4.1. Методы контроля. Химические факторы
Измерение
концентраций ипконазола в воздухе рабочей зоны
и смывах с кожных покровов операторов методом
капиллярной газожидкостной хроматографии
Методические указания
МУК 4.1.2379-08
Настоящие методические указания устанавливают метод капиллярной газожидкостной хроматографии для измерения концентрации ипконазола в воздухе рабочей зоны и смывах с кожных покровов операторов в диапазонах 0,1 - 1,0 мг/м3; 1 - 10 мкг/смыв, соответственно. (1RS, 2SR, 5RS; 1SR, 2SR, 5SR)-2-(4-хлорбензил)-5-изопропил-1-(1Н-1,2,4-триазол-1-илметил)циклопентанол (ИЮПАК),
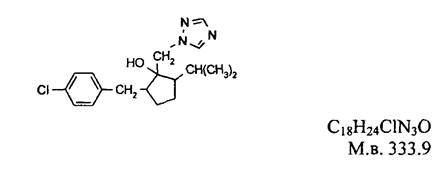
Бесцветное кристаллическое вещество. Существует в виде двух диастереоизомерных пар. Температура плавления 88 - 90 °С. Давление паров 3,58×10-3 мПа (при 25 °С) (диастереомерная пара 1) и 6,99∙10-3 мПа (при 25 °С) (диастереомерная пара 2). Растворимость в воде 6,93 мг/л (20 °С). Хорошо растворим в большинстве органических растворителях. Термически и гидролитически стабилен.
Краткая токсикологическая характеристика:
Острая пероральная токсичность (LD50) для крыс - 1,338 мг/кг; острая дермальная токсичность (LD50) для крыс - > 2000 мг/кг.
Область применения:
Ипконазол - системный фунгицид, являющийся биохимическим ингибитором эргостерольного биосинтеза, широко применяемый на рисе и других зерновых.
ОБУВ в воздухе рабочей зоны - 0,4 мг/м3.
1. Погрешность измерений
Методика обеспечивает выполнение измерений с погрешностью, не превышающей ± 25 %, при доверительной вероятности 0,95.
2. Метод измерений
Измерения концентраций ипконазола выполняют методом капиллярной газожидкостной хроматографии (ГЖХ) с детектором электронного захвата ионов (ЭЗД).
Концентрирование ипконазола из воздушной среды осуществляют на фильтр «синяя лента», экстракцию с фильтров проводят ацетоном, смыв с кожных покровов - этиловым спиртом.
Нижний предел измерения в анализируемом объеме пробы - 1,0 нг. Средняя полнота извлечения с фильтров - 96,95 %, поверхности кожи - 91,32 %.
3. Средства измерений, вспомогательные устройства, реактивы и материалы
3.1. Средства измерений
|
Газовый хроматограф «Кристалл-2000М» снабженный электронозахватным детектором с пределом детектирования по линдану 5×10-14 г/с, предназначенный для работы с капиллярной колонкой |
Номер Госреестра 14516-95 |
|
Весы аналитические ВЛА-200 |
|
|
Меры массы |
|
|
Микрошприц типа МШ-1М, вместимостью 1 мм3 |
ТУ 2.833.105 |
|
Аспиратор ПУ-4Э исп. 1 ЕВКН 4.471.023(-01) РЭ |
Номер Госреестра 14531-03 |
|
Барометр-анероид М-67 |
ТУ 2504-1797-75 |
|
Термометр лабораторный шкальный ТЛ-2, цена деления 1 °С, пределы измерения 0 - 55 °С |
ТУ 215-73Е |
|
Колбы мерные вместимостью 100 см3 |
|
|
Пипетки градуированные 2-го класса точности вместимостью 1,0, 2,0, 5,0, 10 см3 |
Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Ипконазол, аналитический стандарт с содержанием действующего вещества 97,4 %, (фирма «Crompton Evrope Limited») |
|
|
Азот особой чистоты, из баллона |
|
|
Ацетон, осч |
|
|
Вода дистиллированная |
ГОСТ 6790 |
|
Натрий углекислый, хч |
|
|
Спирт этиловый ректификованный |
Допускается использование реактивов иных производителей с аналогичной или более высокой квалификацией.
3.3. Вспомогательные устройства, материалы
|
Аппарат для встряхивания типа АВУ-6с |
ТУ 64-1-2851-78 |
|
Баня водяная |
|
|
Бумажные фильтры «синяя лента», обеззоленные |
ТУ 6-09-2678-77 |
|
Бязь хлопчатобумажная белая |
|
|
Воронка Бюхнера |
|
|
Воронки конусные диаметром 40 - 45 мм |
|
|
Груша резиновая |
|
|
Колба Бунзена |
|
|
Колбы грушевидные на шлифе вместимостью 150 см3 |
|
|
Насос водоструйный |
|
|
Пинцет |
|
|
Стаканы химические с носиком, вместимостью 150 см3 |
|
|
Стекловата |
|
|
Стеклянные емкости вместимостью 100 см3 с герметичной металлической крышкой |
|
|
Стеклянные палочки |
|
|
Ректификационная колонна с числом теоретических тарелок не менее 50 |
|
|
Ротационный вакуумный испаритель В-169 фирмы Buchi, Швейцария |
|
|
Установка для перегонки растворителей |
|
|
Фильтродержатель |
|
|
Хроматографическая колонка капиллярная ZB-5, длиной 15 м, внутренним диаметром 0,5 мм, толщина пленки сорбента 0,53 мкм |
|
Допускается применение другого оборудования с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007, требования по электробезопасности при работе с электроустановками по ГОСТ 12.1.019, а также требования, изложенные в технической документации на газовый хроматограф.
4.2. Помещение должно соответствовать требованиям пожаробезопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009. Содержание вредных веществ в воздухе на должно превышать норм, установленных ГН 2.2.5.1313-03 «Предельно-допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны». Организация обучения работников безопасности труда - по ГОСТ 12.0.004.
5. Требования к квалификации операторов
К выполнению измерений допускают специалистов, имеющих квалификацию не ниже лаборанта-исследователя, с опытом работы на газовом хроматографе.
К проведению пробоподготовки допускают оператора с квалификацией «лаборант», имеющего опыт работы в химической лаборатории.
6. Условия измерений
При выполнении измерений соблюдают следующие условия:
• процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности не более 80 %.
• выполнение измерений на газовом хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к выполнению измерений
Выполнению измерений предшествуют следующие операции: очистка ацетона (при необходимости), приготовление градуировочных растворов, установление градуировочной характеристики, подготовка фильтров и салфеток для отбора проб, отбор проб.
7.1. Очистка ацетона
Ацетон перегоняют над небольшим количеством КМnО4 и прокаленным карбонатом калия или подвергают ректификационной перегонке на колонне с числом теоретических тарелок не менее 50.
7.2. Приготовление градуировочных растворов и растворов внесения
7.2.1. Исходный раствор ипконазола для градуировки (концентрация 100 мкг/см3). В мерную колбу вместимостью 100 см3 помещают 0,01 г ипконазола, растворяют в 50 - 60 см3 ацетона, доводят ацетоном до метки, тщательно перемешивают.
Раствор хранят в холодильнике при температуре 4 - 6 °С в течение месяца.
7.2.2. Рабочие растворы № 1 - 4 ипконазола для градуировки и внесения (концентрация 1,0 - 10,00 мкг/см3). В 4 мерные колбы вместимостью 100 см3 помещают по 1,0; 2,0; 5,0 и 10,0 см исходного раствора с концентрацией 100 мкг/см3 (п. 7.2.1.), доводят до метки ацетоном, тщательно перемешивают, получают рабочие растворы №№ 1 - 4 с концентрацией ипконазола 1,0, 2,0, 5,0 и 10,0 мкг/см3, соответственно.
Растворы хранят в холодильнике при температуре 4 - 6 °С в течение 10-ти дней.
Эти растворы ипконазола используют для приготовления проб с внесением при оценке полноты извлечения действующего вещества методом «внесено-найдено».
7.3. Установление градуировочной характеристики
Градуировочную характеристику, выражающую зависимость площади пика (мВ∙сек) от концентрации ипконазола в растворе (мкг/см3), устанавливают методом абсолютной калибровки по 4-м растворам для градуировки.
В испаритель хроматографа вводят по 1 мм3 каждого градуировочного раствора и анализируют в условиях хроматографирования по п. 7.3.1. Осуществляют не менее 3-х параллельных измерений. Устанавливают площадь пика действующего вещества.
Градуировочный график проверяют перед проведением измерений, анализируя один из градуировочных растворов. Если значения площадей отличаются более, чем на 8 % от данных, заложенных в градуировочную характеристику, ее строят заново, используя свежеприготовленные рабочие растворы для градуировки.
7.3.1. Условия хроматографирования
Измерения выполняют при следующих режимных параметрах:
Газовый хроматограф «Кристалл-2000М», снабженный электронозахватным детектором
Колонка капиллярная ZB-5, длиной 15 м, внутренним диаметром 0,5 мм, толщина пленки сорбента 0,53 мкм.
Температура детектора: 320 °С
испарителя: 220 °С
Температура термостата колонки программированная. Начальная температура - 190 °С, выдержка 2 мин, нагрев колонки со скоростью 20 градусов в минуту до температуры 210 °С, выдержка 3 мин, нагрев колонки со скоростью 25 градусов в минуту до температуры 260 °С, выдержка 3 мин.
Скорость газа 1 (азот): 40,0 см/сек, давление 18,864 кПа, поток 5,5952 см3/мин.
Газ 2: деление потока 1:1,212; сброс 6,786 см3/мин
Хроматографируемый объем: 1 мм3
Ориентировочное время выхода ипконазола: 4,51 мин.
Линейный диапазон детектирования: 1,0 - 10,0 нг
7.4. Подготовка фильтров для отбора проб воздуха
Диаметр бумажного фильтра «синяя лента» должен соответствовать внутреннему диаметру фильтродержателя.
Фильтры последовательно по 3 раза промывают на воронке Бюхнера этанолом, затем ацетоном порциями 25 - 30 см3, сушат с помощью разряжения, создаваемого водоструйным насосом, затем на воздухе при комнатной температуре. До использования фильтры хранят в герметично закрытой стеклянной таре.
7.5. Подготовка салфеток для проведения смыва
Вырезают салфетки (лоскуты) из белой бязи размером 10×10 см, затем их последовательно обрабатывают 5 %-ным раствором углекислого натрия (при кипячении), водой до нейтральной реакции промывных вод, 2-х кратно промывают этиловым спиртом, сушат на воздухе при комнатной температуре. До использования салфетки хранят в герметично закрытой стеклянной таре.
Для оценки квалификации растворителей применительно к задачам подготовки фильтров и салфеток проводят контроль чистоты по процедуре пробоподготовки и измерения, изложенных в п.п. 10.1, 10.2 и 7.3.1.
8. Отбор и хранение проб воздуха
Отбор проб осуществляют в соответствии с требованиями ГОСТ 12.1.005-88 «ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны». Воздух с объемным расходом 2 - 4 дм3/мин аспирируют через бумажный фильтр «синяя лента», помещенный в фильтродержатель.
Для измерения концентрации ипконазола на уровне 0,25 ОБУВ (предел обнаружения) для воздуха рабочей зоны необходимо отобрать 20 дм3 воздуха. Срок хранения отобранных проб, помещенных в полиэтиленовые пакеты, в холодильнике при температуре 4 - 6 °С - 14 дней.
9. Условия проведения смыва
Смывы проводят в конце работы или после выполнения отдельных операций с открытых и закрытых спецодеждой или другими СИЗ участков тела (лоб, лицо, шея, спина, грудь, предплечье, голень, кисти рук, включая межпапьцевые промежутки).
До работы выбирают участок кожи, обрабатывают его для удаления загрязнений, фиксируют площадь (не менее 200 см2). При необходимости отбирают фоновые смывы.
Смыв выполняют способом обмыва фиксированного участка кожи этиловым спиртом, помещая 20 см3 в стеклянную емкостью с металлической крышкой. Тканевой салфеткой, смоченной растворителем, с помощью пинцета (индивидуально) обмывают этот участок сверху вниз. Операцию повторяют дважды.
Срок хранения отобранных проб смывов, помещенных в герметично закрытые емкости, в морозильной камере при температуре -15 °С - 14 дней.
10. Выполнение измерений
10.1. Воздух рабочей зоны
Экспонированный фильтр переносят в химический стакан вместимостью 150 см3, заливают 10 см3 ацетона, помещают на встряхиватель на 15 минут. Растворитель сливают, фильтр еще дважды обрабатывают новыми порциями ацетона объемом 10 см3, выдерживая на встряхивателе по 10 минут.
Объединенный экстракт переносят (через воронку) в круглодонную колбу, упаривают на ротационном вакуумном испарителе при температуре бани не выше 35 °С почти досуха, оставшийся растворитель отдувают потоком теплого воздуха. Остаток растворяют в 2 см3 ацетона и анализируют при условиях хроматографирования, указанных в п. 7.3.1.
10.2. Смывы с кожных покровов
Пробу смыва сливают (через воронку) в колбу для упаривания, с помощью пинцета извлекают салфетку, помещают в конусную химическую воронку, установленную в муфту колбы для упаривания, тщательно отжимают и промывают этиловым спиртом дважды порциями по 10 см3, предварительно ополаскивая растворителем емкость, в которой находилась проба.
Объединенный раствор упаривают в грушевидной колбе на ротационном вакуумном испарителе при температуре бани не выше 40 °С почти досуха, оставшийся растворитель отдувают потоком теплого воздуха. Остаток растворяют в 1 см3 ацетона и анализируют при условиях хроматографирования, указанных в п. 7.3.1.
Пробу вводят в испаритель хроматографа не менее двух раз. Устанавливают площадь пика действующего вещества, с помощью градуировочного графика определяют концентрацию ипконазола в хроматографируемом растворе.
Образцы, дающие пики, большие, чем градуировочный раствор с концентрацией 10,0 мкг/см3, разбавляют ацетоном (не более чем в 50 раз).
11. Обработка результатов анализа
11.1. Воздух рабочей зоны
Массовую концентрацию ипконазола в пробе воздуха (X), мг/м3, рассчитывают по формуле:
X = С∙W/Vt, где
С - концентрация ипконазола в хроматографируемом растворе, найденная по градуировочному графику в соответствии с величиной площади хроматографического пика, мкг/см3;
W - объем экстракта, подготовленного для хроматографирования, см3;
Vt - объем пробы воздуха, отобранный для анализа, приведенный к стандартным условиям (давление 760 мм рт. ст., температура 20° С), дм3.
Vt = R∙P∙ut/(273 + T),
где Т - температура воздуха при отборе проб (на входе в аспиратор), град. С,
Р - атмосферное давление при отборе пробы, мм рт. ст.
u - расход воздуха при отборе пробы, дм3/мин,
t - длительность отбора пробы, мин.
R - коэффициент, равный 0,386 для воздуха рабочей зоны.
За результат анализа (![]() )
принимается среднее арифметическое результатов двух параллельных определений X1
и Х2 (
)
принимается среднее арифметическое результатов двух параллельных определений X1
и Х2 (![]() = (X1
+ Х2)/2), расхождение между которыми не превышает значений
норматива оперативного контроля сходимости (d):
= (X1
+ Х2)/2), расхождение между которыми не превышает значений
норматива оперативного контроля сходимости (d):
|X1 - Х2| ≤ d.
d
= dотн∙![]() /100,
мг/м3
/100,
мг/м3
где d - норматив оперативного контроля сходимости, мг/м3;
dотн. - норматив оперативного контроля сходимости, % (равен 14 %).
11.2. Смывы с кожных покровов
Массовую концентрацию ипконазола в пробе смыва X, мкг/смыв, рассчитывают по формуле:
X = С∙W, где
С - концентрация ипконазола в хроматографируемом растворе, найденная по градуировочному графику в соответствии с величиной площади хроматографического пика, мкг/см3;
W - объем экстракта, подготовленного для хроматографирования, см3;
Примечание: Идентификация и расчет концентрации вещества в пробах могут быть проведены с помощью компьютерной программы обработки хромагографических данных, включенной в аналитическую систему.
12. Оформление результатов измерений
Результат количественного анализа представляют в виде:
• результат анализа ![]() в
мг/м3 или мкг/смыв (с указанием площади смыва в см2),
характеристика погрешности δ, % (±25 %), Р = 0,95 или
в
мг/м3 или мкг/смыв (с указанием площади смыва в см2),
характеристика погрешности δ, % (±25 %), Р = 0,95 или
![]() ± Δ
мг/м3 (мкг/смыв, площадь смыва, см2), Р = 0,95,
± Δ
мг/м3 (мкг/смыв, площадь смыва, см2), Р = 0,95,
где Δ - абсолютная погрешность.
![]()
Результат измерений должен иметь тот же десятичный разряд, что и погрешность.
Если содержание вещества менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание ипконазола в пробе воздуха рабочей зоны - менее 0,1 мг/м3; смыва - менее 1,0 мкг/смыв»*
* - 0,1 мг/м3; 1,0 мкг/смыв - пределы обнаружения при отборе 20 дм3 воздуха рабочей зоны; в пробе смыва (фиксированная площадь смыва, 200 см2), соответственно.
13. Контроль погрешности измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ ИСО 5725-1-6.2002 «Точность (правильность и прецизионность) методов и результатов измерений».
14. Разработчики
Юдина Т.В., Ларькина М.В., Рогачева С.К. (ФГУН «Федеральный научный центр гигиены им. Ф.Ф. Эрисмана Роспотребнадзора»)
СОДЕРЖАНИЕ