Федеральная служба по надзору в сфере защиты прав
потребителей
и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных
количеств химических веществ
в объектах окружающей среды, атмосферном
воздухе, воздухе рабочей зоны
и сельскохозяйственной продукции
Сборник
методических указаний
МУК
4.1.1960, 4.1.1961, 4.1.1963
- 4.1.1980-05
1. Разработаны Московской сельскохозяйственной академией им. К.А. Тимирязева, Учебно-научным консультационным центром «Токсикология пестицидов и агрохимикатов» (Калинин В.А., Калинина Т.С., Рыбакова О.И., Калинин А.В.).
2. Рекомендованы к утверждению Комиссией по санитарно-гигиеническому нормированию Минздрава России (протокол № 1 от 31 марта 2005 г.).
3. Утверждены Главным государственным санитарным врачом Российской Федерации, руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека Главным государственным санитарным врачом Российской Федерации Г.Г. Онищенко 21 апреля 2005 г.
4. Введены в действие с 1 июля 2005 г.
5. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Руководитель
Федеральной службы ______________________ Г.Г. Онищенко 21 апреля 2005 г. Дата введения: 1 июля 2005 г. |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных
количеств протиоконазола
и его основного метаболита протиоконазола-дестио
в воде, протиоконазола и протиоконазола-дестио
по метаболиту протиоконазолу-дестио в почве методом
высокоэффективной жидкостной хроматографии
Методические указания
МУК 4.1.1980-05
Настоящие методические указания устанавливают метод высокоэффективной жидкостной хроматографии для определения массовой концентрации протиоконазола и его основного метаболита протиоконазола-дестио в воде в диапазоне 0,0005 - 0,01 мг/дм3, протиоконазола и протиоконазола-дестио по метаболиту протиоконазолу-дестио в почве в диапазоне 0,01 - 0,2 мг/кг.
2-[(RS)-2-гидрокси-2-(1-хлорциклопропил)-3-(2-хлорфенил)пропил]-2Н-1,2,4-триазол-3(4Н)-тион(IUPAC)
Структурная формула:
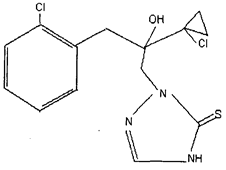
Эмпирическая формула: C14H15Cl2N3OS.
Молекулярная масса: 344,3.
Белое или светло-бежевое твердое вещество без запаха. Температура плавления: 139,1 - 144,5 °С. Давление паров при 20 °С: << 4×10-7 Па. Коэффициент распределения н-октанол/вода: Kow logP = 4,16 (рН 4), 3,82 (рН 7) и 2,0 (рН 9). Растворимость (г/дм3) при 20 °С: ацетон - более 250, этилацетат - более 250, дихлорметан - 88, ацетонитрил - 69; растворимость в воде - 0,005 (рН 4), 0,3 (рН 8) и 2,0 (рН 9).
Вещество стабильно при хранении на воздухе, а также в кислой (DT50 = 120 дней) и щелочной (DT50 > 1 года) средах. В присутствии света в водных фотолитических условиях протиоконазол достаточно быстро деградирует с периодом полураспада 47,7 часа. Основным продуктом фотодеградации является протиоконазол-дестио, его содержание составляет до 56 %.
В почве в полевых условиях протиоконазол подвергается быстрой деградации, ДT50 составляет 1,3 - 2,8 дней (в среднем 1,7 дней), ДT90 - 4,4 - 9,3 дня (в среднем 5,8 дней). Отмечена заметная сорбция протиоконазола почвой. Основным почвенным метаболитом является протиоконазол-дестио. ДT50 протиоконазола-дестио в почве в полевых условиях составляет 16,3 - 72,3 дня (в среднем 42 дня), ДT90 - 54,1 - 240 дней (в среднем 140 дней). Протиоконазол-дестио детектирован на пределе обнаружения (6 мкг/кг) в 10 - 20 см слое. Максимальные его уровни наблюдались в период от 1 до 28 дней после применения, полное исчезновение (менее 6 мкг/кг) после 55 - 240 дней.
Краткая токсикологическая характеристика
Острая пероральная токсичность (LD50) для крыс - более 6200 мг/кг; острая дермальная токсичность (LD50) для крыс - более 2000 мг/кг; острая ингаляционная токсичность (LC50) для крыс - более 4990 мг/м3 воздуха.
Протиоконазол не оказывает раздражающего действия на кожу и слизистую оболочку глаз.
Основной метаболит протиоконазола: протиоконазол-дестио (SXX 0665)
α-(1-хлорциклопропил)-α-(2-хлорфенил)метил-1Н-1,2,4-триазол-1 этанол (С.А.)
Структурная формула:
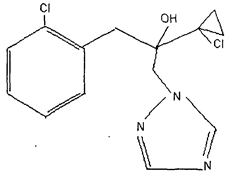
Эмпирическая формула: C14H15Cl2N3O.
Молекулярная масса: 312,2.
Бесцветный порошок без запаха. Температура плавления: 108,5 °С. Давление паров при 20 °С: 2,7×10-7 Па. Коэффициент распределения н-октанол/вода: Kow logP = 3,04.
Растворимость (г/дм3) при 20 °С: гексан - 3, толуол - 84, ацетон - 100, ацетонитрил - 43, дихлорметан - более 200, вода - 0,051. Стабилен в кислой и щелочной средах (DT50 > 5000 ч).
Область применения препарата
Протиоконазол - фунгицид системного действия из группы ингибиторов синтеза эргостерина. Вещество обладает защитным, искореняющим и лечебным действием.
1. Метрологические характеристики метода
Метрологические характеристики метода представлены в таблице.
Таблица
Метрологические параметры
|
Определяемое вещество |
Метрологические параметры, Р = 0,95, n = 20 |
||||
|
предел обнаружения, мг/кг |
диапазон определяемых концентраций, мг/кг |
среднее значение определения, % |
стандартное отклонение S, % |
доверительный интервал среднего результата, % |
|
|
Вода |
|||||
|
Протиоконазол |
0,0005 |
0,0005 - 0,01 |
94,63 |
6,77 |
±3,5 |
|
Протиоконазол-дестио |
0,0005 |
0,0005 - 0,01 |
93,61 |
5,50 |
±2,9 |
|
Почва |
|||||
|
Протиоконазол-дестио |
0,01 |
0,01 - 0,2 |
85,89 |
4,20 |
±2,9 |
2. Метод измерений
Методика основана на определении веществ с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) с ультрафиолетовым детектором. Для концентрирования и очистки пробы воды использованы патроны для твердофазной экстракции С18 Sep Pak. Контроль протиоконазола и его основного метаболита протиоконазола-дестио в образцах почвы осуществляется по содержанию протиоконазола-дестио после экстракции из анализируемого образца смесью ацетонитрил-вода, очистка экстракта перераспределением в системе несмешивающихся растворителей, а также на колонке с оксидом алюминия.
Количественное определение проводится методом абсолютной калибровки.
3. Средства измерений, вспомогательные устройства, реактивы и материалы
3.1. Средства измерений
|
Жидкостный хроматограф с ультрафиолетовым детектором с переменной длиной волны (фирмы Perkin-Elmer, США) |
Номер Госреестра 15945-97 |
|
Весы аналитические ВЛА-200 |
|
|
Весы лабораторные общего назначения, с наибольшим пределом взвешивания до 500 г и пределом допустимой погрешности ±0,038 г |
ГОСТ 7328 |
|
Колбы мерные 2-100-2, 2-1000-2 |
|
|
Меры массы |
ГОСТ 7328 |
|
Пипетки градуированные 2 класса точности вместимостью 1,0; 2,0; 5,0; 10 см3 |
|
|
Пробирки градуированные с пришлифованной пробкой вместимостью 5 см3 |
|
|
Цилиндры мерные 2 класса точности вместимостью 25, 50, 100, 500 и 1 000 см3 |
|
|
Допускается использование средств измерения с аналогичными или лучшими характеристиками. |
|
3.2. Реактивы
|
Протиоконазол, аналитический стандарт с содержанием д.в. 99,8 % (Байер, Германия) |
|
|
Протиоконазол-дестио, аналитический стандарт с содержанием д.в. 98,5 % (Байер, Германия) |
|
|
Ацетонитрил для хроматографии, хч |
ТУ 6-09-4326-76 |
|
Вода деионизованная |
ГОСТ 6702 |
|
н-Гексан, хч |
ТУ 6-09-3375 |
|
Кислота ортофосфорная, хч, 85 % |
|
|
Кислота уксусная, лед |
|
|
Метилен хлористый (дихлорметан), хч |
|
|
Метиловый спирт (метанол), хч |
|
|
Натрий серно-кислый, безводный, хч |
|
|
Натрий хлористый, хч |
|
|
L-Цистеин гидрохлорид, для синтеза (Мерк, ФРГ) |
|
|
Этиловый эфир уксусной кислоты, ч |
|
|
Допускается использование реактивов иных производителей с аналогичной или более высокой квалификацией. |
|
3.3. Вспомогательные устройства, материалы
|
Аппарат для встряхивания типа АВУ-6с |
ТУ 64-1-2851-78 |
|
Баня ультразвуковая фирмы Донау (Швейцария) |
|
|
Бумажные фильтры «красная лента», обеззоленные или фильтры из хроматографической бумаги |
|
|
Ватман 3 мм |
ТУ 6-09-2678-77 |
|
Воронки делительные, вместимостью 250 см3 |
|
|
Воронки конусные диаметром 30 - 37 и 60 мм |
|
|
Груша резиновая |
|
|
Дефлегматор елочный |
ГОСТ 9773 |
|
Колбы плоскодонные, вместимостью 100, 250, 400 - 500 см3 |
|
|
Колбы грушевидные на шлифе, вместимостью 100 - 150 см3 |
|
|
Колонка хроматографическая стеклянная, длиной 25 см, внутренним диаметром 8 - 10 мм |
|
|
Мембранные фильтры капроновые, диаметром 47 мм |
|
|
Набор для фильтрации растворителей через мембрану |
|
|
Насос водоструйный вакуумный |
ГОСТ 10696 |
|
Стаканы химические, вместимостью 100, 500 см3 |
|
|
Стекловата |
|
|
Стеклянные палочки |
|
|
Патроны для твердофазной экстракции С18 Sep Pak (Waters, США) |
|
|
Ректификационная колонна с числом теоретических тарелок не менее 50 |
|
|
Ротационный вакуумный испаритель ИР-1М или ротационный вакуумный испаритель В-169 фирмы Buchi, Швейцария |
ТУ 25-11-917-74 |
|
Установка для перегонки растворителей |
|
|
Холодильник водяной обратный |
|
|
Хроматографическая колонка стальная, длиной 25 см, внутренним диаметром 4,0 мм, содержащая кромасил 100 С18, зернением 8 мкм |
|
|
Шприц для ввода образцов для жидкостного хроматографа, вместимостью 50 - 100 мм3 |
|
|
Шприц медицинский с разъемом Льюера вместимостью 20 см3 |
ГОСТ 22090 |
|
Допускается применение другого оборудования с аналогичными или лучшими техническими характеристиками. |
|
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007, требования электробезопасности при работе с электроустановками по ГОСТ 12.1.019, а также требования, изложенные в технической документации на жидкостный хроматограф.
4.2. Помещение должно соответствовать требованиям пожаробезопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009. Содержание вредных веществ в воздухе не должно превышать норм, установленных ГН 2.2.5.1313-03 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны». Организация обучения работников безопасности труда по ГОСТ 12.0.004.
5. Требования к квалификации операторов
К выполнению измерений допускают специалистов, имеющих квалификацию не ниже лаборанта-исследователя, с опытом работы на жидкостном хроматографе.
К проведению пробоподготовки допускают оператора с квалификацией «лаборант», имеющего опыт работы в химической лаборатории.
6. Условия измерений
При выполнении измерений соблюдают следующие условия:
- процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности не более 80 %.
- выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к выполнению измерений
Измерениям предшествуют следующие операции: очистка органических растворителей (при необходимости), приготовление растворов, подвижной фазы для ВЭЖХ, кондиционирование хроматографической колонки, установление градуировочной характеристики, подготовка колонки с оксидом алюминия и концентрирующих патронов С18 Sep Раk.
7.1. Очистка органических растворителей
7.1.1. Очистка ацетонитрила
Ацетонитрил кипятят с обратным холодильником над пентоксидом фосфора не менее 1 часа, после чего перегоняют, непосредственно перед употреблением ацетонитрил повторно перегоняют над прокаленным карбонатом калия.
7.1.2. Очистка н-гексана
Растворитель последовательно промывают порциями концентрированной серной кислоты до прекращения ее окрашивания в желтый цвет, затем водой до нейтральной реакции промывных вод, перегоняют над поташом.
7.1.3. Очистка этилацетата
Этилацетат промывают последовательно 5 %-м водным раствором карбоната натрия, насыщенным раствором хлористого кальция, сушат над безводным карбонатом калия, перегоняют или подвергают ректификационной перегонке на колонне с числом теоретических тарелок не менее 50.
7.2. Приготовление 0,02 М раствора ортофосфорной кислоты
В мерную колбу вместимостью 1 000 см3 помещают 1,36 см3 85 %-й ортофосфорной кислоты, доводят водой до метки, тщательно перемешивают.
7.3. Приготовление 0,05 %-го раствора уксусной кислоты
В мерную колбу вместимостью 1 000 см3 помещают 300 - 400 см3 дистиллированной воды, вносят 0,5 см3 ледяной уксусной кислоты, перемешивают, доводят водой до метки, вновь перемешивают.
7.4. Подготовка колонки с
оксидом алюминия
для очистки экстракта
Нижнюю часть стеклянной колонки длиной 25 см, внутренним диаметром 8 - 10 мм уплотняют тампоном из стекловаты, медленно выливают в колонку (при открытом кране) суспензию 5 г оксида алюминия в 15 - 20 см3 смеси гексан-этилацетат (85:15, по объему). Дают растворителю стечь до верхнего края сорбента и помещают на него слой безводного сульфата натрия высотой 1 см. Колонку промывают 20 см3 этилацетата со скоростью 1 - 2 капли в с, затем 20 см3 смеси гексан-этилацетат (85:15, по объему). После этого колонка готова к работе.
7.5. Проверка хроматографического поведения
протиоконазола-дестио на колонке с оксидом алюминия
В круглодонную колбу вместимостью 10 см3 помещают 0,5 см3 градуировочного раствора № 1 протиоконазола-дестио с концентрацией 10 мкг/см3 в ацетонитриле (п. 7.9.2), раствор упаривают досуха, остаток растворяют в 0,5 см3 этилацетата, помещая на ультразвуковую баню на 1 мин., добавляют 2,5 см3 гексана, перемешивают, вновь помещают на ультразвуковую баню на 1 мин. Раствор наносят на колонку, подготовленную по п. 7.4. Промывают колонку 25 см3 смеси гексан-этилацетат (85:15, по объему) со скоростью 1 - 2 капли в сек, элюат отбрасывают. Затем колонку промывают 50 см3 смеси гексан-этилацетет (60:40, по объему). Фракционно (по 10 см3) отбирают элюат, упаривают, остатки растворяют в 1 см3 ацетонитрила, помещая на ультразвуковую баню на 1 мин., вносят 1 см3 подвижной фазы, подготовленной по п. 7.3, перемешивают и анализируют на содержание протиоконазола-дестио по п. 9.3.
7.6. Подготовка концентрирующего патрона С18 Sep Pak
Концентрирующий патрон промывают с помощью медицинского шприца 2 см3 метанола со скоростью прохождения растворителя через патрон 1 - 2 капли в с, затем 5 см3 0,05 %-ного раствора уксусной кислоты. Патрон готовят непосредственно перед использованием для концентрирования образца.
7.7. Подготовка подвижной фазы для ВЭЖХ
В мерную колбу вместимостью 1000 см3 помещают 600 см3 ацетонитрила, 400 см3 0,02 М раствора ортофосфорной кислоты, перемешивают, фильтруют через мембранный фильтр.
7.8. Кондиционирование хроматографической колонки
Промывают колонку подвижной фазой (приготовленной по п. 7.7) при скорости подачи растворителя 1 см3/мин. не менее 2-х часов до установления стабильной базовой линии.
7.9. Приготовление градуировочных растворов
7.9.1. Исходные растворы протиоконазола и протиоконазола-дестио для градуировки (концентрация 500 мкг/см3). В мерную колбу вместимостью 100 см3 помещают 0,05 г протиоконазола (или протиоконазола-дестио), растворяют в 40 - 50 см3 ацетонитрила, доводят ацетонитрилом до метки, тщательно перемешивают.
Растворы хранят в морозильной камере при температуре не выше -18 °С в течение 3-х месяцев.
7.9.2. Растворы протиоконазола и протиоконазола-дестио № 1 для градуировки (концентрация 10 мкг/см3). В мерную колбу вместимостью 100 см3 помещают 2 см3 исходного раствора протиоконазола (или протиоконазола-дестио) с концентрацией 500 мкг/см3 (п. 7.9.1), разбавляют ацетонитрилом до метки.
Этот раствор используют для приготовления проб воды с внесением при оценке полноты извлечения протиоконазола и протиоконазола-дестио из исследуемых образцов. Для внесения в образцы почвы используют растворы с концентрацией 10 мкг/см3, приготовленные в смеси метанол-вода-цистеин гидрохлорид (100:900:0,01; объем/объем/вес).
Градуировочные растворы № 1 хранят в морозильной камере при температуре не выше -18 °С в течение месяца.
7.9.3. Рабочие растворы № 2 - 5 протиоконазола и протиоконазола-дестио для градуировки (концентрация 0,05 - 1,0 мкг/см3).
В 4 мерные колбы вместимостью 100 см3 помещают по 0,5; 1,0; 5,0 и 10,0 см3 градуировочного раствора № 1 протиоконазола (или протиоконазола-дестио) с концентрацией 10 мкг/см3 (п. 7.9.2), доводят до метки подвижной фазой, приготовленной по п. 7.7, тщательно перемешивают, получают рабочие растворы №№ 2 - 5 с концентрацией протиоконазола (или протиоконазола-дестио) 0,05; 0,1; 0,5 и 1,0 мкг/см3, соответственно.
Растворы готовят непосредственно перед употреблением.
7.10. Установление градуировочной характеристики
Градуировочную характеристику, выражающую зависимость площади пика (отн. единицы) от концентрации протиоконазола (или протиоконазола-дестио) в растворе (мкг/см3), устанавливают методом абсолютной калибровки по 4 растворам для градуировки.
В инжектор хроматографа вводят по 20 мм3 каждого градуировочного раствора и анализируют в условиях хроматографирования по п. 9.3. Осуществляют не менее 3 параллельных измерений.
8. Отбор и хранение проб
Отбор проб производится в соответствии с правилами, определенными ГОСТами Р 51592-2000 «Вода. Общие требования к отбору проб», 17.4.3.01-83 «Почвы. Общие требования к отбору проб», 26950-89 «Почвы. Отбор проб».
Пробы воды анализируют в день отбора или замораживают и хранят в полиэтиленовой таре в морозильной камере при температуре -18 °С не более 2 недель.
Образцы почвы подсушивают на воздухе в темноте, помещают в герметичную полиэтиленовую тару и хранят в холодильнике при температуре 4 - 6 °С не более 4 недель.
Для длительного хранения образцы почвы замораживают и хранят при температуре -18 °С.
Перед анализом образцы воды фильтруют через неплотный бумажный фильтр, почвы - просеивают через сито с диаметром отверстий 1 мм.
9. Выполнение определения
9.1. Вода
Образец отфильтрованной воды объемом 200 см3 помещают в плоскодонную колбу вместимостью 250 - 300 см3 с пришлифованной пробкой, вносят 0,01 г цистеина гидрохлорида и 0,1 см3 ледяной уксусной кислоты, тщательно перемешивают.
Подготовленную пробу вносят с помощью медицинского шприца на концентрирующий патрон С18 Sep Pak, подготовленный по п. 7.6 со скоростью пропускания раствора 1 - 2 капли в с. Операцию осуществляют в затемненном помещении. После нанесения пробы патрон промывают 5 см3 смеси ацетонитрил - 0,05 %-ая уксусная кислота (2:8, по объему), элюат отбрасывают. Вещества элюируют с патрона 2 см3 смеси ацетонитрил - 0,05 %-ая уксусная кислота (9:1, по объему), собирая элюат в градуированную пробирку с пришлифованной пробкой, перемешивают и анализируют на содержание протиоконазола и протиоконазола-дестио по п. 9.3.
9.2. Почва
9.2.1. Экстракция
Образец сухо-воздушной почвы массой 20 г помещают в плоскодонную колбу вместимостью 250 см3, добавляют 100 см3 смеси ацетонитрил-вода (80:20, по объему) и помещают на встряхиватель на 1 ч.
Раствор (с осадком почвы) фильтруют в мерный цилиндр вместимостью 100 см3 с пришлифованной пробкой через складчатый бумажный фильтр, помещенный на конусную воронку. Осадок на фильтре промывают 25 см3 смеси ацетонитрил-вода (80:20, по объему). Экстракт и промывную жидкость, объединенные в мерном цилиндре, перемешивают, измеряют объем раствора, 1/2 его часть (эквивалентную 10 г образца) переносят в круглодонную колбу. Далее проводят очистку экстракта по п. 9.2.2.
9.2.2. Очистка
экстракта перераспределением в системе
несмешивающихся растворителей
Экстракт, полученный по п. 9.2.1 и помещенный в круглодонную колбу, упаривают на ротационном вакуумном испарителе до водного остатка (~10 см3) при температуре не выше 35 °С, внимательно следя за процессом и не допуская переброса жидкости при вспенивании. К водному остатку прибавляют 40 см3 деионизованной воды и 5 г хлорида натрия, перемешивают до полного растворения соли и переносят в делительную воронку вместимостью 250 см3. В воронку вносят 30 см3 хлористого метилена, интенсивно встряхивают воронку в течение 2 мин. После полного разделения фаз нижний органический слой отделяют, фильтруют через слой безводного сульфата натрия, помещенный на бумажном фильтре в конусной воронке, в круглодонную колбу вместимостью 150 см3. Операцию экстракции водной фазы повторяют еще дважды, используя по 25 см3 хлористого метилена. Объединенную органическую фазу, пропущенную через слой сульфата натрия, упаривают досуха и подвергают дополнительной очистке на колонке по п. 9.2.3.
9.2.3. Очистка экстракта на колонке с оксидом алюминия
Остаток в круглодонной колбе, полученный по п. 9.2.2, растворяют в 0,5 см3 этилацетата, помещая на ультразвуковую баню на 1 мин., добавляют 2,5 см3 гексана, перемешивают, вновь помещают на ультразвуковую баню на 1 мин. Раствор наносят на колонку, подготовленную по п. 7.4. Колбу обмывают трижды порциями по 3 см3 смеси гексан-этилацетат (85:15, по объему), которые также наносят на колонку. Промывают колонку 25 см3 смеси гексан-этилацетат (85:15, по объему) со скоростью 1 - 2 капли в с, элюат отбрасывают. Протиоконазол-дестио элюируют с колонки 40 см3 смеси гексан-этилацетат (60:40, по объему), собирая элюат непосредственно в круглодонную колбу. Раствор упаривают досуха при температуре не выше 35 °С. Остаток в колбе растворяют в 1 см3 ацетонитрила, помещая на ультразвуковую баню на 1 мин., вносят 1 см3 подвижной фазы, подготовленной по п. 7.3, перемешивают и анализируют на содержание протиоконазола-дестио по п. 9.3.
9.3. Условия хроматографирования
Жидкостный хроматограф с ультрафиолетовым детектором (фирмы Perkin-Elmer, США).
Колонка стальная длиной 25 см, внутренним диаметром 4 мм, содержащая кромасил 100 С18, зернением 8 мкм.
Температура колонки: комнатная.
Подвижная фаза: ацетонитрил - 0,02 М ортофосфорная кислота (60:40, по объему).
Скорость потока элюента: 1 см3/мин.
Рабочая длина волны: 213 нм.
Чувствительность: 0,01 ед. абсорбции на шкалу.
Объем вводимой пробы: 20 мм3.
Ориентировочное время выхода протиоконазола-дестио: 6,4 - 6,6 мин.; протиоконазола: 9,4 - 9,7 мин.
Линейный диапазон детектирования 1 - 20 нг.
Образцы, дающие пики, большие, чем градуировочные растворы с концентрацией 1,0 мкг/см3, разбавляют подвижной фазой, приготовленной по п. 7.3.
10. Обработка результатов анализа
10.1. Вода
Содержание протиоконазола в пробе с учетом его основного метаболита протиоконазола-дестио в эквиваленте действующего вещества (X, мг/дм3) рассчитывают по формуле:
|
|
А, Б - концентрации протиоконазола и протиоконазола-дестио, соответственно, найденные по градуировочным графикам, мкг/см3;
V - объем экстракта, подготовленного для хроматографирования, см3;
W - объем анализируемого образца, см3.
К - коэффициент пересчета содержания протиоконазола-дестио на эквивалент протиоконазола, по соотношению молекулярных масс (равен 1,103).
10.2. Почва
Содержание протиоконазола в пробе с учетом его основного метаболита протиоконазола-дестио в эквиваленте действующего вещества (X, мг/кг) рассчитывают по формуле:
|
|
Б - концентрация протиоконазола-дестио, найденная по градуировочному графику, мкг/см3;
V - объем экстракта, подготовленного для хроматографирования, см3;
m - масса анализируемого образца, г.
K - то же, что и в п. 10.1.
С - коэффициент пересчета на полный объем экстракта (равен 2).
11. Контроль погрешности измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ ИСО 5725-1 - 6.2002 «Точность (правильность и прецизионность) методов и результатов измерений».
12. Разработчики
Юдина Т.В., Федорова Н.Е., Волкова В.Н. (Федеральный научный центр гигиены им. Ф.Ф. Эрисмана); Брагина И.В. (Федеральный центр гигиены и эпидемиологии Роспотребнадзора).