РД 52.24.383-2005
Федеральная
служба по гидрометеорологии и мониторингу
окружающей среды
РУКОВОДЯЩИЙ ДОКУМЕНТ
МАССОВАЯ КОНЦЕНТРАЦИЯ
АММИАКА И ИОНОВ
АММОНИЯ В ВОДАХ. МЕТОДИКА ВЫПОЛНЕНИЯ
ИЗМЕРЕНИЙ ФОТОМЕТРИЧЕСКИМ МЕТОДОМ В ВИДЕ
ИНДОФЕНОЛОВОГО СИНЕГО
Предисловие
1. РАЗРАБОТАН ГУ «Гидрохимический институт»
2. РАЗРАБОТЧИКИ Л.В. Боева, канд. хим. наук (руководитель разработки), А.А. Назарова, канд. хим. наук, Ю.А. Андреев
3. УТВЕРЖДЕН Заместителем руководителя Росгидромета 15.06.2005 г.
4. СВИДЕТЕЛЬСТВО ОБ АТТЕСТАЦИИ МВИ Выдано ГУ «Гидрохимический институт» 30.12.2004 г. № 35.24-2004.
5. ЗАРЕГИСТРИРОВАН ГУ ЦКБ ГМП за номером РД 52.24.383-2005 от 30.06.2005 г.
6. ВЗАМЕН РД 52.24.383-95 «Методические указания. Методика выполнения измерений массовой концентрации аммиака и ионов аммония в поверхностных водах суши фотометрическим методом в виде индофенолового синего»
Введение
Аммонийный азот в водах находится, главным образом, в растворенном состоянии в виде ионов аммония и недиссоциированных молекул NH4OH, количественное соотношение которых имеет важное экологическое значение и определяется величиной pH и температурой воды. В то же время некоторая часть аммонийного азота может мигрировать в сорбированном состоянии на минеральных и органических взвесях, а также в виде различных комплексных соединений.
Присутствие в незагрязненных поверхностных водах ионов аммония связано, главным образом, с процессами биохимического разложения белковых веществ, мочевины, дезаминирования аминокислот. Естественными источниками аммиака служат прижизненные выделения гидробионтов. Кроме того, ионы аммония могут образовываться в результате анаэробных процессов восстановления нитратов и нитритов.
Источником антропогенного загрязнения водных объектов ионами аммония являются сточные воды многих отраслей промышленности, бытовые сточные воды, стоки с сельскохозяйственных угодий.
Сезонные колебания концентрации ионов аммония характеризуются обычно понижением весной и в начале лета, в период интенсивной фотосинтетической деятельности фитопланктона, и повышением в конце лета - начале осени при усилении процессов бактериального разложения органического вещества в периоды отмирания водных организмов, особенно в зонах их скопления: в придонном слое водоема, в слоях повышенной плотности фито- и бактериопланктона. В осенне-зимний период повышенное содержание ионов аммония связано с продолжающейся минерализацией органических веществ в условиях слабого потребления фитопланктоном и уменьшения скорости биохимического окисления из-за низких температур.
Аммонийные ионы в водной среде неустойчивы. В присутствии кислорода они легко подвергаются биохимическому и фотохимическому окислению до нитритов, затем до нитратов. По этой причине в малозагрязненных водных объектах обычно содержание аммонийного азота не превышает тысячных долей мг/дм3, иногда повышаясь до сотых долей в осенне-зимний период. В некоторых водных объектах, содержащих значительное количество органического вещества, в конце длительного подледного периода при дефиците кислорода содержание аммонийного азота может возрастать до десятых долей мг/дм3. Повышенное содержание ионов аммония указывает на ухудшение санитарного состояния водного объекта, причем, поскольку аммиак более токсичен, чем ионы аммония, опасность аммонийного азота для гидробионтов возрастает с повышением pH воды.
Увеличение концентрации аммонийного азота в весенне-летний период, как правило, является показателем свежего загрязнения.
Для водных объектов рыбохозяйственного назначения предельно допустимая концентрация (ПДК) ионов аммония 0,4 мг/дм3, аммиака - 0,04 мг/дм3 по азоту; для объектов хозяйственно-питьевого и культурно-бытового назначения ПДК в пересчете на азот равна 1,5 мг/дм3.
РД 52.24.383-2005
РУКОВОДЯЩИЙ ДОКУМЕНТ
МАССОВАЯ КОНЦЕНТРАЦИЯ АММИАКА И ИОНОВ АММОНИЯ В ВОДАХ. МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ ФОТОМЕТРИЧЕСКИМ МЕТОДОМ В ВИДЕ ИНДОФЕНОЛОВОГО СИНЕГО
Дата введения 2005-07-01
1. Область применения
Настоящий руководящий документ устанавливает методику выполнения измерений (далее - методика) массовой концентрации аммиака и ионов аммония в пробах поверхностных вод суши и очищенных сточных вод любой минерализации в диапазоне от 0,02 до 1,0 мг/дм3 в пересчете на азот фотометрическим методом. При анализе проб воды с массовой концентрацией аммонийного азота, превышающей 1,0 мг/дм3, допускается выполнение измерений после соответствующего разбавления пробы водой, не содержащей аммонийного азота.
2. Характеристики погрешности измерения
2.1. При соблюдении всех регламентируемых методикой условий проведения измерений характеристики погрешности результата измерений с вероятностью 0,95 не должны превышать значений, приведенных в таблице 1.
При выполнении измерений в пробах с массовой концентрацией аммонийного азота свыше 1,0 мг/дм3 после соответствующего разбавления погрешность измерения не превышает величины D · η, где D - погрешность измерений концентрации аммонийного азота в разбавленной пробе; η - степень разбавления.
Предел обнаружения азота аммонийного 0,005 мг/дм3.
2.2. Значения показателя точности методики используют при:
- оформлении результатов измерений, выдаваемых лабораторией;
- оценке деятельности лабораторий на качество проведения измерений;
- оценке возможности использования результатов измерений при реализации методики в конкретной лаборатории.
Таблица 1 - Диапазон измерений, значения характеристик погрешности и ее составляющих
|
Диапазон измерений массовой концентрации азота аммонийного X, мг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) sr, мг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости), sR, мг/дм3 |
Показатель правильности (границы систематической погрешности при вероятности P = 0,95), ± Dс, мг/дм3 |
Показатель точности (границы погрешности при вероятности P = 0,95), ± D, мг/дм3 |
|
От 0,020 до 0,050 включ. |
0,002 |
0,005 |
0,004 |
0,010 |
|
Св. 0,050 до 0,500 включ. |
0,04 · Х |
0,11 · Х |
0,08 · Х |
0,22 · Х |
|
Св. 0,50 до 1,00 включ. |
0,02 |
0,06 |
0,04 |
0,11 |
3. Средства измерений, вспомогательные устройства, реактивы, материалы
3.1. При выполнении измерений применяют следующие средства измерений и вспомогательные устройства
3.1.1. Фотометр или спектрофотометр любого типа (КФК-3, КФК-2, СФ-46, СФ-56 и др.)
3.1.2. Весы аналитические 2 класса точности по ГОСТ 24104-2001.
3.1.3. Весы технические лабораторные 4 класса точности по ГОСТ 24104-2001 с пределом взвешивания 200 г.
3.1.4. pH-метр или иономер любого типа (pH-150, pH-155, Экотест-2000, Анион-410 и др.).
3.1.5. Государственный стандартный образец состава водных растворов ионов аммония ГСО 7259-96.
3.1.6. Колбы мерные не ниже 2 класса точности по ГОСТ 1770-74 вместимостью:
50 см3 - 12 шт.
100 см3 - 2 шт.
250 см3 - 1 шт.
500 см3 - 1 шт.
1000 см3 - 1 шт.
3.1.7. Пипетки градуированные не ниже 2 класса точности по ГОСТ 29227-91 вместимостью:
1 см3 - 6 шт.
2 см3 - 3 шт.
5 см3 - 3 шт.
3.1.8. Пипетки с одной отметкой не ниже 2 класса точности по ГОСТ 29169-91 вместимостью:
5 см3 - 2 шт.
10 см3 - 3 шт.
20 см3 - 1 шт.
25 см3 - 3 шт.
3.1.9. Бюретка не ниже 2 класса точности по ГОСТ 29251-91 вместимостью:
25 см3 - 1 шт.
3.1.10. Цилиндры мерные по ГОСТ 1770-74 вместимостью:
10 см3 - 2 шт.
25 см3 - 1 шт.
100 см3 - 3 шт.
250 см3 - 1 шт.
1 дм3 - 1 шт.
3.1.11. Колбы конические или плоскодонные по ГОСТ 25336-82 с притертыми пробками вместимостью:
50 см3 - 30 - 40 шт.
250 см3 - 2 шт.
3.1.12. Воронка лабораторная по ГОСТ 25336-82 диаметром 56 мм
- 1 шт.
3.1.13. Стаканы химические термостойкие по ГОСТ 25336-82 вместимостью:
50 см3 - 3 шт.
100 см3 - 1 шт.
250 см3 - 2 шт.
500 см3 - 1 шт.
1 дм3 - 1 шт.
2 дм3 - 1 шт.
3.1.14. Стаканчики для взвешивания (бюксы) по ГОСТ 25336-82 - 6 шт.
3.1.15. Колбы круглодонные с отводом (колбы Вюрца) по ГОСТ 25336-82: на шлифах вместимостью:
50 см3 - 1 шт.
без шлифов вместимостью: 100 см3 - 1 шт.
3.1.16. Воронка капельная по ГОСТ 25336-82 вместимостью: 50 см3 - 1 шт.
3.1.17. Склянки для промывания газов по ГОСТ 25336-82 вместимостью:
50 - 100 см3 - 2 шт.
200 см3 - 1 шт.
3.1.18. Колонка стеклянная с краном и пористой пластиной высотой 50 - 60 см, диаметром 2 - 4 см или бюретка с прямым краном вместимостью 50 см3 с прокладкой из стеклоткани или стекловаты по ГОСТ 29251-91 - 1 шт.
3.1.19. Пробирки по ГОСТ 25336-82 вместимостью 5 - 6 см3 - 10 шт.
3.1.20. Эксикатор по ГОСТ 25336-82.
3.1.21. Устройство для фильтрования проб с использованием мембранных или бумажных фильтров.
3.1.22. Пробки резиновые.
3.1.23. Шкаф сушильный общелабораторного назначения.
3.1.24. Плитка электрическая с закрытой спиралью и регулируемой мощностью нагрева по ГОСТ 14919-83.
3.1.25. Штатив для пробирок.
Допускается использование других типов средств измерений, посуды и вспомогательного оборудования, в том числе импортных, с характеристиками не хуже, чем у приведенных в 3.1.
3.2. При выполнении измерений применяют следующие реактивы и материалы
3.2.1. Аммоний хлористый (хлорид аммония) по ГОСТ 3773-72, х.ч.
3.2.2. Калий марганцовокислый (перманганат калия) по ГОСТ 20490-75, ч.д.а.
3.2.3. Калий йодистый (иодид калия) по ГОСТ 4232-74, ч.д.а.
3.2.4. Калий двухромовокислый (дихромат калия) по ГОСТ 4220-75, х.ч. или калий двухромовокислый, стандарт-титр 0,1 моль/дм3 эквивалента по ТУ 6-09-2540-72.
3.2.5. Натрий пентацианонитрозилферрат (II) 2-водный (нитропруссид натрия) Na2[Fe(CN)5NO] · 2H2O, ч.д.а. по ТУ 6-094224-76.
3.2.6. Натрий лимоннокислый 5,5-водный (цитрат натрия), по ГОСТ 22280-76, ч.д.а.
3.2.7. Натрий серноватистокислый (тиосульфат натрия) 5-водный, по ГОСТ 27068-86, ч.д.а. или натрий серноватистокислый, стандарт-титр 0,1 моль/дм3 эквивалента по ТУ 6-09-2540-72.
3.2.8. Хлорид кальция безводный по ТУ 6-09-4711-81, ч. (для эксикатора).
3.2.9. Натрия гидроокись (гидроксид натрия) по ГОСТ 4328-77, ч.д.а.
3.2.10. Натрий хлористый (хлорид натрия) по ГОСТ 4233-77, х.ч.
3.2.11. Кислота соляная по ГОСТ 3118-77, ч.д.а.
3.2.12. Кислота серная по ГОСТ 4204-77, ч.д.а.
3.2.13. Кислота борная по ГОСТ 9656-75, х.ч.
3.2.14. Кислота лимонная по ГОСТ 3652-69, х.ч.
3.2.15. Кислота уксусная по ГОСТ 61-75, ч.д.а.
3.2.16. Крахмал растворимый по ГОСТ 10163-76, ч.д.а.
3.2.16. Фенол по ТУ 6-09-40-3245-90, ч.д.а.
3.2.17. Хлороформ по ГОСТ 20015-88, очищенный.
3.2.18. Спирт этиловый по ГОСТ 18300-87
3.2.19. Катионит сильнокислотный КУ-2-8 или КРС-5п-Т40 по ТУ 6-09-10-829-79 или другой, равноценный по характеристикам.
3.2.20. Вода дистиллированная по ГОСТ 6709-72.
3.2.21. Фильтры бумажные обеззоленные «синяя лента» по ТУ 6-09-1678-86.
3.2.22. Фильтры мембранные «Владипор МФАС-ОС-2», 0,45 мкм, по ТУ 6-55-221-1-29-89 или другого типа, равноценные по характеристикам.
3.2.22. Универсальная индикаторная бумага pH 1 - 10 по ТУ 6-09-1181-76.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в 3.2.
4. Метод измерения
Метод измерения основан на образовании индофенолового синего при взаимодействии аммиака в щелочной среде с гипохлоритом и фенолом и фотометрическом измерении оптической плотности ярко-голубого соединения с максимумом в спектре поглощения при 630 нм.
5. Требования безопасности охраны окружающей среды
5.1. При выполнении измерений массовой концентрации аммиака и ионов аммония в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в государственных стандартах и соответствующих нормативных документах.
5.2. По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся ко 2, 3 классам опасности по ГОСТ 12.1.007-76.
5.3. Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005-88.
5.4. Работу с кристаллическим фенолом следует проводить в вытяжном шкафу с использованием средств индивидуальной защиты - очков, резиновых перчаток и фартука. При попадании фенола на кожу, его следует немедленно снять ватным тампоном, обильно смоченным этиловым спиртом, затем тщательно промыть водой с мылом.
5.5. Непригодный к использованию раствор фенола сливают в канализацию, разбавляя большим объемом воды.
5.6. Дополнительных требований по экологической безопасности не предъявляется.
6. Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются лица со средним профессиональным образованием, имеющие стаж работы в лаборатории не менее 6 месяцев и освоившие методику.
7. Условия выполнения измерений
7.1. При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
- температура воздуха (22 ± 5) °C;
- атмосферное давление от 84,0 до 106,7 кПа (от 630 до 800 мм рт. ст.);
- влажность воздуха не более 80 % при 25 °C;
- напряжение в сети (220 ± 10) В;
- частота переменного тока (50 ± 1) Гц.
7.2. В помещении, где выполняют измерения массовой концентрации аммонийного азота, запрещается проводить работы, связанные с применением аммиака и щелочных растворов солей аммония.
8. Отбор и хранение проб
Отбор проб для определения аммиака и ионов аммония производят в соответствии с ГОСТ 17.1.5.05-85 и ГОСТ Р 51592-2000. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04-81 и ГОСТ Р 51592-2000. Пробы помещают в стеклянную или полиэтиленовую (полипропиленовую) посуду с плотно закрывающейся пробкой.
Если анализ не может быть произведен в день отбора пробы, ее консервируют прибавлением 1 см3 раствора серной кислоты 1:1 на 1 дм3 воды и хранят в холодильнике 3 - 4 дня. Для более длительного хранения необходимо замораживание пробы.
Перед определением (консервацией) пробы фильтруют через мембранный фильтр 0,45 мкм, очищенный двукратным кипячением в безаммиачной воде. Чистые фильтры хранят в плотно закрытом бюксе. Фильтрование проб следует проводить под давлением (продавливанием пробы через фильтр), поскольку при фильтровании под вакуумом возможны потери аммиака за счет улетучивания, особенно если pH пробы выше 7,5. При отсутствии мембранных фильтров или установок для фильтрования под давлением, допустимо использовать бумажные фильтры «синяя лента», промытые 1 %-ным раствором соляной кислоты, а затем безаммиачной водой. При фильтровании через любой фильтр первые порции фильтрата следует отбросить.
9. Подготовка к выполнению измерений
9.1. Приготовление растворов и реактивов
9.1.1. Раствор фенола
3,52 г фенола и 0,040 г нитропруссида натрия дигидрата (или 0,035 г безводного препарата) растворяют в 100 см3 безаммиачной воды. Если используют другую навеску фенола, соответственно пересчитывают навеску нитропруссида и объем безаммиачной воды.
Для приготовления раствора фенола можно использовать препарат бесцветный или с едва заметным розоватым оттенком. Если фенол заметно окрашен, его следует очищать перегонкой. Схема установки для перегонки фенола и описание процедуры приведены в приложении А.
Хранят раствор фенола в темной склянке в холодильнике до появления зеленоватой или коричневатой окраски раствора (как правило, не более 10 дней).
9.1.2. Буферный раствор, pH 10,6 - 10,8
33,35 г цитрата натрия (Na3C6H5O7 · 5H2O), 17,0 г борной кислоты, 15,0 г гидроксида натрия и 9,7 г лимонной кислоты растворяют в безаммиачной воде в мерной колбе вместимостью 500 см3, доводят объем до метки и перемешивают. Корректируют pH буферного раствора по pH-метру, добавляя при необходимости гидроксид натрия или лимонную кислоту. При хранении в плотно закрытой склянке раствор устойчив. Если при хранении раствора выпадает кристаллический осадок, перед использованием следует растворить его, слегка подогрев раствор в теплой воде. Один раз в месяц следует проверять pH раствора и, при необходимости, корректировать его.
В тех случаях, когда буферный раствор получается недостаточно чистым (чистоту оценивают по величине холостого опыта), его следует перенести в стакан и нагревать на водяной бане в течение часа для удаления аммиака из раствора.
Примечание - Не рекомендуется использовать лимонную кислоту, хранящуюся в лаборатории более 3 лет, поскольку при хранении возможно загрязнение ее аммиаком.
9.1.3. Гипохлорит натрия, концентрированный раствор
Получение концентрированного раствора гипохлорита натрия приведено в приложении Б.
9.1.4. Определение массовой доли активного хлора в концентрированном растворе гипохлорита
В коническую колбу вместимостью 250 см3 добавляют 80 - 90 см3 дистиллированной воды, приливают пипеткой 2 см3 раствора гипохлорита, 5 см3 раствора иодида калия и 10 см3 раствора уксусной кислоты. Выделившийся йод титруют раствором тиосульфата натрия до бледно-желтой окраски, затем добавляют 1 см3 раствора крахмала и продолжают титрование до обесцвечивания раствора. Одновременно выполняют титрование холостой пробы.
Определение повторяют и при отсутствии расхождения в объемах титранта более 0,1 см3 за результат принимают среднее арифметическое. В противном случае повторяют титрование до получения результатов, расхождение между которыми не превышает 0,1 см3. Массовую долю активного хлора в растворе вычисляют по формуле
Cах = 1,77 · Cт · (Vт - V0), (1)
где Cах - массовая доля активного хлора, %;
Cт - молярная концентрация раствора тиосульфата натрия, моль/дм3;
Vт - объем раствора тиосульфата натрия, пошедший на титрование гипохлорита натрия, см3;
V0 - объем раствора тиосульфата натрия, пошедший на титрование холостой пробы, см3.
9.1.5. Раствор гипохлорита натрия, 0,14 % активного хлора
1,4 см3 концентрированного раствора гипохлорита смешивают с раствором гидроксида натрия, 0,45 моль/дм3, объем которого равен 10 · (Cах - 0,14) см3. При хранении в темной плотно закрытой склянке в холодильнике раствор устойчив 3 дня.
9.1.6. Раствор тиосульфата натрия с молярной концентрацией 0,1 моль/дм3
25 г Na2S2O3 · 5H2O растворяют в 1 дм3 дистиллированной воды, которую предварительно кипятят в течение 1 - 1,5 ч и охлаждают до комнатной температуры. Для консервации добавляют 2 - 3 см3 хлороформа. Раствор используют не ранее, чем через 5 дней после приготовления. Хранят раствор в склянке из темного стекла. Точную концентрацию раствора тиосульфата натрия устанавливают в соответствии с 9.1.7 не реже одного раза в месяц.
9.1.7. Установление точной концентрации раствора тиосульфата натрия
В коническую колбу вместимостью 250 см3 приливают 70 - 80 см3 дистиллированной воды, добавляют с помощью пипетки с одной отметкой 10 см3 раствора дихромата калия, приливают мерным цилиндром 10 см3 раствора иодида калия и 10 см3 раствора соляной кислоты (2:1). Закрывают колбу пробкой и выдерживают в течение 5 мин в темном месте. Затем титруют пробу раствором тиосульфата натрия до слабо-желтой окраски, добавляют 1 см3 раствора крахмала и вновь титруют до исчезновения окраски. Одновременно выполняют титрование холостой пробы.
Определение повторяют и при отсутствии расхождения в объемах титранта более 0,1 см3, за результат принимают среднее арифметическое. Рассчитывают молярную концентрацию тиосульфата натрия в растворе по формуле
![]() (2)
(2)
где Cm - молярная концентрация раствора тиосульфата натрия, моль/дм3;
Vm - объем раствора тиосульфата, пошедший на титрование раствора дихромата калия, см3;
V0 - объем раствора тиосульфата, пошедший на титрование холостой пробы, см3.
9.1.8. Раствор дихромата калия с молярной концентрацией количества вещества эквивалента (КВЭ) 0,1000 моль/дм3
При использовании стандарт-титра последний растворяют в дистиллированной воде в мерной колбе вместимостью 1000 см3, доводят объем дистиллированной водой до метки и перемешивают.
Для приготовления раствора из навески 4,904 г дихромата калия (K2Cr2O7), предварительно высушенного в сушильном шкафу при 105 °C в течение 1 - 2 ч, переносят количественно в мерную колбу вместимостью 1000 см3, растворяют в дистиллированной воде, доводят объем раствора до метки и перемешивают.
Хранят раствор дихромата калия в склянке с притертой пробкой в темном месте не более 6 мес.
9.1.9. Раствор иодида калия, 10 %
9.1.10. Раствор уксусной кислоты, 2 моль/дм3
60 см3 уксусной кислоты растворяют в 440 см3 дистиллированной воды. Раствор устойчив.
9.1.11. Раствор соляной кислоты, 2:1
2 части (по объему) концентрированной соляной кислоты смешивают с 1 частью дистиллированной воды. Раствор устойчив.
9.1.12. Раствор соляной кислоты, 1 моль/дм3
84 см3 концентрированной соляной кислоты растворяют в 920 см3 дистиллированной воды. Раствор устойчив.
9.1.13. Раствор гидроксида натрия, 0,45 моль/дм3
3,6 г гидроксида натрия растворяют в 200 см3 безаммиачной воды. Раствор устойчив при хранении в полиэтиленовой посуде.
9.1.14. Раствор гидроксида натрия, 1 моль/дм3
40 г гидроксида натрия растворяют в 1 дм3 дистиллированной воды. Раствор устойчив при хранении в полиэтиленовой посуде.
9.1.15. Раствор гидроксида натрия, 6 моль/дм3
48 г гидроксида натрия растворяют в 200 см3 дистиллированной воды. Раствор устойчив при хранении в полиэтиленовой посуде.
9.1.16. Раствор крахмала, 0,5 %
0,25 г растворимого (рисового, пшеничного) крахмала перемешивают с 50 см3 дистиллированной воды и нагревают до кипения. Раствор хранят до помутнения.
9.1.17. Подготовка колонки с катионитом в H-форме
Подготовка и регенерация колонки с катионитом приведены в приложении В.
9.1.18. Получение безаммиачной воды
Дистиллированную воду пропускают через колонку, заполненную сильнокислым катионитом в Н-форме, со скоростью 1 - 2 капли в секунду. Первые 100 - 150 см3 воды, прошедшей через колонку, отбрасывают. Хранят безаммиачную воду в плотно закрытой стеклянной посуде не более 3 дней.
9.2. Подготовка посуды
Посуда, используемая при приготовлении растворов и выполнении измерений, должна перед использованием тщательно ополаскиваться безаммиачной водой или прогреваться в течение 1,5 - 2 ч в сушильном шкафу при 110 °C. Прогревание является более эффективным способом удаления следов аммиака с поверхности посуды. Мытье посуды осуществляют разбавленной соляной кислотой и водой. Для очень загрязненной посуды возможно использование концентрированной серной кислоты, либо хромовой смеси с последующим многократным промыванием водопроводной и дистиллированной водой.
9.3. Приготовление градуировочных растворов
9.3.1. Градуировочные растворы готовят из стандартного образца (ГСО) с содержанием ионов аммония 1,00 мг/см3 (0,7765 мг/см3 аммонийного азота).
Для приготовления градуировочного раствора № 1 вскрывают ампулу, и ее содержимое переносят в сухую чистую пробирку. Отбирают 3,20 см3 образца с помощью чистой сухой градуированной пипетки вместимостью 5 см3 и переносят в мерную колбу вместимостью 250 см3. Доводят объем в колбе до метки безаммиачной водой и перемешивают. Массовая концентрация аммонийного азота в градуировочном растворе № 1 составляет 9,94 мг/дм3 (если концентрация ионов аммония в ГСО не равна точно 1,00 мг/см3, рассчитывают массовую концентрацию аммонийного азота в градуировочном растворе № 1 соответственно концентрации конкретного образца). Раствор хранят не более 5 дней.
Для приготовления градуировочного раствора № 2 пипеткой с одной отметкой отбирают 10 см3 градуировочного раствора № 1, помещают его в мерную колбу вместимостью 100 см3 и доводят до метки безаммиачной водой. Массовая концентрация аммонийного азота в градуировочном растворе № 2 составляет 0,994 мг/дм3 Раствор хранению не подлежит.
9.3.2. При отсутствии ГСО допускается в качестве градуировочных растворов использовать аттестованные растворы аммонийного азота, приготовленные из хлорида аммония. Методика приготовления аттестованных растворов приведена в приложении Г.
9.4. Установление градуировочных зависимостей
9.4.1. Установление градуировочной зависимости в диапазоне массовых концентраций аммонийного азота 0 (до 0,10 мг/дм3)
Для приготовления образцов для градуировки в мерные колбы вместимостью 50 см3 приливают градуированной пипеткой 0; 1,0; 2,0; 3,0; 4,0; 5,0 см3 градуировочного раствора № 2 доводят растворы до метки безаммиачной водой и перемешивают. Массовая концентрация аммонийного азота в полученных образцах составит соответственно 0; 0,020; 0,040; 0,060; 0,080; 0,099 мг/дм3. Отбирают пипеткой по 25 см3 каждого из полученных образцов, помещают их в конические или плоскодонные колбы вместимостью 50 см3 с притертой стеклянной или пластиковой пробкой и проводят определение аммонийного азота в соответствии с разделом 10. Оптическую плотность измеряют в кюветах длиной 5 см относительно дистиллированной воды. Оптическую плотность холостого опыта (раствор с нулевой концентрацией аммонийного азота) вычитают из оптической плотности проб.
9.4.2. Установление градуировочной зависимости в диапазоне массовых концентраций аммонийного азота 0,10 - 1,0 мг/дм3
В мерные колбы вместимостью 50 см3 приливают градуированной пипеткой 0; 0,5; 1,0; 2,0; 3,0; 4,0; 5,0 см3 градуировочного раствора № 1, доводят растворы до метки безаммиачной водой и перемешивают. Массовая концентрация аммонийного азота в полученных образцах составят соответственно 0; 0,099; 0,99; 0,398; 0,596; 0,795; 0,994 мг/дм3. Отбирают пипеткой 25 см3 каждого из полученных образцов, помещают их в конические или плоскодонные колбы вместимостью 50 см3 с притертой стеклянной или пластиковой пробкой и проводят определение аммонийного азота в соответствии с разделом «Выполнение измерений». Оптическую плотность измеряют в кюветах длиной 1 см относительно дистиллированной воды. Оптическую плотность холостого опыта вычитают из оптической плотности проб.
9.4.3. Среднее значение оптической плотности холостого опыта вычитают из усредненной оптической плотности растворов, содержащих добавки аммонийного азота.
Градуировочные характеристики рассчитывают в виде линейной зависимости методом наименьших квадратов. Градуировочные зависимости устанавливают заново при приготовлении нового буферного раствора, а также при замене измерительного прибора.
9.5. Контроль стабильности градуировочной характеристики
9.5.1. Контроль стабильности градуировочной характеристики проводят при приготовлении нового раствора фенола или 0,14 %-ного раствора гипохлорита. Средствами контроля являются образцы, используемые для установления градуировочной зависимости по 9.4 (не мене 3 для каждой градуировочной зависимости).
Допускается проводить контроль стабильности одной градуировочной зависимости, если вторая зависимость не будет использована для расчета результатов анализа в анализируемых пробах. Градуировочная характеристика считается стабильной при выполнении условий:
|Х - С| < sR, (3)
где X - результат контрольного измерения массовой концентрации аммонийного азота в образце, мг/дм3;
С - приписанное значение массовой концентрации аммонийного азота в образце, мг/дм3;
sR - показатель воспроизводимости для массовой концентрации аммонийного азота, равной С, мг/дм3 (таблица 1).
Если условие стабильности не выполняется для одного образца для градуировки, необходимо выполнить повторное измерение этого образца для исключения результата, содержащего грубую погрешность. При повторном невыполнении условия, выясняют причины нестабильности, устраняют их и повторяют измерение с использованием других образцов, предусмотренных методикой. Если градуировочная характеристика вновь не будет удовлетворять условию (3), устанавливают новую градуировочную зависимость.
9.5.2. При выполнении условия (3) учитывают знак разности между измеренными и приписанными значениями массовой концентрации аммонийного азота в образцах. Эта разность должна иметь как положительное, так и отрицательное значение, если же все значения имеют один знак, это говорит о наличии систематического отклонения. В таком случае требуется установить новую градуировочную зависимость.
10. Выполнение измерений
10.1. Дважды отбирают пипеткой 25 см3 отфильтрованной анализируемой воды и помещают ее в колбы с притертой стеклянной или пластиковой пробкой вместимостью 50 см3. В вытяжном шкафу к каждой аликвоте последовательно прибавляют 1,5 см3 буферного раствора, 0,7 см3 раствора фенола и 0,7 см3 раствора гипохлорита с массовой долей активного хлора 0,14 %. Прибавление растворов следует производить быстро, закрывая колбу пробкой после добавления очередного раствора. После прибавления растворов фенола и гипохлорита пробу следует перемешивать круговыми движениями. Закрытую пробкой колбу оставляют в темноте на 10 - 12 ч (как правило, до следующего дня). В зависимости от интенсивности окраски оптическую плотность раствора измеряют в кюветах длиной 1 или 5 см на фотометре (спектрофотометре) при длине волны 630 нм. Если используется прибор, снабженный светофильтрами, но не имеющий светофильтра с максимумом пропускания 630 нм, следует использовать ближайший светофильтр со стороны более коротких волн, например, светофильтр с максимумом пропускания при 590 нм. Оптическая плотность раствора (относительно одновременно приготовленного холостого опыта) устойчива, по меньшей мере, в течение недели.
Если проба была законсервирована серной кислотой, перед анализом ее следует нейтрализовать по универсальной индикаторной бумаге, добавляя по каплям раствор гидроксида натрия 6 моль/дм3.
10.2. Одновременно с серией проб воды выполняют анализ холостой пробы, в качестве которой берут дважды по 25 см3 свежей безаммиачной воды. Оптическая плотность холостой пробы в кюветах длиной 5 см при длине волны 630 нм не должна превышать 0,1 (при использовании чистых реактивов и безаммиачной воды хорошего качества значение холостого опыта обычно находится в пределах 0,03 - 0,05). Большее значение указывает на загрязнение безаммиачной воды или буферного раствора ионами аммония. Если получить достаточно чистую безаммиачную воду не удается, допускается выполнять холостой опыт с использованием 5 см3 безаммиачной воды без изменения объема добавляемых реактивов, но перед измерением оптической плотности в колбу следует добавить еще 20 см3 безаммиачной воды и перемешать.
10.3. Если исследуемая вода заметно окрашена или слегка опалесцирует, то дополнительно проводят измерение собственной оптической плотности пробы. Для этого к 25 см3 анализируемой воды добавляют 1,5 см3 буферного раствора и 0,7 см3 раствора гипохлорита, хорошо перемешивают и измеряют оптическую плотность полученного раствора.
10.4. В том случае, когда интенсивная голубая окраска появляется в течение 40 - 60 мин, проводят повторное определение, разбавляя анализируемую пробу безаммиачной водой в 5 - 10 раз (или более, в зависимости от интенсивности окраски).
Примечание - При необходимости получить результат анализа пробы в тот же день, допускается проводить измерение оптической плотности через 3 - 5 ч в зависимости от температуры окружающей среды (чем выше температура, тем быстрее развивается окраска), однако в этом случае одновременно с пробами следует в тех же условиях устанавливать градуировочную зависимость.
11. Вычисление и оформление результатов измерений
11.1. Вычисляют значение оптической плотности Aх, соответствующее концентрации аммонийного азота в пробе воды, по формуле
Aх = A - A1 - A2, (4)
где A - значение оптической плотности анализируемой пробы, в которую добавлены все реактивы;
A1 - значение собственной оптической плотности пробы;
A2 - среднее арифметическое значение оптической плотности холостой пробы.
11.2. По соответствующей градуировочной зависимости находят массовую концентрацию аммонийного азота в анализируемой пробе воды X, согласно полученному значению оптической плотности Aх. Если измерение проводилось после разбавления, массовую концентрацию аммонийного азота в исходной пробе воды рассчитывают по формуле
Х = X' · η, (5)
где X - массовая концентрация аммонийного азота в пробе анализируемой воды, мг/дм3;
X' - массовая концентрация аммонийного азота, найденная по градуировочной зависимости, мг/ дм3;
η - степень разбавления исходной пробы воды.
11.2. При содержании в анализируемой воде нитритного азота более 0,2 мг/дм3 в результат измерения вводят поправку. В этом случае концентрацию аммонийного азота находят по формуле
X = (X' + 0,57 · X' · Xн2) · η, (6)
где Хн - массовая концентрация нитритного азота, мг/дм3 (в том случае, если проба воды была разбавлена, за величину Хн принимают концентрацию нитритного азота в разбавленной пробе);
X, X', η - значения символов те же, что и в формуле (5).
11.3. Результат измерений в документах, предусматривающих его использование, представляют в виде:
`X ± D, мг/дм3 (P = 0,95), (7)
где `X - среднее арифметическое значение двух результатов, разность между которыми не превышает предела повторяемости r (2,77 sr). Значения sr приведены в таблице 1. При превышении предела повторяемости следует поступать в соответствии с 12.2;
± D - границы характеристик погрешности результатов измерений для данной массовой концентрации аммонийного азота (таблица 1).
Численное значение результатов измерений должно оканчиваться цифрой того же разряда, что и значение характеристики погрешности.
11.4. Допустимо представлять результат в виде:
`X ± Dл (P = 0,95) при условии Dл< D, (8)
где ± Dл - границы характеристик погрешности результатов измерений, установленные при реализации методики в лаборатории и обеспечиваемые контролем стабильности результатов измерений.
Примечание - Допустимо характеристику погрешности результатов измерений при внедрении методики в лаборатории устанавливать на основе выражения Dл = 0,84 · D с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов измерений.
11.5. Массовую концентрацию свободного аммиака (в пересчете на азот) рассчитывают, исходя из суммарного содержания аммонийного азота, температуры и pH воды с помощью таблицы 2. Для промежуточных значений pH и температуры мольную долю азота аммиака Д находят методом линейной интерполяции. Приведенные в таблице 2 значения используют для расчета концентрации азота аммиака в диапазоне минерализации от 0 до 1,0 г/дм3. Если минерализация анализируемой пробы воды превышает 1 г/дм3, полученное значение массовой концентрации азота аммиака следует умножить на коэффициент 0,9.
Таблица 2 - Мольная доля азота аммиака в общем содержании аммонийного азота в воде в зависимости от pH и температуры при минерализации 0,5 г/дм3
|
Мольная доля азота аммиака при температуре, °C |
|||||||
|
0 |
5 |
10 |
15 |
20 |
25 |
30 |
|
|
6,0 |
0,0001 |
0,0002 |
0,0002 |
0,0003 |
0,0004 |
0,0005 |
0,0006 |
|
6,5 |
0,0004 |
0,0006 |
0,0008 |
0,0010 |
0,0013 |
0,0016 |
0,0020 |
|
7,0 |
0,0013 |
0,0018 |
0,0024 |
0,0031 |
0,0040 |
0,0051 |
0,0064 |
|
7,5 |
0,0041 |
0,0056 |
0,0075 |
0,0098 |
0,0126 |
0,0160 |
0,0200 |
|
8,0 |
0,0130 |
0,0176 |
0,0233 |
0,0303 |
0,0388 |
0,0488 |
0,0605 |
|
8,2 |
0,0204 |
0,0275 |
0,0364 |
0,0472 |
0,0600 |
0,0751 |
0,0926 |
|
8,4 |
0,0320 |
0,0430 |
0,0565 |
0,0728 |
0,0920 |
0,114 |
0,139 |
|
8,6 |
0,0498 |
0,0665 |
0,0868 |
0,111 |
0,138 |
0,170 |
0,204 |
|
8,8 |
0,0768 |
0,102 |
0,131 |
0,165 |
0,203 |
0,245 |
0,289 |
|
9,0 |
0,116 |
0,152 |
0,193 |
0,238 |
0,287 |
0,339 |
0,392 |
|
9,2 |
0,172 |
0,221 |
0,274 |
0,331 |
0,390 |
0,448 |
0,505 |
|
9,4 |
0,248 |
0,310 |
0,375 |
0,440 |
0,503 |
0,563 |
0,618 |
|
9,6 |
0,344 |
0,416 |
0,487 |
0,544 |
0,616 |
0,671 |
0,719 |
|
9,8 |
0,454 |
0,531 |
0,602 |
0,664 |
0,718 |
0,764 |
0,803 |
|
10,0 |
0,568 |
0,641 |
0,705 |
0,758 |
0,801 |
0,837 |
0,866 |
|
10,5 |
0,806 |
0,850 |
0,883 |
0,908 |
0,927 |
0,942 |
0,953 |
|
11,0 |
0,929 |
0,947 |
0,960 |
0,969 |
0,976 |
0,981 |
0,985 |
11.6. Массовую концентрацию
азота аммиака ![]() , мг/дм3, рассчитывают по
формуле
, мг/дм3, рассчитывают по
формуле
где X - массовая концентрация аммонийного азота, мг/дм3;
Д - мольная доля азота аммиака в общем содержании аммонийного азота.
11.7. Результат расчета массовой концентрации свободного аммиака в документах, предусматривающих его использование, представляют в виде:
![]() (P =
0,95), (10)
(P =
0,95), (10)
где ![]() - рассчитанное по формуле (9)
значение массовой концентрации азота аммиака, мг/дм3;
- рассчитанное по формуле (9)
значение массовой концентрации азота аммиака, мг/дм3;
![]() -
границы характеристик погрешности расчета массовой концентрации азота аммиака,
мг/дм3.
-
границы характеристик погрешности расчета массовой концентрации азота аммиака,
мг/дм3.
11.8. Погрешность расчета массовой
концентрации азота аммиака ![]() , мг/дм3, находят по формуле.
, мг/дм3, находят по формуле.
![]()
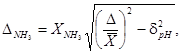 (11)
(11)
где ![]() - рассчитанное значение массовой
концентрации свободного аммиака, мг/дм3;
- рассчитанное значение массовой
концентрации свободного аммиака, мг/дм3;
`X, D - значения символов те же, что и в формуле (7);
δpH - погрешность расчета массовой концентрации свободного аммиака, обусловленная погрешностью измерения pH.
δpH принимает значения:
- 0,21 при pH от 6 до 8,2 включительно;
- (1,1 - 0,11 · pH) при pH от 8,3 до 10,0 включительно;
- 0,03 при pH свыше 10,0.
12. Контроль качества результатов измерений при реализации методики в лаборатории
12.1. Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
- оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки повторяемости и погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
12.2. Алгоритм оперативного контроля повторяемости
12.2.1. Контроль повторяемости осуществляют для каждого из результатов контрольных измерений, полученных в соответствии с методикой. Для этого отобранную пробу воды делят на две части, и выполняют измерения в соответствии с разделом 10.
12.2.2. Результат контрольной процедуры, rк рассчитывают по формуле
rк = |Х1 - Х2|, (12)
где X1, X2 - результаты контрольных измерений массовой концентрации аммонийного азота, мг/дм3.
12.2.3. Предел повторяемости rп рассчитывают по формуле
rп = 2,77sr, (13)
где sr - показатель повторяемости методики, мг/дм3 (таблица 1).
12.2.4. Результат контрольной процедуры должен удовлетворять условию
rк £ rп. (14)
12.2.5. При несоблюдении условия (14) выполняют еще два измерения и сравнивают разницу между максимальным и минимальным результатами с нормативом контроля равным 3,6 · sr. В случае повторного превышения предела повторяемости, поступают в соответствии с разделом 5 ГОСТ Р ИСО 5725-6-2002.
12.3. Алгоритм контроля процедуры выполнения измерений с использованием метода добавок
12.3.1. Контроль исполнителем процедуры выполнения измерений проводят путем сравнения результатов отдельно взятой контрольной процедуры Kк с нормативом контроля K.
12.3.2. Результат контрольной процедуры Kк, мг/дм3, рассчитывают по формуле
Kк = |X' - X - C|, (15)
где X' - результат контрольного измерения массовой концентрации аммонийного азота в пробе с известной добавкой, мг/дм3;
X - результат контрольного измерения массовой концентрации аммонийного азота в рабочей пробе, мг/дм3;
C - величина добавки, мг/дм3.
12.3.3. Норматив контроля погрешности K, мг/дм3, рассчитывают по формуле
![]() (16)
(16)
где DX' - - значение погрешности методики анализа, соответствующее массовой концентрации аммонийного азота в пробе с добавкой, мг/дм3;
DX - значение погрешности методики анализа соответствующее массовой концентрации аммонийного азота в рабочей пробе, мг/дм3.
12.3.4. Если результат контрольной процедуры удовлетворяет условию
|Kк| £ K, (17)
процедуру анализа признают удовлетворительной.
При невыполнении условия (17) контрольную процедуру повторяют. При повторном невыполнении условия (17), выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
12.4. Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
13. Оценка приемлемости результатов, полученных в условиях воспроизводимости
Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение предела воспроизводимости R, мг/дм3, рассчитывают по формуле
R = 2,77sR. (18)
Значения sR, мг/дм3, приведены в таблице 1.
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно раздела 5 ГОСТ Р ИСО 5725-6-2002.
Примечание - Оценка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Приложение А
(обязательное)
Очистка кристаллического фенола перегонкой
Работу с кристаллическим фенолом следует проводить в вытяжном шкафу с использованием средств индивидуальной защиты - очков, резиновых перчаток и фартука. При попадании фенола на кожу, его следует немедленно снять ватным тампоном, обильно смоченным этиловым спиртом, затем тщательно промыть водой с мылом.
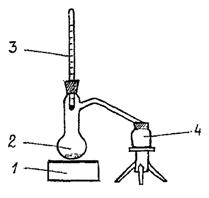
Собирают установку, изображенную на рисунке А.1. Для уменьшения теплообмена колбу 2 следует обернуть стеклотканью или асбестовым полотном. Наличие термометра 3 желательно, но не обязательно. При его отсутствии колбу закрывают хорошо притертой пробкой.
1 - электроплитка; 2 - термостойкая колба с отводом (колба Вюрца); 3 - термометр (или пробка); 4 - бюкс (пробирка)
Рисунок А.1 - Схема установки для перегонки фенола
В колбу помещают определенное количество фенола (в зависимости от потребностей лаборатории), но так, чтобы заполнить не более половины объема колбы. Для удобства переноса фенола в колбу склянку с фенолом следует подогреть в теплой воде (около 50 °C). При этом фенол начинает плавиться, и нужное количество жидкого препарата переливают в колбу. Колбу нагревают. При температуре около 182 °C начинает перегоняться бесцветный фенол, который собирают в чистые сухие бюксы 4, взвешенные вместе с крышкой на технических весах. В каждый бюкс собирают примерно такое количество фенола, которое требуется для однократного приготовления раствора (обычно 1 - 2 см3 или 20 - 30 капель). Перегонку фенола ведут до практически полного испарения его из колбы или до тех пор, пока не начнет перегоняться окрашенный продукт.
Закрытый бюкс с фенолом взвешивают, рассчитывают навеску фенола и растворяют ее в необходимом количестве воды, добавляя воду в бюкс небольшими порциями. Для более быстрого растворения бюкс можно подогреть в теплой воде. Раствор фенола из бюкса через воронку переносят в темную склянку.
Поскольку бюксы не закрываются достаточно герметично, хранить в них фенол можно недолго, постепенно фенол вновь окисляется. Для длительного хранения (не менее года) удобно перегонять фенол в пробирки вместимостью 5 - 6 см3. Пробирки нумеруют и плотно закрывают резиновыми пробками, обернутыми двойным слоем тонкой тефлоновой или полиэтиленовой пленки. Пробирки с пробками также предварительно взвешивают. После отгонки фенола в пробирки их закрывают, помещают в двойной полиэтиленовый пакет и хранят в холодильнике, используя по мере необходимости.
Колбу после перегонки фенола промывают небольшим количеством спирта или раствором гидроксида натрия, затем водой. Для удаления темного налета на стенках колбы можно применять хромовую смесь. Если после применения хромовой смеси налет остается, на него можно не обращать внимание, поскольку он не помешает последующим перегонкам.
Приложение Б
(обязательное)
Получение концентрированного раствора гипохлорита натрия
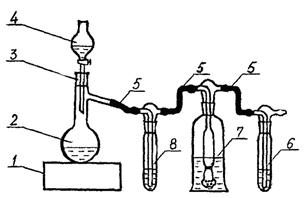
Для получения раствора гипохлорита натрия собирают установку, изображенную на рисунке Б.1.
1 - электроплитка; 2 - колба с отводом без шлифа; 3 - резиновая пробка; 4 - капельная воронка; 5 - соединительные резиновые трубки; 6 - склянка с разбавленным раствором гидроксида натрия; 7 - склянка-приемник; 8 - склянка с безаммиачной водой.
Рисунок Б.1 - Схема установки для получения гипохлорита натрия
Получение гипохлорита необходимо проводить в вытяжном шкафу. В колбу с отводом помещают 25 г перманганата калия и закрывают ее резиновой пробкой, в которую вставлена капельная воронка с 50 см3 концентрированной соляной кислоты. Колба с отводом с помощью резиновых (не силиконовых!) трубок соединяется с промывными склянками. Первая склянка заполняется 25 - 30 см3 безаммиачной воды; во вторую (склянку-приемник) помещают 100 - 120 см3 безаммиачной воды, содержащей около 4 г гидроксида натрия; в третью склянку добавляют немного разбавленного раствора гидроксида натрия в безаммиачной воде для улавливания хлора, не поглощенного в склянке-приемнике. Соединения должны быть выполнены так, чтобы длина резиновых трубок была минимальна.
При добавлении соляной кислоты к перманганату калия выделяется газообразный хлор, который, в основном, поглощается в склянке-приемнике. Чтобы избежать значительных потерь хлора следует обеспечить герметичность соединений элементов установки. При достаточно полном протекании реакции и поглощении хлора в склянке-приемнике можно получить раствор с концентрацией активного хлора 2 - 4 % и более. Пропускание хлора ведут до практически полного прекращения его выделения (2 - 3 ч). Ускорить реакцию можно слабым нагреванием, но не следует допускать слишком бурного выделения хлора, поскольку он при этом не будет достаточно эффективно поглощаться в склянке-приемнике. При эффективном поглощении раствор в склянке постепенно становится зеленовато-желтым.
По окончании реакции отсоединяют склянку-приемник, добавляют в нее понемногу сухой гидроксид натрия до исчезновения явной желтой окраски, затем добавляют еще 2 г гидроксида натрия и перемешивают. Приготовленный раствор гипохлорита хранят в темной склянке, упакованной в полиэтиленовый пакет, в холодильнике в течение года или более, периодически проверяя концентрацию активного хлора (1 - 2 раза в месяц). Аналогично можно поступить с раствором гипохлорита, получающимся в склянке (6), если массовая доля активного хлора в нем более 0,5 %, однако этот раствор будет менее устойчивым.
Примечание - Если соединения стеклянных и резиновых трубок, а также резиновой пробки с колбой, окажутся недостаточно герметичными, можно стыки замазать обычным детским пластилином.
Приложение В
(обязательное)
Подготовка и регенерация колонки с катионитом
50 - 60 г сухого катионита замачивают на 1 - 2 суток в насыщенном растворе хлорида натрия в дистиллированной воде (70 г хлорида натрия растворяют в 200 см3 воды). Через 1 - 2 суток сливают раствор хлорида, промывают катионит 2 - 3 раза дистиллированной водой и переносят его в колонку вместе с водой так, чтобы не образовалось воздушных пузырьков. Предварительно в колонку приливают немного дистиллированной воды. Избыток воды при заполнении колонки периодически сливают через кран. После заполнения пропускают через колонку с катионитом последовательно по 100 см3 раствора соляной кислоты 1 моль/дм3, дистиллированной воды и раствора гидроксида натрия 1 моль/дм3 со скоростью 1 - 2 капли в секунду, повторяя процедуру 8 - 10 раз. Заканчивают обработку смолы пропусканием 100 см3 раствора соляной кислоты. Промывают колонку дистиллированной водой до pH 6 по универсальной индикаторной бумаге, пропуская воду с максимально возможной скоростью. Колонка с катионитом пригодна к работе длительное время. В перерыве между использованием колонку хранят герметично закрытой. Катионит должен постоянно находиться под слоем воды.
При ухудшении качества безаммиачной воды колонку регенерируют, пропуская 100 см3 раствора соляной кислоты 1 моль/дм3 и промывая дистиллированной водой.
Катионит (как сухой, так и влажный) со временем стареет и теряет ионообменные свойства. Для проверки пригодности катионита готовят раствор хлорида натрия с молярной концентрацией 0,010 моль/дм3, для чего взвешивают на аналитических весах 0,0585 г хлорида натрия и растворяют его в дистиллированной воде в мерной колбе вместимостью 100 см3. Через колонку после первоначальной подготовки или после регенерации пропускают 100 см3 дистиллированной воды со скоростью 1 - 2 капли в секунду. Первые 50 - 60 см3 воды, прошедшей через колонку отбрасывают, следующую порцию объемом 30 - 40 см3 собирают в стакан вместимостью 50 см3 и измеряют pH катионированной воды. После этого пропускают с той же скоростью приготовленный раствор хлорида натрия, первые 50 - 60 см3 раствора, прошедшие через колонку отбрасывают, а следующую порцию собирают в стакан и также измеряют pH. За счет замещения ионов натрия в растворе при пропускании через катионит на ионы водорода, pH раствора понижается по сравнению с катионированной дистиллированной водой. Если качество катионита удовлетворительное, разница в величине pH должна составлять 2,5 - 3 единицы.
Приложение Г
(рекомендуемое)
Методика
приготовления аттестованных растворов хлорида аммония для установления
градуировочных характеристик приборов и контроля точности измерений массовой
концентрации аммонийного азота фотометрическим методом AP1-N-NH4+, AP2-N-NH4+,
AP3-N-NH4+
Г.1. Назначение и область применения
Настоящая методика регламентирует процедуру приготовления аттестованных растворов хлорида аммония, предназначенных для установления градуировочных зависимостей и контроля точности результатов измерений массовой концентрации аммонийного азота в природных и очищенных сточных водах фотометрическим методом.
Г.2. Метрологические характеристики
Метрологические характеристики аттестованных растворов приведены в таблице Г.1.
Таблица Г.1 - Метрологические характеристики аттестованных растворов хлорида аммония
|
Шифр аттестованного раствора |
|||
|
АР1-N-NH4+ |
АР2-N-NH4+ |
АР3-N-NH4+ |
|
|
Аттестованное значение массовой концентрации аммонийного азота, мг/дм3 |
500,0 |
10,00 |
1,000 |
|
Предел возможных значений погрешности установления массовой концентрации аммонийного азота (P = 0,95), мг/дм3 |
2,6 |
0,07 |
0,008 |
Г.3. Средства измерений, вспомогательные устройства, реактивы
Г.3.1. Весы аналитические не ниже 2 класса точности по ГОСТ 24104-2001.
Г.3.2. Колбы мерные не ниже 2 класса точности по ГОСТ 1770-74 вместимостью:
500 см3 - 1 шт.
250 см3 - 1 шт.
100 см3 - 1 шт.
Г.3.3. Пипетки с одной отметкой не ниже 2 класса точности по ГОСТ 29169-91 вместимостью:
5 см3 - 1 шт.
10 см3 - 1 шт.
Г.3.4. Стаканчик для взвешивания (бюкс) по ГОСТ 25336-82.
Г.3.5. Воронка лабораторная по ГОСТ 25336-82 диаметром 56 мм.
Г.3.6. Шпатель.
Г.3.7. Промывалка.
Г.3.8. Эксикатор с безводным хлоридом кальция.
Г.3.9. Шкаф сушильный общелабораторного назначения.
Г.3.10. Хлорид аммония NH4Cl по ГОСТ 3773-72, х.ч., содержание основного вещества ³ 99,5 %.
Г.3.11. Катионит сильнокислый КУ-2-8 или КРС-5п-Т40 по ТУ 6-09-10-829-79 или другой, равноценный по характеристикам в H+-форме.
Г.3.12. Вода дистиллированная по ГОСТ 6709-72.
Г.3.13. Вода катионированная (вода дистиллированная, пропущенная через колонку с катионитом в Н+-форме).
Г.4. Процедура приготовления аттестованных растворов хлорида аммония
Г.4.1. Приготовление аттестованного раствора АР1-N-NH4+.
На аналитических весах взвешивают в бюксе с точностью до четвертого знака после запятой 0,962 г NH4Cl, предварительно высушенного в сушильном шкафу при температуре 105 - 110 °C в течение 1 ч и охлажденного до комнатной температуры в эксикаторе. Количественно переносят навеску в мерную колбу вместимостью 500 см3, растворяют в катионированной воде, доводят объем раствора до метки и перемешивают. Переносят раствор в темную склянку с хорошо притертой стеклянной или пластиковой пробкой.
Полученному раствору приписывают массовую концентрацию аммонийного азота 500 мг/дм3.
Г.4.2. Приготовление аттестованного раствора АР2-N-NH4+
Пипеткой с одной отметкой отбирают 5 см3 раствора АР1-N-NH4+, помещают его в мерную колбу вместимостью 250 см3, доводят до метки безаммиачной водой и перемешивают. Переносят раствор в темную склянку с хорошо притертой стеклянной или пластиковой пробкой.
Полученному раствору приписывают массовую концентрацию аммонийного азота 10,0 мг/дм3.
Г.4.3. Приготовление аттестованного раствора АР3-N-NH4+
Пипеткой с одной отметкой отбирают 10 см3 раствора АР2-N-NH4+, помещают его в мерную колбу вместимостью 100 см3, доводят до метки безаммиачной водой и перемешивают. Переносят раствор в темную склянку с хорошо притертой стеклянной или пластиковой пробкой.
Полученному раствору приписывают массовую концентрацию аммонийного азота 1,00 мг/дм3.
Г.5. Расчет метрологических характеристик аттестованного раствора
Г.5.1. Аттестованное значение массовой концентрации аммонийного азота в растворе АР1-N-NH4+ C1 мг/дм3, рассчитывают по формуле
![]() (Г.1)
(Г.1)
где m - масса навески хлорида аммония, г;
14,01 - молярная масса азота, г/моль;
V - вместимость мерной колбы, см3;
53,94 - молярная масса хлорида аммония, г/моль.
Г.5.2. Аттестованное значение массовой концентрации аммонийного азота в растворе АР2-N-NH4+ C2, мг/дм3, рассчитывают по формуле
![]() (Г.2)
(Г.2)
Г.5.3. Аттестованное значение массовой концентрации аммонийного азота в растворе АР3-N-NH4+ C3, мг/дм3, рассчитывают по формуле
![]() (Г.3)
(Г.3)
Г.5.4. Расчет предела возможных значений погрешности приготовления аттестованного раствора АР1-N-NH4+ D1 с массовой концентрацией аммонийного азота 500 мг/дм3 выполняют по формуле
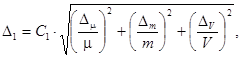 (Г.4)
(Г.4)
где C1 - приписанное раствору значение массовой концентрации аммонийного азота, мг/дм3;
µ - массовая доля основного вещества (NH4Cl) в реактиве, приписанная реактиву квалификации х.ч.;
Dµ - предельное значение возможного отклонения массовой доли основного вещества в реактиве от приписанного значения µ;
m - масса навески хлорида аммония, г;
Dm - предельная возможная погрешность взвешивания, г;
V - вместимость мерной колбы, см3;
Dv - предельное значение возможного отклонения вместимости мерной колбы от номинального значения, см3.
Предел возможных значений погрешности приготовления аттестованного раствора АР1-N-NH4+ равен:
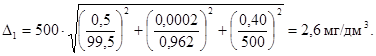
Г.5.5. Расчет предела возможных значений погрешности приготовления аттестованных растворов АР2-N-NH4+ (D2) и АР3-N-NH4+ (D3) с массовой концентрацией аммонийного азота 10,0 и 1,00 мг/дм3 соответственно выполняют по формуле
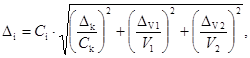 (Г.5)
(Г.5)
где Ci - приписанное растворам АР2-N-NH4+ и АР3-N-NH4+ i-тое значение (i = 2, 3) массовой концентрации аммонийного азота, мг/дм3;
Ck - k-тое (k = 1, 2) значение массовой концентрации аммонийного азота, приписанное раствору, используемому для приготовления раствора АР1-N-NH4+ или АР2-N-NH4+, мг/дм3;
Dk - предел возможного значения погрешности приготовления раствора с массовой концентрацией аммонийного азота Ck;
Vi - вместимость мерной колбы, см3;
DV1 - предельное значение возможного отклонения объема мерной колбы от номинального значения, см3.
V2 - номинальный объем раствора, отбираемого пипеткой, см3;
DV2 - предельное значение возможного отклонения объема раствора, отбираемого пипеткой, от номинального значения, см3.
Предел возможных значений погрешности приготовления аттестованного раствора АР2-N-NH4+ равен:
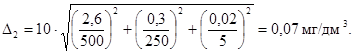
Предел возможных значений погрешности приготовления аттестованного раствора АР3-N-NH4+ равен:
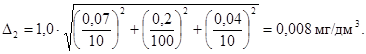
Г.6. Требования безопасности
Необходимо соблюдать общие требования техники безопасности при работе в химических лабораториях.
Г.7. Требования к квалификации операторов
Аттестованные растворы может готовить инженер или лаборант со средним специальным образованием, прошедший специальную подготовку и имеющий стаж работы в химической лаборатории не менее 6 мес.
Г.8. Требования к маркировке
На склянки с аттестованными растворами должны быть наклеены этикетки с указанием шифра раствора, массовой концентрации аммонийного азота, погрешности ее установления и даты приготовления.
Г.9. Условия хранения
Аттестованный раствор АР1-N-NH4+ хранят не более 3 мес. при комнатной температуре и до 6 мес. в холодильнике.
Аттестованный раствор АР2-N-NH4+ хранят не более 5 сут. при комнатной температуре и до 10 дней - в холодильнике.
Аттестованный раствор АР3-N-NH4+ хранят не более суток.
Федеральная служба по гидрометеорологии и мониторингу окружающей среды
ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ «ГИДРОХИМИЧЕСКИЙ ИНСТИТУТ»
|
344090, г. Ростов-на-Дону пр. Стачки, 198 |
Факс: (8632) 22-44-70 Телефон (8632) 22-66-68 E-mail ghi@aaanet.ru |
СВИДЕТЕЛЬСТВО № 35.24-2004
об аттестации методики
выполнения измерений
Методика выполнения измерений массовой концентрации аммиака и ионов аммония в водах фотометрическим методом в виде индофенолового синего,
разработанная ГУ «Гидрохимический институт» (ГУ ГХИ)
и регламентированная РД 52.24.383-2005
аттестована в соответствии с ГОСТ Р 8.563-96 с изменениями 2002 г.
Аттестация осуществлена по результатам экспериментальных исследований
В результате аттестации установлено, что методика соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
1. Диапазон измеряемых концентраций, значения показателей точности и ее составляющих при доверительной вероятности P = 0,95
|
Диапазон измерений массовых концентраций азота аммонийного, X, мг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) sr, мг/дм |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости), sR, мг/дм3 |
Показатель правильности (границы систематической погрешности при вероятности P = 0,95), ± Dc, мг/дм3 |
Показатель точности (границы погрешности при вероятности P = 0,95) ± D, мг/дм3 |
|
|
От 0,020 до 0,050 включ. |
0,002 |
0,005 |
0,004 |
0,010 |
|
|
Св. 0,050 до 0,500 включ. |
0,04 · X |
0,11 · X |
0,08 · X |
0,22 · X |
|
|
Св. 0,50 до 1,00 включ. |
0,02 |
0,06 |
0,04 |
0,11 |
|
2. Диапазон измерений, значения пределов повторяемости и воспроизводимости при доверительной вероятности P = 0,95
|
Диапазон измерений массовых концентраций азота аммонийного, X, мг/дм3 |
Предел повторяемости (для двух результатов параллельных определений) r, мг/дм3 |
Предел воспроизводимости (значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях, при вероятности P = 0,95), R, мг/дм3 |
|
От 0,020 до 0,050 включ. |
0,005 |
0,014 |
|
Св. 0,050 до 0,500 включ. |
0,11 · X |
0,30 · X |
|
Св. 0,50 до 1,00 включ. |
0,05 |
0,17 |
2. При реализации методики в лаборатории обеспечивают:
- оперативный контроль исполнителем процедуры выполнения (на основе оценки повторяемости и погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
Алгоритм контроля исполнителем процедуры выполнения измерений приведен в РД 52.24.383-2005.
Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
Дата выдачи свидетельства 30 декабря 2004 г.
Главный метролог ГУ ГХИ А.А. Назарова
СОДЕРЖАНИЕ