ФЕДЕРАЛЬНАЯ СЛУЖБА ПО ГИДРОМЕТЕОРОЛОГИИ
И МОНИТОРИНГУ ОКРУЖАЮЩЕЙ СРЕДЫ
(РОСГИДРОМЕТ)
|
РУКОВОДЯЩИЙ ДОКУМЕНТ |
РД 52.24.439-2007 |
МАССОВАЯ КОНЦЕНТРАЦИЯ НЕИОНОГЕННЫХ
СИНТЕТИЧЕСКИХ ПОВЕРХНОСТНО-АКТИВНЫХ
ВЕЩЕСТВ И ПОЛИЭТИЛЕНГЛИКОЛЕЙ В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ЭКСТРАКЦИОННО-ФОТОМЕТРИЧЕСКИМ МЕТОДОМ
Ростов-на-Дону
2007
Предисловие
1 РАЗРАБОТАН ГУ «Гидрохимический институт».
2 РАЗРАБОТЧИК Л.В. Боева, канд. хим. наук.
3 СОГЛАСОВАН с УМЗА и ГУ «НПО «Тайфун» Росгидромета
4 УТВЕРЖДЕН Заместителем Руководителя Росгидромета 26.01.2007 г.
5 АТТЕСТОВАН ГУ «Гидрохимический институт», свидетельство об аттестации № 93.24-2006 от 29.08.2006.
6 ЗАРЕГИСТРИРОВАН ЦКБ ГМП за номером РД 52.24.439-2006 от 14.02.2007 г.
7 ВЗАМЕН РД 52.24.439-95 «Методические указания. Методика выполнения измерений массовой концентрации неионных синтетических поверхностно-активных веществ и полиэтиленгликолей в водах экстракционно-фотометрическим методом».
Введение
Подавляющая часть неионогенных синтетических поверхностно-активных веществ (СПАВ) представляет собой продукты присоединения оксида этилена к веществам, имеющим подвижный атом водорода (фенолам, спиртам, кислотам, аминам, амидам). Общая формула их R-Х-(СН2-СН2О)nН, где R - алкильный или алкиларильный радикал; X-О-; -СОО-; -СONН и др. Общим для этой группы СПАВ является присутствие полиоксиэтиленовой цепи, на реакциях которой и основано определение суммарного содержания неионогенных СПАВ.
Неионогенные СПАВ достаточно широко используются при добыче и переработке нефти, газа, в металлургии, текстильной, химической и других областях промышленности в качестве моющих и чистящих средств, эмульгаторов, присадок. Значительные количества неионогенных СПАВ используются в быту, а также в составе пестицидов, используемых для различных целей в сельском хозяйстве.
Причиной появления неионогенных СПАВ в природных водах являются, главным образом, сбросы неочищенных сточных вод, некоторое количество СПАВ может поступать с грунтовыми водами, куда они попадают в процессе очистки на полях фильтрации, а также с атмосферными осадками.
Попадая в воду, неионогенные СПАВ оказывают неблагоприятное влияние на её органолептические показатели. Наиболее неприятным свойством СПАВ является их способность к пенообразованию. В пене на поверхности водоёма концентрируются как сами СПАВ, так и другие загрязняющие вещества и микроорганизмы, в том числе патогенные. При наличии пены в водоёмах ухудшается аэрация воды, следствием чего является замедление процессов самоочищения, угнетение деятельности гидробионтов.
В слабозагрязнённых природных водах неионогенные СПАВ, как правило, отсутствуют. Значительное превышение ПДК неионогенных СПАВ может наблюдаться при поступлении их со сточными водами в маловодные реки или водоёмы. Понижение концентрации растворённых в воде СПАВ связано, в основном, с двумя процессами - сорбцией на взвешенных частицах и донных отложениях и биохимическим разложением.
Полиэтиленгликоли в природных водах обычно не обнаруживаются, наиболее вероятно их присутствие в сточных водах предприятий по производству неионогенных СПАВ.
Содержание неионогенных СПАВ в воде нормируется. Поскольку неионогенные СПАВ представляют собой большую группу оксиэтилированных соединений различных классов, значения предельно допустимых концентраций (ПДК) для индивидуальных веществ имеют достаточно большой разброс, например, для водных объектов хозяйственно-питьевого и культурно-бытового назначения ПДК синтанолов и оксиэтиленалкилфенолов составляет 0,1 мг/дм3, неонолов - 0,1 - 0,3 мг/дм3, стеароксов - 0,5 - 1 мг/дм3. Для водных объектов рыбохозяйственного назначения ПДК различных синтанолов колеблется от 0,0005 до 0,002 мг/дм3, неонолов - от 0,0001 до 0,3 мг/дм3, ПДК стеарокса-980 составляет 0,08 мг/дм3. При определении суммарной концентрации неионогенных СПАВ в водах условно принято считать ПДК равной 0,1 мг/дм3.
РУКОВОДЯЩИЙ ДОКУМЕНТ
МАССОВАЯ КОНЦЕНТРАЦИЯ
НЕИОНОГЕННЫХ
СИНТЕТИЧЕСКИХ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ
И ПОЛИЭТИЛЕНГЛИКОЛЕЙ В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ЭКСТРАКЦИОННО-ФОТОМЕТРИЧЕСКИМ МЕТОДОМ
Дата введения 2007-02-19
1 Область применения
1.1 Настоящий руководящий документ устанавливает методику выполнения измерений (далее - методика) массовой концентрации неионогенных СПАВ, имеющих полиоксиэтиленовые фрагменты в молекуле, а также полиэтиленгликолей (ПЭГ) с молекулярной массой более 400 в пробах природных и очищенных сточных вод в диапазоне от 20 до 500 мкг/дм3 экстракционно-фотометрическим методом.
Допускается выполнение измерений в пробах воды с массовой концентрацией неионогенных СПАВ и ПЭГ, превышающей 500 мкг/дм3 после соответствующего разбавления пробы дистиллированной водой.
1.2 Настоящий руководящий документ предназначен для использования в лабораториях, осуществляющих анализ природных и очищенных сточных вод.
2 Нормативные ссылки
В настоящем руководящем документе использованы ссылки на следующие нормативные документы:
ГОСТ 12.1.005-88 ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 ССБТ. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 17.1.5.04-81 Охрана природы. Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Общие технические условия
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб
МИ 2881-2004 Рекомендация. ГСИ. Методики количественного химического анализа. Процедуры проверки приемлемости результатов анализа.
Примечание - Ссылки на остальные нормативные документы приведены в разделе 4.
3 Приписанные характеристики погрешности измерения
3.1 При соблюдении всех регламентируемых методикой условий проведения измерений характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице 1.
Таблица 1 - Диапазон измерений, значения характеристик погрешности и ее составляющих при измерении массовой концентрации неионогенных СПАВ без отделения ПЭГ (Р = 0,95).
|
Диапазон измеряемых концентраций неионогенных СПАВ, X, мкг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) sr, мкг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) sR, мкг/дм3 |
Показатель правильности (границы систематической погрешности при вероятности Р = 0,95) ± Dс, мкг/дм3 |
Показатель точности (границы погрешности при вероятности Р = 0,95) ± D, мкг/дм3 |
|
от 20 до 150 включ. |
1 + 0,069×Х |
1 + 0,099×Х |
2 + 0,011×X |
10 + 0,13×Х |
|
от 150 до 500 включ. |
9 |
13 |
2 + 0,011×X |
10 + 0,13×Х |
Таблица 2 - Диапазон измерений, значения характеристик погрешности и ее составляющих при измерении массовой концентрации неионогенных СПАВ с отделением ПЭГ (Р = 0,95).
|
Показатель повторяемости (среднеквадратическое отклонение повторяемости) sr, мкг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) sR, мкг/дм3 |
Показатель правильности (границы систематической погрешности при вероятности Р = 0,95) ± Dс, мкг/дм3 |
Показатель точности (границы погрешности при вероятности Р = 0,95) ± D, мкг/дм3 |
|
|
от 40 до 500 включ. |
2 + 0,046×Х |
2 + 0,066×Х |
10 + 0,078×X |
6 + 0,19×Х |
При выполнении измерений в пробах с массовой концентрацией неионогенных СПАВ и ПЭГ свыше 500 мкг/дм3 после соответствующего разбавления погрешность измерения не превышает величины D×h, где D - погрешность измерения концентрации неионогенных СПАВ в разбавленной пробе; h - степень разбавления.
Предел обнаружения неионогенных СПАВ составляет 10 мкг/дм3, ПЭГ - 20 мкг/дм3.
3.2 Значения показателя точности методики используют при:
- оформлении результатов измерений, выдаваемых лабораторией;
- оценке деятельности лабораторий на качество проведения измерений;
- оценке возможности использования результатов измерений при реализации методики в конкретной лаборатории.
4 Средства измерений, вспомогательные устройства, реактивы, материалы
4.1 Средства измерений, вспомогательные устройства
При выполнении измерений применяют следующие средства измерений и другие технические средства:
4.1.1 Фотометр или спектрофотометр любого типа (КФК-2, КФК-3, СФ-46, СФ-56 и др.).
4.1.2 Весы лабораторные высокого (II) класса точности по ГОСТ 24104-2001.
4.1.3 Весы для статического взвешивания по ГОСТ 29329-92 с наибольшим пределом взвешивания 200 г.
4.1.4 Государственный стандартный образец состава оксиэтилированного изононилфенола ГСО 7197-95.
4.1.5 Термометры лабораторные по ГОСТ 29224-91 с диапазоном от 0 °С до 100 °С и от 0 °С до 200 °С.
4.1.6 Колбы мерные 2 класса точности, исполнения 2, 2а по ГОСТ 1770-74 вместимостью: 25 см3 - 10 шт.
50 см3 - 2 шт.
100 см3 - 3 шт.
4.1.7 Пипетки градуированные 2 класса точности, исполнения 1, 2 по ГОСТ 29227-91 вместимостью: 1 см3 - 4 шт.
2 см3 - 2 шт.
5 см3 - 7 шт.
10 см3 - 3 шт.
4.1.8 Пипетки с одной отметкой 2 класса точности, исполнения 2 по ГОСТ 29169-91 вместимостью: 5 см3 - 2 шт.
10 см3 - 1 шт.
4.1.9 Пробирки градуированные исполнения 2 с взаимозаменяемым конусом 14/23 с притертой стеклянной пробкой по ГОСТ 1770-74 вместимостью 25 см3- 10 шт.
4.1.10 Пробирки конические исполнения 1 по ГОСТ 1770-74
вместимостью: 10 см3 - 20 шт.
4.1.11 Цилиндры мерные исполнения 1, 3 по ГОСТ 1770-74 вместимостью:
50 см3 - 2 шт.
100 см3 - 2 шт.
250 см3 - 2 шт.
500 см3 - 1 шт.
1000 см3 - 1 шт.
4.1.12 Колбы конические Кн, исполнение 2, ТХС по ГОСТ 25336-82 вместимостью:
50 см3 - 10 шт.
100 см3 - 2 шт.
250 см3 - 1 шт.
4.1.13 Воронки делительные ВД, исполнение 1, 3 по ГОСТ 25336-82 вместимостью:
100 см3 - 3 шт.
1 дм3 - 3 шт.
4.1.14 Воронки лабораторные по ГОСТ 25336-82 диаметром:
25 - 36 мм - 4 шт.
75 - 100 мм - 1 шт.
4.1.15 Воронки фильтрующие ВФО с отводом и взаимозаменяемым конусом 19/26, с пористой пластиной (ПОР 160; ПОР 250) или воронка фильтрующая ВФ исполнения 2 и колба с тубусом (Бунзена) исполнения 1, 2 вместимостью 0,5 - 1,0 дм3 или пробирка П40 с взаимозаменяемым конусом 19/26 и отводом, высотой 150 мм по ГОСТ 25336-82.
4.1.16 Стаканы, тип В исполнения 1, ТС по ГОСТ 25336-82 вместимостью:
50 см3 - 3 шт.
250 см3 - 2 шт.
400 см3 - 1 шт.
600 см3 - 1 шт.
4.1.17 Стаканчики для взвешивания (бюкс) СВ-19/9 по ГОСТ 25336-82 - 2 шт.
4.1.18 Эксикатор исполнения 2, диаметром 190 мм по ГОСТ 25336-82
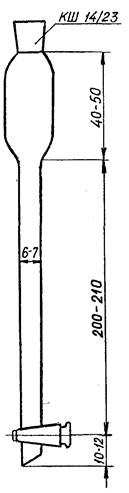
4.1.19 Хроматографическая колонка (рисунок 1)
4.1.20 Установка из термически стойкого стекла для перегонки растворителей (круглодонная колба К-1 вместимостью 1 дм3 с конусным шлифом 29/32, елочный дефлегматор длиной не менее 250 мм с конусными шлифами 19/26 - 29/32, , насадка Н1 с взаимозаменяемыми конусами 19/26 - 14/23 - 14/23, холодильник прямой ХПТ, исполнения 1, длиной не менее 400 мм и аллонж АИ-14/23) по ГОСТ 25336-82.
4.1.21 Склянки вместимостью 1 дм3 и флаконы (аптечные) вместимостью 40 - 50 см3 с завинчивающимися пробками с полиэтиленовыми вкладышами для хранения водных проб и экстрактов.
4.1.22 Посуда полиэтиленовая и стеклянная (светлого и темного стекла) для хранения растворов
4.2.23 Воронка Бюхнера № 1 или № 2 по ГОСТ 9147-80.
4.2.24 Ступка № 4 или № 5 по ГОСТ 9147-80
4.2.25 Чашки выпарительные № 3 или № 4 по ГОСТ 9147-80 - 2 шт.
4.1.26 Палочки фторопластовые или стеклянные - 2 шт.
4.1.27 Шпатели - 2 шт.
4.1.28 Шприц стеклянный медицинский без силиконовых уплотнений с иглой длиной около 10 см
4.1.29 Штатив для делительных воронок
4.1.30 Штатив металлический для пробирок
Размеры даны в миллиметрах
Рисунок 1 - Хроматографическая колонка
4.1.31 Центрифуга настольная типа ОПн-3Ухл4.2 по ТУ 5.375-4260.
4.1.32 Насос вакуумный лабораторный любого типа.
4.1.33 Электроплитка с закрытой спиралью и регулируемой мощностью нагрева по ГОСТ 14919-83.
4.1.34 Баня водяная.
4.1.35 Шкаф сушильный общелабораторного назначения с рабочей температурой до 200 °С.
4.1.36 Аппарат для встряхивания делительных воронок вместимостью 1 дм3 любого типа.
4.1.37 Респиратор.
Допускается использование других типов средств измерений, вспомогательных устройств, в том числе импортных, с характеристиками не хуже, чем у приведенных в 4.1.
При выполнении измерений применяют следующие реактивы и материалы:
4.2.1 Фосфорномолибденовая кислота водная (ФМК) по ТУ 6-09-3540-78, ч.д.а.
4.2.2 Пирокатехиновый фиолетовый (ПКФ) индикатор по ТУ 6-09-07-1087-78, ч.д.а.
4.2.3 N-додецилпиридиний (ДДП) бромистый по ТУ 6-09-13-620-77, ч. или
N-цетилпиридиний (ЦП) бромистый (хлористый) по ТУ 6-09-09-70-77, ч.
4.2.4 Барий хлорид 2-водный по ГОСТ 4108-72, ч.д.а.
4.2.5 Кислота соляная по ГОСТ 3118-77, ч.д.а.
4.2.6 Кислота уксусная по ГОСТ 61-75, ч.д.а.
4.2.7 Натрия гидроокись (гидроксид натрия) по ГОСТ 4328-77, ч.д.а.
4.2.8 Натрий хлористый (хлорид натрия) по ГОСТ 4233-77, ч.д.а.
4.2.9 Натрий сернокислый, безводный (сульфат натрия) по ГОСТ 4166-76, ч.
4.2.10 Силикагель крупнопористый КСК-2 или другой марки с аналогичными характеристиками, гранулированный или измельченный (фракция 0,1 - 0,25 мм).
4.2.11 Хлороформ (трихлорметан) по ГОСТ 20015-88, очищенный.
4.2.12 Спирт изобутиловый (изобутанол) по ГОСТ 6016-77, ч. или бутанол-1 по ГОСТ 6006-78, ч.
4.2.13 Спирт этиловый ректификованный технический по ГОСТ 18300-72.
4.2.14 Вода дистиллированная по ГОСТ 6709-72.
4.2.15 Фильтры обеззоленные «белая лента» и «синяя лента» по ТУ 6-09-1678-86.
4.2.16 Вата медицинская гигроскопическая по ГОСТ 5556-81.
4.2.17 Стеклоткань или стекловата.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
5 Метод измерений
Выполнение измерений массовой концентрации неионогенных СПАВ экстракционно-фотометрическим методом основано на экстракции их из воды смесью изобутанол (бутанол)-хлороформ, осаждении неионогенных СПАВ в экстракте раствором ФМК в присутствии хлорида бария, отделении осадка центрифугированием, растворении его в щелочи и определении эквивалентного неионогенным СПАВ молибдена (VI) по его реакции с ПКФ в присутствии катионного СПАВ - ДДП или ЦП, в результате чего образуется комплекс синего (сине-зеленого) цвета. Максимум оптической плотности полученного соединения наблюдается при l = 690 нм.
Угол наклона градуировочной зависимости преимущественно определяется числом оксиэтильных групп в молекуле. Влияние алкильного или алкиларильного радикала менее существенно. При выполнении измерений суммарного содержания неионогенных СПАВ и ПЭГ для приготовления градуировочных растворов могут использоваться оксиэтилированные алкилфенолы или спирты с 10 - 12 оксиэтильными группами, имеющие средний угол наклона градуировочной зависимости по отношению к другим неионогенным СПАВ (например, препараты ОП-10, АФ-12, а также государственные стандартные образцы неионогенных СПАВ, изготовляемые на основе индивидуальных веществ с 10 - 12 оксиэтильными группами в молекуле).
Поскольку осаждение комплекса неионогенных СПАВ с ФМК происходит при достижении определенной их концентрации, то часто наблюдается искривление начальной части градуировочной зависимости.
Для устранения влияния этого фактора во все пробы, в том числе и холостые, добавляется точно отмеренный объем градуировочного раствора, содержащий 10 мкг неионогенных СПАВ.
Если в пробе воды присутствуют ПЭГ с молекулярной массой более 400, также имеющие полиоксиэтиленовые фрагменты в молекуле, то они определяются совместно с неионогенными СПАВ. Для отделения ПЭГ экстракт пропускают через колонку с силикагелем, а затем элюируют из колонки неионогенные СПАВ. ПЭГ остаются сорбированными на силикагеле. Определяют содержание ПЭГ по разности.
6 Требования безопасности, охраны окружающей среды
6.1 При выполнении измерений массовой концентрации неионогенных СПАВ и ПЭГ в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в национальных стандартах и соответствующих нормативных документах.
6.2 По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся ко 2, 3, 4 классам опасности по ГОСТ 12.1.007.
6.3 Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005.
6.4 Вредно действующие вещества подлежат сбору и регенерации или утилизации в соответствии с установленными правилами.
6.5 Выполнение измерений следует проводить при наличии вытяжной вентиляции. При измельчении и просеивании силикагеля следует пользоваться респиратором.
7 Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются лица с высшим профессиональным образованием или средним профессиональным образованием и стажем работы в лаборатории не менее года, освоившие методику.
8 Условия выполнения измерений
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
- температура окружающего воздуха (22 ± 5) °С;
- атмосферное давление от 84,0 до 106,7 кПа (от 630 до 800 мм рт. ст.);
- влажность воздуха не более 80 % при 25 °С;
- напряжение в сети (220 ± 10) В;
- частота переменного тока в сети питания (50 ± 1) Гц.
9 Отбор и хранение проб
Отбор проб производят в соответствии с ГОСТ 17.1.5.05 и ГОСТ Р 51592. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04 и ГОСТ Р 51592. Пробы помещают в стеклянную посуду. Из-за биохимической нестойкости и возможности необратимой сорбции неионогенных СПАВ на стенках посуды и на взвешенных веществах при длительном хранении, анализ проб следует проводить в течение 3 - 4 ч после отбора. Если анализ не может быть выполнен в указанное время, то отмеривают 0,70 дм3 воды, помещают в склянку вместимостью 1 дм3, приливают 30 см3 экстракционной смеси (см. 10.1.7) и закрывают завинчивающейся пробкой с полиэтиленовым вкладышем. Встряхивают пробу несколько раз, открывая пробку после каждого встряхивания, до тех пор, пока при следующем встряхивании не будет избыточного давления в склянке. Законсервированную таким образом пробу можно хранить до 10 дней при комнатной температуре. При необходимости хранения проб более длительное время следует провести полную экстракцию в соответствии с разделом 11. Экстракты отделяют от воды и помещают во флаконы (аптечные) вместимостью 40 - 50 см3 с завинчивающимися пробками и полиэтиленовыми вкладышами и хранят в темноте.
Объем отбираемой пробы не менее 0,7 дм3.
10 Подготовка к выполнению измерений
10.1 Приготовление растворов и реактивов
10.1.1 Раствор гидроксида натрия, 2 моль/дм3
В 0,25 дм3 дистиллированной воды растворяют 20 г гидроксида натрия. Раствор хранят в полиэтиленовой посуде.
10.1.2 Раствор уксусной кислоты, 2 моль/дм3
К 440 см3 дистиллированной воды приливают 60 см3 уксусной кислоты и перемешивают. Раствор устойчив
10.1.3 Раствор ФМК водный
В мерную колбу вместимостью 50 см3 помещают 0,50 г ФМК, приливают 30 - 40 см3 дистиллированной воды и перемешивают. Добавляют в ту же колбу 0,25 г хлорида бария, 3 см3 концентрированной соляной кислоты, доводят до метки дистиллированной водой и перемешивают. На следующий день раствор фильтруют через фильтр «синяя лента» и хранят в склянке из темного стекла в холодильнике не более 4 мес.
10.1.4 Раствор ФМК спиртовый
Смешивают 2 см3 водного раствора ФМК с 98 см3 этилового спирта. Хранят в холодильнике в склянке с притертой пробкой. Раствор пригоден до появления зеленого или голубого оттенка.
Внимание! Этиловый спирт, используемый для приготовления раствора ФМК должен строго соответствовать требованиям ГОСТ 18300 по содержанию воды. Присутствие избытка воды препятствует осаждению неионогенных СПАВ и делает невозможным их определение.
10.1.5 Раствор ПКФ, 0,05 %-ный
В 100 см3 дистиллированной воды растворяют 0,050 г ПФК. Фильтруют через фильтр «белая лента». Хранят раствор в темной склянке не более 3 дней.
10.1.6 Раствор ДДП, 0,15 %-ный
В 100 см3 этилового спирта растворяют 0,30 г ДДП или ЦП, добавляют к раствору 100 см3 дистиллированной воды и перемешивают. Полученный раствор хранят не более 3 мес.
Смешивают 100 см3 изобутанола (н-бутанола) с 400 см3 хлороформа. Смесь хранят в темной склянке.
10.1.8 Приготовление элюента
Смешивают 25 см3 этилового спирта, 100 см3 хлороформа и 0,3 см3 дистиллированной воды. Раствор хранят в колбе с притертой пробкой не более недели.
10.1.9 Подготовка силикагеля
Подготовка силикагеля описана в приложении А.
10.1.10 Подготовка хроматографической колонки
Подготовка хроматографической колонки к работе описана в приложении Б.
10.2 Приготовление градуировочных растворов
10.2.1 Градуировочный раствор с массовой концентрацией неионогенных СПАВ 1,0 мг/см3 готовят из ГСО, содержащего (0,1000 ± 0,0005) г оксиэтилированного изононилфенола с содержанием основного вещества не менее 99,8 %. Вскрывают ампулу ГСО, количественно переносят ее содержимое в мерную колбу вместимостью 100 см3, тщательно обмывая внутреннюю поверхность ампулы этиловым спиртом из пипетки. Доводят раствор в колбе до метки спиртом и перемешивают.
Полученный раствор хранят в течение года во флаконе с хорошо притертой пробкой или завинчивающейся пробкой с плотным полиэтиленовым вкладышем, обеспечивающими достаточную герметичность флакона.
10.2.2 Для приготовления раствора с массовой концентрацией неионогенных СПАВ 200,0 мкг/см3 с помощью пипетки с одной отметкой вместимостью 10 см3 помещают 10,0 см3 раствора неионогенных СПАВ с массовой концентрацией 1,0 мг/см3 в мерную колбу вместимостью 50 см3, доводят до метки этиловым спиртом и перемешивают.
Раствор хранят в склянке с хорошо притертой или завинчивающейся пробкой с плотным полиэтиленовым вкладышем не более 3 мес.
10.2.3 Для приготовления раствора с массовой концентрацией неионогенных СПАВ 10,0 мкг/см3 с помощью пипетки с одной отметкой вместимостью 5 см3 помещают 5,0 см3 раствора неионогенных СПАВ с массовой концентрацией 200,0 мг/см3 в сухую мерную колбу вместимостью 100 см3, доводят до метки хлороформом и перемешивают.
Раствор хранят в склянке с притертой пробкой не более 3 дней.
10.2.4 Допускается использовать для приготовления градуировочного раствора ГСО других типов, изготовленные на основе оксиэтилированных алкилфенолов или спиртов с 10 - 12 оксиэтильными группами. При использовании ГСО состава водных растворов неионогенных СПАВ в хлороформный раствор после доведения его до метки следует добавить немного безводного сульфата натрия для осушения.
10.3 Установление градуировочной зависимости
Для приготовления градуировочных образцов в конические (центрифужные) пробирки с помощью градуированной пипетки вместимостью 5 см3 помещают 0; 0; 0,5; 1,0; 1,5; 2,0; 2,5; 3,0 см3 раствора с массовой концентрацией неионогенных СПАВ 10 мкг/см3. Доводят объём раствора в каждой пробирке до 5 см3 хлороформом. Содержание неионогенных СПАВ в образцах будет равно соответственно 0; 0; 5,0; 10,0; 15,0; 20,0; 25,0; 30,0 мкг. Добавляют в каждую пробирку ещё 1,0 см3 того же раствора неионогенных СПАВ, 2 см3 спиртового раствора ФМК и далее проводят определение в соответствии с 11.2.
Примечание - Отсутствие явного светложелтого осадка в двух-трех последних образцах после центрифугирования прежде всего может быть вызвано присутствием избыточной воды в этиловом спирте, использованном для приготовления раствора ФМК; в таких случаях спирт следует осушить и перегнать (см. приложение В).
Усреднённую оптическую плотность двух первых образцов, которые являются холостыми, вычитают из оптической плотности остальных образцов. Процедуру повторяют дважды и для установления градуировочной характеристики используют средние значения оптических плотностей.
Градуировочную зависимость оптической плотности от содержания неионогенных СПАВ в образце рассчитывают методом наименьших квадратов.
Градуировочную зависимость устанавливают при замене прибора или использовании новых партий ФМК и ПКФ, но не реже одного раза в квартал.
10.4. Контроль стабильности градуировочной характеристики
10.4.1 Контроль стабильности градуировочной характеристики проводят при приготовлении нового спиртового раствора ФМК.
Средствами контроля являются образцы, используемые для установления градуировочной характеристики по 10.3 (не мене 3). Градуировочная характеристика считается стабильной при выполнении условий:
|Х - С| £ d, (1)
где X - результат контрольного измерения содержания неионогенных СПАВ в образце, мкг;
С - приписанное значение содержания неионогенных СПАВ в образце, мкг;
d - допустимое расхождение между измеренным и приписанным значением содержания неионогенных СПАВ в образце, мкг (таблица 2).
Таблица 3 - Допустимые расхождения между измеренными и приписанными значениями содержания неионогенных СПАВ в образце при контроле стабильности градуировочной характеристики
|
Приписанное значение содержания неионогенных СПАВ в образце, мкг |
5,0 |
10,0 |
15,0 |
20,0 |
25,0 |
30,0 |
|
Допустимое расхождение d, мкг |
0,7 |
1,2 |
1,6 |
2,2 |
1,9 |
1,9 |
Если условие стабильности не выполняется для одного образца для градуировки, необходимо выполнить повторное измерение этого образца для исключения результата, содержащего грубую погрешность. При повторном невыполнении условия, выясняют причины нестабильности, устраняют их и повторяют измерение с использованием других образцов, предусмотренных методикой. Если градуировочная характеристика вновь не будет удовлетворять условию (1), устанавливают новую градуировочную зависимость.
10.4.2 При выполнении условия (1) учитывают знак разности между измеренными и приписанными значениями содержания неионогенных СПАВ в образцах. Эта разность должна иметь как положительное, так и отрицательное значение, если же все значения имеют один знак, это говорит о наличии систематического отклонения. В таком случае требуется установить новую градуировочную зависимость.
11 Выполнение измерений
11.1 Выделение неионогенных СПАВ из воды
В делительную воронку вместимостью 1 дм3 помещают 0,70 дм3 воды, добавляют 30 г хлорида натрия, 30 см3 экстракционной смеси и экстрагируют неионогенные СПАВ в течение 10 мин вручную или с помощью аппарата для встряхивания. После расслаивания экстракт вместе с эмульсией сливают в коническую колбу с притёртой пробкой. К водной пробе добавляют 5 см3 хлороформа и экстрагируют ещё 2 мин. Экстракт после расслаивания сливают в ту же колбу.
Если проба была законсервирована на месте отбора экстракционной смесью, то её переносят из склянки в делительную воронку вместе с растворителем, добавляют 30 г хлорида натрия и проводят экстракцию, не добавляя больше экстракционную смесь.
Склянку, в которой хранилась проба, споласкивают 5 см3 хлороформа и используют его для проведения второй экстракции.
Для разрушения эмульсии полученный экстракт фильтруют под небольшим вакуумом через воронку с пористой пластиной, на которую дополнительно кладут фильтр «белая лента», вырезанный точно по размеру пластины. Если воронка имеет шлиф и отвод, то фильтрование проводят в делительную воронку вместимостью 100 см3. Если используется воронка без отвода, то фильтрат собирают в колбу Бунзена или пробирку с отводом вместимостью 100 см3, а затем переносят его в делительную воронку.
Осадок на фильтре промывают дважды по 5 см3 этилового спирта, нагретого почти до кипения. Первой порцией спирта промывают также колбу или флакон, в которых находился экстракт. К экстракту добавляют 50 см3 дистиллированной воды и промывают его, встряхивая воронку в течение 1,5 - 2 мин. После расслоения фаз хлороформный экстракт переносят через воронку с комочком хлопковой или стеклянной ваты, смоченной хлороформом, в мерную колбу или градуированную пробирку вместимостью 25 см3 с притертой пробкой. Промывают вату небольшим количеством хлороформа и доводят объём экстракта до метки. Если экстракт получился мутным, добавляют безводного сульфата натрия до осветления экстракта.
Если экстракт, полученный при экстракции исходной пробы воды, прозрачен, не содержит эмульсии или взвешенных частиц, то его можно сразу фильтровать через вату в мерную колбу или пробирку.
С помощью сухой пипетки с одной отметкой вместимостью 5 см3 отбирают 5,0 см3 полученного экстракта, переносят в сухую центрифужную коническую пробирку, добавляют 1,0 см3 раствора с массовой концентрацией неионогенных СПАВ 10 мкг/см3, 2 см3 спиртового раствора ФМК и тщательно перемешивают содержимое пробирки фторопластовой (или стеклянной) палочкой. Оставляют пробирки стоять в течение 10 мин, затем центрифугируют их в течение 5 мин при скорости 1500 об/мин. После остановки центрифуги хлороформ из пробирок осторожно сливают, плавно переворачивая пробирку, или отбирают его с помощью шприца с длинной иглой так, чтобы не взмутить осадок. В пробирке при этом должно остаться около 0,2 см3 растворителя.
Затем стенки пробирки из пипетки промывают 1,5 см3 смеси 3 частей хлороформа с 1 частью этилового спирта и вновь центрифугируют 5 мин. Промывной раствор также осторожно удаляют. В пробирки добавляют по 0,5 см3 раствора гидроксида натрия 2 моль/дм3, и ставят на водяную баню с температурой 80 - 100 °С (низкий стакан вместимостью 250 см3 с небольшим количеством дистиллированной воды).
Через 5 мин пробирки вынимают, содержимое пробирок разбавляют до 5 - 7 см3 дистиллированной водой и переносят в мерные колбы (или градуированные пробирки) вместимостью 25 см3, ополаскивая центрифужные пробирки еще дважды дистиллированной водой. Добавляют к полученному раствору 3,0 см3 раствора уксусной кислоты, 1,0 см3 раствора ПКФ, доводят дистиллированной водой до метки и перемешивают. Добавляют 1,0 см3 раствора ДДП или ЦП и вновь перемешивают, переворачивая колбу вверх-вниз (не встряхивать!).
Через 10 мин измеряют оптическую плотность полученных проб в кюветах с толщиной поглощающего слоя 3 см относительно дистиллированной воды на спектрофотометре или фотометре с непрерывной разверткой спектра при длине волны 690 нм, на фотометре, снабженном светофильтрами - со светофильтром, максимум пропускания которого находится при длине волны от 670 до 700 нм.
Одновременно с пробами выполняют холостой опыт. Для этого в две центрифужные пробирки помещают 5 см3 хлороформа, добавляют 1 см3 хлороформного раствора с массовой концентрацией неионогенных СПАВ 10 мкг/см3, 2 см3 раствора ФМК и далее проводят те же операции, что и с пробами. Усреднённое значение холостого опыта вычитают из оптической плотности проб.
Если оптическая плотность пробы выходит за пределы градуировочной зависимости, следует выполнить повторное определение, используя меньшую аликвоту экстракта (от 1 до 3 см3), разбавленную хлороформом до 5 см3.
Анализ каждого экстракта выполняют дважды, полученные оптические плотности усредняют, если расхождение между ними не превышает 25 % по отношению к среднему значению при оптической плотности, соответствующей содержанию неионогенных СПАВ 10 мкг и менее, и 20 % при более высоких значениях оптической плотности.
В том случае, когда полученное по градуировочной зависимости содержание неионогенных СПАВ составляет 5 мкг или менее, для уточнения результата отбирают 10 - 15 см3 экстракта в стакан вместимостью 50 см3 и упаривают на водяной бане до объёма примерно 4 см3. Переносят упаренный экстракт в центрифужную пробирку, доводят объём до 5 см3, сполоснув стакан хлороформом, и вновь проводят определение.
11.3 Отделение ПЭГ
Если в пробе могут присутствовать ПЭГ, определяющиеся совместно с неионогенными СПАВ, последние отделяют пропусканием экстракта через колонку с силикагелем, подготовленную, как описано в приложении Б. Для этого пипеткой отбирают аликвоту экстракта от 2 до 8 см3, содержащую не более 30 мкг неионогенных СПАВ и помещают её в хроматографическую колонку. Вносить пробу в колонку следует осторожно, так, чтобы не взмутить силикагель. Пробу пропускают через колонку со скоростью 0,5 - 1 см3/мин. Когда уровень растворителя в колонке достигнет уровня силикагеля, промывают стенки верхней части колонки 0,5 - 1 см3 хлороформа и также пропускают его через слой силикагеля. Необходимо следить, чтобы уровень растворителя в колонке не опускался ниже уровня силикагеля.
После пропускания пробы в колонку приливают около 10 см3 элюента и также пропускают его со скоростью 0,5 - 1 см3/мин. Первые 3 см3 элюата отбрасывают, последующие 4 - 5 см3 отбирают в центрифужную пробирку и проводят определение неионогенных СПАВ, как описано в 11.2. ПЭГ в этих условиях остаются в колонке.
12 Вычисление и оформление результатов измерений
12.1 По градуировочной зависимости находят содержание неионогенных СПАВ, мкг, во взятой аликвоте экстракта, соответствующее полученному значению оптической плотности.
Массовую концентрацию неионогенных СПАВ в анализируемой пробе воды в пересчете на используемый стандарт X, мкг/дм3, рассчитывают по формуле
![]() (2)
(2)
где Х - массовая концентрация неионогенных СПАВ в анализируемой пробе, мкг/дм3;
q - содержание неионогенных СПАВ в аликвоте экстракта, найденное по градуировочной зависимости, мкг;
V1 - объём аликвоты экстракта, см3.
V2 - объем пробы воды, взятый для анализа, дм3.
Массовую концентрацию ПЭГ ХПЭГ, мкг/дм3, в пересчете на тот же стандарт вычисляют по разности между массовой концентрацией неионогенных СПАВ, найденной до и после пропускания экстракта через колонку с силикагелем.
12.2 Результат измерения в документах, предусматривающих его использование, представляют в виде:
Х ± D, мг/дм3 (Р = 0,95), (3)
где ± D - границы характеристик погрешности результатов измерения для данной массовой концентрации неионогенных СПАВ, мкг/дм3 (таблица 1).
Численные значения результата измерения должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности.
12.3 Погрешность расчета массовой концентрации ПЭГ DПЭГ, мкг/дм3, вычисляют по формуле
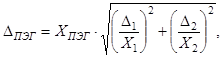 (4)
(4)
где D1, D2 - значения характеристик погрешности, соответствующие массовой концентрации неионогенных СПАВ, найденной до (X1) и после (Х2) пропускания экстракта через колонку с силикагелем, мкг/дм3.
12.4 Допустимо представлять результат в виде:
Х ± Dл (Р = 0,95) при условии Dл < D, (5)
где ± Dл - границы характеристик погрешности результатов измерений, установленные при реализации методики в лаборатории и обеспечиваемые контролем стабильности результатов измерений, мкг/дм3.
Примечание - Допустимо характеристику погрешности результатов измерений при внедрении методики в лаборатории устанавливать на основе выражения Dл = 0,84×D с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов измерений.
12.5 Результаты измерения оформляют протоколом или записью в журнале, по формам, приведенным в Руководстве по качеству лаборатории.
13 Контроль качества результатов измерений при реализации методики в лаборатории
13.1 Общие положения
13.1.1 Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
- оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
13.1.2 Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
13.2 Алгоритм оперативного контроля процедуры выполнения измерений с использованием метода добавок
13.2.1 Контроль исполнителем процедуры выполнения измерений проводят путем сравнения результатов отдельно взятой контрольной процедуры Кк с нормативом контроля К.
13.2.2 Результат контрольной процедуры Кк, мкг/дм3, рассчитывают по формуле
Кк = |Х¢ - Х - С|, (6)
где X¢ - результат контрольного измерения массовой концентрации неионогенных СПАВ в пробе с известной добавкой, мкг/дм3;
X - результат измерения массовой концентрации неионогенных СПАВ в рабочей пробе мкг/дм3;
С - величина добавки, мкг/дм3.
13.2.3 Норматив контроля погрешности К, мг/дм3, рассчитывают по формуле
![]() (7)
(7)
где DХ¢ - значение характеристики погрешности методики, соответствующее массовой концентрации нефтяных компонентов в пробе с добавкой, мг/дм3;
DХ - значение характеристики погрешности методики, соответствующее массовой концентрации нефтяных компонентов в пробе без добавки, мг/дм3.
Примечание - Допустимо для расчета норматива контроля использовать значения характеристик погрешности, полученные расчетным путем по формулам DлХ¢ = 0,84×DХ¢ и DлХ¢ = 0,84×DХ.
13.2.4 Если результат контрольной процедуры удовлетворяет условию
|Кк| £ К, (8)
процедуру анализа признают удовлетворительной.
При невыполнении условия (8) контрольную процедуру повторяют. При повторном невыполнении условия (8), выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
14 Проверка приемлемости результатов, полученных в условиях воспроизводимости
Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости R. При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение предела воспроизводимости рассчитывают по формуле
R = 2,77sR. (9)
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно разделу 5 ГОСТ Р ИСО 5725-6 или МИ 2881.
Примечание - Проверка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Приложение А
(обязательное)
Подготовка силикагеля
Силикагель измельчают в ступке, если необходимо, и просеивают через сита с размером отверстий 0,25 мм и 0,1 мм. Для работы используют фракцию, прошедшую через первое сито и задержавшуюся на втором. Полученный силикагель увлажняют дистиллированной водой (примерно 100 см3 воды на 100 г силикагеля). Промывают силикагель 150 - 160 см3 70 %-ного этилового спирта несколько минут, затем дают отстояться и спирт декантируют. После этого промывают силикагель 150 - 160 см3 смеси хлороформа с этиловым спиртом (1:1), удаляя растворитель декантацией. Затем заливают силикагель таким же объёмом хлороформа, взмучивают и фильтруют через фильтр «белая лента» на воронке Бюхнера под вакуумом. Силикагель на воронке промывают еще 2 раза по 70 - 80 см3 хлороформа. Отсасывают хлороформ, силикагель переносят в фарфоровые чашки, распределяя его тонким слоем и дают хлороформу испариться в вытяжном шкафу. Полученный силикагель хранят в склянке с хорошо пришлифованной пробкой.
Перед использованием необходимое количество силикагеля активируют 5 - 6 ч в сушильном шкафу при температуре 160 - 165 °С и охлаждают в эксикаторе. Охлажденный силикагель взвешивают, помещают в колбу с притертой пробкой вместимостью 100 см3 и постепенно, встряхивая колбу, добавляют дистиллированную воду из расчета 1,5 см3 воды на каждые 10 г силикагеля. Колбу закрывают пробкой и встряхивают до полного исчезновения комков. Выдерживают силикагель в течение суток, периодически перемешивая, после чего силикагель готов к работе. При хранении в герметично закрытой посуде в эксикаторе подготовленный силикагель пригоден к использованию 2 - 3 недели.
Регенерацию использованного силикагеля осуществляют аналогично.
Приложение Б
(обязательное)
Подготовка хроматографической колонки к работе
Б.1 Заполнение колонки
В хроматографическую колонку (рисунок 1) помещают небольшой комочек чистой стекловаты или распушенной стеклоткани. Колонку дважды промывают хлороформом (по 3 - 4 см3) и затем заполняют хлороформом на высоту 8 - 10 см. Силикагель, подготовленный в соответствии с приложением А, размешивают в небольшом количестве хлороформа и заливают в колонку. Избыток хлороформа сливают через кран, затем вновь добавляют взмученный в хлороформе силикагель, пока слой силикагеля в колонке не достигнет высоты 17 - 18 см. Необходимо следить, чтобы не образовывались воздушные пузырьки в слое силикагеля и он постоянно был покрыт хлороформом. После окончания заполнения колонки сливают избыток хлороформа до уровня примерно на 1 - 2 мм выше уровня силикагеля. В таком виде колонка готова к работе.
Колонка заполняется каждый раз свежей порцией силикагеля. Для ее заполнения требуется около 1 г сухого силикагеля.
Б.2 Проверка качества работы колонки и определение объёма элюата, отбираемого для анализа
Параметры полученной колонки могут несколько колебаться для каждой колонки и каждой партии силикагеля. Для их определения следует построить кривую элюирования. В подготовленную согласно Б.1 колонку помещают 3 - 4 см3 хлороформного градуировочного раствора с массовой концентрацией неионогенных СПАВ 10 мкг/см3 и пропускают раствор через колонку со скоростью 0,5 - 1 см3/мин. Промывают колонку ещё 0,5 - 1 см3 хлороформа, после чего в колонку заливают элюент. Добавление всех растворов следует проводить осторожно, так, чтобы не взмучивать силикагель. Элюент пропускают через колонку со скоростью 0,5 - 1 см3/мин и отбирают фракции по 1 см3 в центрифужные пробирки. Всего отбирают 10 фракций.
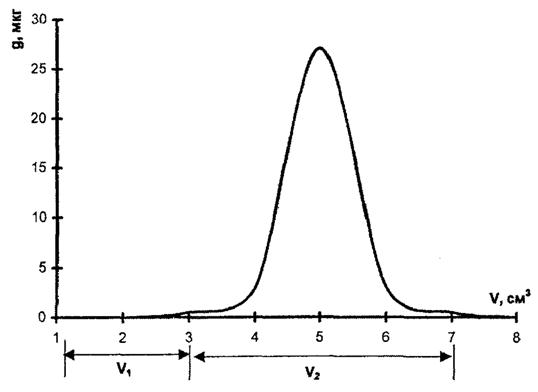
Объём раствора в каждой пробирке доводят до 5 см3 хлороформом и далее выполняют определение неионогенных СПАВ, как описано в разделе «Выполнение измерений». Вид кривой элюирования представлен на рисунке Б.1. В колонке хорошего качества неионогенные СПАВ элюируются в виде достаточно узкого пика (максимум в 4-х фракциях). На рисунке показан объём элюата (V1 = 3 см3), который должен быть отброшен (применительно к данной колонке и силикагелю) и объём, который отбирается для анализа (V2 = 4 - 5 см3). Проверка качества работы колонки проводится один раз для данной колонки и данной партии силикагеля.
Рисунок Б.1 - Кривая элюирования неионогенных СПАВ
Приложение В
(рекомендуемое)
Регенерация хлороформа
Хлороформные экстракты после окончания анализа собирают в отдельную темную склянку с небольшим количеством дистиллированной воды и затем регенерируют. Для этого слив хлороформа помещают в делительную воронку вместимостью 1 дм3, добавляют равный объем дистиллированной воды и встряхивают воронку 2 мин. После отстаивания хлороформ переносят в другую воронку, вновь добавляют равный объем воды и повторяют промывание, после чего хлороформ фильтруют через слой ваты или 2 - 3 неплотных бумажных фильтра в кругло-донную (перегонную) колбу.
Перегоняют хлороформ, отбирая фракцию, кипящую при температуре 60,5 - 62,0 °С. Первую порцию отгона, кипящую ниже 60,5 °С, возвращают в слив, а остаток после отгонки отбрасывают.
Федеральная служба по гидрометеорологии и мониторингу
окружающей среды
ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ
«ГИДРОХИМИЧЕСКИЙ ИНСТИТУТ»
|
344090, г. Ростов-на-Дону пр. Стачки, 198 |
Факс: (8632) 22-44-70 Телефон (8632) 22-66-68 Е-mail ghi@aaanet.ru |
СВИДЕТЕЛЬСТВО № 93.24-2006
об аттестации методики выполнения
измерений
Методика выполнения измерений массовой концентрации неионогенных СПАВ и полиэтиленгликолей в водах экстракционно-фотометрическим методом,
разработанная ГУ «Гидрохимический институт» (ГУ ГХИ)
и регламентированная РД 52.24.439-2006
аттестована в соответствии с ГОСТ Р 8.563-96 с изменениями 2002 г.
Аттестация осуществлена по результатам экспериментальных исследований
В результате аттестации установлено, что методика соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
1 Диапазон измерений, значения характеристик погрешности и ее составляющих при измерении массовой концентрации неионогенных СПАВ без отделения ПЭГ (Р = 0,95)
|
Диапазон измеряемых концентраций неионогенных СПАВ, X, мкг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) sr, мкг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) sR, мкг/дм3 |
Показатель правильности (границы систематической погрешности при вероятности Р = 0,95) ± Dс, мкг/дм3 |
Показатель точности (границы погрешности при вероятности Р = 0,95) ± D, мкг/дм3 |
|
от 20 до 150 включ. |
1 + 0,069×Х |
1 + 0,099×Х |
2 + 0,011×Х |
10 + 0,13×Х |
|
от 150 до 500 включ. |
9 |
13 |
2 + 0,011×Х |
10 + 0,13×Х |
2 Диапазон измерений, значения характеристик погрешности и ее составляющих при измерении массовой концентрации неионогенных СПАВ с отделением ПЭГ (Р = 0,95)
|
Диапазон измеряемых концентраций неионогенных СПАВ, X, мкг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) sr, мкг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) sR, мкг/дм3 |
Показатель правильности (границы систематической погрешности при вероятности Р = 0,95) ± Dс, мкг/дм3 |
Показатель точности (границы погрешности при вероятности Р = 0,95) ± D, мкг/дм3 |
|
от 40 до 500 включ. |
2 + 0,046×Х |
2 + 0,066×Х |
10 + 0,078×Х |
6 + 0,19×Х |
3 Диапазон измерений, значения пределов воспроизводимости при измерении массовой концентрации неионогенных СПАВ без отделения ПЭГ (Р = 0,95)
|
Диапазон измеряемых концентраций неионогенных СПАВ, X, мкг/дм3 |
Предел воспроизводимости (значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях, при вероятности Р = 0,95) R, мг/дм3 |
|
от 20 до 150 включ. |
3 + 0,28×Х |
|
от 150 до 500 включ. |
36 |
4 Диапазон измерений, значения предела воспроизводимости при измерении массовой концентрации неионогенных СПАВ с отделением ПЭГ (Р = 0,95)
|
Диапазон измеряемых концентраций неионогенных СПАВ, X, мкг/дм3 |
Предел воспроизводимости (значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях, при вероятности Р = 0,95) R, мг/дм3 |
|
от 40 до 500 включ. |
6 + 0,18×Х |
5 При реализации методики в лаборатории обеспечивают:
- оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
Алгоритм оперативного контроля исполнителем процедуры выполнения измерений приведен в РД 52.24.439-2006.
Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
Дата выдачи свидетельства 29 августа 2006 г.
Главный метролог ГУ ГХИ А.А. Назарова
СОДЕРЖАНИЕ