Государственное санитарно-эпидемиологическое нормирование
Российской Федерации
4.2. МЕТОДЫ КОНТРОЛЯ, БИОЛОГИЧЕСКИЕ И
МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
Выявление бактерий
Legionella pneumophila
в объектах
окружающей среды
Методические указания
МУК 4.2.2217-07
Москва 2007
1. Разработаны: Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека (Г.Ф. Лазикова, Ю.М. Федоров); ФГУЗ «Федеральный центр гигиены и эпидемиологии» Роспотребнадзора (И.В. Брагина, М.В. Зароченцев, Э.Ф. Опочинский); ГУ «Научно-исследовательский институт эпидемиологии и микробиологии им. Н.Ф. Гамалеи» РАМН (И.С. Тартаковский. Т.И. Карпова, Ю.Е. Дронина, Ю.С. Аляпкина, Ю.М. Романова, А.Л. Гинцбург); ФГУЗ «Российский научно-исследовательский противочумный институт «Микроб» (А.Н. Куличенко, С.А. Портенко, Н.А. Осина, В.В. Кутырев); ФГУЗ «Ростовский-на-Дону научно-исследовательский противочумный институт» (Ю.М. Ломов, А.Н. Терентьев, Г.Л. Карбышев, Л.И. Шелохович, Г.Д. Харабаджахян, И.К. Савельева); ФГУЗ «Центр гигиены и эпидемиологии в г. Москве» (Н.Я. Салова); Управлением Роспотребнадзора по г. Москве (Л.В. Родина); ФГУЗ Причерноморская ПЧС (В.И. Малай, Н.Д. Темежникова); Федеральным научным центром гигиены им. Ф.Ф. Эрисмана (Г.М. Трухина); ГУП «Мосводоканал» (Г.П. Кашкарова); МГУ инженерной экологии (А.Н. Цедилин, Е.М. Иванникова).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Роспотребнадзора (прот. № 1 от 29 марта 2007 г.).
3. Утверждены и введены в действие Главным государственным санитарным врачом Российской Федерации, Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека Г.Г. Онищенко 30 мая 2007 г.
СОДЕРЖАНИЕ
УТВЕРЖДАЮ
Главный государственный санитарный
врач Российской Федерации,
Руководитель Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека
Г.Г. Онищенко
30 мая 2007 г.
Дата введения: 1 августа 2007 г.
4.2. МЕТОДЫ КОНТРОЛЯ, БИОЛОГИЧЕСКИЕ И МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
Выявление бактерий Legionella pneumophila в объектах окружающей среды
Методические указания
МУК 4.2.2217-07
1. Область применения
1.1. Настоящие методические указания устанавливают методику проведения лабораторных исследований объектов окружающей среды по выявлению в них бактерий Legionella pneumophila - возбудителя болезни легионеров.
Проведение мониторинга объектов окружающей среды на наличие Legionella pneumophila позволит определить степень их контаминации возбудителем и дать оценку эффективности принимаемых мер в целях профилактики болезни легионеров и обеспечения безопасности здоровья населения.
1.2. Методические указания предназначены для применения в лабораториях учреждений Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека Российской Федерации, осуществляющих контроль за объектами окружающей среды; в лабораториях других организаций, аккредитованных в установленном порядке на право осуществления контроля безопасности объектов окружающей среды на наличие возбудителя болезни легионеров.
1.3. Методические указания являются обязательными:
• в порядке надзора за соблюдением установленных требований в области обеспечения безопасности объектов окружающей среды, в т.ч. в соответствии с СанПиН 2.1.2.1331-03 «Гигиенические требования к устройству, эксплуатации и качеству воды аквапарков», СанПиН 2.1.2.1188-03 «Плавательные бассейны. Гигиенические требования к устройству, эксплуатации и качеству воды. Контроль качества»;
• в ходе проведения противоэпидемических мероприятий и при эпидемиологическом расследовании возможных эпидемических вспышек и спорадических случаев болезни легионеров.
1.4. Предлагаемый метод выявления бактерий Legionella pneumophila в окружающей среде согласуется с международным стандартом ISO 11731 и руководством ВОЗ «Legionella and the prevention of legionellosis» (2006 г.).
2. Нормативные ссылки
2.1. Федеральный закон «О санитарно-эпидемиологическом благополучии населения» от 30 марта 1999 г. № 52-ФЗ.
2.2. Постановление Правительства Российской Федерации от 24 июня 2000 г. № 554 «Об утверждении Положения о государственной санитарно-эпидемиологической службе Российской Федерации и Положения о государственном санитарно-эпидемиологическом нормировании».
2.3. СанПиН 2.1.2.1331-03 «Гигиенические требования к устройству, эксплуатации и качеству воды аквапарков».
2.4. СанПиН 2.1.2.1188-03 «Плавательные бассейны. Гигиенические требования к устройству, эксплуатации и качеству воды. Контроль качества».
2.5. МУК 4.2.1884-04 «Санитарно-микробиологический и санитарно-эпидемиологический анализ воды поверхностных вод».
2.6. Методические рекомендации МЗ СССР «Эпидемиология, клиника, лечение и профилактика легионеллеза», 1988.
2.7. Санитарно-эпидемиологические правила СП 1.2.731-99 «Безопасность работы с микроорганизмами III - IV групп патогенности и гельминтов».
2.8. Методические указания МУ 1.3.1888-04 «Организация работы при исследованиях методом ПЦР материала, инфицированного патогенными биологическими агентами III - IV групп патогенности».
2.9. Методические указания МУ 3.5.5.1034-01 «Обеззараживание исследуемого материала, инфицированного бактериями I - IV групп патогенности, при работе методом ПЦР».
2.10. European Guidelines for Control and Prevention of Travel associated Legionnaires Disease, 2002.
2.11. ISO 1998.ISO 11731:1998 Water Quality-detection and enumeration of Legionella.
2.12. Legionella and the prevention of Legionellosis. - WHO guidelines. 2006.
3. Характеристика возбудителя болезни легионеров
Legionella pneumophila - грамотрицательная бактерия, возбудитель острых тяжелых пневмоний с высоким процентом летальных исходов (5 - 10 %) и респираторных заболеваний. В природных условиях легионеллы обитают повсеместно в пресноводных водоемах, преимущественно в некультивируемой форме, и паразитируют в амебах и других простейших, не представляя серьезной опасности для человека. Размножение легионелл активно идет в теплой воде в диапазоне температур 25 - 45 °С, хотя их выделяют и из холодной воды.
Высокие адаптивные способности легионелл позволяют им успешно колонизировать искусственные водные системы - системы охлаждения и кондиционирования, градирни, компрессорные устройства, джакузи, фонтаны, медицинское оборудование и др. Условия для размножения легионелл в искусственных водных системах более благоприятны, чем в естественных, что приводит к накоплению в них возбудителя в высокой концентрации. Легионеллы активно колонизируют синтетические и резиновые поверхности промышленного, водопроводного, медицинского оборудования с образованием биопленок, в которых легионеллы значительно более устойчивы к действию дезинфицирующих веществ. В состав естественных биопленок помимо легионелл входят бактерии рода Pseudomonas, Klebsiella, Acinetobacter и др. Важная роль в персистенции легионелл в биопленках принадлежит амебам в которых легионеллы активно размножаются перед образованием сложных биопленок в ассоциации с другими микроорганизмами.
Эпидемические вспышки и спорадические случаи болезни легионеров преимущественно выявляют в местах общественного назначения: у посетителей и персонала гостиниц; торговых, спортивных и выставочных комплексов; промышленных предприятий, больниц, учреждений; круизных судов и др. Фактором передачи служит водный мелкодисперсный аэрозоль, содержащий возбудителя и генерируемый системами водных коммуникаций.
Сочетание высокой концентрации легионелл в водной среде с источниками мелкодисперсного аэрозоля позволяет возбудителю инфекции вследствие ингаляции микробного аэрозоля попадать в нижнюю часть респираторного тракта и легкие человека, где происходит контакт с альвеолярными макрофагами, в которых вирулентные штаммы возбудителя активно размножаются.
При спорадическом легионеллезе и отдельных нозокомиальных вспышках заболевания возможна аспирация воды, контаминированной легионеллами без образования аэрозоля (бассейны, емкости для хранения и транспортирования воды и др.). Это обусловлено возрастанием восприимчивости к легионеллезу лиц со сниженной иммунологической реактивностью на фоне сопутствующих заболеваний, иммунодепрессивной терапии и др.
Эпидемические вспышки и спорадические случаи легионеллеза выявляют повсеместно. Особое значение в последние годы уделяется случаям болезни легионеров, возникающим во время поездок, путешествий и диагностируемым после возвращения из них. Инкубационный период составляет от 2 до 10 дней. Более 30 % случаев спорадического легионеллеза, многочисленные эпидемические вспышки в гостиницах, на круизных судах послужили причиной создания международной системы эпидемиологического надзора за случаями легионеллеза, связанного с поездками.
В настоящее время известно около 50 видов легионелл, преимущественно выделенных из окружающей среды, из которых собственно болезнь легионеров вызывает вид Legionella pneumophila, насчитывающий 16 серогрупп. Причем более 80 % случаев заболевания вызывают штаммы 1-й серогруппы. Среди других представителей рода Legionella в качестве микробов-оппортунистов, вызывающих заболевание при нарушении клеточного иммунитета и\или на коморбидном фоне, следует отметить L. micdadei, L. longbeachae, L. dumqffii и L. bozemanii. Остальные виды Legionella spp. не патогенны для человека.
4. Материально-техническое обеспечение*
|
рН метр - рН 410; диапазон рН от - 1 до 14, точность 0,01 рН, температура анализируемой среды от - 10 до 100 °С (Белоруссия) Весы Adventurer™ - прецизионные одночашечковые электронные цифровые с функцией обнуления тары и другими вспомогательными функциями, стандартного уровня, максимальная загрузка - 210 г, погрешность при измерении - 0,001 г (OHAUS, США) |
|
|
Весы ScoutPro - портативные одночашечковые электронные цифровые с функцией обнуления тары, максимальная нагрузка - 2000 г, погрешность при измерении - 0,1 г (OHAUS, США) |
|
|
4.2. Оборудование |
|
|
Шкаф сушильный стерилизационный ШСС-80П, поддерживающий температуру плюс (160 ± 5) °С (Россия) |
|
|
Термостат суховоздушный ТС-1/80, объем 80 л с температурой до 60 °С (Россия) СО2 инкубатор МСО 5АС, персональный, объем 49 л, тепловая рубашка, ТС-датчик СО2 (Sanyo) или анаэростат GasPak 100 (на 11 чашек), GasPak 150 (на 36 чашек) |
|
|
Стерилизатор паровой ВК-30 с вертикальной камерой, объем 150 л |
|
|
Дистиллятор, обеспечивающий качество дистиллированной воды |
|
|
Облучатель бактерицидный настенный УФИК 1´30 |
|
|
Холодильник бытовой электрический с температурой в камере плюс 4 - 6 °С Морозильная камера с температурой в камере до -20 °С |
|
|
* Указанное оборудование и расходные материалы могут быть заменены на аналогичные по характеристикам производства других фирм. |
|
|
Водяная баня TW 2.03, автоматическое регулирование температуры до 85/90 °С, объем 8,5 л, внутренняя и внешняя циркуляция (Elmi, Латвия) Батометр Молчанова ГР-18, предназначенный для взятия проб воды с различной глубины водоемов, с одновременным измерением температуры воды исследуемого слоя, при температуре окружающей среды от 1 до 40 °С (Россия) Прибор для мембранной фильтрации под вакуумом с диаметром фильтрующей поверхности 35 или 47 мм и устройство для создания разрежения 0,5 - 1,0 атм. (САРТОГОСМ, Россия) Прибор для подсчета колоний бактерий (Schuett) Мешалка магнитная BioMMS-3000, без подогрева, максимальный объем 2 л, скорость вращения 0 - 3000 об./мин, размер платформы 150´150 мм Универсальная центрифуга для пробирок до 50 мл «Ева 21» с роторами 6´50 мл (угловая скорость - до 6000 об./мин), 12´15 мл (угловая скорость - до 6000 об./мин), 30´2 мл (угловая скорость - до 12000 об./мин) (Hettich-Zentrifugen, Германия) |
|
|
Микроцентрифуга/встряхиватель ТЭТА 2 (Биоком, Россия) |
|
|
Малогабаритная высокоскоростная лабораторная микроцентрифуга «МиниСпин®», угловая скорость - до 13400 об./мин, 12´1,5 (2,0) мл (Ерpendorf, Германия) |
|
|
Твердотельный термостат Термо 24-15 с диапазоном рабочих температур от 0 до 120 °С (Биоком, Россия) |
|
|
Охладитель проб ОП-1 с диапазоном температур от -4 до 30 °С (Биоком, Россия) Амплификатор Терцик МС-2 (ДНК-Технология, Россия) |
|
|
Амплификатор iCycler для проведения ПЦР с учетом результатов в режиме реального времени, оптический и реакционный модули, комплект фильтров iQ5 Optical System (BIORAD, США) Источник тока Эльф-4 (ДНК-технология, Россия) |
|
|
Камера для горизонтального электрофореза SE-2 (Хеликон, Россия) |
|
|
Фотодокументирующая система GelDoc 2000 (BIORAD, США) |
|
|
4.3. Вспомогательные изделия и расходные материалы |
|
|
Пинцет медицинский |
|
|
Пинцет для работы с мембранными фильтрами |
|
|
Ножницы медицинские |
ГОСТ 21239-89 |
|
Скальпель хирургический, 15 см |
|
|
Термометр ртутный с диапазоном измерений от 0 до 100 °С |
|
|
Лупа микробиологическая |
|
|
Воронки стеклянные |
ГОСТ 25-336-82 |
|
Часы механические сигнальные |
|
|
Емкости эмалированные |
|
|
Пробки различных размеров: силиконовые, резиновые и другие, выдерживающие стерилизацию сухим жаром или автоклавированием |
|
|
Тампоны (свабы) в полипропиленовой пробирке в упаковке с аппликатором-палочкой |
|
|
Вата хлопковая медицинская гигроскопическая |
|
|
Марля медицинская |
ГОСТ 9412-77 |
|
Маркеры водостойкие Лейкопластырь Перчатки резиновые Шпагат |
|
|
Бумага плотная для упаковки посуды Пленка Parafilm A |
|
|
Газогенераторные пакеты CampyPak для факультативных анаэробов, 10 шт./уп. Индикаторные полоски СО2, 50 шт./уп. Мембранные фильтры на основе ацетата целлюлозы для микробиологических целей с диаметром пор не более 0,45 мкм и размером диска 35 или 47 мм или другие фильтрующие мембраны с аналогичной способностью фильтрации, имеющие сертификат качества |
|
|
Мембранные фильтры поликарбонатные с диаметром пор не более 0,45 мкм и размером диска 35 или 47 мм Петли бактериологические |
|
|
Чашки Петри пластиковые микробиологические, стерильные (Россия) |
|
|
Стекла предметные для микропрепаратов |
|
|
Пробирки типов П1, П2 |
|
|
Бутыли стеклянные градуированные с крышкой автоклавируемые или пластиковые флаконы (одноразовые), емкостью 500 и 1000 мл (Wheaton, США) |
|
|
Пакеты полиэтиленовые стерильные для отбора проб воды на 100 мл типа «вихрь» |
|
|
Центрифужные пробирки, объемом 50 и 15 мл Микроцетрифужные пробирки, объемом 0,2, 0,6 и 1,5 мл (QSP, США) |
|
|
Автоматические пипетки переменного объема автоклавируемые «Ленпипет» серия Дигитал: 1 - 10, 5 - 40, 40 - 200, 200 - 1000 мкл (Россия) Автоматические пипетки переменного объема Eppendorf 500 - 5000, 1000 - 10000 мкл Наконечники до 10 мкл (QSP, США) Наконечники до 200 мкл с фаской (QSP, США) Наконечники до 1000 мкл (QSP, США) Наконечники до 5000 мкл (Eppendorf, Германия) Наконечники до 10000 мкл (Eppendorf, Германия) Наконечники с фильтром до: 10, 100, 200, 1000 мкл (QSP, США) |
|
|
Штативы для центрифужных пробирок, объемом 50 и 15 мл (Германия) |
|
|
Штатив «рабочее место» для микропробирок, объемом 1,5 мл (Хеликон, Россия) Штатив «рабочее место» для микропробирок, объемом 0,6 мл (Хеликон, Россия) Штатив «рабочее место» для микропробирок, объемом 0,2 мл (Хеликон, Россия) Штатив для пипеток переменного объема (Ленпипет, Россия) |
|
|
Штатив для хранения микропробирок, объемом1,5 мл (Хеликон, Россия) |
|
|
Штативы для наконечников до: 10, 200, 1000 мкл (Россия) |
|
|
4.4. Реагенты, реактивы и питательные среды |
|
|
Кислота соляная |
|
|
Калий хлористый |
|
|
Калия гидроокись |
|
|
Натрий серноватисто-кислый (тиосульфат натрия) 5-водный |
|
|
Натрий двууглекислый |
|
|
Спирт этиловый ректифицированный медицинский |
|
|
Спирт этиловый технический |
|
|
Активированный уголь |
Р 72.270.3 |
|
Глицин, Biotechnology Grade 99 % (Amresco, США) |
|
|
L-цистеин (Япония) |
|
|
a-кетоглютаровая кислота |
|
|
Пирофосфат железа растворимый (Sigma, США) |
|
|
Полимиксин В сульфат 500000 ед. (Германия) |
|
|
Ванкомицина гидрохлорид (Германия) |
|
|
Циклогексимид (Германия) |
|
|
ACES-буфер (М-2-ацетамидо-2-аминоэтан-сульфанильная кислота) |
|
|
Агар микробиологический |
ГОСТ 17206-84 |
|
Дрожжевой экстракт |
|
|
Буферный угольно-дрожжевой агар (БУДРАГ, BCYEa) |
|
|
Селективная добавка для среды БУДРАГ(BCYEa) |
|
|
Ростовая добавка для среды БУДРАГ (BCYEa) |
|
|
Легионелбакагар (НПГЦП, Оболенск, Россия) |
|
|
Среда СЭЛ (НИПЧИ, Ростов, Россия) |
|
|
Тест-системы для видовой идентификации |
|
|
Legionella pneumophila в латекс-агглютинации (OXOID, Великобритания, BIORAD, США) |
|
|
Тест-системы для выявления ДНК Legionella pneumophila методом ПЦР с учетом результатов методом электрофореза в агарозном геле: |
|
|
1) набор для выделения ДНК методом нуклеосорбции на силикагеле в присутствии гуанидинтиоцианата; |
|
|
2) набор для осуществления амплификации; |
|
|
3) набор для проведения электрофореза в агарозном геле |
|
|
Тест-системы для количественного выявления ДНК Legionella pneumophila и Legionella spp. в пробах воды гибридизационно-флуоресцентным методом в режиме реального времени: |
|
|
1) набор для выделения ДНК бактерий из проб воды (Aquadien, BIORAD, США); |
|
|
2) набор для количественного выявления ДНК Legionella pneumophila и Legionella spp. гибридизационно-флуоресцентным методом в режиме реального времени Референс-штамм Legionella pneumophila 1-й серогруппы Philadelphia может быть получен в ГНИЙ стандартизации и контроля медицинских биологических препаратов им. Л.А. Тарасевича или в лаборатории легионеллеза ГУНИИЭМ им. Н.Ф. Гамалеи РАМН |
|
5. Приготовление питательных сред и растворов для выделения легионелл
Для выделения легионелл используют стандартную среду - буферный угольно-дрожжевой агар (БУДРАГ, BCYEa) с ростовой и селективной добавкой. Среды промышленного изготовления готовятся в соответствии с прописями на этикетке или в соответствии с инструкцией изготовителя.
Допускается применение сред лабораторного приготовления. Их подготовку осуществляют по следующей схеме:
Компоненты основы среды БУДРАГ (на 1 л)
Дрожжевой экстракт - 10,0 г
Агар - 13,0 г
Активированный уголь - 2,0 г
a-Кетоглютаровой кислоты калийная соль - 1,0 г
ACES-буфер, рН 6,9 - 10 г
1М раствор КОН - 40 мл
Глицин - 3 г
Компоненты ростовой добавки (на 1 л)
L-цистеин - 0,4 г
Пирофосфат железа растворимый - 0,25 г
Компоненты селективной добавки (на 1 л)
Полимиксин В - 80000 ед.
Ванкомицин - 5 мг
Циклогексимид - 80 мг
К навеске ACES-буфера добавляют 500 мл дистиллированной воды и выдерживают на водяной бане при 50 °С, помешивая до полного растворения. К 440 мл дистиллированной воды добавляют 40 мл 1М раствора КОН и осторожно смешивают с первым раствором. Полученным раствором заливают смесь навесок дрожжевого экстракта, агара, активированного угля, калийной соли a-кетоглютаровой кислоты и глицина и выдерживают на водяной бане при 50 °С, осторожно помешивая до полного растворения всех компонентов. Среду автоклавируют 15 мин при 121 °С, охлаждают до 50 °С и добавляют стерильно компоненты ростовой и селективной добавки. Растворяют в 10 мл дистиллированной воды каждую из навесок L-цистеина и пирофосфата железа растворимого, стерилизуют фильтрацией через мембранный фильтр и добавляют в среду. Концентрированные растворы антимикробных препаратов также добавляют в среду до требуемой конечной концентрации.
Конечное значение рН среды - 6,95 ± 0,02. Среду разливают в стерильные чашки Петри по 25 мл и подсушивают в термостате при 37 °С в течение часа. Среда имеет характерный черно-серый цвет.
В качестве контрольной среды, не поддерживающей рост легионелл, используют среду БУДРАГ без добавления селективной и ростовой добавки. Для пересева колоний легионелл и дальнейшего культивирования используют среду БУДРАГ с ростовой, но без селективной добавки.
Для культивирования легионелл можно использовать среду СЭЛ, легионелбакагар, а также шоколадный агар, используемый для культивирования возбудителя туляремии. Ростовые потребности легионелл и возбудителя туляремии весьма близки. Но легионеллы исключительно требовательны к рН среды (6,95), который удается сохранить в условиях длительного (до 10 дней) выделения из окружающей среды за счет компонента среды БУДРАГ - ACES-буфера, отсутствующего в других прописях сред. Музейные штаммы легионелл не столь требовательны к рН и растут на более широком спектре питательных сред, в т.ч. и без ACES-буфера.
При использовании для выделения легионелл сред, отличных от БУДРАГ, необходимо осуществлять дополнительный контроль среды с помощью вирулентного штамма Legionella pneumophila серогруппы 1 Philadelphia 1 (LD50 для морских свинок не более 105 КОЕ при высеве на среду БУДРАГ). Количество колоний на проверяемой партии среды должно соответствовать титру контрольной вирулентной культуры, в качестве которой используется селезеночная суспензия морской свинки, зараженной вирулентным штаммом L. pneumophila Philadelphia 1. Ампулы с селезеночной суспензией вирулентного штамма L. pneumophila Philadelphia 1 для проверки качества питательных сред могут храниться в течение 2 лет при -70 °С.
Для приготовления кислотного КСl-НСl буфера к 39 мл 0,4М раствора НСl добавляют 250 мл 0,4М раствора КСl. Доводят значение рН буфера до 2,2 с помощью 1М раствора КОН. Хранят в темном флаконе при 4 °С не более 1 месяца.
6. Отбор, хранение и транспортирование проб
Отбор проб осуществляют в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб» и ГОСТ Р 51593-2000 «Вода питьевая. Отбор проб»; МУК 4.2.1018-01 «Методические указания по санитарно-микробиологическому анализу питьевой воды»; МУК 4.2.1884-04 «Санитарно-микробиологический и санитарно-паразитологический анализ воды поверхностных водных объектов».
Пробы воды объемом 0,5 - 1,0 л для микробиологического анализа на наличие легионелл отбирают в стерильные емкости. Для отбора проб воды используют специально предназначенную для этих целей одноразовую посуду или емкости многократного применения, изготовленные из материалов, не влияющих на жизнедеятельность микроорганизмов.
Емкости должны быть оснащены плотно закрывающимися пробками (силиконовыми, резиновыми или из других материалов) и защитным колпачком (из алюминиевой фольги, плотной бумаги), или завинчивающимися крышками с резиновыми уплотнителями. Многоразовая посуда, в т.ч. пробки, должна выдерживать стерилизацию сухим жаром или автоклавированием.
С целью дехлорирования воды в стерильные флаконы емкостью 500 мл вносят 2 мл 1,5 %-ного раствора гипосульфита натрия, простерилизованного в автоклаве, или для забора используют емкости, содержащие кристаллы гипосульфита натрия из расчета 20 мг на 1 л воды.
Поверхностные и глубинные пробы отбирают специальными батометрами, предназначенными для этих целей. Допустимо использовать другие приспособления, установленные в приложении к ГОСТ Р 51592-2000.
Забор материала осуществляют стерильно, избегая соприкосновения пробки и края емкости с любыми поверхностями. После наполнения емкость закрывают стерильной пробкой, обеспечивающей герметичность и не намокающей при транспортировании (ватные пробки не применять), и стерильным колпачком.
Смывы с объектов (оборудования для кондиционирования и вентиляции, водонагревательных и охладительных систем, медицинского инструментария и т.д.) берут тампоном (свабом), смоченным стерильным физиологическим раствором и помещают в пробирку со стерильным физиологическим раствором.
С учетом способности легионелл к образованию биопленок на поверхности водопроводного, промышленного, лабораторного и иного оборудования, связанного с циркуляцией и хранением воды, соответствующие участки поверхности также могут исследоваться на наличие легионелл. Соскобы влажных биопленок с поверхности, находящейся под водой или на границе соприкосновения воды и воздуха, берут сухими тампонами и помещают во флакон или пробирку. Соскобы биопленок с высохшей поверхности берут тампонами, смоченными стерильным физиологическим раствором, и помещают в пробирку, содержащую стерильный физиологический раствор.
Отбор проб производит специалист после прохождения инструктажа по технике выполнения отбора проб для микробиологического анализа.
Отобранную пробу маркируют и сопровождают документом отбора проб воды с указанием места, времени забора, фамилии специалиста, отбиравшего пробу, и другой информации (температура воды, погодные условия).
Доставку проб воды осуществляют в контейнерах при температуре 6 - 24 °С. При соблюдении указанной температуры транспортирования и хранения срок начала исследований от момента отбора проб не должен превышать 48 ч. Хранение проб в холодильнике при температуре ниже 6 °С может привести к негативным результатам исследования в связи с возможным переходом легионелл в некультивируемое состояние (Hussong D.et.al.1987). Если проба содержит дезинфектанты, и их нейтрализация не проведена сразу же после отбора, анализ проводят в течение 4 ч после забора.
7. Подготовка проб к исследованию
В случае сильной загрязненности исходного образца воды механическими или масляными примесями, определяемыми визуально, его предварительно фильтруют на стеклянной воронке через стерильный ватно-марлевый или бумажный фильтр. Подготовленную таким образом воду пропускают через мембранный фильтр. После окончания фильтрации мембранные фильтры переносят обожженным анатомическим пинцетом в стерильный флакон или стерильный пластиковый пакет объемом 100 мл с 10 мл физраствора. Отфильтрованную воду обеззараживают добавлением сухой хлорной извести из расчета 200 г на 1 л.
Для десорбции микрофлоры с фильтров флакон помещается на встряхиватель на 1 - 2 мин или качалку на 10 мин. Фильтр внутри пластикового пакета растирается вручную в течение 1 мин. Далее смыв с поверхности фильтра помещают в центрифужную пробирку объемом 15 мл и центрифугируют при 6000 об./мин в течение 30 мин. Надосадочную жидкость полностью удаляют для последующего обеззараживания. Осадок тщательно ресуспендируют стерильной пипеткой в 1 мл физиологического раствора и переносят в стерильную пробирку.
Подготовленную таким образом пробу помещают в холодильную камеру при 4 °С до окончания исследования. При необходимости допускается ее хранение в течение года.
Для снижения уровня загрязненности сконцентрированной пробы посторонней микрофлорой одну ее часть подвергают прогреванию, а другую обрабатывают кислотным буфером.
Для прогревания из подготовленного сконцентрированного образца отбирают 0,2 мл и переносят в стерильную пробирку, после чего помещают пробирку на водяную баню при 50 °С и прогревают в течение 30 мин. Для обработки кислотным буфером 0,2 мл сконцентрированного образца переносят в стерильную пробирку и добавляют 0,2 мл раствора кислотного буфера КСl-НСl, рН 2,2, инкубируют при комнатной температуре в течение 4 мин. Кислотную обработку проводят непосредственно перед посевом на плотные питательные среды.
Образцы биопленок, смывы с поверхностей подвергают концентрированию с помощью центрифугирования, кислотной и термической обработки.
8. Проведение микробиологического анализа
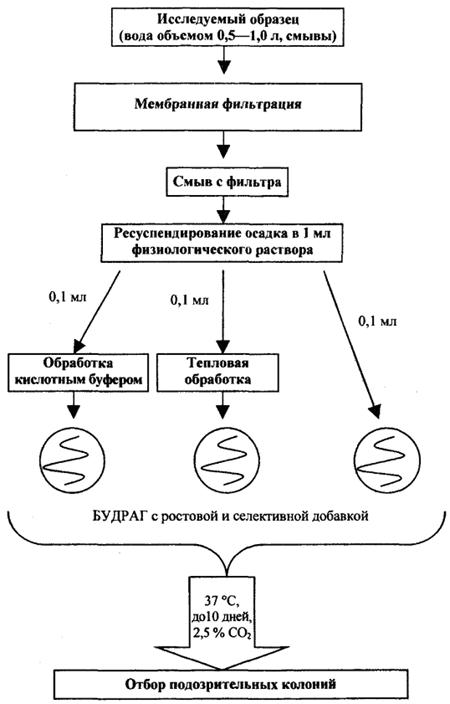
По 0,1 мл концентрированного, обработанного кислотным буфером и прогретого при 50 °С образца высевают на чашки со средой БУДРАГ с ростовой и селективной добавкой (рис. 1А). Образец распределяется по поверхности питательной среды шпателем или стеклянной палочкой. Чашки инкубируют при 37 °С до 10 дней во влажной атмосфере и в присутствии 2,5 % СO2.
Просмотр чашек начинают со 2-х суток, хотя из воды колонии легионелл могут вырастать на 5 - 7-е сутки и в более поздние сроки. В случае массивной контаминации проб посторонней микрофлорой, несмотря на кислотную и термическую обработку, не позволяющей проводить подсчет колоний, сконцентрированную пробу разводят в 100 раз и производят повторный высев.
Подозрительные на легионеллы колонии выявляют при стереомикроскопическом просмотре чашек или под лупой. На селективной среде колонии легионелл обычно имеют вросший центр, гранулярную или блестящую поверхность, серовато-голубоватую, иногда зеленоватую окраску. Колонии легионелл на 3 - 5-е сутки небольшие, диаметром 1 - 2 мм, плоско-выпуклые, гладкие с острым краем.
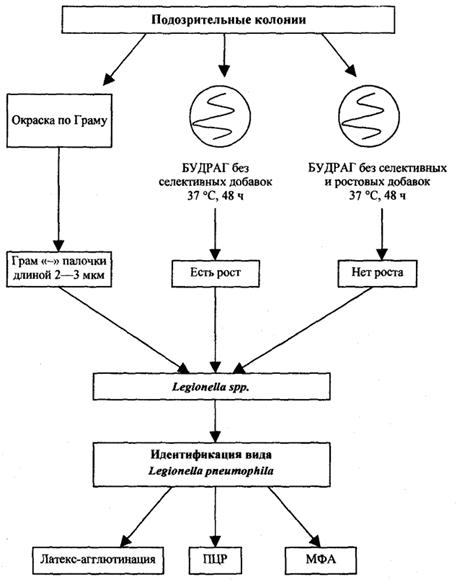
Для идентификации бактерий рода Legionella spp. используют окраску мазков по Граму и посев на среду БУДРАГ без селективной и ростовой добавок, на которой колонии легионелл не вырастают (рис. 1Б).
Для этого с каждой чашки отбирают 2 - 3 подозрительные колонии, которые отсевают параллельно на среду БУДРАГ без селективной добавки и на среду БУДРАГ без селективной и ростовой добавки (контрольная среда), инкубируют при 37 °С в течение 48 ч, а также приготавливают мазки для окраски по Граму (рис. 1Б).
В мазках легионеллы выглядят как небольшие грамотрицательные палочки длиной 2 - 3 мкм. В мазках с 4 - 5-дневных колоний длина легионелл может достигать 10 - 15 мкм.
Легионеллы растут на среде БУДРАГ без селективной добавки и не растут на контрольной среде.
Рис. 1А. Схема выделения Legionella spp. из объектов внешней среды: выделение культуры.
Рис. 1Б. Схема выделения Legionella spp. из объектов внешней среды: идентификация подозрительных колоний.
Идентифицированные подобным образом колонии относят к роду Legionella. Типичные для Legionella spp. колонии подсчитывают количественно для последующего определения количества легионелл в 1 л воды. Для биопленок, в которых возбудитель присутствует, как правило, в высоких концентрациях, проводят только качественную оценку обсемененности.
Идентификация Legionella pneumophila
Легионеллы не ферментируют углеводы, разжижают желатин, не образуют уреазу, не восстанавливают нитраты, положительны в пробе на каталазу, вариабельны в пробе на оксидазу (табл. 1). Отсутствие способности к ферментации углеводов у бактерий Legionella spp. не позволяет быстро и достоверно провести идентификацию легионелл до вида на основе биохимических тестов. Для быстрой идентификации бактерий Legionella pneumophila используют латекс-агглютинацию с моновалентными и групповыми сыворотками и метод флуоресцирующих антител (МФА). В случае необходимости принадлежность выделенной культуры к виду Legionella pneumophila определяют с помощью полимеразной цепной реакции с видоспецифичными праймерами.
Окончательную идентификацию легионелл до вида и серовара проводят в национальной референс-лаборатории по легионеллезу (ГУ НИИЭМ им. Н.Ф. Гамалеи РАМН, Москва).
Идентификация Legionella pneumophila в латекс-агглютинации
Для определения принадлежности выросших колоний к виду Legionella pneumophila используют реакцию латекс-агглютинации. Для постановки реакции каплю физиологического раствора вносят в каждую из трех лунок на стекле для агглютинации. С помощью бактериологической петли отбирают подозрительные колонии, выросшие на среде БУДРАГ с ростовой добавкой, и тщательно суспендируют их в лунках с физиологическим раствором 2 мин. Затем в одну лунку добавляют одну каплю латексного реагента Legionella 1, в другую - одну каплю латексного реагента Legionella 2 - 15, а в третью - одну каплю латексного реагента Legionella spp. В каждой лунке латексную суспензию тщательно перемешивают с помощью стеклянной палочки (для каждой лунки отдельная) и, осторожно покачивая стекло, наблюдают за появлением агглютинации в течение 2 мин. Размер агглютината и скорость его появления вариабельна и зависит от концентрации антигена легионелл в суспензии. Оценку полученных результатов реакции проводят в соответствии с табл. 2.
Основные фенотипические признаки Legionella spp.
|
L. pneumophila |
L. bozemanii |
L. dumoffii |
L. micdadei |
L.feeleii |
L. longbeachae |
|
|
Рост на BCYEa-агаре |
+ |
+ |
+ |
+ |
+ |
+ |
|
Рост на кровяном агаре или на BCYEa без L-цистеина |
- |
- |
- |
- |
- |
- |
|
Каталаза |
+ |
+ |
+ |
+ |
+ |
+ |
|
Восстановление нитратов |
- |
- |
- |
- |
- |
- |
|
Ферментация углеводов |
- |
- |
- |
- |
- |
- |
|
Гидролиз гиппурата натрия |
+ |
- |
- |
- |
- |
- |
|
Аутофлюоресценция |
- |
+ |
+ |
- |
- |
- |
|
Желатиназная активность |
+ |
+ |
+ |
- |
- |
+ |
|
Образование коричневого пигмента на среде, содержащей тирозин |
+ |
+ |
+ |
- |
+ |
+ |
|
Р-лактамазная активность |
+ |
В |
+ |
- |
В |
В |
|
Оксидаза |
В |
В |
- |
+ |
В |
+ |
Результаты: «+» - положительный; «-» - отрицательный; «В» - вариабельный.
Учет результатов латекс-агглютинации
|
Реакция с латексным реагентом L. pneumophila 1 |
Реакция с латексным реагентом L. pneumophila 2 - 15 |
Реакция с латексным реагентом Legionella spp. |
Учет результатов |
|
+ |
- |
+ |
выделена культура L. pneumophila сepoгруппы 1 |
|
- |
+ |
+ |
выделена культура L. pneumophila серогрупп 2 - 15 |
|
- |
- |
+ |
выделенная культура относится к Legionella spp., но не к виду L. pneumophila |
Контроль специфичности латексного реагента: в отдельные лунки вносят по одной капле каждого латексного реагента, затем добавляют по капле физиологического раствора и, осторожно покачивая стекло в течение 2 мин, наблюдают за появлением возможной агглютинации. В случае образования агглютината латексный реагент или физиологический раствор дают неспецифичную реакцию и должны быть заменены. В качестве положительного контроля используют культуру Legionella pneumophila или соответствующий антиген, в т.ч. коммерческого производства.
Идентификация легионелл с помощью МФА
На предметном стекле из капли исследуемого материала делают тонкий мазок, который подсушивают на воздухе при комнатной температуре и фиксируют в ацетоне в течение 15 мин. Препараты хранят при 4 °С до обработки люминесцирующей сывороткой. На поверхность фиксированного мазка наносят «рабочее разведение» легионеллезной люминесцирующей сыворотки. Препарат окрашивают 20 мин при 37 °С во влажной камере. Затем мазки промывают 10 - 15 мин в фосфатном буфере (рН 7,2), ополаскивают дистиллированной водой, высушивают на воздухе, наносят глицериновую или другую нефлуоресцирующую иммерсионную среду, покрывают покровным стеклом и просматривают в люминесцентном микроскопе при увеличении 90.
В положительном случае после обработки данного препарата специфической легионеллезной люминесцирующей сывороткой обнаруживается специфическое изумрудно-зеленое свечение легионеллезных бактерий.
Степень яркости люминесценции бактерий, окрашенных люминесцирующими антителами, принято обозначать в крестах. Специфическим считается свечение с яркостью 4+ и 3+, свечение с яркостью 2+ и 1+ принято считать неспецифическим. Обнаружение светящегося ореола хотя бы у 3 - 5 клеток в каждом поле зрения свидетельствует о наличии в исследуемом материале легионеллы.
Отрицательный результат говорит об отсутствии микроорганизма или о содержании в исследуемом материале в низкой концентрации, не выявляемой иммунофлуоресцентным методом при прямом исследовании без подращивания или обогащения. При исследовании препаратов необходимо иметь в качестве положительного контроля мазок, приготовленный из 500 млн взвеси легионеллезных бактерий, обработанных люминесцирующей сывороткой.
Идентификация легионелл с помощью ПЦР
Для идентификации полученных на среде БУДРАГ культур легионелл используют суспензию выделенной культуры в 0,1 мл физиологического раствора. Для постановки ПЦР используют 5 - 10 мкл обеззараженной кипячением бактериальной взвеси. Для постановки ПЦР используют сертифицированные ПЦР тест-системы, основанные на выявлении фрагментов генов, специфичных для бактерий рода Legionella и вида Legionella pneumophila. Амплификацию выполняют согласно прилагаемой к тест-системе инструкции на программируемых термоциклерах отечественного и зарубежного производства.
Определение количества легионелл в исследуемом материале
Для определения количества легионелл в исследуемой пробе берут чашку с посевом предварительного сконцентрированного материала (п. 7) без тепловой и кислотной обработки. Для расчета используют следующую формулу:
![]() где
где
Х - количество легионелл на 1 л в исследуемой пробе;
а - количество легионелл, выросших на чашке;
b - объем концентрата пробы (по завершении этапов фильтрации и центрифугирования), мл;
с - объем, высеянный на чашку, мл;
s - объем исходной пробы, л.
9. Проведение ПЦР-анализа
Достоинствами полимеразной цепной реакции (ПЦР) являются высокие чувствительность и специфичность, а также быстрота получения результатов, возможность выявления низких концентраций возбудителя в исследуемом материале.
Проведение ПЦР осуществляют в соответствии с МУ 1.3.1888-04 «Организация работы при исследованиях методом ПЦР материала, инфицированного патогенными биологическими агентами III - IV групп патогенности».
Исследование проб методом ПЦР с учетом результатов исследования методом электрофореза в агарозном геле
Метод используют для ускоренного качественного выявления легионелл в нативном материале. Для анализа используют 0,1 мл предварительно сконцентрированного образца из объектов внешней среды (п. 7).
Обеззараживание исследуемого материала осуществляют в соответствии с МУ 3.5.5.1034-01 «Обеззараживание исследуемого материала, инфицированного бактериями I - IV групп патогенности, при работе методом ПЦР». Для этого сконцентрированную пробу из объектов внешней среды переносят в микроцентрифужную пробирку объемом 1,5 мл и добавляют 300 мкл буфера, содержащего 6М гуанидинтиоцианата, инкубируют при 65 °С в течение 10 мин. После такой обработки пробы считаются обеззараженными.
Выделение ДНК. Из подготовленных таким образом проб из объектов внешней среды проводят выделение ДНК, используют сертифицированные наборы, в основе которых лежит метод сорбции ДНК на силикагеле в присутствии гуанидинтиоцианата. Работу осуществляют в соответствии с инструкцией, прилагаемой к набору.
Постановка ПЦР. Для постановки ПЦР используют сертифицированные ПЦР-тест-системы, основанные на выявлении фрагментов генов, специфичных для бактерий рода Legionella spp. и вида L. pneumophila. Работу выполняют согласно прилагаемой к тест-системе инструкции. Амплификацию проводят на программируемых термоциклерах отечественного или зарубежного производства.
Учет результатов. Для учета результатов ПЦР используют электрофорез в агарозном геле. Условия проведения электрофореза, визуализации результатов, учет и анализ полученных данных отражены в инструкциях к ПЦР-тест-системам. Качественное исследование методом ПЦР на наличие Legionella pneumophila может быть использовано для предварительного ориентировочного скрининга проб воды, т. к. широкое распространение некультивируемых форм легионелл, не представляющих опасности для человека, в естественных и искусственных водных системах не позволяет в данном случае оценить уровень контаминации легионеллами объектов окружающей среды (п. 3).
Исследование проб с помощью гибридизационно-флуоресцентного метода в режиме реального времени
Метод используют для ускоренного количественного выявления легионелл в нативном материале. Гибридизационно-флуоресцентный метод позволяет сократить время анализа проб по сравнению с бактериологическим методом с 7 - 10 до 1 - 2 суток.
Для выделения ДНК используют образцы воды или суспензию биопленки в объеме 0,1 - 1,0 л. Для фильтрации используют поликарбонатные фильтры с размером пор 0,4 мкм. Фильтрацию образца осуществляют в соответствии с п. 7. Последующее выделение ДНК проводят с помощью набора для выделения ДНК из водных образцов в соответствии с инструкцией, прилагаемой к набору. Для дальнейшего анализа используют наборы для количественного определения ДНК Legionella spp. и Legionella pneumophila. Анализ выделенной ДНК проводят в амплификаторе отечественного или зарубежного производства с учетом результатов в режиме реального времени в соответствии с инструкцией изготовителя.
При использовании диагностических препаратов с учетом результатов в режиме реального времени определяют количество ДНК легионелл в исследуемых пробах. Расчет количества ДНК легионелл в исследуемом образце проводят в соответствии с инструкцией по применению препарата. Окончательный результат в таком случае представляют в виде числа геномных копий на 1 л воды. При положительном ответе, свидетельствующем о наличии в пробе легионелл в количестве 1´103 геномных копий на 1 л и выше, необходимо его подтверждение выделением культуры возбудителя бактериологическим методом в соответствии с п. 8.
10. Оформление и выдача результатов
Ответ о выявлении в исследуемой пробе легионелл представляют следующим образом.
• Если легионеллы не выявлены в исследуемой пробе: Legionella pneumophila не обнаружена.
• При выявлении Legionella spp.: в исследуемой пробе выявлены Legionella spp.; Legionella pneumophila не обнаружена.
• При выявлении Legionella pneumophila: в исследуемой пробе выявлена Legionella pneumophila в установленном количестве бактерий (геномных копий) на 1 л.
• При исследовании пробы биопленки: в исследуемой пробе выявлена Legionella spp. или Legionella pneumophila.
11. Требования безопасности
Исследования объектов окружающей среды на наличие Legionella pneumophila проводят в соответствии с СП 1.2.731-99 «Безопасность работы с микроорганизмами III - IV групп патогенности и гельминтов». Постановку ПЦР проводят в соответствии с МУ 1.3.1888-04 «Организация работы при исследованиях методом ПЦР материала, инфицированного патогенными биологическими агентами III - IV групп патогенности».
Приложение
(справочное)
Рекомендуемые значения для оценки уровня контаминации Legionella pneumophila различных объектов окружающей среды
Легионеллы являются естественными обитателями пресноводных водоемов. Присутствие Legionella pneumophila в воде различных объектов окружающей среды, воде бассейнов, аквапарков, джакузи, систем кондиционирования воздуха и других в концентрации менее 1´102 м.к. на 1 л является допустимым и не требует проведения профилактических мероприятий. При обнаружении легионелл в концентрации в диапазоне от 1´102 до 9´103 м.к. на 1 л делается вывод о колонизации данного объекта легионеллами в концентрации, не представляющей эпидемической опасности, но требующей регулярного ежемесячного микробиологического контроля и проведения профилактических мероприятий. При обнаружении легионелл в концентрации 1´104 м.к. на 1 л и выше делается вывод о колонизации данного объекта легионеллами в концентрации, представляющей эпидемическую опасность и требующей дезинфекционных и профилактических мероприятий.