| Обозначение: |   ГОСТ ISO/TS 21726-2021 ГОСТ ISO/TS 21726-2021 |
| Статус: | действует |
| Название рус.: | Изделия медицинские. Система оценки биологического действия. Руководство по применению порога токсической опасности для оценки биосовместимости компонентов медицинских изделий |
| Название англ.: | Medical devices. Evaluation system of biological effects. Application of the threshold of toxicological concern for assessing biocompatibility of medical device constituents |
| Дата актуализации текста: | 01.06.2022 |
| Дата актуализации описания: | 01.07.2023 |
| Дата регистрации: | 26.08.2021 |
| Дата издания: | 10.12.2021 |
| Дата введения: | 01.03.2022 |
| Аутентичен стандартам: | ISO/TS 21726:2019 |
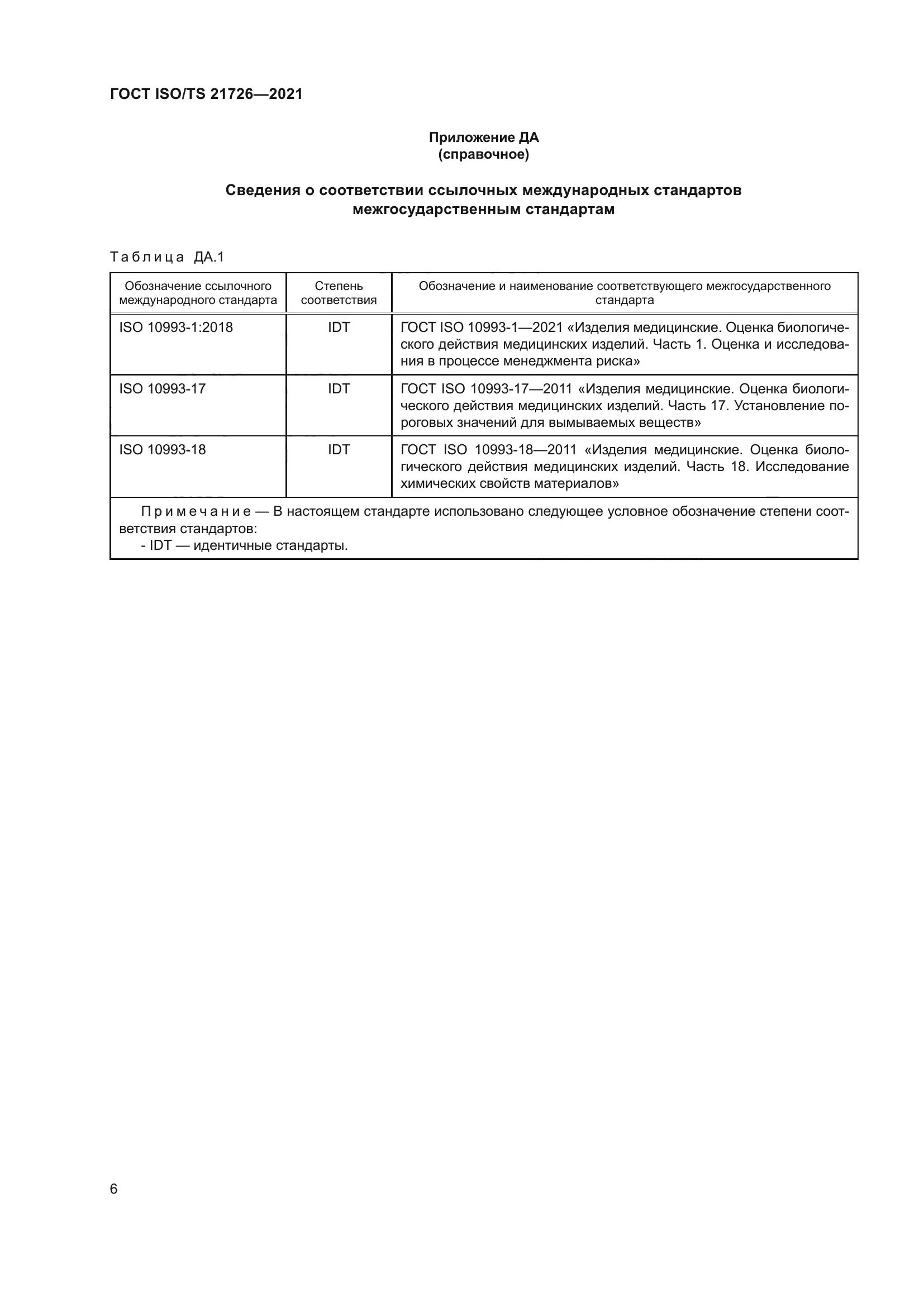
| Нормативные ссылки: | ISO 10993-1:2018;ISO 10993-17;ISO 10993-18 |
| Область применения: | Настоящий стандарт представляет собой руководство по обоснованию, выбору и применению порога токсической опасности (ПТО) для оценки биосовместимости компонентов, присутствующих в медицинском изделии (МИ) или высвобождаемых из МИ. Значения ПТО, установленные в настоящем стандарте, допускается применять для: - сравнения с допустимой максимальной концентрацией идентифицированного или неидентифицированного компонента в экстракте (см. ISO 10993-18); - подтверждения токсикологической безопасности; - сравнения максимальной дозы воздействия идентифицированного компонента при оценке биологического действия МИ (см. ISO 10993-17) |
| Приложение №1: | Поправка к ГОСТ ISO/TS 21726-2021 |
|
| Расположен в: |
|

 ГОСТ ISO/TS 21726-2021
ГОСТ ISO/TS 21726-2021
 ГОСТ ISO/TS 21726-2021
ГОСТ ISO/TS 21726-2021