ГОСТ Р 58162-2018
ГОСТ Р 58162-2018
Упаковка для медицинских изделий, подлежащих финишной стерилизации. Руководство по применению ИСО 11607-1 и ИСО 11607-2
| Обозначение: |  ГОСТ Р 58162-2018 ГОСТ Р 58162-2018 |
| Обозначение англ: |  GOST R 58162-2018 GOST R 58162-2018 |
| Статус: | введен впервые |
| Название рус.: | Упаковка для медицинских изделий, подлежащих финишной стерилизации. Руководство по применению ИСО 11607-1 и ИСО 11607-2 |
| Название англ.: | Packaging for terminally sterilized medical devices. Guidance on the application of ISO 11607-1 and ISO 11607-2 |
| Дата добавления в базу: | 01.01.2019 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.01.2019 |
| Область применения: | Данные технические условия представляют руководство по применению требований стандартов ИСО 11607-1 и ИСО 11607-2. Данный документ не дополняет и не изменяет каким-либо иным образом требования стандартов ИСО 11607-1 и/или ИСО 11607-2. Этот документ является справочным, а не нормативным. Он не включает требования, которые необходимо брать за основу при осуществлении контроля регулирующим органом или при аттестационной оценке. Это руководство можно использовать для лучшего понимания требований ИСО 11607-1 и/или ИСО 11607-2, оно также иллюстрирует ряд методов и подходов, использующихся для удовлетворения требований этих стандартов. При этом данный документ не требуется использовать для демонстрации соответствия стандартам ИСО 11607-1 и ИСО 11607-2. Руководящие указания даются для оценивания, выбора и использования упаковочных материалов, предварительно сформированных барьерных систем для стерилизации, барьерных системам для стерилизации и упаковочных систем. |
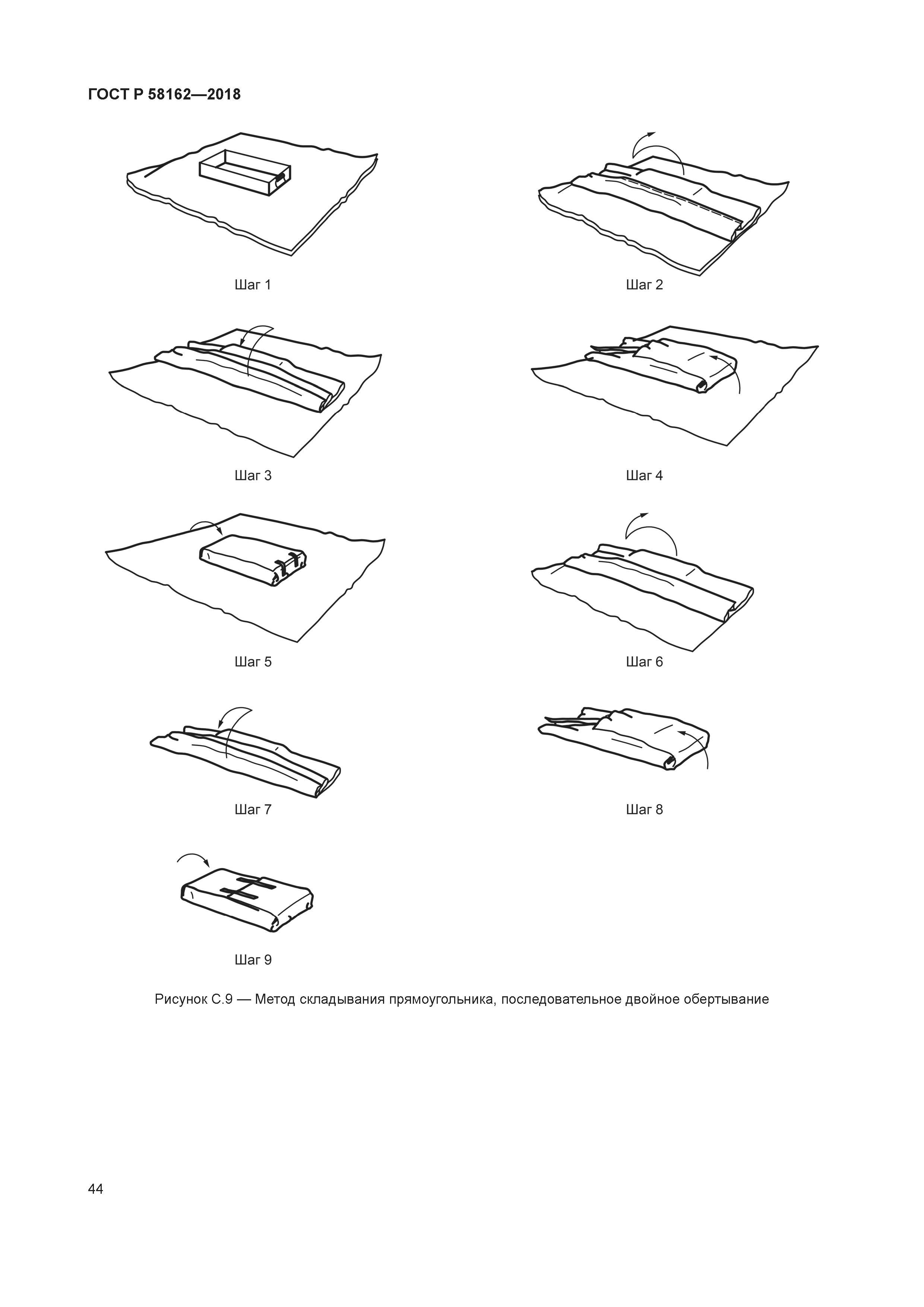
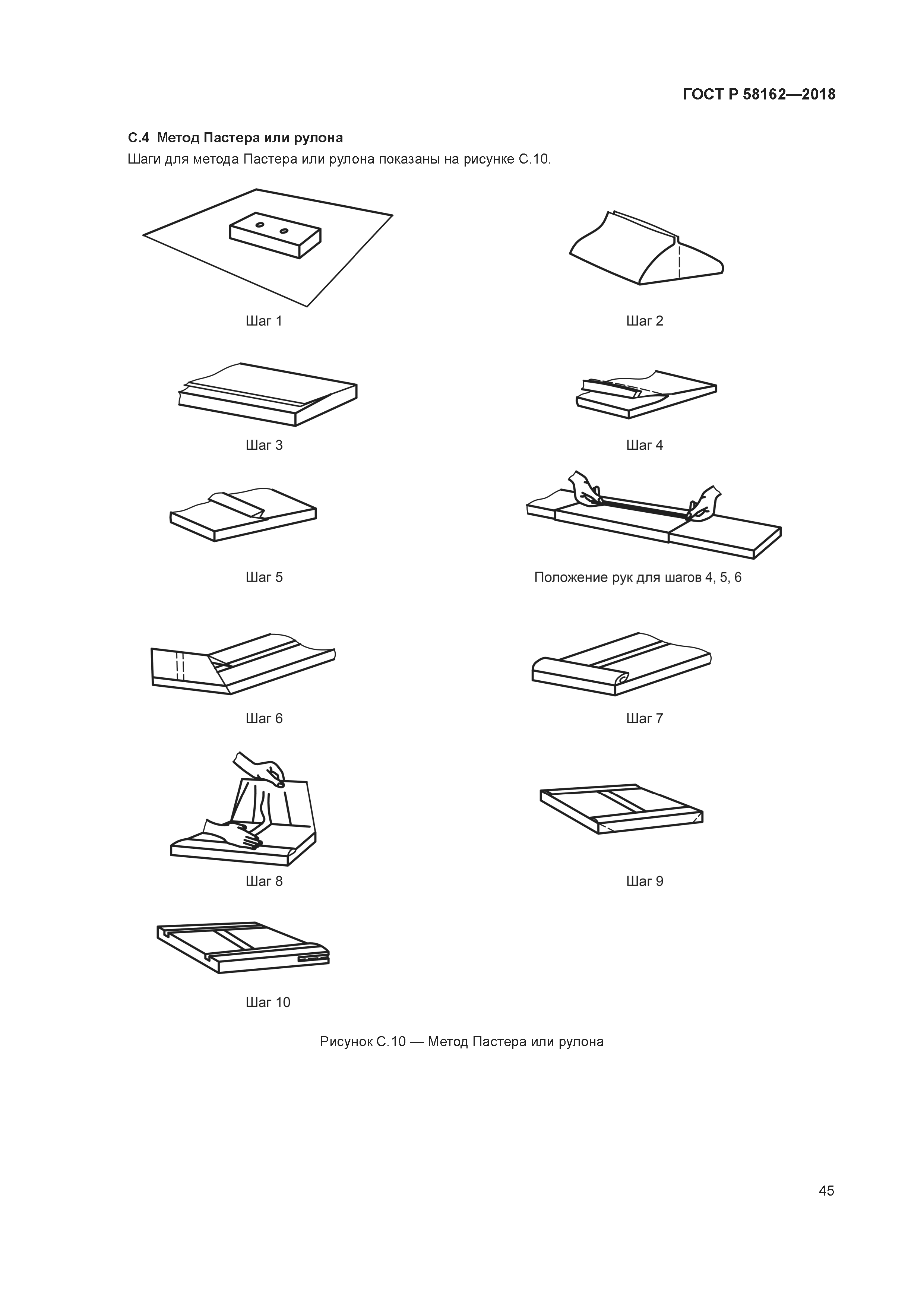
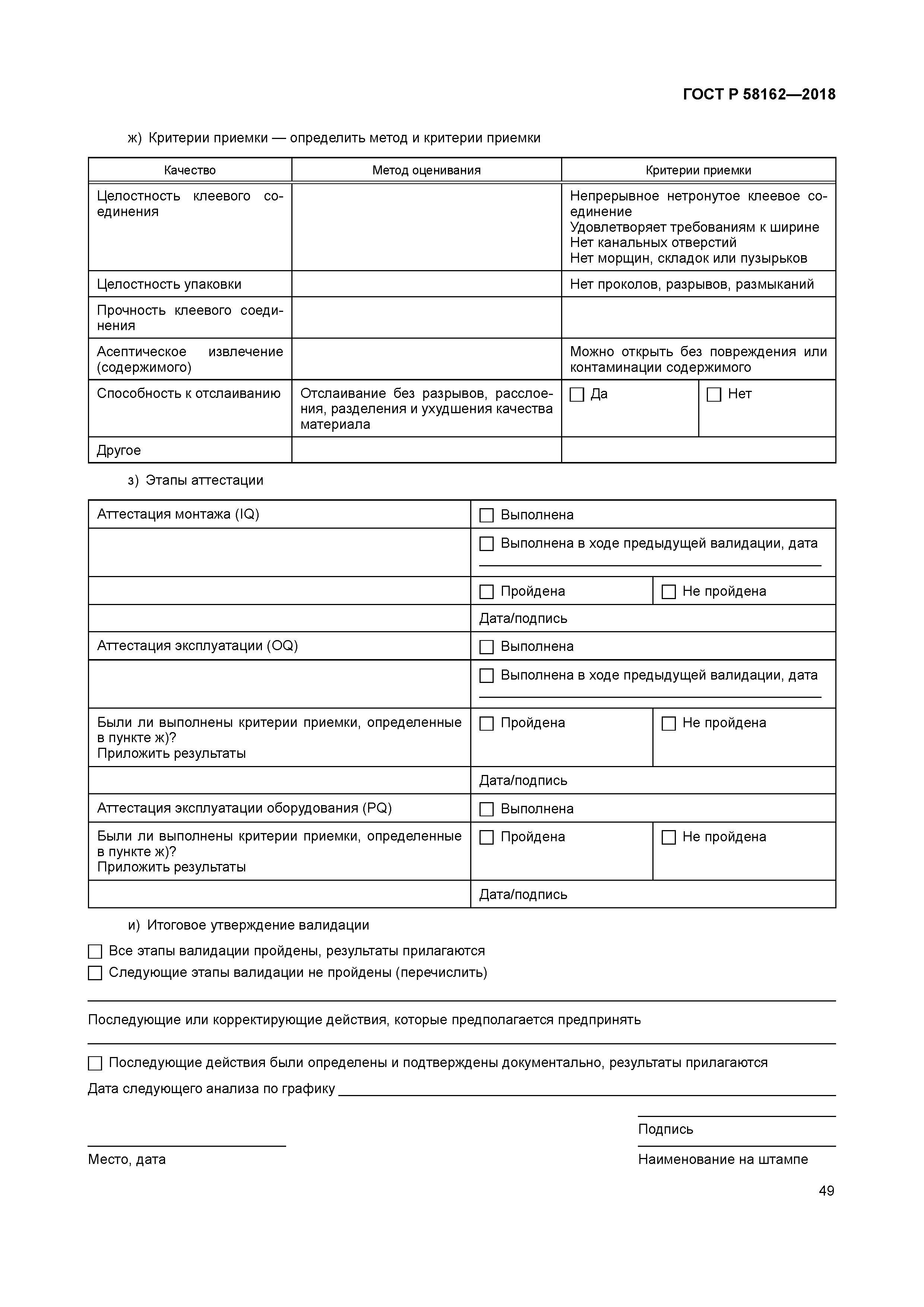
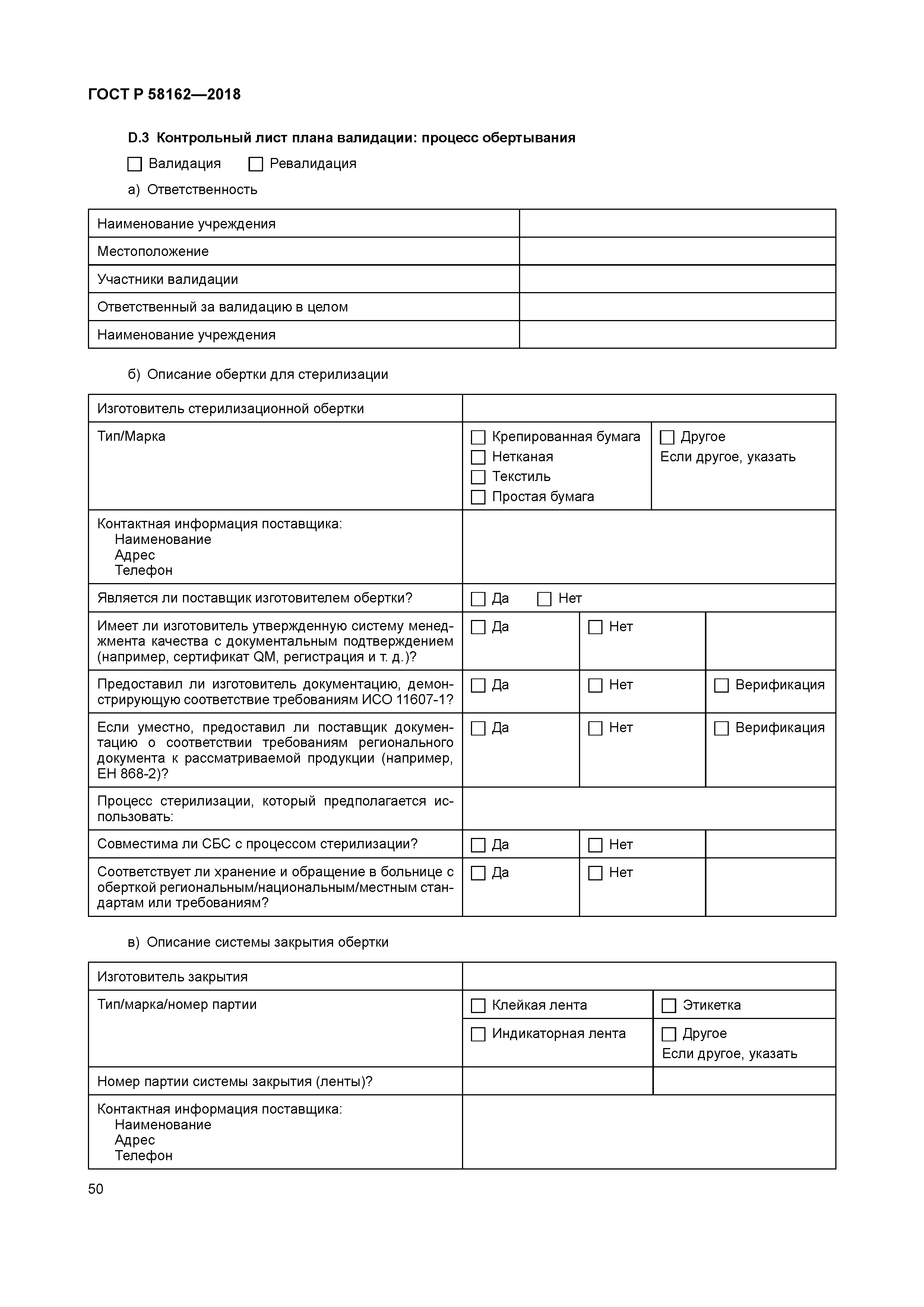
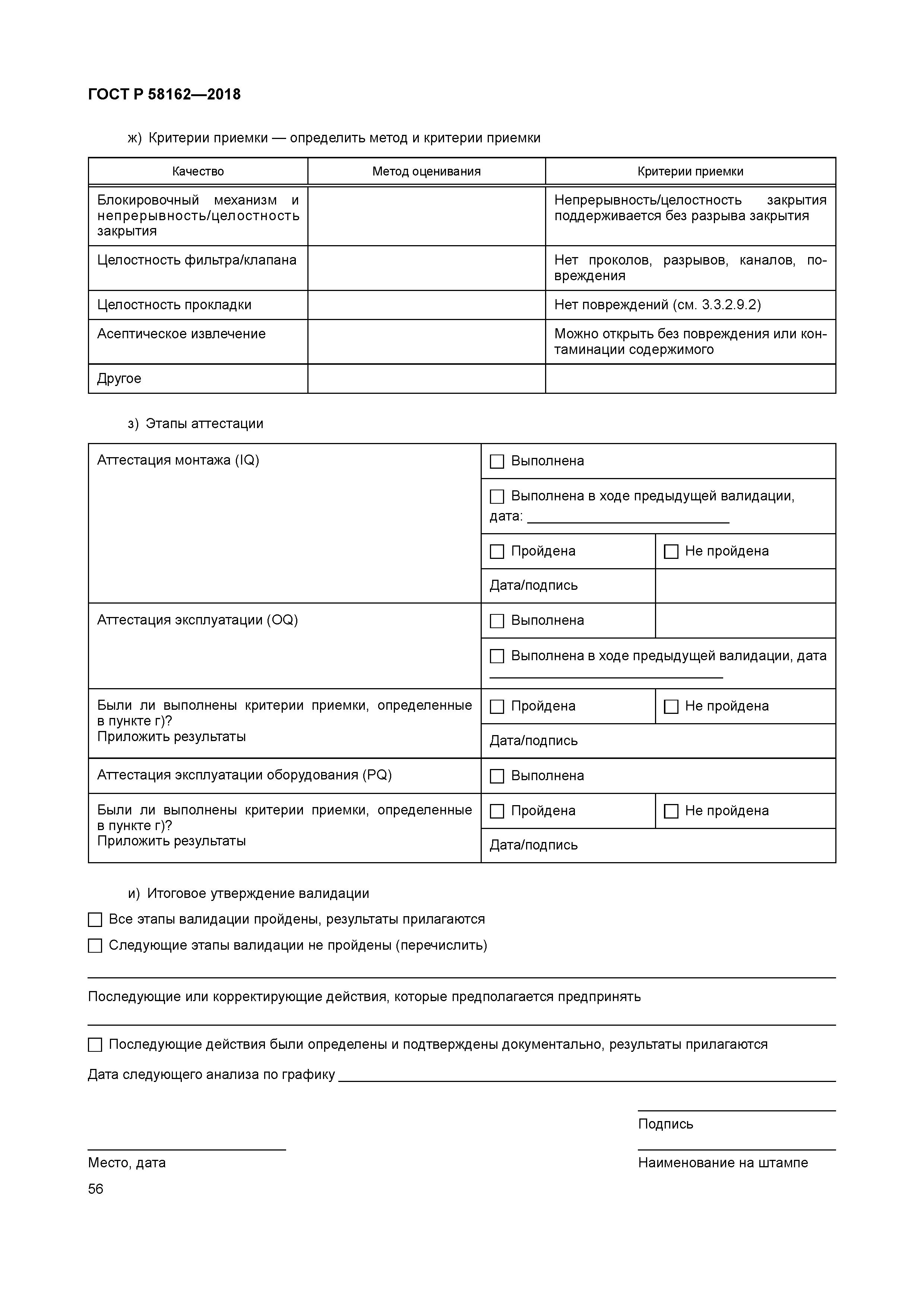
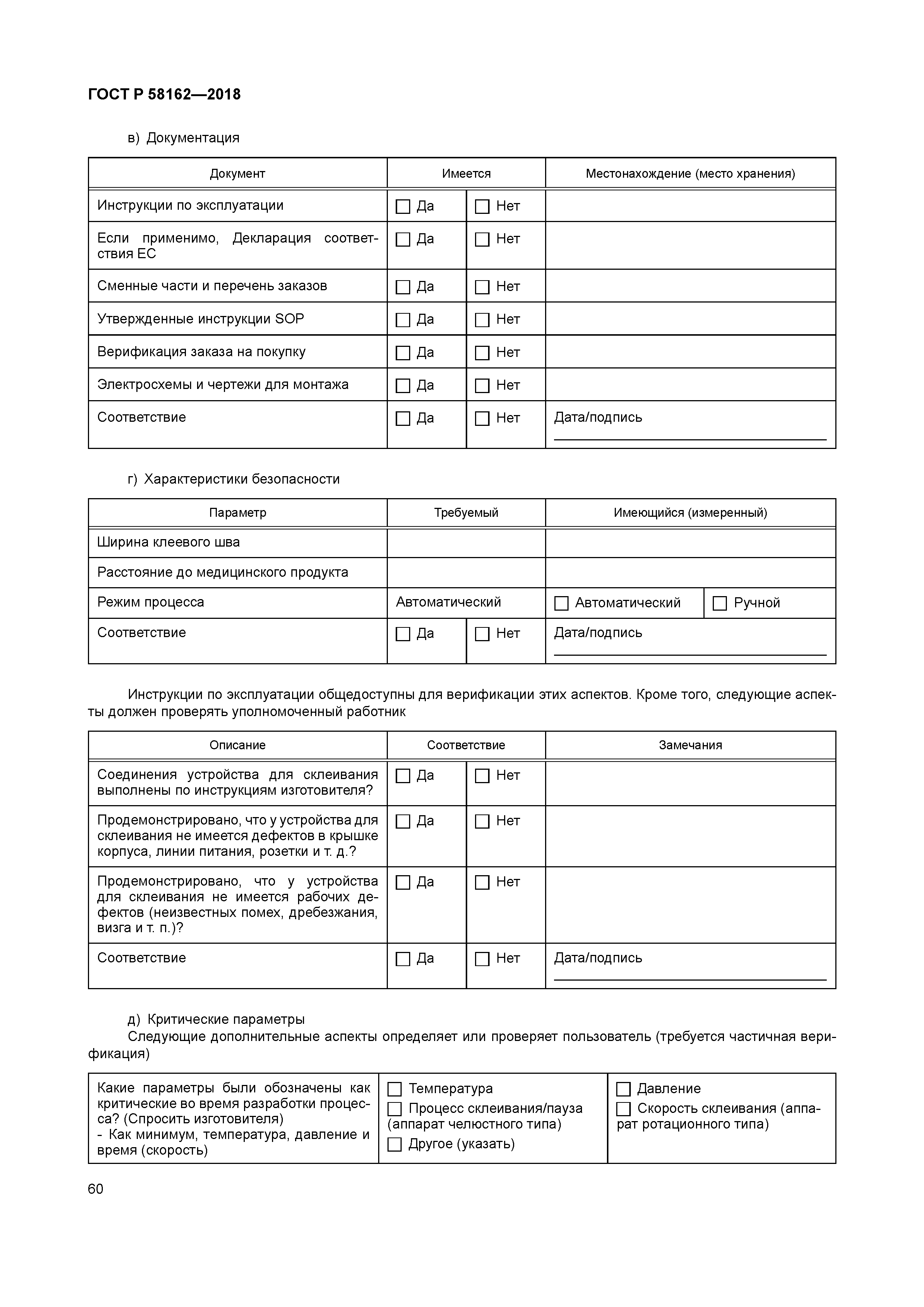
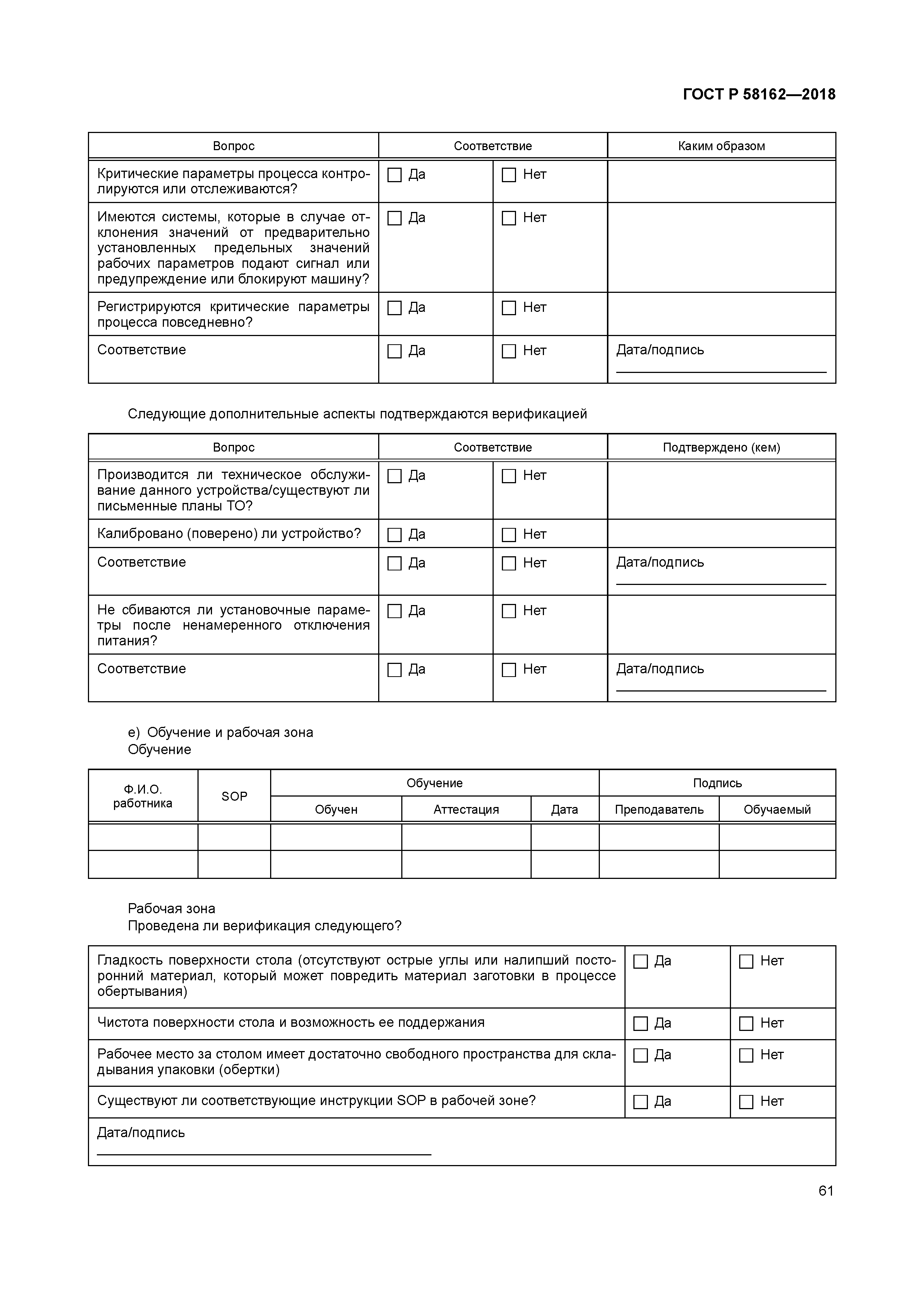
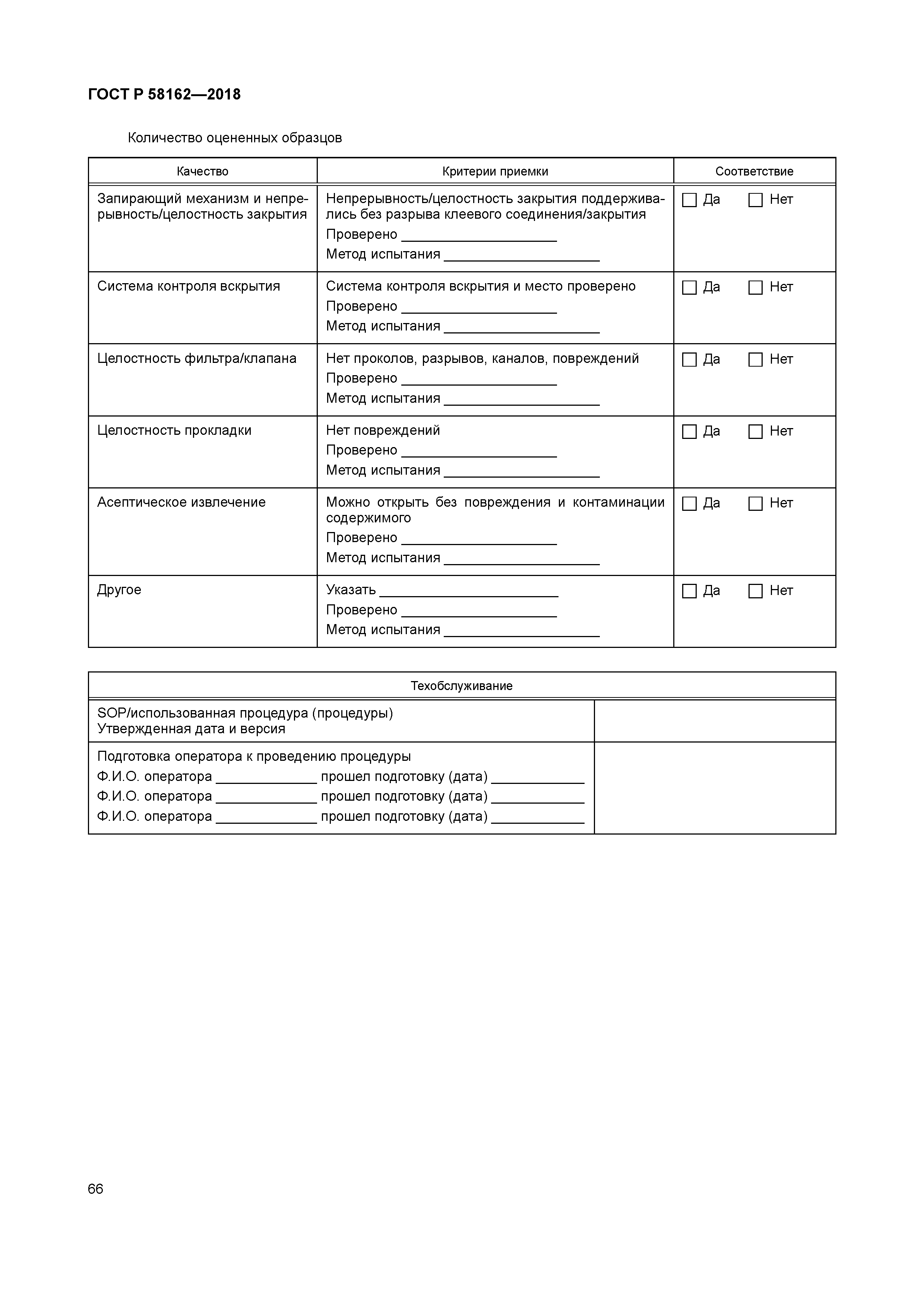
| Оглавление: | 1 Область применения 2 Термины и определения 3 Руководство для объектов здравоохранения 3.1 Методы испытания 3.2 Руководство по соответствию требованиям ИСО 11607-1 3.3 Руководство по соответствию ИСО 11607-2. Требования валидации процессов формирования, склеивания и сборки 3.4 Система качества 4 Руководство для промышленности 4.1 Общее руководство 4.2 Проектные задания 4.3 Выбор и оценивание материалов 4.4 Проектирование барьерной системы для стерилизации и защитной упаковки (разработка упаковочной системы) 4.5 Оценка реализуемости процесса упаковывания 4.6 Оценка реализуемости проектирования барьерной системы для стерилизации 4.7 Валидация процесса производства барьерной системы для стерилизации 4.8 Валидация конструкции упаковочной системы 4.9 Повторная валидация (ревалидация) Приложение A (справочное) Выбор, оценка и испытания упаковочных материалов и барьерных систем для стерилизации. Руководство для промышленных и медицинских учреждений Приложение B (справочное) Вопросы стерилизации. Руководство для производства и медицинских учреждений Приложение C (справочное) Примеры способов обертывания. Руководство для медицинских учреждений Приложение D (справочное) Документация планов валидации. Руководство для медицинских учреждений Приложение E (справочное) Документация по аттестации монтажа. Руководство для медицинских учреждений Приложение F (справочное) Документация аттестации эксплуатации. Руководство для медицинских учреждений Приложение G (справочное) Документация аттестации эксплуатируемого оборудования. Руководство для медицинских учреждений Приложение H (справочное) Требования к использованию условий наиболее худшего случая. Руководство для промышленных и медицинских учреждений Приложение I (справочное) Составление протокола валидации конечной упаковочной системы. Руководство для промышленных предприятий Приложение J (справочное) Вводные данные проектирования. Качественные характеристики медицинских изделий. Руководство для промышленных предприятий Приложение K (справочное) Механизмы анализа риска. Руководство для промышленных предприятий и медицинских учреждений Приложение L (справочное) Обсуждение планов выборочного контроля. Руководство для медицинских учреждений Приложение M (справочное) Испытание на стабильность (ИСО 11607-1:2006, пункт 6.4). Руководство для промышленных предприятий Приложение N (справочное) Использование Интернета. Руководство для промышленных предприятий и медицинских учреждений Приложение O (справочное) Валидация метода испытания. Руководство для промышленных предприятий Приложение P (справочное) Использование подрядчиков для упаковывания. Руководство для промышленных предприятий и медицинских учреждений Приложение Q (справочное) Руководство по установлению параметров процесса. Руководство для промышленных предприятий Приложение R (справочное) Расследование (причин) отказа. Руководство для промышленных предприятий и медицинских учреждений Приложение S (справочное) Процесс изготовления упаковки и проектирование упаковочной системы. Оценка осуществимости. Руководство для промышленных предприятий Библиография |
| Разработан: | ООО ФАРМСТЕР |
| Утверждён: | 05.07.2018 Федеральное агентство по техническому регулированию и метрологии (383-ст) |
| Издан: | Стандартинформ (2018 г. ) |
| Расположен в: |