Государственное
санитарно-эпидемиологическое нормирование
Российской Федерации
Федеральная
служба по надзору в сфере защиты прав потребителей
и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение химических соединений и
элементов в биологических средах, молочной
продукции и объектах окружающей среды
Сборник методических указаний
МУК
4.1.3474 - 4.1.3482-17
Выпуск 2
Москва 2018
1. Подготовлены коллективом авторов ФГБНУ «Восточно-Сибирский институт медико-экологических исследований», Федеральным бюджетным учреждением науки ФНЦ «Федеральный научный центр медико-профилактических технологий управления рисками здоровью населения», ФБУН «Нижегородский НИИ гигиены и профпатологии» Роспотребнадзора, ФБУЗ «Федеральный центр гигиены и эпидемиологии» Роспотребнадзора.
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 22 декабря 2016 г. № 2).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 15 июня 2017 г.
4. Введены впервые.
СОДЕРЖАНИЕ
Введение
Включенные в сборник 9 методических указаний по определению химических соединений в биологических средах, объектах окружающей среды и молочной продукции предназначены для использования в химико-аналитических исследованиях при проведении биомониторинга состояния здоровья населения, для практического использования в рамках социально-гигиенического мониторинга на территориях с высокой антропогенной нагрузкой, а также могут быть использованы для диагностических целей в рамках осуществления государственного санитарного надзора, контроля, экспертизы, расследований. Методические указания предназначены для специалистов химико-аналитических лабораторий системы Роспотребнадзора, научно-исследовательских институтов, работающих в области экологии человека, гигиены окружающей среды и защиты прав потребителей.
Методические указания, включенные в сборник, разработаны и подготовлены в соответствии с требованиями ГОСТ Р 8.563-96 «Государственная система обеспечения единства измерений. Методики выполнения измерений», ГОСТ Р 1.5-92 «ГСС. Общие требования к построению, изложению, оформлению и содержанию стандартов», МИ 2335-95 «Внутренний контроль качества результатов количественного химического анализа», МИ 2336-95 «Характеристики погрешности результатов количественного химического анализа. Алгоритм оценивания».
Все методики измерения прошли метрологическую аттестацию в соответствии с правилами ПР 50.2.002-94 «ГСИ. Порядок осуществления государственного метрологического надзора за выпуском, состоянием и применением средств измерений, аттестованными методиками выполнения измерений, эталонами и соблюдением метрологических правил и норм».
В методических указаниях, включенных в сборник, приведены методы определения 6 органических соединений в биологических средах (моча, кровь) и молочной продукции, 4 тяжелых металлов в молочной продукции и 20 тяжелых металлов и элементов в атмосферном воздухе. Определение токсичных веществ и элементов основано на использовании современных высокочувствительных методов физико-химического анализа - капиллярной газожидкостной хроматографии, хромато-масс-спектрометрии, масс-спектрометрии с индуктивно связанной плазмой, высокоэффективной жидкостной хроматографии, потенциометрии с применением ионселективного электрода.
Методические указания рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека.
|
УТВЕРЖДАЮ Руководитель Федеральной службы _______________________ А.Ю. Попова 15 июня 2017 г. |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение массовой
концентрации витамина К1
в сыворотке крови методом высокоэффективной
жидкостной хроматографии (ВЭЖХ)
Методические указания
МУК 4.0482-17
Свидетельство о метрологической аттестации № РОСС RU.0001. 310430/0200.10.07.14 от 10.07.2014.
Настоящие методические указания устанавливают порядок применения метода высокоэффективной жидкостной хроматографии для измерения массовой концентрации витамина К1 в сыворотке крови в диапазоне 2,5 - 44,0 нг/см3.
Методические указания носят рекомендательный характер.
Витамин К1 - витамин коагуляции, антигеморрагаческий витамин, 2-метил-3-фитил-1,4-нафтохинон.
Структурная формула:
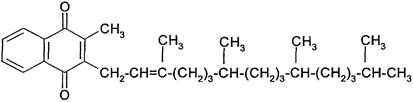
Эмпирическая формула: С31Н46O2
Молекулярная масса: 450,7.
Регистрационный номер СAS: 84-80-0.
Физико-химические свойства. Светло-желтое маслянистое вещество, липофильно (жирорастворимо), гидрофобно, растворимо в хлороформе, диэтиловом эфире, этиловом спирте и других органических растворителях. Тпл = -20 °С, Ткип = 115 - 145 °С (в вакууме). Растворы поглощают УФ-лучи.
Метаболическая роль витамина К. Витамин К необходим, прежде всего, для механизмов свертывания и регуляции крови. Также витамин К играет важную роль в формировании и восстановлении костей, обеспечивает синтез белка костной ткани (остеокальцина), на котором кристаллизуется кальций. Он способствует предупреждению остеопороза, участвует в регуляции окислительно-восстановительных процессов в организме. Дефицит витамина К в организме приводит к развитию геморрагического синдрома, который проявляется внутрикожными и подкожными кровоизлияниями, кровоточивостью десен, носовыми и желудочно-кишечными кровотечениями.
Витамин К представлен в природе двумя формами: растительным филлохиноном (К1) и менахиноном (К2), синтезируемым бактериями и образующимся из формы К1. Биомаркерами витамина К являются концентрация филлохинона (витамина К1) в плазме крови и процент некарбоксилированного остеокальцина в плазме крови.
Физиологическая функция витамина К заключается в образовании дополнительных карбоксильных групп в протромбине, проконвертине и других белковых факторов, которые вместе с ионами кальция инициируют процесс образования тромбина. Ферментативное действие тромбина на первом этапе способствует превращению растворимого в плазме белка фибриногена в мономерную форму белка фибрина, на следующем этапе образованию регулярной структуры растворимого фибрин-полимера. Образованный рыхлый сгусток под воздействием фибринстабилизирующего фактора свертывания крови, тромбина и ионов кальция превращается в нерастворимый фибрин, стабилизирующий структуру сгустка, необходимого для прекращения кровотечения.
Нормальный уровень содержания витамина К1 в сыворотке крови составляет 5,0 - 30,0 нг/см3.
Содержание в продуктах питания. Витамин К1 содержится в большом перечне пищевых источников растительной природы, включая зеленые овощи (брокколи, шпинат, капуста белокочанная, фасоль и др.), в которых он находиться в комплексе с хлорофиллом, и некоторые растительные масла (соевое, хлопковое, оливковое, рапсовое). Гидрогенизация масел приводит к снижению биодоступности и биоэффективности витамина. В молоке, яйцах, рыбе, мясе и зерновых продуктах его содержание не превышает 7 мкг в 100 г съедобной части. Кулинарные потери при тепловой обработке продуктов незначительны.
Нормы потребления. Установленный уровень потребления витамина К в разных странах варьируется от 55 до 120 мкг/сутки, а физиологическая потребность для взрослых - 120 мкг/сутки, для детей - от 30 до 75 мкг/сутки.
1. Погрешность измерений
1.1. Нормы погрешности измерений
Нормы погрешности измерений массовой концентрации витамина К1 в сыворотке крови в нормативной документации не регламентированы.
1.2. Приписанные характеристики погрешности
измерений и
ее составляющих
При соблюдении всех регламентируемых условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерения при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1 для соответствующего диапазона массовых концентраций витамина К1 в сыворотке крови.
Приписанные характеристики погрешности МВИ и
ее составляющих при доверительной вероятности 0,95
|
Диапазон определяемых концентраций, нг/см3 |
Показатель точности (границы относительной погрешности, p = 0,95), ±δ, % |
Показатель повторяемости (среднеквадратичное отклонение повторяемости), σr, нг/см3 |
Показатель воспроизводимости (среднеквадратичное отклонение воспроизводимости), σR, нг/см3 |
Предел повторяемости (значение допустимого расхождения между двумя результатами параллельных определений), r, нг/см3 |
Предел воспроизводимости (значение допустимого расхождения между двумя результатами измерений, полученных в одной лаборатории), R, нг/см3 (p = 0,95) |
Средняя степень извлечения, % |
|
От 2,5 до 44,0 вкл. |
19 |
0,018· |
0,036· |
0,051· |
0,101· |
81,69 |
Значения показателя точности используют:
- при оформлении результатов измерений, выдаваемых лабораторией;
- при оценке деятельности лабораторий по вопросу качества проведения измерений;
- при оценке возможности использования результатов измерений при реализации методики измерений в конкретной лаборатории.
2. Метод измерений
Выполнение измерений массовой концентрации витамина К1 в сыворотке крови проводят методом высокоэффективной жидкостной хроматографии с использованием спектрофотометрического детектора и предварительным проведением экстракции витамина из сыворотки гексаном, высушивания гексанового экстракта, растворения высушенного остатка в элюенте. Идентификация витамина осуществляется по времени удерживания. Количественное определение витамина К1 проводится методом абсолютной градуировки.
Измерению не мешают другие компоненты матрицы сыворотки, в частности, витамины А и Е.
3. Средства измерений, вспомогательные устройства, материалы и реактивы
При выполнении измерений применяют следующие средства измерений, вспомогательные устройства, материалы и реактивы.
3.1. Средства измерений
|
Хроматограф жидкостный: ОСКО выходных сигналов не более 3 %; относительное отклонение выходного сигнала от первоначального значения через 8 часов работы не более 6 %; время выхода на режим не более 1 часа |
|
|
Спектрофотометрический детектор: диапазон длин волн 190 - 600 нм; точность установки ±1 нм; воспроизводимость ±0,5 нм; источник света - дейгеривая лампа |
|
|
Насос для ВЭЖХ изократический; диапазон производительности 0,01 - 10 см3/мин, максимальное рабочее давление 40 МПа, точность поддерживаемой скорости подачи растворителя 1 см3/мин ±1 % |
|
|
Аналитический инжекторный клапан: максимальное операционное давление - 35 МПа; управление - ручное; инжекторная петля объемом 100 мм3; материал - нержавеющая сталь; игла 22/51/3 |
|
|
Весы лабораторные электронные специального класса точности: дискретностью не более 0,1 мг; наименьший предел взвешивания - 0,01 г; наибольший предел взвешивания - 200 г |
|
|
Одноканальные дозаторы пипеточные переменного объема 5 - 50, 20 - 200, 500 - 5000 мм3 |
ТУ 9452-002-33189998-06 ТУ 9446-005-33189998-07 ТУ 9443-008-33189998-09 |
|
Цилиндры 3-50-1, 3-100-1,3-250-1 |
|
|
Пробирки со шлифом П-2-5-0,1; П-1-10-0,1 |
|
|
Колбы мерные, 2-10-2, 2-25-2, 2-500-2 |
|
|
Микропробирки полиэтиленовые конические с колпачком типа Эппендорф, объем 1,5 см3 |
|
Примечание. Допускается использование средств измерений с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Вода дистиллированная |
|
|
Метанол, осч, для хроматографии |
ТУ 6-09-2192-85 |
|
Ацетонитрил, осч, доя жидкостной хроматографии |
ТУ 6-09-14-2167-84 |
|
Метилен хлористый, осч |
ТУ 6-09-14-2149-83 |
|
Гексан, хч, для хроматографии |
ТУ 6-00-4521 |
|
Спирт этиловый ректификованный |
|
|
Витамин К1 (количественное содержание, включая Z и Е изомеры, - 97,69 %) |
|
|
Подвижная фаза (элюент) доя хроматографии - метанол:ацетонитрил:хлористый метилен (45:50:5 об.%) |
|
Примечание. Допускается использование других реактивов с аналогичной, или более высокой квалификацией, не требующих дополнительной очистки растворителей.
3.3. Вспомогательные устройства, материалы
|
Аналитическая хроматографическая колонка из нержавеющей стали С18, 250×4,60 mm ×5 μм |
|
|
Картриджная защитная система С18 4×3,0 mm |
|
|
Вакуумный насос |
|
|
Колба Бунзена 1-1000-45 |
|
|
Воронка фильтрующая Шотта, пористость - S4, диаметр - 60 мм, высота - 191 мм |
|
|
Центрифуга лабораторная: |
|
|
Скорость центрифигурирования - от 100 до 3000 об./мин; максимальная центрифугальная сила - до 1900 g |
|
|
Перемешивающее устройство: регулируемая частота колебаний платформы 0 - 250 кол./мин; максимальное перемещение платформы - 25 мм; максимальная регулируемая температура нагрева платформы - 80 °С |
ТУ 64-1-1081-73 |
|
Встряхиватель: скорость вращения гнезда - 50 - 4000 об./мин; орбитальное вращение |
|
|
Шкаф сушильный: диапазон рабочих температур - от 50 до 320 °С; точность измерения температуры - ±0,5 °С |
|
|
Микрошприц объемом 500 мкл |
|
|
Азот газообразный |
Примечание. Допускается применение оборудования с аналогичными или лучшими техническими характеристиками.
4. Требования к безопасности
4.1. При выполнении измерений соблюдают требования безопасности, установленные для работы с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005-88 и по ГОСТ 12.1.007-76.
4.2. При работе с легковоспламеняющимися веществами необходимо соблюдать меры противопожарной безопасности по ГОСТ 12.1.004-91. Должны быть в наличии средства пожаротушения по ГОСТ 12.4.009-83.
4.3. При выполнении измерений на жидкостном хроматографе необходимо соблюдать правила электробезопасности в соответствии с ГОСТ Р 12.1.019-09 и инструкцией по эксплуатации прибора.
4.4. При работе со сжатыми газами необходимо соблюдать Федеральные нормы и правила в области промышленной безопасности «Правила промышленной безопасности опасных производственных объектов, на которых используется оборудование, работающее под избыточным давлением» (утв. Ростехнадзором приказом от 25.03.2014 № 116) и ГОСТ 12.2.085-02. Запрещается открывать вентиль баллона, не установив на нем понижающий редуктор.
4.5. Помещение лаборатории должно быть оборудовано приточно-вытяжной вентиляцией. Содержание вредных веществ в воздухе рабочей зоны не должно превышать ПДК (ОБУВ), установленных ГН 2.2.5.1313-03 (ГН 2.2.5.2308-07).
4.6. Необходимо провести обучение работающих безопасности труда согласно ГОСТ 12.0.004-90.
5. Требования к квалификации оператора
Измерения в соответствии с настоящей методикой может выполнять специалист, имеющий опыт работы на жидкостном хроматографе, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений.
6. Требования к условиям измерений
6.1. При выполнении измерений в лаборатории должны быть выполнены следующие условия:
- температура воздуха: (20 ± 5) °С;
- атмосферное давление: 84 - 106 кПа (630 - 800 мм рт. ст.);
- относительная влажность воздуха: не более 80 %.
6.2. Выполнение измерений на жидкостном хроматографе проводят при следующих условиях:
- напряжение питания: (220 ± 10) В;
- частота переменного тока: (50 ± 10) Гц.
6.3. Выполнение измерений на жидкостном хроматографе проводят в соответствии с руководством по эксплуатации используемого оборудования.
6.4. Для предотвращения разрушения витамина К1 анализ сыворотки и стандартов проводят, предохраняя пробы от попадания прямого солнечного света и воздействия повышенных температур. Анализ сыворотки крови необходимо проводить в течение 2 - 6 часов после забора крови.
7. Подготовка к выполнению измерений
При подготовке к выполнению измерений проводят следующие работы: подготовка хроматографических колонок, приготовление растворов, установление градуировочной характеристики, отбор и подготовку крови для анализа.
7.1. Подготовка хроматографических колонок
На хроматограф последовательно устанавливают предколонку, колонку.
Перед проведением измерения необходимо установить скорость подачи элюента 1 см3/мин до установления равновесия в колонке, которое определяется по стабильности нулевой линии детектора.
7.2. Приготовление растворов
Элюент для хроматографии - метанол:ацетонитрил:хлористый метилен (45:50:5). В мерную колбу вместимостью 500 см3 помещают 250 см3 ацетонитрила, 25 см3 хлористого метилена и доводят объем смеси до метки метанолом. Раствор тщательно перемешивают, дегазируют фильтрованием через воронку Шотта в колбу Бунзена, присоединенную к вакуумному насосу (или дегазируют с помощью блока автоматической дегазации и фильтрации растворителя). Срок хранения полученного раствора в холодильнике при температуре 2 - 8 °С в темной посуде 1 год.
Растворы витамина К1.
Раствор А - основной раствор с массовой концентрацией витамина К1 220 мкг/см3. В мерную колбу вместимостью 25 см3 вносят около 1/3 объема этилового спирта, закрывают пробкой и взвешивают, затем иглой вносят каплю (0,0038 г) витамина К1 и снова взвешивают. Тщательно перемешивают до полного растворения витамина, доводят до метки этиловым спиртом, затем содержимое вновь перемешивают. Полученный раствор хранят в холодильнике при температуре 2 - 8 °С в темной посуде не более 6 месяцев.
Раствор Б с массовой концентрацией витамина К1 0,22 мкг/см3. В мерную колбу вместимостью 25 см3 с помощью дозатора вносят 0,025 см3 раствора А, доводят этиловым спиртом до метки и содержимое тщательно перемешивают. Полученный раствор хранят в холодильнике при температуре 2 - 8 °С не более 2 месяцев.
Рабочие градуировочные растворы. В мерные колбы вместимостью 10 см3 сначала вносят 2 - 3 см3 этилового спирта, затем с помощью дозатора вносят определенный объем раствора Б, в соответствии с табл. 2, и добавляют этиловый спирт до метки, содержимое тщательно перемешивают. Срок хранения в холодильнике при температуре 2 - 8 °С не более 2 недель.
Приготовление градуировочных растворов витамина К1
|
№ градуировочного раствора |
Объем раствора Б (V), см3 |
Концентрация витамина К1 в градуировочном растворе (С), нг/см3 |
|
1 |
2,000 |
44,0 |
|
2 |
1,000 |
22,0 |
|
3 |
0,500 |
11,0 |
|
4 |
0,200 |
4,4 |
|
5 |
0,057 |
2,5 |
7.3. Установление градуировочной характеристики
Градуировочную характеристику, выражающую зависимость величины аналитического сигнала от массовой концентрации витамина К1 (нг/см3), устанавливают путем измерения высот пиков витамина К1 в градуировочных растворах, приготовленных по п. 7.2.
Каждый из градуировочных растворов в количестве 0,5 см3 шприцем вводят в хроматографическую систему, с помощью петлевого дозатора отсекается по 0,1 см3, которые анализируются без термостатирования колонки в следующих условиях:
- скорость движения элюента 1 см3/мин
- длина волны спектрофотометрического детектора 248 нм
- время удерживания витамина К1 17 - 18 мин
Для каждого анализируемого раствора проводят 5 параллельных измерений. По средним арифметическим значениям из пяти результатов измерения высот пиков в программе сбора и обработки хроматографических данных строится градуировочный график в координатах: «концентрация витамина (Спр), нг/см3» - «высота пика витамина (Н), мВ». Различие между измеренными значениями аналитических сигналов и времен удерживания не должно превышать 5 % от средних значений. Линейная зависимость должна соблюдаться во всем диапазоне определяемых концентраций.
7.4. Отбор и подготовка проб крови для анализа
Венозную кровь отбирают в количестве 5 см3 утром натощак. Для получения сыворотки кровь термостатируют в течение 30 мин при 37 °С, затем аккуратно обводят по всему радиусу пробирки стеклянной палочкой и центрифугируют в течение 15 мин со скоростью 3000 об./мин. Далее сыворотку (верхний слой) отделяют в пробирки типа Эппендорф и используют для анализа.
В центрифужные стеклянные пробирки с притертой пробкой помещают по 0,8 см3 сыворотки, добавляют равное количество этилового спирта (для осаждения белка), встряхивают в течение 2 - 3 с на встряхивателе со скоростью вращения гнезда 2000 об./мин. Затем к смеси добавляют 0,8 см3 гексана, пробирки плотно закрывают пробкой и перемешивают в течение 15 мин на перемешивающем устройстве, при этом пробирки закрывают черной бумагой для предотвращения прямого воздействия света. Далее пробы центрифугируют в течение 10 мин со скоростью 3000 об./мин. Аликвоты гексановых экстрактов в количестве 0,5 см3 переносят в пробирки типа Эппендорф и упаривают в токе азота досуха. Остатки растворяют в 0,5 см3 элюента. Для каждой пробы выполняют два параллельных измерения.
Примечание. Процедуры перемешивания и центрифугирования необходимо проводить в темноте, при охлаждении.
8. Выполнение измерений
После выхода хроматографа на режим в дозирующее устройство прибора микрошприцем вводят 0,5 см3 одного из градуировочных растворов (обычно с концентрацией, лежащей в середине рабочего диапазона) и анализируют в условиях, указанных в п. 7.3. По окончании хроматографического анализа определяют время удерживания витамина К1 и высоту пика. Далее величина высоты полученного пика наносится на градуировочный график (с целью корректировки градуировочной характеристики).
Затем в дозирующее устройство вводят 0,5 см3 анализируемого раствора и так же анализируют в условиях, указанных в п. 7.3. По окончании хроматографического анализа проводят ручную разметку пиков и идентификацию обнаруженных пиков. Витамин К1 идентифицируют по времени удерживания: совпадение времени удерживания витамина К1 в пробе с временем удерживания витамина К1 в градуировочном растворе (с ошибкой не более 5 %) свидетельствует о правильной идентификации.
9. Обработка результатов измерения
Количественный расчет массовой концентрации витамина К1 осуществляют с помощью программы сбора и обработки хроматографических данных. Используют метод абсолютной градуировки. При этом концентрация витамина 1 ч в пробе (Спр, нг/см3) считается автоматически.
Вычисляют среднее арифметическое двух параллельных измерений Спр1, Спр2, расхождение между которыми не должно превышать 5 % от среднего значения:
|
|
Спр - массовая концентрация витамина К1 в сыворотке крови, нг/см3.
Результат считают удовлетворительным, если выполняется следующее неравенство:
|
|
(4) |
Cmax и Сmin - максимальный и минимальный результат единичных измерений;
r - предел повторяемости (допускаемое расхождение между результатами единичных измерений), %.
Значения предела повторяемости r представлены в табл. 1.
При превышении предела повторяемости определение повторяют. При повторном превышении норматива повторяемости выясняют причины, приводящие к получению неудовлетворительных результатов, и устраняют их.
10. Оформление результатов анализа
Результат количественного анализа «С», нг/см3 представляют в виде:
|
|
С - среднее арифметическое результатов параллельных определений, признанных приемлемыми, нг/см3,
δ - относительная погрешность определения массовой концентрации витамина К1, %, приведенная в табл. 1.
Примечание. Числовые значения результата измерений оканчиваются цифрой того же разряда, что и значение показателя точности методики измерений (абсолютной погрешности измерений массовой доли определяемого компонента).
11. Контроль качества результатов измерений
11.1. Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводится каждый раз перед началом анализа и через каждые пять проб по раствору стандартного образца. Рекомендуется, чтобы концентрация уточняющего стандарта находилась примерно в середине диапазона концентраций, в котором предполагается проводить измерения, в случае же если он заранее неизвестен, то в середине диапазона градуировочного графика.
Контроль стабильности градуировочной характеристики осуществляется путем сравнения данных о содержании витамина К1 полученных с помощью градуировочной характеристики, с реальным содержанием витамина К1 в контрольном растворе.
Стабильность градуировочной характеристики считают удовлетворительной, если для контрольной точки выполняется следующее условие:
|
|
С0 - Сг - расхождение между аттестованным значением массовой концентрации раствора стандартного образца и концентрацией, определенной с помощью градуировочной характеристики, нг/см3;
С0 - концентрация раствора, приготовленного из ГСО, нг/см3;
Сг - массовая концентрация витамина К1, определенная по градуировочной характеристике, нг/см3;
Кг - норматив контроля стабильности градуировочной характеристики: Кг = 1,96·σR, где
σR - показатель воспроизводимости, приведен в табл. 1.
Градуировочная характеристика считается стабильной, если отклонение не превышает ±Кг. Если условие не выполняется, эксперимент повторяют. Если результат повторного сравнения неудовлетворителен, то выясняют причины, приводящие к получению неудовлетворительных результатов контроля, и устраняют их. В случае невозможности устранения причин, приводящих к превышению норматива контроля стабильности градуировочной характеристики, градуировку проводят заново.
11.2. Контроль внутрилабораторной прецизионности
Для контроля внутрилабораторной прецизионности используют рабочие пробы. Две параллельные пробы анализируют в соответствии с прописью методики, максимально варьируя условия проведения анализа, т.е. в разное время, разными исполнителями, с использованием разных наборов посуды.
Внутрилабораторную прецизионность результатов измерений считают удовлетворительной, если расхождение между результатами анализа, полученными в одной лаборатории (в разное время, разными исполнителями, с использованием разных партий средств измерений) не превышает предела внутрилабораторной прецизионности Rл = 0,84R:
|
|
Сmax, Сmin - максимальный и минимальный результаты анализа при контроле внутрилабораторной прецизионности, нг/см3;
Сmax - Сmin - фактическое расхождение между результатами анализа, нг/см3;
R - предел прецизионности, приведенный в табл. 1.
При удовлетворительных результатах контроля внутрилабораторной прецизионности приемлемы оба результата анализа, а в качестве окончательного может быть использовано их среднее арифметическое значение.
При превышении предела внутрилабораторной прецизионности Rл могут быть использованы методы оценки приемлемости результатов анализа согласно раздела 5 ГОСТ Р ИСО 5725-6.
11.3. Оперативный контроль точности
Контроль точности результатов измерений проводят методом добавок в рабочие сыворотки крови.
Отобранную сыворотку крови делят на две части, первую из которых анализируют в точном соответствии с прописью методики и получают результат определения витамина К1 в пробе (C), нг/см3. Во вторую часть вносят добавку (Сд) определяемого элемента, используя стандартные растворы. Содержание добавки должно составлять 50 - 150 % от содержания витамина К1 в пробе.
Результат контроля считается удовлетворительным при выполнении условия:
|
Кк = |(С′ - С) - Сд| ≤ Кд, где |
С′ - результат определения массовой концентрации витамина К1 в пробе с добавкой, нг/см3;
С - результат определения массовой концентрации витамина К1 в рабочей пробе без добавки, нг/см3;
Сд - действительное содержание элемента в добавке к пробе, рассчитанное исходя из значения его содержания в стандартном образце, нг/см3.
Кд - норматив оперативного контроля точности.
Норматив оперативного контроля точности рассчитывают по формуле:
|
|
Δ1 и Δ2 - абсолютные погрешности определения массовой концентрации витамина К1 в пробе (С) и в пробе с добавкой (С′) соответственно. Значения Δ1 и Δ2 рассчитывают по формулам:
|
Δ1 = 0,01·δ·С; Δ2 = 0,01·δ·С′, где |
δ - относительная погрешность определения массовой концентрации витамина К1, приведенная в табл. 1.
Методические указания разработаны ФБУН «Нижегородский НИИ гигиены и профпатологии» Роспотребнадзора (Соколова О.В., Потапова И.А.).