Методические указания
по санитарно-микробиологическому анализу лечебных грязей*
(утв.
Главным государственным санитарным врачом СССР
11 сентября 1989 г. № 143-9/316-17)
____________
* Взамен Методических рекомендаций "Оценка санитарно-бактериологического состояния лечебных грязей различных типов", утвержденных МЗ СССР 12 марта 1985 года.
Аннотация
В методических рекомендациях представлены современные методы определения санитарно-показательных, потенциально-патогенных бактерий и установлены их нормативные уровни, гарантирующие эпидемическую безопасность использования пелоидов в лечебных целях.
Методические указания предназначены и являются обязательными для всех лечебно-профилактических и санаторно-курортных учреждений, использующих лечебные грязи, а также организаций, осуществляющих работы по изучению и использованию лечебных грязей, разведке, эксплуатации и охране грязевых месторождений.
Введение
В настоящее время оценка санитарного состояния пелоидов в отношении микробного загрязнения проводится по санитарно-микробиологическим показателям (бактериям группы кишечной палочки, C. perfringens), определенные уровни которых гарантируют эпидемическую безопасность использования пелоидов в лечебных целях.
Специфика использования лечебных грязей в бальнеотерапевтических процедурах (аппликации на поверхности кожи, раневые поверхности, слизистые оболочки) требует их строгого санитарно-микробиологического контроля.
Проведенными исследованиями была установлена широкая циркуляция потенциально патогенной микрофлоры в лечебных грязях (P. aeruginosa, энтерококков). Учитывая, что в современных условиях растет роль вышеуказанных потенциально патогенных бактерий в формировании эпидемического процесса, обоснована необходимость контролирования лечебных грязей также по P. aeruginosa, что предусматривают настоящие Методические указания.
Методические указания распространяются на лечебные грязи всех типов (торфяные, сапропелевые, иловые минеральные, сопочные) и устанавливают методы их санитарно-микробиологического анализа.
Методические указания являются обязательными при исследовании качества лечебных грязей по микробиологическим показателям:
- при разведке, оценке и эксплуатации месторождений пелоидов;
- при использовании пелоидов в лечебных целях (нативной и регенерированной грязи);
- при неблагоприятной санитарной и эпидемической ситуации на прилегающей территории к месторождению или объекту использования и хранения лечебных грязей.
Методические указания предназначены для санэпидслужбы при проведении выборочного государственного санитарного надзора, для лечебно-профилактических и санаторно-курортных учреждений, использующих грязи, а также организаций, осуществляющих работы по изучению и использованию грязей, разведке, эксплуатации и охране грязевых месторождений.
1. Санитарно-микробиологические показатели оценки качества пелоидов (требования и нормы)
Основными санитарно-микробиологическими показателями, характеризующими степень фекального загрязнения пелоидов, являются лактозоположительные кишечные палочки (ЛКП), сульфитвосстанавливающие клостридии, общее микробное число (ОМЧ). Обнаружение потенциально патогенных и патогенных микроорганизмов (синегнойная палочка - P. aeruginosa, стафилококки - S. aureus) сигнализирует об эпидемической опасности лечебных грязей; обнаружение фекальных колиформных бактерий, энтерококков подтверждает наличие свежего фекального загрязнения.
В зависимости от поставленной цели санитарно-микробиологические исследования пелоидов проводятся в виде краткого и полного анализа.
Санитарно-микробиологический анализ пелоидов по краткой схеме включает определение основных показателей: ЛКП, сульфитвосстанавливающих клостридий, ОМЧ и проводится в следующих случаях:
- при общей поисковой разведке грязевых месторождений;
- при текущем контроле за санитарным состоянием месторождений (анализ проводится не реже 1 раза в квартал).
При превышении нормативных уровней основных показателей следует проводить исследования по определению энтерококков, фекальных колиформных бактерий, синегнойной палочки, патогенных стафилококков.
В случае обнаружения патогенной микрофлоры необходимо выявление источника и характера загрязнения и проведение специальных мероприятий по санации данного месторождения.
Санитарно-микробиологический анализ по полной схеме включает определение ЛКП, сульфитвосстанавливающих клостридий, ОМЧ, P. aeruginosa, патогенных стафилококков и проводится в следующих случаях:
- при детальном поиске, при эксплуатационной разведке, технологической схеме, детальном обследовании;
- при контроле оценки качества пелоидов, используемых в лечебных целях. Анализу подвергается каждая новая партия лечебной грязи, подготовленная к использованию. В случае превышения нормативных уровней основных показателей и обнаружении P. aeruginosa и S. aureus лечебную грязь выдерживают определенные сроки в регенерационных бассейнах грязелечебницы до восстановления регламентирующих величин санитарно-микробиологических показателей;
- при обследовании действующего грязевого хозяйства анализируется грязь после лечебных процедур, заложенная в регенерационные бассейны, а также после окончания сроков регенерации. Обследование проводится не реже 2-х раз в год. При превышении нормативных уровней основных санитарно-микробиологических показателей следует проводить дополнительные исследования на наличие показателей свежего фекального загрязнения (энтерококков, фекальных колиформных бактерий).
Санитарно-микробиологический анализ по полной и краткой схеме выполняется:
- при детальном поиске, предварительной разведке (2 анализа с каждого месторождения), при детальной разведке, доразведке (5 анализов с каждого месторождения).
Количественное соотношение тех и других видов анализов решается в каждом конкретном случае.
По эпидемическим показателям органами санитарно-эпидемиологической службы проводятся дополнительные исследования по определению патогенных энтеробактерий.
Схема контроля и оценки качества пелоидов по санитарно-микробиологическим показателям представлена в таблице.
Таблица
Схема контроля оценки качества пелоидов по санитарно-микробиологическим показателям
|
Объект |
Частота анализа |
Показатели и их нормативные уровни* |
||||
|
Основные показатели |
Патогенные стафилококки |
P. aeruginosa |
||||
|
ОМЧ, кл/г |
Титр ЛКП |
Титр клостридий |
||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
1. Месторождение пелоидов |
|
|
|
|
|
|
|
Общая поисковая разведка, детальный поиск, предварительная разведка, детальная разведка, доразведка |
от 5 до 50 |
500000 |
10 |
0,1 |
не определяется |
не определяется |
|
при текущем контроле |
1 раз в квартал |
500000 |
10 |
0,1 |
не определяется |
не определяется |
|
при детальном поиске, предварительной разведке, доразведке, эксплуатационной разведке, технологической схеме, детальном обследовании |
от 5 до 50 |
500000 |
10 |
0,1 |
отсутств. в 10 |
отсутств. в 10 |
|
2. Грязелечебница |
|
|
|
|
|
|
|
Лечебная грязь для процедур |
перед использованием |
500000 |
10 |
0,1 |
отсутств. в 10 г |
отсутств. в 10 г |
|
Обследование грязевого хозяйства |
2 раза в год |
500000 |
10 |
0,1 |
отсутств. в 10 г |
отсутств. в 10 г |
___________
* Определение фекальных колиформ, энтерококков проводится в случае превышения основных нормативных показателей. Обнаружение в 10 г грязи фекальных колиформ и энтерококков свидетельствует о свежем фекальном загрязнении.
2. Отбор, хранение и транспортировка проб пелоидов
Пробы на санитарно-микробиологический анализ при поисковой и детальной разведках месторождений отбираются по окончании бурения, определения гидрогеологических условий и выявления источников возможного бактериального загрязнения грязевой залежи.
Количество отбираемых на анализ проб грязи зависит от размеров площади месторождения, его сложности (три группы сложности месторождения) и санитарной обстановки.
На малых месторождениях (до 0,01 км2) при отсутствии видимых источников загрязнения участки отбора проб грязи определяются в зависимости от группы сложности, т.е. от устойчивости гидрологогидрохимического режима, колебаний качественных показателей и мощности грязевой залежи, ее конфигурации, элементов рельефа и т.д. На анализ отбирается до 4 проб грязи.
На крупных месторождениях второй и третьей группы сложности при благоприятной санитарной обстановке определение количества точек для санитарно-микробиологического анализа производится согласно следующим рекомендациям:
- на каждые 100 га изучаемого месторождения намечается к отбору проб грязи до 10 участков площадью 25 м2.
При наличии одного источника загрязнения выделяется два участка: один вблизи источника загрязнения, другой - вдали (заведомо незагрязненный).
Если на изучаемом месторождении имеется несколько источников загрязнения, то необходимо выделить несколько опытных участков около каждого загрязняющего внешнюю среду.
На крупных месторождениях второй и третьей группы сложности, расположенных в неблагоприятной санитарной обстановке, на санитарно-микробиологический анализ отбирают не менее 40 - 50 проб грязей.
При разработке грязевой залежи санитарно-микробиологический контроль пелоида производится в каждом заборе перед началом его отработки.
Образцы грязей на санитарно-микробиологический анализ отбираются в каждой выбранной точке месторождения или бассейна на площади 25 м2 по принципу конверта (из четырех углов и из середины). При поисковой разведке пробы грязи отбирают с глубины 0 - 0,5 м, при детальной - из каждого выделенного горизонта грязевой залежи. Пробы грязи отбираются с соблюдением стерильности.
Глубина отбора проб грязей из бассейнов зависит от их конструкции: при верхней подаче пелоида на процедуры пробы отбираются из интервала 0 - 0,5 м; при нижней подаче - со дна бассейна и из пристенных слоев грязи.
Взятые образцы грязи перемешивают и среднюю пробу в количестве 500 г помещают в стерильную стеклянную банку, не допуская воздушных прослоев. Банки с грязью закрывают простерилизованными полиэтиленовыми или металлическими крышками. Проба снабжается техническим паспортом с указанием: даты, места и глубины отбора, типа месторождения, фамилии пробоотборщика. Анализ должен проводиться в течение 2-х часов после отбора проб. При невозможности приступить к исследованию допускается хранение пробы не более 24 часа при температуре 4 - 5 °С.
3. Санитарно-микробиологический анализ пелоидов Подготовка и обработка пелоидов для анализа
Банку с пробой вскрывают, окисленный слой удаляют стерильным шпателем, грязь перемешивают. Отбор проб из банки проводят методом "режущего кольца" с помощью стерильной трубки с внутренним диаметром 10 мм. Для этого трубку погружают в банку на полную глубину. Пробу извлекают из трубки с помощью поршня на стерильную чашку Петри и тщательно перемешивают.
Для анализа отбирают навеску грязи 15 - 30 г, помещают в колбу с 135 - 270 мл стерильной водопроводной воды. Пробы грязи в колбах встряхивают на шуттель-аппарате в течение 15 - 20 минут. Для лучшего перемешивания грязи в колбу можно поместить стерильные стеклянные бусы (шарики) в количестве 30 - 50 штук.
В результате встряхивания образуется грязевая "болтушка" с разведением грязи 1:10, которая считается "основным" разведением. Из основного разведения готовят последующие десятикратные разведения. Для этого в пробирку с 9 мл стерильной водопроводной воды вносят 1 мл основного разведения (1:10) и так далее. Обычно приготовляют 3 - 4 последующих разведения. Из приготовленных разведений посевы вносят в соответствующие питательные среды для определения микроорганизмов. Исследуются следующие объемы грязевой суспензии:
100 мл, 10 мл, 1 мл основного разведения, что соответствует 10 г грязи, 1 г и 0,1 г, по 1 мл последующих разведений (0,1 мл; 0,01 и т.д. до 0,0001), что соответствует 0,01 г грязи, 0,001 и т.д.
Все исследования проводятся в 2-кратной повторности.
3.1. Определение количества ЛКП, фекальных колиформных бактерий, энтерококков, P. aeruginosa
Определение количества ЛКП, фекальных колиформных бактерий, энтерококков, P. aeruginosa проводится в соответствии со схемой исследования (Приложение 1). В качестве накопительной универсальной среды используется лактозопептонная среда (ЛПС).
Выполнение анализа
К 100 мл основного разведения грязевой суспензии добавляют 10 мл концентрированной ЛПС, к 10 мл основного разведения - 1 мл концентрированной ЛПС, в пробирки с 9 мл неконцентрированной ЛПС добавляют 1 мл основного разведения и последующих.
Инкубацию проводят при температуре 37 °С в течение 24 - 48 часов. Через 24 часа посевы просматривают и отмечают в них наличие или отсутствие газообразования и помутнения среды. При отсутствии через 48 часов помутнения в колбах и пробирках дают отрицательный ответ.
3.1.1. Определение лактозоположительных кишечных палочек
В качестве основного показателя степени фекального загрязнения пелоидов определяют лактозоположительные кишечные палочки (ЛКП) или колиформные бактерии, которые входят в семейство Enterobacteriaceae. К ним относятся грамотрицательные, не образующие спор палочки, ферментирующие лактозу до кислоты и газа при 37 °С в течение 21 часа, с отрицательным оксидазным тестом.
При наличии в колбах и пробирках газообразования и помутнения через 24 часа инкубации производят высев на среду Эндо, разделенную на 3 - 4 сектора с таким расчетом, чтобы получить изолированные колонии. Чашки инкубируют 16 - 18 часов при температуре 37 °С.
При наличии типичных колоний красных с металлическим блеском, розовых с красным центром, розовых выпуклых слизистых и др. проверяют оксидазную активность. Оксидазный тест предназначается для дифференциации бактерий семейства Enterobacteriaceae от грамотрицательных бактерий Pseudomonadaceae и других видов сапрофитных бактерий; на среде Эндо P. aeruginosa растут в виде плоских колоний сиреневого цвета с неровными краями, оксидазоположительные.
Постановка оксидазного теста при этом осуществляется следующим образом: петлей или стеклянной палочкой снимают изолированные колонии со среды Эндо и наносят штрихом на фильтровальную бумагу, смоченную специальным реактивом (Приложение 3, п. 5).
Через 1 - 3 минуты культура окрашивается в ярко-синий цвет при положительной реакции на оксидазу и не изменяется при отрицательной. Если оксидазный тест со среды Эндо проявляется недостаточно четко, то для подтверждения результата изолированные колонии можно пересеять на скошенный питательный агар и после подращивания повторить оксидазный тест. Оксидазный тест можно определять системой индикаторных бумажек (СИБ).
При наличии на поверхности среды Эндо розовых или красных колоний с отрицательной оксидазной активностью их микроскопируют.
При наличии грамотрицательных палочек засевают по 2 - 3 колонии каждого типа в полужидкую или жидкую с поплавком среду с лактозой для подтверждения ферментации лактозы. Учет производят через 4 - 5 и 18 часов инкубации при 37 °С. Если за это время происходит образование кислоты и газа, то это свидетельствует о наличии лактозоположительных кишечных палочек в исследуемом разведении грязи. Признаком газообразования является появление пузырьков газа; об образовании кислоты свидетельствует изменение цвета среды. При наличии только кислоты пробирки оставляют в термостате для окончательного ответа через 24 часа. При отсутствии газообразования через этот срок получают окончательный отрицательный ответ, при наличии газообразования - положительный результат.
В тех лабораториях, где учет на полужидкой среде с лактозой не может производиться через 4 - 5 часов, следует применять лактозопептонную среду с поплавками. В этом случае учет результатов производят через 10 - 24 часа.
Обнаружение в грязи колиформных бактерий следует рассматривать как показатель фекального загрязнения грязи, а их количество позволяет судить о степени этого загрязнения. Количество колиформных бактерий выражают через коли-титр.
После выделения колиформных бактерий устанавливается титр, при этом принимается то предельное разведение грязи, которое дало положительный ответ.
Например: если положительный результат отмечается в пробирке с 1 мл основного разведения, а в последующем разведении бактерии ЛКП не обнаружены, то коли-титр будет равен 0,1.
3.1.2. Определение фекальных колиформных бактерий
К группе фекальных колиформных бактерий относятся E. Coli, Klebsiella и др. - грамотрицательные, не образующие спор палочки, способные ферментировать лактозу до кислоты и газа при 44 ± 0,5 °С. Обнаружение фекальных колиформных бактерий указывает на наличие свежего фекального загрязнения.
Для подтверждения принадлежности лактозоположительных колоний к фекальным колиформным бактериям со среды Эндо несколько колоний каждого типа с отрицательным оксидазным тестом пересевают в пробирки с лактозным бульоном, содержащим борную кислоту.
Засеянные пробирки инкубируют при температуре 44 ± 0,5 °С в течение 24 часов. Положительный ответ дают при наличии помутнения и газообразования.
Срок анализа можно сократить, если из сред накопления, где обнаружен газ, одновременно с высевом на среду Эндо для подтверждения наличия лактозоположительных кишечных палочек производят высев пипеткой в количестве 2 - 3 капли в лактозный бульон с борной кислотой. Посевы инкубируют при температуре 44 ± 0,5 °С, определяя при этом преимущественно фекальные колиформные бактерии.
3.1.3. Определение энтерококков
Энтерококки - грамположительные, полиморфные круглые, чаще слегка вытянутые с заостренными концами диплококки, располагающиеся попарно или в коротких цепочках. Определяют для подтверждения фекального загрязнения.
Из накопительной среды (ЛПС), где имеет место помутнение, делают высев на сектора элективной молочно-ингибиторной среды (МИС). Через 24 - 48 часов инкубации посевов на МИС при температуре 37 °С в качестве положительных результатов отмечают наличие аспидно-черных выпуклых с металлическим блеском, а также сероватых мелких колоний.
Молочно-ингибиторная среда позволяет дифференцировать виды энтерококков: S. faecalis образуют аспидно-черные выпуклые колонии с металлическим блеском; S. faecalis биовар liguefaciens такие же колонии, окруженные зоной просветления с выпадением по периферии осадка параказеина повышенной мутности; S. faecium и биовар durans мелкие серые плоские колонии.
Типичные колонии микроскопируют и отсевают на косяк с МПА. Вместо среды МИС можно использовать также среду Турчинского. Обнаружение грамположительных, слегка вытянутых с заостренными концами диплококков, часто располагающихся короткими цепочками, свидетельствует о наличии энтерококков. С культурой, выросшей на косяке, ставится каталазная проба. Для этого на газон роста наносится 3-процентная перекись водорода. При наличии пузырьков газа культура считается каталазоположительной (сарцины, стафилококки и др.).
Энтерококки - каталазоотрицательные микроорганизмы.
3.1.4. Определение P. aeruginosa
P. aeruginosa - грамотрицательные, мелкие подвижные, оксидазоположительные палочки. Спор не образуют, не ферментируют, но окисляют глюкозу до кислоты, имеют пигмент сине-зеленой окраски.
Посев исследуемого материала осуществляют из накопительной среды ЛПС (3.1) на среду "Блеск", и чашки инкубируют при 42 °С 24 часа. Высев следует производить с расчетом получения максимального количества изолированных колоний. Колонии P. aeruginosa на среде "Блеск" темно-красного цвета, плоские, нередко принимают веретенообразную форму, сплошь покрыты золотистым налетом либо содержат многочисленные вкрапления, иногда окруженные светло-красным ободком или бесцветным венчиком.
Культура P. aeruginosa обладает специфическим ароматическим запахом земляничного мыла, жасмина, фиалки, цветов липы и др. Для идентификации P. aeruginosa со среды "Блеск" снимают 1 - 3 наиболее типичных колонии с золотистым блеском, микроскопируют. Грамотрицательные культуры засевают уколом в столбик среды Хью-Лейфсона (OF) для определения оксидации и ферментации глюкозы и одновременно макроколониями (бляшками) на среду Кинг-А, а также на косяк с МПА. На среде Кинг-А на одной чашке можно разместить от 16 - 18 до 24 макроколоний.
Посевы инкубируют при температуре 37 °С в течение 24 - 48 часов, а затем учитывают результаты. Р. aeruginosa окисляют глюкозу, но не ферментируют ее, первоначальный зеленый цвет среды OF изменяется в верхней части столбика на желтый (+), нижняя остается зеленой (-). Результат учитывается как OF (±). Enterobacteriaceae изменяют среду OF в желтый цвет (+/+) и не учитываются.
На среде Кинг-А колонии плоские, с шероховатой поверхностью, неровными краями и кружевным венчиком; при косом освещении улавливается серебристый блеск. Характерно наличие окрашиваемого пигмента. При отсутствии пигмента посевы оставляют еще на сутки при комнатной температуре. Пигмент образуется вокруг колоний и диффундирует в толщу среды. Культуру, выросшую на косяке, проверяют на оксидазную активность. При этом колонии P. aeruginosa в течение 15 - 20 секунд становятся темно-синими.
При наличии оксидазоположительных бактерий, продуцирующих пигмент и дающих на среде "Блеск" золотистый налет, идентификацию P. aeruginosa можно считать законченной.
Количественный учет P. aeruginosa выражается в титре аналогично коли-титру.
3.2. Определение сульфитвосстанавливающих клостридий в лечебных грязях
Сульфитвосстанавливающие клостридии, преимущественно C. perfingens, - крупные неподвижные палочки, не образующие цепочки, грамположительные, анаэробные, толстые с "обрубленными" или слегка закругленными концами, жгутиков не имеют, образуют споры. Характерным признаком является высокая ферментативная активность, расщепление сахаров с образованием кислоты и газа, быстрое и бурное свертывание молока с образованием сгустка и отделением сыворотки, а также способность редуцировать сульфит натрия (NA2SO3) при 45 ± 1 °С в течение 16 - 18 часов на железо-сульфитной среде.
1 мл основного и последующих разведений лечебной грязи (0,1; 0,01) переносятся в два ряда параллельных пробирок. Один ряд пробирок прогревают при температуре 80 °С в течение 15 минут или 90 °С в течение 10 минут для уничтожения вегетативной микрофлоры. Затем во все пробирки наливают по 9 - 10 мл среды Вильсон-Блера, приготовленной extempore.
Пробирки заливают расплавленной средой (50 - 60 °С) и быстро опускают в холодную воду для немедленного охлаждения и удаления воздуха из среды.
Инкубируют посевы при температуре 44 - 45 °С в течение 24 часов. При наличии клостридий в пробирках через 4 - 5 часов образуются колонии черного цвета. Микроорганизмы фекального происхождения при 45 °С такую реакцию не дают.
После учета черных колоний производят их пересев на молочную среду для дальнейшей идентификации. Для этого петлей переносят колонии в пробирки с молочной средой, которые инкубируют при 44 - 45 °С 24 часа.
При развитии клостридий наблюдается образование губчатого сгустка молока, приподнятого кверху, жидкость при этом становится прозрачной, слегка желтоватой.
Для подтверждения наличия клостридий проводят микроскопирование. Обнаружение грамположительных палочек указывает на присутствие клостридий.
Титр устанавливают по максимальному разведению, в котором обнаружены клостридии.
3.3. Определение общего микробного числа (ОМЧ)
Для характеристики общего микробного загрязнения пелоидов определяют численность сапрофитных микроорганизмов, способных расти на мясо-пептонном агаре при 30 °С 48 - 72 часов.
1 мл приготовленных грязевых разведений вносят в стерильные чашки Петри и заливают расплавленным и остуженным до 45 °С мясо-пептонным агаром в количестве 15 - 20 мл. Учитывая практический опыт, целесообразно проводить высев из разведений 0,01; 0,001; 0,0001. Посев каждого разведения производят не менее чем на 2 чашки. Содержимое чашки Петри быстро смешивают, равномерно распределяя его по всей поверхности, после застывания агара чашки помещают в термостат и инкубируют при температуре 30 °С в течение 48 - 72 часов.
Для подсчета выросших колоний берут такие разведения, при которых на чашках вырастает от 30 до 300 колоний. Если вырастает более 300 колоний, то ведется счет на 1/4 площади чашки с последующим перерасчетом на всю площадь. Из суммы колоний, подсчитанных на всех чашках, выводят среднее арифметическое и затем определяют число колоний на 1 г почвы (с учетом разведений).
Результат можно представить на основании подсчета колоний на одной чашке, если на других чашках:
- рост расплывчатых колоний распространился на всю поверхность чашки;
- число колоний превышает 300;
- при посеве из разбавлений выросло менее 30 колоний.
Если рост расплывчатых колоний распространяется на всю поверхность чашки и подсчет невозможен, то посев проб производят повторно. Чтобы помешать развитию на поверхности агара спорообразующих микробов и бактерий рода Proteus в Н-форме, чашки Петри заливают голодным агаром, расплавленным и остуженным до 45 - 50 °С слоем толщиной 3 - 4 мм.
3.4. Определение стафилококков
Стафилококки объединяются в род Staphylococcus. Это грамположительные кокки, имеющие правильную шаровидную форму, обладающие активной каталазой, ферментирующие глюкозу в анаэробных условиях с выделением кислоты, как правило, образующие пигмент на питательных средах.
S. aureus - потенциально патогенный микроорганизм, отличительным признаком является способность коагулировать плазму крови, ферментировать маннит в анаэробных условиях, обладающий лецитовителлазной активностью. S. epidermidis - вегетирует на кожных покровах человека, не являясь болезнетворным, но в отдельных случаях может вызвать септические процессы у ослабленных больных.
Выполнение анализа: к 100 мл основного разведения грязевой болтушки добавляют 10 мл 25-процентного пептона и 10 г хлорида натрия. К 10 мл основного разведения грязевой болтушки добавляют 1 мл 25-процентного пептона и 1 г хлорида натрия. Посевы инкубируют при 37 °С в течение 24 - 48 часов. Высев из флаконов и пробирок проводят на молочно-желточно-солевой агар (МЖСА) и инкубируют при 37 °С в течение 24 - 48 часов.
Учитывают блестящие выпуклые колонии белого, палевого, золотистого цвета, окруженные радужной с перламутровым блеском зоной, что свидетельствует о наличии лецитовителлазной активности; отмечают пигментообразование, микроскопируют. Далее с МЖСА на скошенный агар снимают в первую очередь колонии стафилококков, образующие радужный венчик, пигментированные колонии с отрицательной лецитовителлазной реакцией. При отсутствии на чашках пигментированных колоний и колоний с положительной лецитовителлазной реакцией для исследования снимают беспигментные колонии, похожие по морфологии на стафилококки. При одновременном наличии на чашках колоний стафилококка, отличающихся по пигменту, следует отсевать не менее двух колоний различного вида.
Для подтверждения принадлежности таких бактерий к S. aureus определяют плазмокоагулазную активность в соответствии с "Методическими рекомендациями по видовой идентификации стафилококков" № 1922-78.
При наличии мелких грамположительных кокков, располагающихся в виде гроздей, способных коагулировать плазму и чаще всего обладающих лецитовителлазной активностью, дают положительный ответ.
Приложение 1
Схема определения ЛКП, фекальных колиформ, P. AERUGINOSA, энтерококков в лечебных грязях
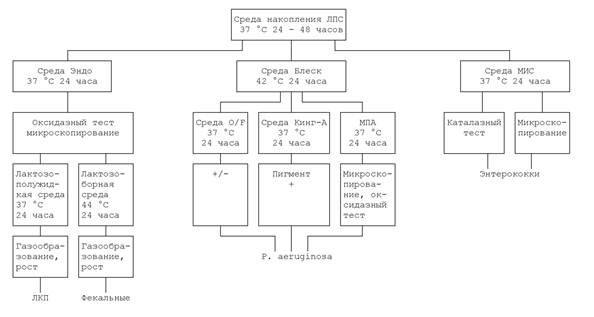
Приложение 2
Аппаратура, лабораторное оборудование
Оборудование
Автоклав электрический по ГОСТ 9586-61
Термостат электрический с автоматическим регулированием
Холодильник бытовой электрический с температурой в камере +4 - 6 °С
Холодильник походный (сумка) для транспортировки проб
Микроскоп биологический по ГОСТ 8284-78 или другого типа, обеспечивающий увеличение в 600 раз, с осветителем
Осветитель ОИ-19
Лупа по ГОСТ 8309-57
Аквадистиллятор Д-4-2 или другого типа
Прибор для счета колоний
рН метр (ионометр)
Шкаф сушильный стерилизационный, обеспечивающий температуру 180 °С в течение 1 - 2 часов
Аппарат для встряхивания жидкостей в пробирках и колбах (шуттель-аппарат)
Весы лабораторные общего назначения по ГОСТ 24104-80 4-го класса точности
Разновесы
Лотки эмалированные.
Лабораторная посуда
Колбы различной емкости (50, 100, 250, 500 и 1000 мл)
Чашки бактериологические Петри по ГОСТ 7900-56
Шпатели стеклянные и металлические
Пипетки емкостью 1,2, 5 и 10 мл
Стеклянные банки разные
Стеклянные бусы
Воронки стеклянные
Цилиндры вместимостью 100, 200 и 500 мл
Стаканы лабораторные по ГОСТ 10394-63
Стекла покровные для микропрепаратов
Стекла предметные для микропрепаратов
Пробки разные (резиновые, ватные).
Реактивы и материалы для приготовления сред и проведения исследований
Реактивы
|
Альфа-нафтол |
ГОСТ 172-71 |
|
Борная кислота |
|
|
Диметил-пара-фенилендиамин |
ТУ 6-09-28-72 |
|
Калий едкий |
|
|
Натрий хлористый |
|
|
Перекись водорода |
|
|
Сернокислый натрий (тиосульфат натрия) |
ГОСТ 4215-66 |
|
Сульфат калия |
|
|
2,3,5 трифенил тетразолий хлористый (ТТХ) |
ТУ 6-09-3338-78 |
|
Фосфорнокислый калий двузамещенный (безводный) |
|
|
Фосфорнокислый калий однозамещенный (безводный) |
|
|
Хлорид магния |
|
|
Хлорид натрия |
|
|
Хлорное железо |
Углеводы, спирты
|
Глюкоза |
ГОСТ 5893-75 |
|
Д-Лактоза |
МРТУ 6-09-2211-65 |
|
Сахароза |
ГОСТ 5893-75 |
|
Спирт ректификованный |
Аминокислоты
|
L-аргинин гидрохлорид |
МРТУ 6-09-124-63 |
Индикаторы
|
Бриллиантовый зеленый |
ВТУ 11Р-53 |
|
Бромтимоловый синий |
ТУ 6-09-2045-77 |
|
Кристаллический фиолетовый |
ТУ 6-09-4119-75 |
|
Розоловая кислота |
|
|
Феноловый красный |
|
|
Фуксин |
|
Материалы для приготовления питательных сред
|
Агар - агар в волокнах и порошке |
ГОСТ 17206-84 |
|
Вода дистиллированная |
|
|
Дрожжи прессованные хлебопекарные |
|
|
Калий теллуристокислый |
ТУ 6-09-2060-77 |
|
Молоко коровье пастеризованное |
|
|
Пептон сухой для бактериологических целей |
|
|
Полимиксин "М" |
|
|
Яйца куриные |
|
Приложение 3
Рецептура питательных сред
1. Среда для определения бактерий группы кишечной палочки
Приготовление лактозопептонной среды:
а) нормальной концентрации: 10 г пептона, 5 г натрия хлористого (NaCl), 5 г лактозы растворяют при нагревании в 1000 мл дистиллированной воды рН 7,4 - 7,6.
Разливают по 10 мл в пробирки и стерилизуют в автоклаве при 112 °С (0,5 кгс/см2) 30 минут;
б) концентрированная: готовят так же, как и среду нормальной концентрации, но с добавлением на 1000 мл дистиллированной воды 50 г NaCl, 50 г лактозы, 100 г пептона.
2. Приготовление полужидкой среды с лактозой
В 1000 мл дистиллированной воды растворяют 10 г пептона, 5 г NaCl, 4 - 5 г агар-агара, доводят до кипения, устанавливают рН 7,2 - 7,4; добавляют 1 мл 1,6-процентного спиртового раствора бромтимолового синего. Стерилизуют при 120° ± 2 °С в течение 20 минут. В расплавленную среду вносят 5 г лактозы, нагревают до кипения. Разливают в стерильные пробирки столбиком высотой 3 см и стерилизуют при 112 °С (0,5 кгс/см2) 12 минут. Срок хранения не более 2-х недель.
Приготовление полужидкой среды с лактозой из сухого препарата с ВР - по прописи на этикетке. Срок хранения - не более 7 суток.
3. Приготовление среды Эндо (модификация)
Готовят из сухого препарата по прописи на этикетке. Чашки перед посевом подсушивают в термостате. Срок хранения - не более двух суток в темноте. В готовую и охлажденную до 60 - 70 °С среду перед разливкой в чашки до 20 - 25 мл допускается добавлять на 100 мл среды: 0,2 мл 100 %-ного спиртового раствора основного фуксина для повышения дифференцирующих свойств среды и 0,2 мл 5 % - спиртового раствора розоловой кислоты во избежание зарастания посевов споровыми аэробами. Чашки со средой перед посевом необходимо подсушить. Срок хранения раствора фуксина и розоловой кислоты - не более одного месяца.
4. Приготовление борнокислой буферной среды с лактозой
10 г пептона, 12,2 г калия фосфорнокислого двузамещенного (безводного), 4,1 г калия фосфорнокислого однозамещенного (безводного), 4,1 г калия фосфорнокислого однозамещенного (безводного), 3,2 г борной кислоты (требуется точное взвешивание), 5 г лактозы растворяют в 1 л дистиллированной воды, разливают по 5 мл в пробирки с поплавками, стерилизуют при температуре 112° (0,5 кгс/см2) 12 минут. Срок хранения - не более двух недель. Каждую новую партию среды целесообразно проверять на штамме E. Coli.
5. Приготовление реактива для определения оксидазной активности бактерий
30 - 40 мг альфа-нафтола растворяют в 2,5 мл ректификованного этилового спирта, добавляют 7,5 мл дистиллированной воды и растворяют 40 - 60 мг диметил-фенилендиамина. Раствор готовят непосредственно перед определением.
6. Приготовление питательного агара
Готовят из сухого препарата по прописи на этикетке, стерилизуют при 120 °С (1 кгс/см2) 30 минут.
7. Приготовление среды Вильсон-Блер
К 100 мл расплавленного и затем охлажденного до температуры 80 °С щелочного питательного агара с 1 % глюкозы добавляют 10 мл 20 % раствора сернистокислого натрия и 1 мл 8 % раствора хлорного железа. Можно использовать и обычный питательный агар, но перед применением дополнительно добавляют 10 мл 25 % глюкозы и 0,5 мл 10 % щелочи. Водные растворы солей готовят на стерильной дистиллированной воде и стерилизуют в течение часа текучим паром. Сернистокислый натрий можно заменить серноватистокислым натрием, а хлорное железо - сернокислым.
8. Приготовление среды для определения оксидации и ферментации (OF) (среда Хью-Лейфсона)
К 100 мл дистиллированной воды добавить 0,2 г пептона, 0,5 г хлорида натрия, 0,03 г K2HPO4, 0,3 г агар-агара, 1 г углевода (глюкоза, фруктоза), 0,3 мл 1 % водного раствора бромтимолового синего. Среду кипятить до полного растворения ингредиентов, установить рН 7,0 - 7,2, разлить по 3 - 4 мл в пробирки, стерилизовать при температуре 112 °С (0,5 кгс/см2) 15 минут. Остудить столбиком.
9. Среда "Блеск" и "Кинг-А" для идентификации P. aeruginosa
9.1. Среда "Блеск". Мясопептонного стерильного 2 % агара 100 мл, молока стерильного снятого 10 мл, 10 % водного раствора трифенилтетразола хлорида 8 мл, аргинина гидрохлорида 0,3 г. В расплавленный мясопептонный агар прибавить аргинин, раствор трифенилтетразол хлорида (самостерилизуется после хранения при комнатной температуре 2 - 3 дня) и стерильное снятое молоко размешать и разлить в 6 - 7 чашек.
9.2. Среда Кинг-А. Пептона 2 г, агар-агара 1,5 г, глицерина 1,0 г, сульфата калия 1,0 г, хлорида магния 0,14 г, воды дистиллированной до 100 мл, рН 7,2. Стерилизовать при температуре 112 °С (0,5 кгс/см2) 15 минут, разлить на 6 чашек.
10. Приготовление среды Турчинского
К 600 мл дистиллированной воды добавляют 400 мл желчи, 35 - 40 г сухого питательного агара, по 5 г фосфата калия однозамещенного и двузамещенного, 5 г натрий-аммоний фосфата. Расплавляют при нагревании, разливают во флакон и стерилизуют при 120 °С (1 кгс/см2) 20 минут. Перед употреблением в расплавленный и охлажденный агар добавляют на каждые 100 мл среды 0,5 г глюкозы; 1 мл 1 % водного раствора ТТХ, 0,6 мл 1 % водного раствора метиленового синего (хранить не более 14 дней), 20000 ЕД полимиксина М, 1 - 2 мл 0,1-процентного спиртового раствора фурациллина. Тщательно размешать, разлить в чашки Петри толстым слоем 20 - 25 мл.
11. Приготовление молочно-ингибиторной среды (МИС)
Готового питательного агара 85 мл, стерильного снятого молока 15 мл, 0,01 %-ного раствора водного кристаллического фиолетового 1,25 мл, теллурита калия 2 %-ного водного раствора 1 мл. Все хорошо смешать и разлить в чашки Петри.
12. Тест Грегерсена
Простой, быстрый способ, заменяющий окраску по Граму и не требующий оптики.
В капле 3 % раствора KOH на предметном стекле эмульгируют бактериальную массу, взятую с плотной среды. После нескольких секунд перемешивают петлей, взвесь ослизняется и за петлей тянутся слизистые нити, что указывает на принадлежность испытуемых микроорганизмов к грамотрицательным. У грамположительных микроорганизмов реакция отрицательная.
13. Молоко по Тукаеву
К 1 %-ной пептонной воде прибавляют 5 - 6 % обезжиренного молока, среду стерилизуют при 112 °С (0,5 кгс/см2) 12 минут.
14. Каталазный тест
Каплю 3 % раствора перекиси водорода наносят на предметное стекло и вносят петлю испытуемой культуры. В присутствии каталазы образуются пузырьки водорода.
15. Приготовление молочно-желточно-солевого агара (МЖСА)
Сухой питательный агар по прописи на этикетке и 90 г хлорида натрия растворяют при нагревании в 1000 мл дистиллированной воды, разливают мерно в сосуды, стерилизуют при 120 °С 20 минут.
Перед употреблением в расплавленный и остуженный до 50 - 55 °С солевой агар добавляют:
- стерильное обезжиренное молоко - 60 мл;
- один яичный желток, тщательно смешанный с 50 мл физиологического раствора с помощью стеклянных бус;
- полимиксин М (раствор хранят не более 14 суток) 300000 ЕД (при наличии постороннего роста).
Тщательно смешивают и разливают в чашки Петри.
|
Заместитель
Главного |
В.И. Чибураев |