ИНСТРУКЦИЯ
ПО САНИТАРНО-МИКРОБИОЛОГИЧЕСКОМУ КОНТРОЛЮ
ТУШЕК, МЯСА ПТИЦЫ, ПТИЦЕПРОДУКТОВ, ЯИЦ И
ЯЙЦЕПРОДУКТОВ НА ПТИЦЕВОДЧЕСКИХ И
ПТИЦЕПЕРЕРАБАТЫВАЮЩИХ ПРЕДПРИЯТИЯХ
СОГЛАСОВАНО
Заместитель Главного государственного санитарного врача СССР В.И. Чибураев 30 августа 1990 года
СОГЛАСОВАНО
Генеральный директор ВПНО ''Союзптицепром'' В.И. Фисинин 28 августа 1990 года
УТВЕРЖДАЮ
Начальник Главного управления ветеринарии с Государственной ветеринарной инспекцией В.И. Касюк 30 августа 1990 года
ВВЕДЕНИЕ
Настоящая Инструкция распространяется на все предприятия и цехи по переработке птицы, а также производству и выпуску готовой продукции из нее.
Инструкция предусматривает микробиологический контроль при переработке птицы, признанной ветеринарно-санитарным надзором здоровой, а также производства птицепродуктов, яиц и яйцепродуктов.
Основной задачей микробиологического контроля птицеперерабатывающего предприятия является обеспечение выпуска продукции высокого качества, безопасного в эпидемическом и эпизоотическом отношениях.
Микробиологическому контролю подвергают санитарное состояние производства, поступающие материалы и сырье, продукты в процессе технологической обработки, готовую продукцию.
Результаты микробиологического исследования качества готовой продукции являются ретроспективными и позволяют оценивать санитарно-гигиеническое благополучие предприятия, по ним судят о соблюдении технологических процессов. В случаях ухудшения микробиологических показателей готовой продукции контроль должен быть направлен на выявление источников и причин повышения микробной обсемененности с целью их ликвидации.
Для улучшения санитарно-гигиенического и технологического режимов на предприятиях микробиологическую оценку качества готовой продукции, мойки и дезинфекции технологического оборудования, а также соблюдение личной гигиены следует включать в оценку качества труда цехового персонала при выплате премиальных доплат.
Микробиологические исследования проводят специалисты-микробиологи предприятия. В случае отсутствия названных специалистов на предприятии контроль осуществляют по особому графику контрольно-производственные лаборатории головных предприятий или заключается договор с ветеринарными или другими лабораториями о проведении микробиологических исследований на предприятии с указанием периодичности контроля.
Плановые микробиологические исследования на предприятиях проводят в соответствии с настоящей Инструкцией, исследования по эпидемиологическим показаниям - в соответствии с требованиями территориальной санэпидемслужбы.
1. САНИТАРНО-МИКРОБИОЛОГИЧЕСКИЙ КОНТРОЛЬ НА ПРЕДПРИЯТИЯХ
1.1. Контроль санитарного состояния производства и рук работников
Санитарно-гигиеническое состояние оборудования, тары, инвентаря, рук работников оценивают путем исследования смывов не реже двух раз в месяц, каждой единицы оборудования и каждого работника. Смывы берутся с поверхностей, которые непосредственно контактируют с пищевым сырьем и готовым продуктом.
Взятие смывов осуществляют без предупреждения перед началом работы. Каждый смыв исследуют на выделение бактерий группы кишечных палочек (БГКП), а по мере необходимости определяют содержание аэробных и факультативно-анаэробных микроорганизмов (общее микробное число - ОМЧ на 1 см2 поверхности), а также другие виды микроорганизмов в случае выявления источника обсеменения продуктов (сальмонеллы, клостридии и др.).
Смывы берут стерильными увлажненными ватно-марлевыми тампонами размером 5 - 7 см3, удерживаемыми стерильным пинцетом, или ватными, марлевыми тампонами, закрепленными на стержне из проволоки или дерева.
Тампоны стерилизуют завернутыми в бумагу В случае закрепления тампона на металлической или деревянной палочке, пропущенной через ватную пробку, его вставляют в пробирку с 10 см3 смывной жидкости (водопроводная вода, физраствор, пептонная вода) или с 10 см3 жидкой питательной среды для обнаружения БГКП (среда Кода, Кесслер, Хейфеца и др.). Тампон не должен касаться жидкости. Все вместе стерилизуют при (121 ± 1) °С в течение 30 мин.
Непосредственно перед взятием смыва тампон на палочке увлажняют наклонением пробирки или опусканием тампона вниз. Тампоны без палочки, находящиеся в стерильной чашке Петри, увлажняют стерильной смывной жидкостью из расчета 10 мл на 1 тампон. Смывы крупного оборудования и инвентаря берут с поверхности 100 см2. При взятии смывов с ровной поверхности используют металлические рамки-трафареты, ограничивающие площадь 100 см2. Перед каждым употреблением трафарет обжигают.
После взятия смыва тампон без палочки погружают либо в пробирку со средой для БГКП, либо в пробирку со смывной жидкостью, используемую в дальнейшем для посевов на питательные среды.
Смывы с мелких объектов (поверхность которых менее 100 см2) берут со всей поверхности.
После взятия смыва пробку с тампоном на палочке вновь вставляют в пробирку так, чтобы тампон погрузился в смывную жидкость или жидкую питательную среду для БГКП. Посевы термостатируют при (37 ± 1) °С в течение 18 - 24 ч. В случае помещения тампона в смывную жидкость, она является после тщательного перемешивания исходным материалом для посева.
При определении ОМЧ из смывной жидкости готовят разведения 10-1 и 10-2 и по 1 см3 из приготовленных разведений проводят посев в чашки Петри с заливкой мясо-пептонным агаром или средой, приготовленной из сухого питательного агара, и термостатируют при (30 ± 1) °С в течение 48 ч.
Оставшееся количество смывной жидкости по 1 см3 или тампон засевают в 10 см3 жидкой питательной среды для БГКП и термостатируют, как указано выше.
Допускается контроль на наличие БГКП производить с помощью индикаторных бумажек.
При анализе чистоты рук работников, которые непосредственно соприкасаются с чистым оборудованием или продукцией, смоченным тампоном тщательно обтирают обе ладони и пальцы. Исследования смывов проводят не реже двух раз в месяц. Контроль за обработкой рук проводится перед работой, после туалета, при переходе с одного участка на другой.
При превышении микробиологических показателей в смывах (табл. 1.1.1) проводят внеочередную санитарную обработку объекта в соответствии с Инструкцией по мойке и профилактической дезинфекции на предприятиях мясной и птицеперерабатывающей промышленности с последующим микробиологическим контролем.
Оценка санитарного состояния поверхностей оборудования, тары, инвентаря, соприкасающихся с продуктами, а также рук работников
|
Наименование цеха |
Исследуемый объект |
Исследуемая поверхность (см2) или количество |
БГКП |
ОМЧ КОЕ*/см2 |
||
|
хорошо |
плохо |
хорошо |
плохо |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Переработка птицы и полуфабрикаты |
Крупное оборудование, тара, ванны шпарки, охлаждения, машины снятия оперения и др. |
100 см2 |
Отсутствие |
Наличие |
Менее 5,0×102 |
Более 5,0×102 |
|
Мелкий инвентарь, детали машин (например, потрошителя), мелкая тара |
Вся поверхность (до 100 см2) |
То же |
То же |
- |
- |
|
|
Руки работников |
То же |
" |
" |
- |
- |
|
|
Колбасно-кулинарный |
Крупное оборудование, волчок, мешалка, куттер, тара и др. |
100 см2 |
Отсутствие |
Наличие |
Менее 5,0×102 |
Более 5,0×102 |
|
Мелкий инвентарь, детали машин и др. |
Вся поверхность |
То же |
То же |
- |
- |
|
|
Руки работников |
То же |
" |
" |
- |
- |
|
|
Консервный (консервов общего спроса, диетического и детского питания, спецназначения, пастеризованных консервов) |
Крупное оборудование |
100 см2 |
Отсутствие |
Наличие |
Менее 3,0×102 |
Более 3,0×102 |
|
Мелкие объекты (инвентарь, детали машин и др.) |
Вся поверхность |
То же |
То же |
То же |
То же |
|
|
Консервная банка с крышкой |
То же |
" |
" |
На всей поверхности |
||
|
3,0×102 |
3,0×102 |
|||||
|
Руки работников |
" |
" |
" |
- |
- |
|
|
Производство яичного меланжа, яичного порошка |
Крупное оборудование, тара |
100 см2 |
Отсутствие |
Наличие |
Менее 3,0×102 |
Более 3,0×102 |
|
Мелкий инвентарь |
Вся поверхность |
То же |
То же |
То же |
То же |
|
|
Руки работников |
То же |
" |
" |
- |
- |
|
|
Производство продуктов сублимационной сушки |
Крупное оборудование, тара |
100 см2 |
" |
" |
" |
" |
|
Мелкий инвентарь |
Вся поверхность |
" |
" |
" |
" |
|
|
Руки работников |
То же |
" |
" |
- |
- |
|
|
Пищевых гидролизаторов и ферментных препаратов |
Крупное оборудование |
100 см2 |
" |
" |
" |
" |
|
Мелкий инвентарь |
Вся поверхность |
" |
" |
" |
" |
|
|
Руки работников |
То же |
" |
" |
- |
- |
|
|
Кормовых |
Крупное оборудование |
100 см2 |
" |
" |
" |
" |
|
Мелкий инвентарь |
Вся поверхность |
" |
" |
" |
" |
|
|
Руки работников |
То же |
" |
" |
- |
- |
|
____________
КОЕ* - колониеобразующие единицы.
Результаты микробиологических исследований регистрируют в журнале (Приложение 1).
1.2. Контроль воды и воздуха
Питьевая вода, используемая на бытовые и производственные нужды, должна подвергаться микробиологическому анализу не реже 1 раза в месяц.
Отбор проб и анализ проводят по ГОСТ 18963-73 "Вода питьевая. Методы санитарно-бактериологического анализа".
Пробы воды исследуют на определение количества аэробных и факультативно-анаэробных микроорганизмов (общее микробное число - ОМЧ), на наличие бактерий группы кишечных палочек (БГКП), спор клостридий.
Согласно ГОСТ 2874-82 в 1 см3 не должно содержаться более 1,0×102 КОЕ, число БГКП в 1 л воды (коли-индекс) не более 3, а споры клостридий должны отсутствовать в 100 см3 воды.
Анализ воздуха проводят по показаниям путем размещения во время работы в производственных помещениях открытых чашек Петри со средой для определения ОМЧ и в случаях необходимости со средой для определения количества дрожжей и плесневых грибов. Чашки выдерживают открытыми 5 мин, затем закрывают и термостатируют для определения ОМЧ при (30 ± 1) °С в течение 72 ч, для определения дрожжей и плесневых грибов при (24 ± 1) °С в течение 5 сут. (ГОСТ 26888-86).
Таблица 1.2.2
Санитарная оценка воздуха помещений
|
Объект анализа |
Оценка |
|||||
|
хорошо |
удовлетворительно |
|||||
|
ОМЧ КОЕ |
количество |
ОМЧ КОЕ |
количество |
|||
|
плесеней |
дрожжей |
плесеней |
дрожжей |
|||
|
Выросших на шашках Петри |
||||||
|
Воздух цеховых помещений предприятий |
20 - 50 |
До 5 |
До 5 |
50 - 70 |
До 5 |
До 5 |
|
Воздух остальных помещений предприятия |
30 - 70 |
5 - 10 |
До 5 |
70 - 100 |
10 - 15 |
5 - 10 |
Результаты микробиологических исследований воды и воздуха регистрируют в лабораторном журнале (Приложение 1), где в случае необходимости дополнительно записывают о наличии спор анаэробов в воде и количество плесеней и дрожжей в воздухе.
1.3. Контроль сырья, продуктов в процессе технологической обработки, готовой продукции
1.3.1. Контроль тушек птицы, потрохов, мяса фасованного, бескостного мяса
Тушки кур, цыплят, индеек, индюшат, уток, утят, гусей, цесарок, цесарят, перепелов, а также их потроха (печень, мышечный желудок, сердце), фасованное мясо, бескостное мясо (кусковое и механической обвалки сепарированием) от здоровой птицы подвергают микробиологическому контролю после выработки или перед отгрузкой не реже двух раз в месяц, а также по показаниям производства и требованию ветсанслужбы.
Исследования проводят:
- в партиях для торговли, производства полуфабрикатов, колбасно-кулинарных изделий, сублимационной сушки по показателям ОМЧ и наличия сальмонелл в 25 г продукта, а по показаниям производства и требованиям ветсанслужбы дополнительно по показателям: содержание спор аэробных и факультативно-анаэробных бактерий (бацилл); содержание спор сульфитредуцирующих клостридий (СРК); наличие протея, коагулазоположительных стафилококков, БГКП;
- в партиях для выработки стерилизованных и пастеризованных консервов по показателям: ОМЧ, содержание спор мезофильных клостридий;
- в партиях для выработки консервов детского питания и спецназначения по показателям: ОМЧ, содержание спор мезофильных клостридий, содержание спор термофильных клостридий, содержание спор факультативно-анаэробных термофильных бактерий плоскокислой порчи консервов.
Тушки птицы (с потрохами и внутренними органами) с признаками заболеваний, в сомнительных случаях для установления диагноза по патологоанатомической картине направляют в ветеринарные бактериологические лаборатории.
Для анализа мяса здоровой птицы от партии отбирают не менее трех тушек. Оценку результатов исследования проводят по каждой тушке в отдельности. Отбор проб от каждой тушки проводят одним из трех методов:
- методом вырезания кусочков мышц и других тканей из различных участков тушек;
- методом смыва со всей поверхности тушки смывной стерильной жидкостью;
- методом смыва с поверхности тушки тампоном.
Метод вырезания кусочков тканей (мышц) используют для выявления сальмонелл, а также для определения других микробиологических показателей тушки.
Масса отобранной пробы должна составлять не менее 100 г Пробу измельчают, после чего 25 г продукта используют для исследования на сальмонеллы, а 10 г продукта служат исходным материалом для приготовления серии десятикратных разведений в исследованиях на другие предусмотренные микробиологические показатели (ОМЧ и др.).
Метод смыва со всей поверхности потрошеной тушки смывной стерильной жидкостью (водой), как и метод смыва тампоном, используют для оценки санитарного состояния производства. В смывах определяют микробиологические показатели: ОМЧ, споры клостридий и бацилл, а также другие микроорганизмы по показаниям производства. Оценку тушек птицы на наличие сальмонелл по анализу смывов не производят.
Отбор проб методом смыва со всей тушки проводят следующим образом. Тушку массой не более 0,5 кг помешают в новый пакет из полимерного материала, разрешенного Минздравом СССР для контакта с пищевыми продуктами.
В пакет с тушкой наливают стерильную водопроводную воду в количестве, равном массе тушки, встряхивают содержимое пакета в течение 2 мин. Полученная смывная жидкость служит исходным материалом, из которого готовят серию десятикратных разведений. Расчет количества микроорганизмов проводят на 1 см3 смывной жидкости.
Отбор проб методом смыва стерильным тампоном применим к потрошеным тушкам любой массы. В связи со сложной конфигурацией поверхности тушки птицы применяют фламбированный проволочный металлический трафарет малой площадью (4 см2).
С тушек птицы малых размеров, например, перепелов, смыв берут от разных участков тушки, при этом общая площадь смывной поверхности должна составлять 10 см2. Смыв осуществляют с разных участков тушки одним и тем же стерильным увлажненным тампоном.
Использованный тампон помещают пробирку с 10 см3 стерильной жидкости (водопроводной воды, физраствора, пептонной воды), после чего жидкость тщательно перемешивают.
С тушек крупной птицы (кур, цыплят-бройлеров и др.) общая площадь смывной поверхности должна составлять 100 см2. При этом смыв осуществляют 2 - 5 тампонами и все их помещают в колбу с 100 см3 стерильной жидкости (воды и др. - см. выше). Колбу с тампонами встряхивают в течение 2 мин. Смывная жидкость служит исходным материалом для серии десятикратных разведений. Расчет количества микроорганизмов проводят на 1 см2 поверхности тушки. Отбор проб методами смывов допускается в помещении производственных цехов. Тушки, подвергнутые смывам, допускается использовать для пищевых целей.
В соответствии с требованиями методических указаний "Лабораторная диагностика сальмонеллезов человека и животных, обнаружение сальмонелл в кормах, продуктах питания и объектах внешней среды" (1990 г.) для обнаружения сальмонелл на потрошеных и полупотрошеных тушках используют метод смыва тампоном со всей поверхности тушки. При этом с тушек массой до 3-х кг используют один стерильный тампон, увлажненный предварительно средой обогащения для сальмонелл (забуференной пептонной водой). После взятия смыва тампон помешают в пробирку с 10 см3 пептонной воды.
С тушек массой более 3-х кг для смывов со всей поверхности используют несколько тампонов (число тампонов зависит от размера тушки); после взятия смыва все тампоны помещают в одну колбу со средой обогащения (пептонной водой) из расчета 10 см3 среды на один тампон. Далее исследования проводят по принятой схеме (п. 3.3 настоящей Инструкции).
Для полупотрошеных тушек при исследовании на сальмонеллы используют и паренхиматозные органы (25 г) по ГОСТ 7702.2-74.
При выделении сальмонелл вводится система профилактических и противоэпизотологических мероприятий, предусмотренная Инструкцией по борьбе и профилактике сальмонеллезов у людей и животных.
Отбор проб потрохов и бескостного кускового мяса проводят следующим образом. От партии продукта каждого наименования отбирают из разных мест точечные пробы (10 - 50 г), помещают в стерильную посуду, составляют в ней общую пробу массой не менее 150 г. Измельчают с соблюдением правил асептики, тщательно перемешивают и отбирают навеску 25 г для посева на сальмонеллы и 10 г для приготовления серии десятикратных разведений. Для получения 1 разведения к 10 г мясной массы добавляют 90 см3 стерильной воды или физраствора, или пептонной воды.
Для мышечных желудков и кускового мяса для определения микробиологических показателей, кроме выделения сальмонелл, допускается отбор проб методом смыва в полимерном пакете. При этом общую пробу одного наименования продукта массой не менее 150 г помещают в новый пакет, взвешивают, добавляют стерильную смывную жидкость в количестве, равном массе пробы. Встряхивают в течение 2 мин. 1 см3 смывной жидкости используют для серии последовательных десятикратных разведений.
Расчет количества микроорганизмов проводят для 1 г продукта (табл. 1.3.3) или на 1 см3 смывной жидкости по массе, равной массе пробы продукта.
Санитарная оценка качества тушек птицы, потрохов, бескостного мяса
|
Объект исследования |
Наличие сальмонелл в 25 г продукта |
ОМЧ (КОЕ/г; КОЕ/см3; КОК/см2) |
||
|
хорошо |
удовлетворительно |
плохо |
||
|
Тушки птицы |
Не допускается |
Менее 2,0×105 |
Менее 1,0×107 |
Более 1,0×107 |
|
Потроха (печень с сердцем, мышечные желудки) |
То же |
То же |
То же |
То же |
|
Мясо бескостное кусковое |
То же |
То же |
То же |
То же |
|
Мясо мехобвалки |
То же |
Менее 1,0×106 |
То же |
То же |
Превышение уровня бактериальной обсемененности продуктов, приведенного в табл. 1.3.3, свидетельствует о неудовлетворительном санитарном состоянии производства и качества продуктов.
Результаты микробиологических исследований регистрируют в журнале (Приложение 2).
При показателе ОМЧ более 1,0×107 КОЕ/г при отсутствии признаков органолептической порчи названные выше продукты не подлежат хранению в охлажденном состоянии. Их срочно отправляют на заморозку или на изготовление термически обработанных продуктов. Реализация их в охлажденном состоянии возможна в течение 4 - 6 ч. Партии продукта с показателем ОМЧ более 1,0×107 КОЕ/г и признаками органолептической порчи направляют на утилизацию.
При обнаружении сальмонелл в нереализованных партиях тушек птицы, бескостного кускового мяса, мяса мехобвалки эти партии должны быть направлены на изготовление консервов в соответствии с Правилами ветеринарного осмотра убойных животных и ветеринарно-санитарной экспертизы мяса и мясных продуктов (1988 г.).
1.3.2. Контроль полуфабрикатов кусковых и рубленых
Полуфабрикаты из мяса птицы подвергают микробиологическому контролю после выработки или перед отгрузкой не реже 2 раз в месяц, а также по требованию ветслужбы.
От партии кусковых и рубленых одного наименования полуфабрикатов отбирают не менее трех образцов. Из них готовят общую среднюю пробу массой не менее 50 г Для этого в стерильную посуду отбирают равные массы от каждого образца, кусочки мякотных тканей из разных участков полуфабрикатов, измельчают при соблюдении правил асептики. Из подготовленной средней пробы 25 г продукта используют для посева для выделения сальмонелл, а 10 г продукта - для серии последовательных десятикратных разведений.
Для кусковых полуфабрикатов допускается отбор проб от каждого образца методом смыва в новом полимерном пакете. Оценку результатов проводят по каждому образцу в отдельности. Каждый образец кускового полуфабриката помещают в стерильный пакет, взвешивают. В пакет с образцом наливают стерильную воду в количестве, равном массе исследуемого полуфабриката. Встряхивают в течение 2 мин. Смывную жидкость в количестве 1 см3 используют для приготовления серии десятикратных разведений (табл. 1.3.4). Образцы, подвергнутые смыву, пригодны для пищевых целей.
Таблица 1.3.4
Санитарная оценка качества полуфабрикатов при микробиологическом контроле
|
Вид полуфабрикатов |
Наличие сальмонелл в 25 г |
ОМЧ (КОЕ/г; КОЕ/см3) |
||
|
хорошо |
удовлетворительно |
плохо |
||
|
Кусковые |
Не допускается |
Менее 2,0×105 |
2,0×105 - 1,0×107 |
Более 1,0×107 |
|
Рубленые |
Не допускается |
5,0×105 |
6,0×105 - 1,0×107 |
Более 1,0×107 |
При обнаружении сальмонелл в полуфабрикатах нереализованных партий эти партии должны быть направлены на изготовление консервов в соответствии с Правилами ветсанэкспертизы.
Нереализованные полуфабрикаты с показателем ОМЧ более 1,0×107 КОЕ/г при отсутствии признаков органолептической порчи не подлежат хранению в охлажденном состоянии. Их срочно отправляют или на заморозку, или на тепловую обработку для получения готовых кулинарных изделий. Мясопродукты с показателем ОМЧ более 1,0×107 КОЕ/г и признаками органолептической порчи направляют на утилизацию.
При производстве полуфабрикатов из мяса птицы каждую партию материалов, припасов рецептурных компонентов, применяемых в производстве, подвергают микробиологическому контролю на ОМЧ, БГКП, а также в том случае, если при контроле технологических процессов и готовой продукции выявляется необходимость проверить, не являются ли припасы рецептурных компонентов и материалы источником бактериального загрязнения или загрязнения другими, не свойственными технологическому процессу микроорганизмами.
В необходимых случаях производят дополнительные исследования на специфическую для данного вида материалов, припасов микрофлору (таблица 1.3.5).
Таблица 1.3.5
Микробиологические показатели для оценки результатов контроля материалов и припасов рецептурных компонентов
|
Контролируемый объект |
ОМЧ (КОЕ/г) |
БГКП в 1 г |
Специфическая микрофлора |
||
|
хорошо |
плохо |
хорошо |
плохо |
||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
Пергамент (100 см2) |
Менее 100 |
|
Отсутствие |
Наличие |
Наличие грибов 10 - плохо |
|
Полимерные подложки (100 см2) |
То же |
|
То же |
|
То же |
|
Полимерные пакеты (100 см2) |
Менее 100 |
|
Отсутствие |
|
Наличие грибов 10 - плохо |
|
Соль |
Менее 100 |
|
- |
- |
- |
|
Мука, крахмал |
1,0×104 |
|
- |
- |
- |
1.3.3. Контроль колбасно-кулинарных изделий
Готовую продукцию колбасно-кулинарного производства подвергают микробиологическому контролю в сроки, предусмотренные "Указанием о применении метода микробиологического анализа колбасных изделий и продуктов из мяса в производственных лабораториях предприятий мясной промышленности" для групп продуктов из мяса птицы:
вареных, запеченных, жареных - не реже 1 раза в 15 дней;
копчено-вареных, копчено-запеченных - не реже 1 раза в месяц;
колбас ливерных, студней, паштетов - не реже 1 раза в 5 дней.
Исследования колбасно-кулинарных изделий с использованием мяса птицы, потрохов, яиц проводят по показателям: ОМЧ, наличия БГКП в 1 г продукта, сальмонелл в 25 г, коагулазоположительных стафилококков в 1 г, сульфитредуцирующих клостридий в 0,1 г; 0,01 г (ГОСТ 9958-81).
Отбор проб производят после выработки продукции или перед отгрузкой. Для анализа от партии готовой продукции отбирают не менее двух образцов. Из каждого образца в отдельности готовят объединенную пробу массой не менее 50 г, составленную из кусочков следующим образом.
Колбасные изделия в оболочке и кулинарные изделия в оболочке помещают в металлический или эмалированный тазик (поддон), тщательно протирают ватным тампоном, смоченным спиртом, и дважды обжигают над пламенем горелки.
Затем батоны разрезают продольно стерильным (фламбированным) ножом или скальпелем на две половинки, не рассекая оболочку противоположной стороны батона. Пробу отбирают из нескольких участков центральной части и из-под оболочки обеих половинок батона.
Из кулинарных продуктов в оболочке из мяса птицы на костях и бескостных из различных участков обожженного образца вырезают кусочки предпочтительно ближе к кости.
Изделия без оболочки (палочки куриные, паштеты и др.) исследуют с поверхности и в глубине продукта. Для анализа поверхности изделий без оболочки после развертывания упаковки с поверхности исследуемых образцов делают смыв (с каждого образца новым стерильным увлажненным тампоном) с тех участков, с которыми могли соприкасаться руки упаковщиков. Тампоны помещают в пробирки с жидкой питательной средой (среда Хейфеца, Кесслер) для выделения БГКП.
Для анализа глубинных участков неупаковочного продукта образцы помещают в металлический или эмалированный тазик (поддон), смачивают спиртом и обжигают. Затем делают продольный разрез и отбирают навеску методом, указанным для колбасных изделий и продуктов в оболочке, составляя из них одну объединенную пробу для каждого образца в отдельности, которую помещают в предварительно взвешенную стерильную посуду.
Объединенную пробу каждого образца измельчают с соблюдением правил асептики.
Из каждой пробы по 25 г высевают для определения сальмонелл, а 10 г для приготовления десятикратных разведений (табл. 1.3.6).
Таблица 1.3.6
Допустимые микробиологические показатели для колбасно-кулинарных изделий из птицепродуктов
|
№ пп |
Наименование продуктов |
ОМЧ (КОЕ/г) |
отсутствие в продукте (г) |
|||
|
БГКП |
сальмонеллы |
стафилококки коагулазоположительные |
сульфитредуцирующие клостридии |
|||
|
1. |
Вареные колбасы |
5×102 - 1×103 |
1,0 |
25 |
1,0 |
0,1 |
|
2. |
Мясные хлебы |
1×103 |
1,0 |
25 |
1,0 |
0,1 |
|
3. |
Сосиски, сардельки |
1×103 |
1,0 |
25 |
1,0 |
0,1 |
|
4. |
Яичные колбаски |
1×103 |
1,0 |
25 |
1,0 |
0,1 |
|
5. |
Ливерные колбаски с растительными добавками |
2×102 - 5×103 |
0,5 |
25 |
1,0 |
0,1 |
|
6. |
Варено-копченые колбасы, изделия |
1×103 |
1,0 |
25 |
1,0 |
0,1 |
|
7. |
Готовые рубленые изделия |
5×102 - 1×103 |
0,5 |
25 |
1,0 |
0,1 |
|
8. |
Паштеты |
1×103 |
0,1 - 1,0 |
25 |
0,1 |
0,1 |
|
9. |
Тушки и изделия запеченные, копчено-запеченные |
1×103 |
1,0 |
25 |
1,0 |
0,1 |
При получении неудовлетворительных результатов все последующие мероприятия направлены на установление источников и причин выпуска продукции, не соответствующей санитарным требованиям по микробиологическим показателям, и устранение этих источников и причин.
Для этой цели проводят серии микробиологических исследований. При превышении норматива ОМЧ готовой продукции исследуют содержание спор бацилл в сырье; показатель ОМЧ тары для готовой продукции; ОМЧ упаковочных материалов.
При превышении норматива БГКП готовой продукции необходимо проверять правильность режимов тепловой обработки продуктов, обсемененность БГКП тары, инвентаря, упаковочных материалов, рук работников, контактирующих с продуктом.
При обнаружении сальмонелл, стафилококков в готовой продукции проводят бактериологические исследования тех же объектов, которые приведены выше для БГКП.
При превышении норматива сульфитредуцирующих клостридий в готовой продукции исследуют сырье на споры названных клостридий, а также тару, инвентарь, упаковочные материалы, руки работников на наличие вегетативных и споровых клеток сульфитредуцирующих клостридий.
Результаты микробиологических исследований готовых колбасно-кулинарных изделий из мяса птицы и птицепродуктов записывают в журнале по форме Приложения 3.
Результаты микробиологических исследований оборудования, тары, инвентаря, упаковочных материалов, рук работников регистрируют в журнале по форме Приложения 1.
Результаты микробиологических исследований сырья - в журнале по форме Приложения 2.
1.3.4. Контроль продуктов сублимационной сушки
Продукты сублимационной сушки на основе мяса птицы и яиц, полученные из качественного сырья, подвергают микробиологическому контролю после выработки. Исследуют каждую партию продукта. Для микробиологических анализов отбирают 1 % упаковок от каждой партии, но не менее трех единиц.
Микробиологические исследования проводят по следующим показателям: ОМЧ, БГКП и наличие сальмонелл в 25 г восстановленного продукта, а по показаниям производства и требованиям ветсанслужбы дополнительно определяют содержание спор и вегетативных форм сульфитредуцирующих клостридий (СРК) в 0,1 г продукта, коагулазоположительных стафилококков в 1 г продукта.
Вскрытие упаковок с продуктом, подготовленных к микробиологическому анализу, приготовление разведений и высев продукта в питательные среды проводят в боксе при соблюдении асептических условий.
Упаковку с пробой (пакет из фольги и пр.) вскрывают в месте, предварительно обработанном тампоном, пропитанным спиртом, который удаляют путем свободного испарения, затем упаковку вскрывают и отбирают массу (объем) продукта в количестве, необходимом для приготовления одной или нескольких навесок. Масса (объем) должна быть установлена в НТД на конкретный вид продукта или метод анализа, но не менее 50 г.
Навеску от проб порошкообразных или сыпучих продуктов отбирают стерильной ложкой или шпателем из разных мест продукта, затем переносят в предварительно взвешенную стерильную посуду с крышкой, взвешивают. К навеске добавляют стерильные физраствор или пептонную воду в количестве, необходимом для приготовления исходного разведения. Смесь перемешивают или взбалтывают до получения однородной консистенции продукта.
Навеску от проб набухающих в воде продуктов отбирают и готовят исходное разведение в соответствии с требованиями НТД на конкретный вид продукта.
Навеску от проб нерастворимых в воде твердых продуктов гомогенизируют в случаях, указанных в НТД. Допускается гомогенизацию нестерильного продукта проводить путем растирания его до достижения однородной консистенции в стерильной ступке с соблюдением условий асептики.
Если это проба мяса сублимированного (ломтики), то отбор проводится от различных кусочков, затем все измельчают с помощью стерильных ножниц и пинцета, постепенно добавляя 90 см3 физраствора или пептонной воды, а затем проводят гомогенизацию. Полученную взвесь выдерживают при температуре (18 - 20) °С в течение 15 мин для осаждения крупных частиц. Верхний слой суспензии используют для проведения микробиологических анализов. Первое десятикратное разведение навески является исходным. Из него получают последующие разведения.
Интервал между приготовлением продукта, его разведением и посевом в питательные среды не должен превышать 30 мин.
Главной отличительной особенностью при подготовке пробы сублимированного продукта является то, что продукт предварительно необходимо восстановить, а затем проводить его исследование.
Проведение микробиологических анализов и обработка полученных результатов проводятся по общепринятым методикам (табл. 1.3.7).
Таблица 1.3.7
Допустимые микробиологические показатели для продуктов сублимационной сушки
|
Наименование продукта |
Определение бакпоказателей |
|
|
наименование показателя |
допустимые величины не более |
|
|
Мясо цыплят сублимационной сушки для лечебного и диетического питания детей "Цыпленок" |
ОМЧ в 1 г продукта |
1,0×104 |
|
БГКП в 1 г продукта |
Не допускаются |
|
|
Сальмонеллы в 25 г восстановленного продукта |
Не допускаются |
|
|
Стафилококки коагулазоположительные в 1 г продукта |
Не допускаются |
|
|
Фарш из мяса цыплят сублимационной сушки |
ОМЧ в 1 г |
1,0×104 |
|
БГКП в 0,001 г продукта |
Не допускаются |
|
|
Патогенные бактерии, в т.ч. сальмонеллы в 25 г восстановленного продукта |
Не допускаются |
|
|
Яйцепродукты сублимационной сушки: порошок, желток, белок |
БГКП в 0,01 г продукта (белок в 1 г) |
Не допускаются |
|
Сальмонеллы в 25 г продукта |
Не допускаются |
|
|
Протей в 0,1 г продукта |
Не допускаются |
|
Если после микробиологического анализа будут получены неудовлетворительные результаты, то данную партию продукта необходимо подвергнуть вторичной проверке. При этом отбор проб проводится так же, но количество образцов, отобранных для проведения анализов, увеличивается в два раза.
Если при повторном исследовании установлено, что микробиологические показатели партии соответствуют санитарным требованиям, то продукт реализуют в соответствии с НТД.
Для установления источника и причин получения недоброкачественной продукции необходимо провести микробиологический анализ сырья в процессе технологической обработки, санитарного состояния оборудования, инвентаря, тары и т.д. Анализ следует проводить с учетом тех показателей, по которым данная партия продукта после его выработки не соответствовала санитарным требованиям.
При превышении норматива ОМЧ в продуктах, не подвергавшихся тепловой обработке перед сублимационной сушкой, контролируют показатель ОМЧ сырья, оборудования, тары, упаковки, рук работников.
В продуктах, прошедших тепловую обработку перед сублимационной сушкой, при превышении ОМЧ, кроме исследований, перечисленных выше, проводят исследования на содержание спор бацилл в сырье; при превышении показателей БГКП, сальмонелл, стафилококков основное внимание уделяют проверке режимов тепловой обработки; при превышении норматива сульфитредуцирующих клостридий (СРК) исследуют сырье на содержание спор СРК (табл. 1.3.8).
Таблица 1.3.8
Микробиологические требования к сырью для продуктов сублимационной сушки
|
Наименование микроорганизмов |
Отсутствие в массе мясного сырья, г |
|
БГКП |
0,001 |
|
Сальмонеллы |
25 |
|
Протей |
0,1 |
|
Споры СРК |
0,1 |
|
Споры бацилл |
0,001 |
|
Стафилококки коагулазоположительные |
1,0 |
Результаты микробиологических исследований оборудования, тары, инвентаря, упаковочных материалов, рук работников регистрируют в журнале по форме Приложения 1, а результаты микробиологических исследований сырья, продуктов в процессе технологической обработки, готовой продукции - в журнале по форме Приложений 2 и 3.
1.3.5. Контроль консервов
В соответствии с положениями Инструкции о порядке санитарно-технического контроля на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания консервы из птицепродуктов стерилизованные относятся к группе А, а пастеризованные - к группе Д.
Микробиологический контроль консервов каждой группы имеет свои особенности, но во всех случаях при их производстве ежесменно осуществляют микробиологический контроль консервных банок и крышек перед их наполнением путем исследования смывов с одной единицы тары в начале, середине и в конце смены. Допустимые микробиологические показатели консервных банок и крышек приведены в табл. 1.1.1. Результаты микробиологического контроля регистрируют в рабочем журнале (Приложение 4).
1.3.5.1. Контроль стерилизованных консервов
Основой микробиологического контроля этой группы консервов в условиях производства является систематическая проверка микробной обсемененности содержимого банок перед стерилизацией, периодический контроль сырья, полуфабрикатов и вспомогательных материалов, входящих в состав консервов.
Исследования содержимого консервов перед стерилизацией проводят по следующим показателям: ОМЧ, наличие спор мезофильных облигатных анаэробов в 0,5 см3 или в 0,5 г продукта, а в случаях, предусмотренных нормативно-технической документацией, - наличие спор термофильных анаэробных бактерий в 0,5 см3 или в 0,5 г продукта; содержание в 1 г продукта спор термофильных бактерий, возбудителей плоскокислой порчи консервов.
Для анализа продукта перед стерилизацией от каждой партии консервов отбирают по 3 образца не ранее чем через час после начала работы линии.
Контроль сырья, полуфабрикатов, вспомогательных материалов, входящих в состав консервов, проводят в случаях превышения микробиологических показателей продукта перед стерилизацией с целью установления и ликвидации источника повышенной бактериальной обсемененности продукта перед стерилизацией (табл. 1.3.9).
Таблица 1.3.9
Допустимые микробиологические показатели продукта перед стерилизацией сырья и других компонентов
|
№ пп |
Наименование продукта перед стерилизацией |
ОМЧ (КОЕ/г) не более |
Споры |
||
|
мезофилов-клостридий |
термофилов |
||||
|
клостридий |
плоской порчи консервов (КОЕ/г) |
||||
|
1. |
Мясо птицы в собственном соку |
5,0×105 |
В 0,5 г или 0,5 см3 не допускаются |
В 0,5 г или в 0,5 см3 не допускаются |
Менее 5,0 |
|
2. |
Фаршевые консервы из мяса птицы |
1,0×106 |
То же |
То же |
То же |
|
3. |
Паштетные консервы из мяса птицы |
5,0×104 |
" |
" |
" |
|
4. |
Мясо-растительные консервы при закладке мяса птицы с: |
|
|
|
|
|
|
предварительной тепловой обработкой |
5,0×104 |
" |
" |
" |
|
|
без предварительной тепловой обработки |
5,0×105 |
" |
" |
" |
|
5. |
Мясо тушек птицы |
5,0×105 |
В 0,1 г не допускается |
В 0,1 г не допускается |
Менее 10 |
|
6. |
Кусковое бескостное мясо птицы |
5,0×105 |
То же |
То же |
То же |
|
7. |
Мясо птицы механической обвалки, полученное сепарированием |
1,0×106 |
" |
" |
" |
|
8. |
Бланшированное мясо птицы |
2,0×104 |
" |
" |
" |
|
9. |
Растительные компоненты |
5,0×104 |
" |
" |
" |
Результаты микробиологического исследования продукта перед стерилизацией сырья и прочих продуктов регистрируют в журнале (Приложение 5).
Готовые консервы (не менее трех банок от партии) исследуют на промышленную стерильность, определяя наличие мезофильных аэробных и факультативно-анаэробных микроорганизмов в 1 г продукта, облигатных анаэробов в 1 г по методам ГОСТ 10444.3-85 (Консервы. Метод определения мезофильных аэробных и факультативно-анаэробных микроорганизмов); ГОСТ 10444.4-85 (Консервы. Метод определения мезофильных анаэробных микроорганизмов); а в случаях необходимости и по ГОСТ 10444.5-85 (Консервы. Метод определения термофильных аэробных и факультативно-анаэробных микроорганизмов); ГОСТ 10444.6-85 (Консервы. Метод определения термофильных анаэробных микроорганизмов).
В случаях обнаружения в 1 г готовых консервов клостридий или неспорообразующих микроорганизмов в готовых консервах проводят дополнительные микробиологические исследования в соответствии с положениями Инструкции о порядке санитарно-технического контроля консервов на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания.
Вопрос о реализации консервов решают в соответствии с положениями Инструкции о порядке санитарно-технического контроля консервов на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания.
1.3.5.2. Контроль пастеризованных консервов
Микробиологический контроль пастеризованных консервов из мяса птицы проводят в соответствии с положениями контроля консервов группы Д Инструкции о порядке санитарно-технического контроля консервов на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания с учетом нижеизложенного.
Основой является контроль санитарного состояния оборудования, сырья, материалов, продукта перед тепловой обработкой, готовой продукции.
Контроль оборудования, тары, инвентаря, рук работающих проводят по пункту 1.1 настоящей Инструкции.
Контроль продукта перед пастеризацией сырья, материалов проводят по следующим показателям: ОМЧ, наличие или содержание в 1 г продукта спор мезофильных облигатных анаэробов; спор мезофильных аэробных и факультативно-анаэробных микроорганизмов (табл. 1.3.10).
Таблица 1.3.10
Периодичность исследования и допустимые микробиологические показатели продукта перед пастеризацией сырья, материалов
|
Наименование продукта |
Периодичность контроля |
ОМЧ |
Споры |
|
|
клостридий |
аэробов и факульт.- анаэробов |
|||
|
Консервируемый продукт перед пастеризацией |
Каждая партия |
2,0×105 |
В 0,5 г продукта не допускаются |
10 КОЕ/г |
|
Тушка птицы |
Не реже 2-х раз в месяц и по усмотрению ОПВК |
2,0×105 |
То же |
То же |
|
Рассол |
То же |
1,0×103 |
" |
В 1 см3 не допускаются |
Отбор проб продукта перед пастеризацией производят из 3-х банок от каждой партии консервов, при этом в начале, середине и конце процесса расфасовки продукта в банки из одной незакатанной банки при соблюдении правил асептики отбирают не менее 50 г продукта и проводят микробиологические исследования каждого образца. Результаты оценивают по каждой банке отдельно.
Отбор проб от тушек птицы проводят согласно п. 1.3.1 настоящей Инструкции.
Отбор проб рассола производят перед закладкой в него мяса птицы.
Микробиологические исследования по определению ОМЧ проводят по общепринятым методикам, а наличие содержания спор - в соответствии с положением Инструкции о порядке санитарно-технического контроля консервов на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания и п. 1.3.5.1 настоящей Инструкции.
Контроль готовых пастеризованных консервов каждой партии проводят по следующим показателям: ОМЧ; коагулазоположительных стафилококков, бациллус цереус; наличие клостридий мезофилов в 1 г и 0,1 г продукта; наличие сальмонелл в 25 г продукта; БГКП в 1 г продукта (табл. 1.3.11).
Таблица 1.3.11
Микробиологические показатели пастеризованных консервов из мяса птицы
|
№ пп |
Наименование показателей |
Количество исследуемого продукта, г |
Нормируемая величина |
|
1. |
ОМЧ |
1,0 |
2,0×102 КОЕ/г |
|
2. |
Наличие стафилококков |
1,0 |
Не допускается |
|
3. |
Наличие Bacillus cereus |
0,1 |
Не допускается |
|
4. |
Наличие сальмонелл |
25,0 |
Не допускается |
|
5. |
Наличие мезофильных клостридий |
0,1 |
Не допускается |
|
6. |
Наличие патогенных и токсигенных мезофильных клостридий |
1,0 |
Не допускается |
Отбор проб проводят сразу после изготовления пастеризованных консервов, не менее 3 банок от каждой партии. Пастеризованные консервы исследуют по следующим ГОСТам: 10444.3-85; 10444.4-85; 10444.2-75; 10444.7-86; 10444.8-88; 10444.9-88; 10444.15-75; 9958-81.
1.3.6. Контроль продуктов детского и диетического питания
К названной группе продуктов относятся консервы для питания детей раннего возраста (до 1 года); консервы для питания детей дошкольного и школьного возраста, а также взрослых, нуждающихся в диетическом питании; готовые колбасно-кулинарные изделия для детского и диетического питания; полуфабрикаты для детского и диетического питания.
Санитарно-микробиологический контроль производства названных продуктов проводят в соответствии с Санитарно-гигиеническими требованиями к производству мясных консервов для питания детей раннего возраста; Инструкцией о порядке санитарно-технического контроля консервов на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания; нормативно-технической документацией на продукты; требованиями настоящей Инструкции.
Контроль производства продуктов детского питания предусматривает визуальную оценку и микробиологический контроль оборудования, тары и т.п., сырья, рецептурных компонентов, продукта в процессе технологической обработки, а также готового продукта.
Контроль санитарного состояния оборудования, тары, инвентаря и рук работников проводят в соответствии с п. 1.1 настоящей Инструкции. Результаты микробиологического контроля регистрируют в рабочем журнале (Приложение 1).
1.3.6.1. Контроль консервов для питания детей раннего возраста
Контроль этой группы продуктов при их производстве включает в себя микробиологическую проверку всех тех объектов, которые предусмотрены для стерилизованных консервов (п. 1.3.5), а именно: систематическую проверку микробной обсемененности содержимого банок перед стерилизацией, периодический контроль сырья, полуфабрикатов, вспомогательных материалов, входящих в состав консервов, а также обязательный контроль готовых консервов на промышленную стерильность.
Исследование содержимого консервов перед стерилизацией проводят по следующим показателям: ОМЧ, наличие спор облигатных мезофильных анаэробов в 0,5 см3 или в 0,5 г продукта; наличие спор облигатных термофильных анаэробов в 0,5 см3 или в 0,5 г продукта; содержание в 1 г (1 см3) продукта спор термофильных бактерий, возбудителей плоскокислой порчи консервов.
Для анализа продукта перед стерилизацией от каждой партии консервов отбирают не менее трех образцов.
Контроль сырья, полуфабрикатов, вспомогательных материалов проводят периодически (табл. 1.3.12), а также в случаях превышения микробиологических показателей перед стерилизацией с целью установления и ликвидации источника повышенной микробной обсемененности продукта.
Таблица 1.3.12
Периодичность микробиологического контроля сырья и других рецептурных компонентов продукта перед стерилизацией
|
Объект исследования |
Периодичность контроля |
Определяемые показатели |
Допустимое число микроорганизмов (не более) |
|
1 |
2 |
3 |
4 |
|
Тушки птицы |
По графику, утвержденному ОПВК предприятия |
ОМЧ |
2,0×105 КОЕ/г |
|
Споры анаэробов: |
В 0,1 г/см3 продукта не допускается |
||
|
мезофилов |
|||
|
термофилов |
|||
|
Субпродукты |
" |
ОМЧ |
2,0×105 КОЕ/г |
|
Споры анаэробов: |
В 0,1 г/см3 продукта не допускается |
||
|
мезофилов |
|||
|
термофилов |
|||
|
Ингредиенты (крахмал, мука) |
Каждая поступающая партия и по графику |
ОМЧ |
1,0×104 |
|
Споры анаэробов: |
В 0,1 г/см3 продукта не допускается |
||
|
мезофилов |
|||
|
термофилов |
|||
|
Консервируемый продукт перед стерилизацией |
Ежесменно |
ОМЧ |
2,0×102 - при горячей фасовке; |
|
1,0×104 - при холодной фасовке |
|||
|
Споры анаэробов: |
В 0,5 г/см3 продукта не допускается |
||
|
мезофилов |
|||
|
тормофилов |
|||
|
Споры термофилов плоско-кислой порчи |
5 КОЕ/г |
||
|
Готовая продукция |
Каждая партия |
Мезофилы - ОМЧ |
5,0×101 |
|
Мезофилы - анаэробы |
Не допускается |
||
|
Термофилы |
В соответствии с п. 28 Инструкции о порядке санитарно-технического контроля на производственных предприятиях |
Результаты микробных исследований продукта перед стерилизацией сырья и вспомогательных материалов регистрируют в журнале (Приложение 2).
Готовые консервы каждой партии подвергают микробиологическому контролю на промышленную стерильность. При этом для исследований отбирают не менее 3 банок консервов для выявления мезофильных микроорганизмов (по методам ГОСТ 10444.3-85, ГОСТ 10444.4-85) и не менее 3 банок консервов для выявления термофильных микроорганизмов (по методам ГОСТ 10444.5-85, ГОСТ 10444.6-85).
Результаты микробиологических исследований готовых консервов регистрируют в журнале (Приложение 5).
Оценку и реализацию партии готовой продукции проводят в соответствии с Санитарно-гигиеническими требованиями к производству мясных консервов для питания детей раннего возраста и Инструкцией о порядке санитарно-технического контроля консервов на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания.
1.3.6.2. Контроль консервов для питания детей дошкольного и школьного возраста и для диетического питания
Микробиологический контроль названной группы продуктов проводят в соответствии с требованиями Инструкции о порядке санитарно-технического контроля консервов на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания и п. 1.3.5 настоящей Инструкции.
1.3.6.3. Контроль готовых колбасно-кулинарных изделий и полуфабрикатов для детского и диетического питания
Контроль производства полуфабрикатов для детского и диетического питания и готовых колбасно-кулинарных изделий проводят в соответствии с пунктами 1.3.2 и 1.3.3 настоящей Инструкции.
По микробиологическим показателям полуфабрикаты для детского и диетического питания должны соответствовать требованиям, представленным в табл. 1.3.13.
Таблица 1.3.13
Микробиологические показатели полуфабрикатов для детского и диетического питания
|
Вид полуфабрикатов |
Наличие сальмонелл в 25 г |
ОМЧ (КОЕ/г; КОЕ/см3) не более |
|
Кусковые |
Не допускается |
1,0×106 |
|
Рубленые |
Не допускается |
5,0×106 |
При превышении микробиологических показателей (табл. 1.3.13) проводят мероприятия, как указано в п. 1.2 настоящей Инструкции.
Готовые колбасно-кулинарные изделия для детского и диетического питания по микробиологическим показателям должны соответствовать требованиям, представленным в табл. 1.3.14.
Таблица 1.3.14
Допустимые микробиологические показатели колбасно-кулинарных изделий для детского и диетического питания
|
Вид продукта |
ОМЧ (КОЕ/г) не более |
Отсутствие в продукте (г) |
|||
|
БГКП |
сальмонеллы |
стафилококки коагулазоположит. |
сульфитредуцирующие клостридии |
||
|
Колбасы |
1,0×103 |
1 |
25 |
1 |
0,1 |
|
Готовые рубленые изделия |
1,0×103 |
1 |
25 |
1 |
0,1 |
При превышении микробиологических показателей (табл. 1.3.14) проводят мероприятия, как указано в п. 1.3 настоящей Инструкции.
1.3.7. Контроль продуктов ферментированного гидролиза и пепсина
Продукты ферментированного гидролиза: бульон пищевой, полученный из малоценных пищевых продуктов (голов, ног, шей, крыльев и костного остатка от механической обвалки кур, цыплят и цыплят-бройлеров), кормовая белковая добавка, полученная из технических отходов переработки птицы (кровь, кишечник, зоб, железистый желудок, пищевод, трахея, почки, селезенка, яйцевод, яичники, желчный пузырь, несформировавшиеся яйца, легкие, ветконфискаты и тушки павшей птицы, допущенные ветеринарно-санитарным надзором к переработке на кормовые продукты, головы и ноги, не используемые на пищевые цели; перо покровное, разрешенное к использованию на кормовые цели, подкрылок цыплят, цыплят-бройлеров и кур ОСТ 49 136-82, отходы от выработки перо-пухового сырья), и пепсин (куриный) пищевой, применяемый в сыродельной промышленности при производстве сыров и других молочных продуктов, подвергают микробиологическому контролю. Исследуется каждая партия выработанного продукта.
Отбор проб для микробиологических анализов производят до отбора на физико-химические и органолептические анализы.
Посуду, инструменты и материалы, соприкасающиеся с продуктом во время отбора проб, стерилизуют в автоклаве при температуре (121 ± 1) °С в течение 30 мин или погружением в этиловый спирт с последующим фламбированием.
Пробы от пищевых бульонов и кормовых белковых добавок отбирают асептическим способом в стерильную посуду. Масса точечных проб из различных мест и глубины продукта не должна быть менее 100 г, а общая масса объединенной пробы не менее 500 г.
Пробы пепсина отбирают из разных мест партии в объеме 1 % банок или пакетов, но не менее трех. Из каждой отобранной единицы берут точечную пробу пепсина массой 100 г.
Микробиологические исследования проводят по следующим показателям: ОМЧ, БГКП, наличие сальмонелл в 25 г, дополнительно в продуктах ферментативного гидролиза определяют содержание сульфитредуцирующих клостридий (СРК).
Проведение микробиологических анализов и обработка полученных результатов проводятся по общепринятым методикам (табл. 1.3.15).
Таблица 1.3.15
Санитарные требования к продуктам ферментированного гидролиза и пепсина
|
Наименование показателей |
Бульон пищевой |
Добавка кормовая белковая |
Пепсин куриный |
|
1. Общее количество микроорганизмов в 1 г |
5,0×104 |
5,0×105 |
8,0×103 |
|
2. БГКП не допускаются в г |
1,0 |
1,0 |
3,0 |
|
3. Сальмонеллы не допускаются в г ГОСТ 25311-82 |
25 |
50 |
25 |
|
4. Сульфитредуцирующие клостридии в 1 г не более |
50 |
- |
- |
Примечание: (-) не нормируются.
1.3.8. Контроль яиц, мороженых и сухих яйцепродуктов
Настоящий раздел Инструкции распространяется на все соответствующие цехи производства яйцепродуктов птицеводческих и птицеперерабатывающих предприятий (птицефабрики, птицекомбинаты).
Он включает санитарно-микробиологический контроль поступающего сырья (яиц куриных), готовых продуктов: яичного меланжа, яичного порошка, сухого яичного белка, сухого яичного желтка, а также контроль соблюдения технологических и санитарно-гигиенических режимов производства яйцепродуктов. Контроль санитарного состояния производства и рук работников проводят в соответствии с п. 1.1 настоящей Инструкции.
Для микробиологического анализа яиц, предназначенных для производства яйцепродуктов, отбирают из разных мест партии методом случайной выборки пробу в количестве 30 штук.
Отобранные пробы упаковывают в чистую тару и транспортируют в условиях, исключающих их повреждение и вторичную контаминацию.
При микробиологическом исследовании содержимого яиц поверхность скорлупы яиц обмывают щелочным теплым (30 ± 2) °С раствором 0,2 %-ной концентрации каустической соды или 0,5 %-ной кальцинированной соды в течение 1,5 - 2 мин. После мойки яйцо ополаскивают водопроводной водой, дают воде стечь, яйцо погружают в этиловый (70 %) спирт, после смачивания спиртом обжигают пламенем.
На остром конце яйца делают стерильным скальпелем отверстие диаметром около 1 см и тоже обжигают. Содержимое одного яйца или нескольких яиц выливают в широкогорлую колбу Эрленмейера и смешивают с помощью стерильных бус или палочками. Полученный гомогенат обрабатывают сразу.
10 см3 яичной массы (пробы) с помощью стерильной пипетки переносят в колбу, содержащую 90 см3 физиологического раствора хлористого натрия, и получают таким образом разведение 1:10 (разведение 1). После перемешивания 1 см3 разведения 1 переносят с помощью пипетки в пробирку, содержащую 9 см3 физиологического раствора, и получают таким образом разведение 1:100 (разведение 2). Подобным методом получают требуемое количество других разведений.
При микробиологическом исследовании поверхности скорлупы яиц используют смывы, полученные методом тампона или ополаскивания, или измельчения.
При получении смыва методом тампона яйцо погружают в ступку, содержащую 10 см3 стерильной водопроводной воды или стерильного физиологического раствора хлористого натрия, и с помощью стерильного тампона обмывают поверхность яйца в течение 2 - 3 мин. Яйцо удаляют, смыв используют для исследования.
При получении смыва методом ополаскивания в стерильную посуду или полиэтиленовый пакет наливают 10 см3 стерильной водопроводной воды или стерильного физиологического раствора хлористого натрия и погружают яйцо. Затем осуществляют встряхивание в течение 3 - 5 мин. Предварительно посуду закрывают стерильной крышкой, верхнюю часть пакета достаточно сжимают, чтобы не допустить разлива жидкости. Размер пакета 15×25 см. Яйцо удаляют, смыв используют для исследования.
При получении смыва методом измельчения скорлупу и подскорлупные оболочки отделяют от содержимого яиц и помещают в стерильные банки. В последних измельчают стеклянными палочками, после чего встряхивают со стеклянными бусами в стерильной водопроводной воде или стерильном физиологическом растворе хлористого натрия. После отстаивания в течение 3 - 5 мин надосадочную жидкость используют для исследования.
Скорлупу и подскорлупные оболочки можно измельчать пестиком со стерильным стеклянным песком в ступках.
На 90,0 см3 жидкости берется скорлупа от 3 яиц.
Для исследования используют смыв без разведения или же готовят десятикратные разведения в зависимости от степени загрязнения поверхности скорлупы яиц.
Математически поверхность яйца вычисляют по формуле:
![]()
где: S - площадь поверхности;
В - ширина;
Р - длина окружности;
π - 3,14.
При микробиологическом исследовании яичных мороженых продуктов (меланжа, белка, желтка) для проверки соответствия качества яичных мороженых продуктов требованиям действующей нормативно-технической документации из разных мест партии отбирают 3 % ящиков, но не менее шести. Из общего количества отобранных ящиков отбирают по одному пакету, мешку-вкладышу, банке из каждого отобранного в выборку ящика. Из разных мест каждого пакета, мешка-вкладыша или банки стерильным масляным щупом отбирают не менее четырех столбиков продукта в стерильную посуду.
Отобранные пробы соединяют, размораживают, тщательно перемешивают и получают объединенную пробу массой не более 0,5 кг, которую помещают в стерильную посуду с притертой пробкой.
В случае необходимости отправки проб в лабораторию, находящуюся вне места их отбора, пробы упаковывают в общую тару (ящик, пакет), которую опечатывают, пломбируют и доставляют, не допуская оттаивания продукта.
Из объединенной пробы (массой не более 0,5 кг) стерильным инструментом в стерильную посуду с притертой пробкой отбирают 100 г продукта для проведения микробиологического анализа, остальную часть используют для проведения органолептических и физико-химических методов анализа.
Перед проведением микробиологического исследования оттаивание проб проводится в водяной бане при температуре не выше 45 °С до температуры внутри продукта не выше 1 - 5 °С.
При микробиологическом исследовании яичных сухих продуктов (порошка, белка, желтка) для оценки санитарно-микробиологического качества от партии из разных мест отбирают 3 % единиц упаковки, но не менее 3-х единиц.
Из разных мест каждой отобранной в выборку упаковочной единицы отбирают не менее трех точечных проб, взятых в равном количестве.
Отбор проб осуществляют щупом, отборником, черпаком, ложкой, металлической трубкой, шпателем или другим приспособлением, которые каждый раз перед использованием стерилизуют фламбированием или в автоклаве.
Масса пробы, отобранной из каждой бочки, барабана, мешка, ящика или банки № 15, должна быть 0,2 кг. От партии яичного сухого продукта, фасованного в пакеты, отбирают из разных мест каждого отобранного в выборку ящика по три пакета. Из выборки яичного продукта, фасованного в банки, из каждой групповой упаковочной единицы отбирают по одной банке.
Пробы, отобранные, как указано выше, соединяют, тщательно перемешивают, подвергают квартованию и получают объединенную пробу массой 0,5 кг.
Объединенную пробу яичного порошка делят на две равные части, которые помещают в чистые стерильные стеклянные банки с притертыми пробками или полиэтиленовые пакеты.
Полиэтиленовые пакеты завязывают следующим образом: верхнюю часть наполненного пакета собирают в пучок, перегибают и плотно завязывают.
Одну часть направляют в лабораторию для анализа, другую пломбируют, снабжают этикеткой и хранят один месяц при температуре на выше 20 °С и относительной влажности 65 - 75 % на случай разногласий при определении качества яичного сухого продукта. На этикетке указывают: наименование предприятия-изготовителя; наименование продукта; дату выработки; номер и размер партии; дату и место отбора проб; фамилии лиц, отобравших пробу; обозначение действующего нормативно-технического документа.
Из объединенной пробы стерильным щупом, отборником, черпаком, ложкой, металлической трубкой, шпателем или другим приспособлением в стерильную посуду отбирают 100 г яичного сухого продукта для проведения микробиологического анализа, остальную часть пробы используют для проведения органолептических и физико-химических анализов.
Для приготовления разведений навеску сухих яичных продуктов массой 10 г, взвешенную с погрешностью ±0,01 г, вносят в колбочку с 90 см3 или массой 20 г в 180 см3 стерильной водопроводной воды или стерильного физилогического раствора, соблюдая правила асептики, и готовят серию десятикратных разведений яичных продуктов в зависимости от предполагаемого обсеменения продукта.
При выполнении микробиологических анализов из проб сухих яичных продуктов навески отвешивают на стерильных бумажках или в стерильных чашках, из проб жидких набирают стерильными пипетками.
Содержимое яиц, смывы с их скорлупы, яичные мороженые продукты (меланж, белок, желток), сухие яйцепродукты (порошок, белок, желток) подвергают микробиологическому исследованию по методикам, изложенным в данной Инструкции, и в соответствии с действующей нормативно-технической документацией на эти продукты.
Исследования яиц на сальмонеллы проводят в соответствии с Методическими указаниями "Лабораторная диагностика сальмонеллезов человека и животных, обнаружение сальмонелл в кормах, продуктах питания и объектах внешней среды" (1990 г.), при этом используют смывы с яичной скорлупы и желток яиц.
При взятии смывов с яичной скорлупы один тампон используют для исследования 10 яиц. После взятия смывов тампон помешают в 10 см3 предварительной среды обогащения с последующим исследованием по схеме п. 3.3 настоящей Инструкции.
При исследовании желтков в стерильную посуду помещают 5 желтков (одна проба), их гомогенизируют и используют для посева.
Микробиологические показатели яиц, мороженых и сухих яичных продуктов, их оценка представлены в таблице 1.3.16.
Таблица 1.3.16
Микробиологические показатели яиц, мороженых и сухих яичных продуктов (Медико-биологические требования и санитарные нормы качества продовольственного сырья и пищевых продуктов. МЗ СССР, М., 1989)
|
Наименование продуктов |
Количество мезофильных аэробных и факультативно-анаэробных микроорганизмов, КОЕ/г не более |
Масса продукта (г), в которой не допускаются |
Примечание |
|
|
БГКП (колиформы) |
патогенные микроорганизмы, в т.ч. сальмонеллы |
|||
|
Яйцо куриное диетическое |
5×102 - 5×103 |
0,1 |
5×25 |
*) В желтках 5 яиц сальмонеллы не допускаются |
|
Яйцо куриное столовое |
5×104 - 5×105 |
0,1-0,01 |
25 |
|
|
Меланж яичный мороженый; желтки и белки яичные мороженые*) |
5×105 |
0,1 |
25 |
*) Не допускаются St. aureus и протей в 1 г |
|
Продукты яичные мороженые: меланж яичный мороженый |
5×105 |
0,1 |
25 |
Дополнительно к ОСТ 4911 197-83, а также протей и St. aureus в 1 г не допускаются |
|
Меланж яичный мороженый с солью и сахаром |
5×105 |
0,1 |
25 |
То же |
|
Яичный порошок |
- |
0,1 |
25 |
Протей в 1 г не допускается |
|
Яичный порошок для продуктов энтерального питания |
1×105 |
0,1 |
25 |
Протей в 0,1 г не допускается St. aureus в 1 г не допускается |
Примечание: БГКП - сбраживающие лактозу с образованием кислотного газа при 37 ± 0,5 °С.
Микробиологический контроль качества проводят в каждой партии выпускаемого продукта.
При несоответствии яиц и яйцепродуктов требованиям по микробиологическим показателям их направляют на выработку термически обрабатываемых продуктов.
2. УСЛОВИЯ ПРОВЕДЕНИЯ МИКРОБИОЛОГИЧЕСКИХ АНАЛИЗОВ
2.1. Помещения для микробиологических исследований
Микробиологическая лаборатория включает в себя следующие помещения:
комнату (около 24 м2) с боксом для посевов;
средоварочную (18 м2) с боксом;
автоклавную (16 м2);
моечную (18 м2);
препараторскую.
Комната для бакисследований с застекленным боксом и предбоксником. Бокс оборудован подвесными бактерицидными лампами, осветительными лампами. Количество бактерицидных ламп из расчета мощности облучения 2,5 Вт/м3.
В боксе находятся:
стол, винтовой стул;
склянка с дезраствором;
склянка со спиртом;
склянка с ватой и ватными тампонами;
склянка с инструментами (пинцет, скальпель, петля бактериологическая, шпатель, консервный нож, пробойник, ножницы);
склянка для отработанных пипеток;
склянка с карандашами по стеклу;
спиртовка или газовая горелка Бунзена;
металлический поддон.
Посевы производят в боксе. Бокс комплектуется из двух отделений: собственно бокса и предбоксника. Предбоксник служит для надевания специальной санитарной одежды (халаты, колпаки или косынки) и вспомогательных работ. Выключатель к бактерицидным лампам устанавливается на наружной стенке бокса. Бактерицидные лампы включаются по окончании работы и уборки помещения в отсутствие персонала на 30 - 60 мин.
Ежедневно после окончания работ помещение бокса моют горячей водой с мылом или порошком и протирают досуха.
Дезинфекцию помещений производят протиранием всех поверхностей хлорным или другими дезинфицирующими препаратами по соответствующей для каждого препарата инструкции и с помощью бактерицидных ламп.
Воздух в боксе регулярно, не менее 2 раз в неделю, следует проверять на бактериальную загрязненность. Чашки с мясо-пептонным агаром и средой Сабуро оставляют открытыми на 15 мин. Посев на МПА, средой из СПА выдерживают в термостате 48 ч при 37 °С, чашки со средой Сабуро - 96 ч при 22 °С. Допустимым ростом считаются 5 колоний на чашках.
В комнате - не менее 2-х письменных столов со стульями для бактериологов, лабораторные столы для оборудования (микроскоп - 2 шт.; весы - 3 шт. (торзионные, циферблатные, рычаговые); баня водяная с электроподогревом; микроизмельчитель тканей; аппарат для встряхивания колб, анаэростат; склянка и кювета для окраски мазков);
шкафы для красок, химреактивов, сухих питательных сред; стерильной посуды: пипеток, пробирок, чашек Петри и др.;
термостаты - не менее 3 шт. (на 30°, 37°, 55°);
холодильники - 2 шт. (для выделенных культур и для чистых сред);
умывальник с предметами личной гигиены.
Средоварочная обеспечивается:
шкафами с лабораторной посудой (колбы плоскодонные разные, пробирки в металлических корзинах, цилиндры, стаканы и др.); с посудой для варки (кастрюли, металлические кюветы и др.); электро- или газовой плитой на 4 конфорки;
электроплитками - 2 - 3 шт.;
pH-метром;
холодильником - 2 шт.;
раковинами и умывальником с предметами личной гигиены.
Автоклавная оборудуется:
автоклавами - 2 шт. (один для чистых материалов, второй для инфицированных);
сушильно-стерилизационными шкафами;
перегонными аппаратами (один для дистиллированной, второй для бидистиллированной воды);
столами - 2 шт. (один для чистых, второй для инфицированных материалов).
Моечная оборудуется:
нагревательными приборами для подогрева воды;
раковинами;
досками для сушки посуды;
сушильными шкафами;
баками с дезрастворами;
шкафами для посуды и хранения моечных средств.
Препараторская служит для хранения запасов имущества (посуды, красок, химикалиев, питательных сред, аппаратов, приборов и пр.). В ней устанавливают шкафы, столы, холодильник. Здесь готовят растворы красок, солей, дезинфицирующих средств; ватные пробки.
2.2. Оборудование, аппаратура, материалы и реактивы для лаборатории
Микробиологический отдел производственной лаборатории должен быть оснащен всем необходимым для проведения бактериологических анализов.
Количество единиц оборудования, аппаратуры и реактивов зависит от ассортимента выпускаемой продукции и количества ежедневных анализов.
Примерный перечень аппаратуры, материалов, реактивов для оснащения микробиологической лаборатории представлен ниже.
Оборудование и аппаратура, инструменты:
Автоклав для стерилизации чистой посуды и питательных сред
Автоклав для убивки отработанного материала и бактериальных культур
Аппарат для встряхивания (шуттель)
Анаэростат
Баня водяная с терморегулятором, обеспечивающим температуру до 100 °С с точностью до ±0,5 °С
Весы лабораторные
Гомогенизатор по ГОСТ 9111-59
Горелки газовые и спиртовые по ГОСТ 10090-74
Дистиллятор электрический Д-4
Лампы бактерицидные ДБ-30 или ДБ-60 (1,5 - 2,5 Вт на 1 м3 воздуха)
Лупа с увеличением 8 - 10× по ГОСТ 8309-75
Микроскоп биологический МБИ, МБВ или другой марки по ГОСТ 8284-67
Мясорубка по ГОСТ 4025-73
Ножи из нержавеющей стали
Нож консервный
Ножницы из нержавеющей стали
Палочки стеклянные по ГОСТ 9425-71
Петля бактериологическая
Пинцеты разные
Плита газовая или электрическая бытовая
Прибор Зейца с воронками (фильтр Зейца) и прибор для подсчета колоний
Пробоотборники, ложки, долота из нержавеющей стали
Скальпели разные
Сушильный шкаф
Ступка фарфоровая вместимостью 300 - 500 см3 с пестиками по ГОСТ 10444.1-84
Термостаты с диапазоном температур 24 - 70 °С
Термометры от 0 - 5 °С до 50 - 100 °С, 100 - 150 °С по ГОСТ 2823-73
Треножник металлический
Холодильники бытовые
Часы песочные на 1, 2, 3, 5 мин по ГОСТ 10576-74
Шпатели стеклянные
Штативы для пробирок разной вместимости
Электроплитки по ГОСТ 306-69.
Материалы:
Бумага оберточная
Бумага пергамент, полупергамент
Бумага фильтровальная по ГОСТ 12026-76
Вата медицинская гигроскопическая по ГОСТ 5556-75
Карандаши по стеклу
Марля медицинская по ГОСТ 9412-77
Мыло
Порошки стиральные
Сетка асбестовая
Фильтр асбестовый
Шпагат
Щетки, ерши для мойки посуды.
Реактивы, краски, среды, препараты:
Агар микробиологический по ГОСТ 17206-71
Агар сухой питательный, выпускаемый Минмедпромом, готовят по прописи на этикетке
Агар висмут-сульфитный
Альфа-нафтол (ГОСТ 5838-79)
Бромкрезолпурпур (ТУ 6-09-1386-76)
Бромтимоловый синий (ТУ 6-09-2045-72)
Вазелин медицинский (ГОСТ 3882-52)
Вода дистиллированная (ГОСТ 6709-72)
Генциан фиолетовый Глицерин, х.ч. (ГОСТ 6824-76)
Глюкоза, х.ч., ч.д.а. (ГОСТ 6038-79)
Дезоксирибонуклеиновая кислота (ДНК) высокополимеризованная (ТУ 6-09-4230-78)
Дрожжи хлебопекарные прессованные (ГОСТ 171-69)
Дрожжевой автолизат
Дрожжевой экстракт
Железо сернокислое (ГОСТ 4148-78)
Желчь крупного рогатого скота или медицинская (билирубин, ТУ 6-09-10-364-75)
Зелень бриллиантовая (ТУ 6-09-42-78-76)
Йод кристаллический (ГОСТ 4159-79)
Калий гидрат окиси (едкий) технический (ГОСТ 9285-78)
Калий йодистый (ГОСТ 4232-74)
Калий фосфорнокислый двузамешенный (ГОСТ 2493-75)
Калий фосфорнокислый однозамешенный (ГОСТ 4198-75)
Калий углекислый (мел, ГОСТ 83-79)
Кальций фосфорнокислый двузамешенный (ГОСТ 3204-76)
Кальций хлористый (ГОСТ 4460-77)
Картофель свежий продовольственный (ГОСТ 7176-68)
Кислота лимонная (ГОСТ 908-79Е)
Кислота соляная (ГОСТ 3118-67)
Кислота фосфорная (ГОСТ 10678-76)
Кислота уксусная (ГОСТ 61-75)
Крахмал растворимый (ГОСТ 10163-76)
Кристаллический фиолетовый (ТУ 6-09-4119-75)
Лактоза (ТУ 6-09-229-72)
Лакмус (ТУ 6-09-4313-76)
Магний хлористый
Мальтоза (ТУ 6-09-3476-73)
Масло вазелиновое (ГОСТ 3164-78)
Масло иммерсионное (ТУ 81-05-79-69)
Метиловый красный (ГОСТ 5853-51)
Молоко свежее пастеризованное (ГОСТ 13277-79)
Мочевина (ГОСТ 6691-77)
Натрий гидрат окиси (едкий, ГОСТ 11078-78)
Натрий селенистокислый
Натрий сернокислый (ГОСТ 429-76)
Натрий фосфорнокислый двузамещенный 12Н2O (ГОСТ 4172)
Натрий фосфорнокислый однозамещенный (ГОСТ 246-76)
Натрий фосфорнокислый двузамещенный безводный (ГОСТ 11773-76)
Натрий хлористый (ГОСТ 4233-77)
Парафин (ГОСТ 23683-79)
Пептон бактериологический (ГОСТ 13805-76)
Перекись водорода (ГОСТ 10929-76)
Печень говяжья, свиная
Плазма сухая или свежеприготовленная кроличья или человека, приготовленная по ГОСТ 10444.2-75
Сахароза, ч.д.а. (ГОСТ 5833-75)
Спирт этиловый 70- и 96-процентный (ГОСТ 18300-72 и ГОСТ 5962-67)
Среды сухие питательные, выпускаемые Минпищепромом или Минмедпромом, готовят по прописи на этикетке:
с маннитом и индикатором ВР;
с глюкозой и индикатором ВР;
среда Кода;
среда Левина;
среда Плоскирева;
среда Эндо
Трифенилтетразолий хлорид 2, 3, 5 (ТУ 6-09-3838-78)
Яйца куриные свежие
Растворы буферные для проверки pH-метра.
Дезинфицирующие вещества:
Хлорная известь
Хлорамин
Пергидроль
Фенол, едкий натр
и другие хлорсодержащие вещества, разрешенные Минздравом СССР.
2.3. Лабораторная посуда, ее подготовка и хранение
В микробиологическом отделе производственной лаборатории должна быть следующая посуда:
Ведра эмалированные с крышками
Воронки стеклянные по ГОСТ 8613-64
Кастрюли эмалированные разной вместимости (0,5 л, 1 л, 2 л, 3 л) по ГОСТ 17151-71
Колбы стеклянные широкогорлые плоскодонные на 50, 100, 150, 200, 300, 500, 1000, 2000, 3000 см3 по ГОСТ 10972-72
Лотки эмалированные
Пипетки пастеровские
Пипетки бактериологические вместимостью 1, 2, 5, 10, 20 см3 с ценой деления 0,01 см3 на полное опорожнение по ГОСТ 1770-74
Поплавки стеклянные (маленькие пробирки, преципитационные)
Пробирки бактериологические по ГОСТ 10515-75
Стеклянные банки с крышками 0,5 - 1,5 л
Стекла покровные по ГОСТ 6672-75
Стекла предметные по ГОСТ 9284-75
Стекла часовые одиночные 600 - 800 мм
Стаканчики для взвешивания (бюкса) разной вместимости
Цилиндры стеклянные мерные вместимостью 50, 100, 500 см3
Чашки Петри бактериологические по ГОСТ 10973-75.
Лабораторная посуда для микробиологических исследований подвергается мойке, сушке, упаковке в бумагу или специальные металлические закрывающиеся футляры и стерилизации.
При подготовке новой посуды ее погружают в ведро с теплой водой, в которой растворяют хозяйственное мыло, и ставят на слабый огонь. После 15-минутного кипячения посуду вынимают, ополаскивают чистой водой. Затем кипятят в течение 15 мин в подкисленной воде (1 - 2 %-ные растворы соляной кислоты), ополаскивают водопроводной и дистиллированной водой.
Посуду, бывшую в употреблении, моют 0,5 %-ным щелочным раствором с помощью ершей и щеток и ополаскивают водопроводной водой.
Посуда, в которой содержался зараженный материал, поступает в мойку после предварительной дезинфекции (убивки в автоклаве), гарантирующей гибель находящихся в ней патогенных микроорганизмов. Сильно загрязненную посуду со следами жира, красок и иммерсионного масла опускают на 2 ч в хромовую смесь, подогретую до 45 °С, затем тщательно промывают проточной водопроводной водой.
Посуду с питательными средами после подсчета на них споровых микроорганизмов обеззараживают перед мойкой путем стерилизации в автоклаве при 121 °С в течение 1,5 ч.
Вымытую посуду не вытирают, а сушат при комнатной температуре (холодная сушка) или горячим воздухом в сушильном шкафу при температуре 100 - 105 °С.
Предметные стекла после мойки и ополаскивания вытирают чистой салфеткой или помешают в склянку с притертой пробкой в смесь спирта и этилового эфира в соотношении 1:1.
Лабораторную посуду перед использованием стерилизуют. Стерилизуют сухим паром в сушильном шкафу при температуре 150, 160 и 180 °С соответственно 2 ч, 1 ч и 30 мин; или в автоклаве при давлении 1 атм. (121 °С) в течение 30 мин - 1 ч.
Пробирки, флаконы, бутыли, матрацы и колбы закрывают ватно-марлевыми пробками. Поверх пробок на каждый сосуд (кроме пробирок) надевают бумажные колпачки.
Чашки Петри стерилизуют завернутыми в бумагу по 1 - 5 шт. Пастеровские пипетки по 3 - 15 шт. заворачивают в плотную оберточную бумагу. В верхнюю часть каждой пипетки вкладывают кусочек ваты.
Изготовленные ватные или марлевые тампоны стерилизуют каждый в отдельности или несколько штук заворачивают в плотную бумагу. Стерилизуют в автоклаве при температуре 121 °С в течение 30 мин.
Тампон может быть закреплен на конце металлической проволоки или деревянной палочки, пропущенной через ватную пробку. В этом случае его вместе с пробкой вставляют в пробирку с 3 - 4 или 10 см3 физиологического раствора.
Стерильную посуду хранят в плотно закрывающихся шкафах или ящиках с крышками.
Срок хранения стерильной посуды не более 30 суток
3. МЕТОДЫ МИКРОБИОЛОГИЧЕСКОГО КОНТРОЛЯ
3.1. Определение общего количества мезофильных аэробных и факультативно-анаэробных микроорганизмов - общее микробное число (ОМЧ)
Метод основан на количественном подсчете колоний микроорганизмов, вырастающих на плотном питательном агаре при температуре 30 °С в течение 72 ч.
При исследовании образцов на ОМЧ руководствуются ГОСТ 26670-86, ГОСТ 9958-81 с учетом нижеизложенных рекомендаций.
Для определения ОМЧ следует выбирать разведения, при посеве которых на чашках Петри вырастает не менее 30 и не более 300 колоний. При посеве продуктов, не требующих разведения, учитывают все выросшие на чашках колонии (т.е. и менее 30).
При посеве по 1 см3 цельного продукта или каждого соответствующего его разведения вносят в 2 чашки Петри (параллельное определение) и заливают в каждую чашку по 15 - 20 см3 агаризованной питательной среды, расплавленной на водяной бане и остуженной до 45 °С. Сразу после заливки агара содержимое чашки Петри тщательно перемешивают путем легкого вращательного покачивания для равномерного распределения посевного материала.
После застывания агара чашки с посевами помещают в термостат дном вверх, ингибируют при 30 °С в течение 72 ч; при необходимости предварительный учет производят через 48 ч.
Количество колоний подсчитывают на каждой из высеянных чашек. Счет колоний на чашках производят с помощью прибора для счета колоний бактерий или лупы. Для лучшей видимости считают колонии на темном фоне (под чашку кладут темную бумагу), чашки помещают дном кверху. Каждую колонию отмечают на дне чашки чернилами или тушью.
При подсчете придерживаются следующих правил:
- если на чашке выросло небольшое количество колоний, примерно до 100, подсчитывают все колонии;
- если колонии распределены равномерно и их количество измеряется несколькими сотнями (200 - 300 колоний), допускается подсчет колоний не менее чем на 1/3 площади чашки. В этих случаях дно чашки делят карандашом на 6 секторов и считают колонии в 3 секторах. Затем делают пересчет на всю площадь чашки: вычисляют среднее количество колоний на площади одного сектора и полученное количество колоний на одном секторе умножают на 6.
Число колоний, выросших на чашке, должно отражать количество жизнеспособных микроорганизмов, содержащихся в засеянном объеме исследуемого материала. Поскольку последний, как правило, засевают в разведенном виде, число выросших на чашке колоний умножают на степень взятого разведения, рассчитывают среднее арифметическое и устанавливают количество мезофильных аэробных и факультативно-анаэробных микроорганизмов в 1 см3 продукта.
При установлении количества мезофильных бактерий не все чашки могут быть использованы для вычисления среднего арифметического:
- нельзя использовать посевы для вычисления среднего арифметического, если количество выросших колоний на чашках менее 30. В этом случае в протокол исследований вносят показатели обсемененности, полученные при подсчете колоний только по одной или двум чашкам, число колоний на которых больше 30. В случае роста колоний на засеянных чашках в количестве менее 30 в результатах анализа рекомендуется следующая формулировка: "Рост единичных колоний при посеве (указать количество засеянного продукта)";
- не используются посевы для вычисления среднего арифметического показателя на тех чашках, на поверхности которых более чем на 1/2 площади отмечается ползучий рост спорообразующих микроорганизмов; последние могут маскировать рост прочих бактерий. Возможны случаи, когда на чашках из всех разведений получен рост споровых микроорганизмов, и подсчет изолированных колоний практически невозможен. В этих случаях в протоколе исследования следует указать: "Рост спорообразующих микроорганизмов".
Пример расчета: если на чашках Петри при посеве 0,1 г продукта выросло в среднем 135 колоний, а при посеве 2-го разведения (0,01 г продукта) - 9 колоний, то в результатах исследования учитывают цифровые данные, полученные при посеве 1-го разведения, т.е. количество микроорганизмов 135×10 = 1350 в 1 г продукта.
Для получения более точных данных по количеству мезофильных бактерий целесообразно сопоставлять результаты подсчета колоний, полученные на чашках с посевами материала из последовательных разведений. Числа подсчитанных колоний должны примерно соответствовать кратности взятых разведений.
Если количество колоний на чашках с посевами из последующих разведений (1:10, 1:100) почти совпадает или мало между собой разнится, то это указывает на недостаточное перемешивание посевного материала при приготовлении разведений и перед посевом.
3.2. Определение бактерий группы кишечных палочек
В соответствии с принятой международной номенклатурой в настоящей Инструкции к бактериям группы кишечных палочек (БГКП) отнесены грамотрицательные не образующие спор палочки, сбраживающие лактозу с образованием кислоты и газа при температуре 37 °С в течение 24 - 48 ч, в основном являющиеся представителями родов Esheriehia Citrobacter, Enterobacter, Klebsiella, Seiratia (т.е. учитываются как цитратотрицательные, так и цитратположительные варианты БГКП).
Методы исследования на БГКП приведены в ГОСТ 7702.2-74, ГОСТ 9988-81, при этом следует учитывать следующие методические рекомендации.
Для посева используют то количество продукта (1 г и т.д.), в котором предусматривается отсутствие БГКП (колиформных бактерий). Посев производят в среду Кесслер с лактозой (с поплавками), либо в среду Хейфеца с лактозой (с поплавками) с соблюдением соотношения продукта и среды 1:10. Применение среды Кода не допускается.
Посевы ингибируют при температуре 37 °С в течение 24 ч. При отсутствии признаков роста - газообразования и изменения среды - дают заключение об отсутствии БГКП (колиформных бактерий) и о соответствии исследуемого продукта нормативу на БГКП.
При наличии признаков роста на среде Кесслер или Хейфеца для окончательного заключения о наличии в продукте БГКП из подозрительных пробирок производят посев на чашки со средой Эндо или Левина. Посев производят петлей из каждой пробирки так, чтобы получить рост изолированных колоний. Чашки с посевами ингибируют при температуре 37 °С в течение 18 - 24 ч.
При отсутствии на среде Эндо или Левина колоний, типичных для БГКП (на среде Эндо - красных с металлическим блеском или без него, розовых и бледно-розовых, на среде Левина - черных с металлическим блеском, темных с черным центром, сиреневых с темным центром), засеянная навеска продукта считается не загрязненной ими, т.е. исследуемый продукт соответствует нормативу на бактерии группы кишечных палочек.
При наличии на среде Эндо или Левина типичных для кишечных палочек (колиформных бактерий) колоний их продолжают изучать. Из изолированных колоний, характерных или подозрительных на БГКП, делают препараты, окрашивая их по Граму, и микроскопируют. Обнаружение типичных для кишечных палочек грамотрицательных не содержащих спор палочек указывает на наличие бактерий группы кишечных палочек в анализируемой массе продукта и несоответствие продукта микробиологическому нормативу.
СХЕМА
исследования образцов на наличие бактерий группы кишечных палочек
(колиформных бактерий)
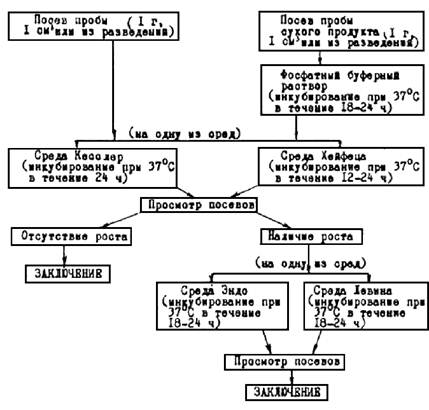
3.3. Определение бактерий из рода сальмонелл
Сальмонеллы - обширный род семейства энтеробактерий, включающих более 2200 серотипов, большинство из которых обладает патогенными свойствами. К сальмонеллам относятся аэробные и факультативно-анаэробные грамотрицательные подвижные (за исключением S.gallinarum-pullorum) палочки, хорошо растущие на обычных питательных средах и разнообразных пищевых субстратах.
При исследовании образцов на наличие сальмонелл руководствуются ГОСТ 7702.2-74; ГОСТ 9958-81; ГОСТ 25311-82 с учетом нижеизложенных методических рекомендаций.
Навеску продукта (25 г или др.) высевают в пептонную буферную воду в соотношении 1:9. Посевы ингибируют при 37 °С в течение 18 - 24 ч.
После этого производят пересев по 1 см3 культуры из пептонной буферной воды в одну из сред: Мюллера, Кауфмана, хлормагниваемую М, селенитовый бульон в соотношении посевного материала и среды 1:9. Посевы инкубируют 24 - 48 ч при 37 °С.
Через 24 ч и 48 ч со второй среды обогащения (Мюллера, Кауфмана, магниевой, селенитового бульона) пересевают на две любые дифференциальные среды (по выбору): Эндо, Плоскирева, Левина, висмут-сульфитный агар.
Посевы просматривают через 18 - 24 ч термостатирования при 37 °С. При отсутствии роста подозрительных колоний инкубирование посевов продолжают ещё 24 ч.
Сальмонеллы на средах Эндо и Плоскирева растут в виде прозрачных бесцветных колоний, на среде Левина - бледно-розовых, голубоватых, розовато-фиолетовых колоний. На висмут-сульфитном агаре сальмонеллы растут в виде черных колоний с характерным металлическим блеском, при этом наблюдается прокрашивание в черный цвет участка среды под колонией. Исключение составляют S.paratyph, S.cholerasuis, S.abortusovis, S.gallinarum-pullorum и некоторые другие, которые при росте на висмут-сульфитном агаре образуют нежные светло-зеленые или серовато-зеленые колонии.
Из каждой среды на чашке Петри из подозрительных колоний (не менее трех) производят посев штрихом и уколом на одну из комбинированных сред (Олькеницкого, Клиглера, Ресселя).
Пробирки с посевами выдерживают в термостате при 37 °С 24 ч. Производят идентификацию культур, высеянных на комбинированные среды, по ферментации лактозы, глюкозы, сахарозы и расщеплению мочевины.
Покраснение или пожелтение скошенной части столбика среды Олькеницкого указывает на образование кислоты в результате ферментации лактозы, сахарозы или обоих сахаров. Покраснение или пожелтение самого столбика указывает на расщепление глюкозы. Восстановление цвета среды до исходного (бледно-розовый) свидетельствует о расщеплении мочевины.
Механизм действия среды Клипера и Ресселя идентичен со средой Олькеницкого. Об образовании сероводорода судят по почернению среды в столбике.
Если культуры сбраживают лактозу с образованием газа и расщепляют мочевину, они не принадлежат к бактериям рода сальмонелл.
Культуры, не ферментирующие лактозу и не расщепляющие мочевину, но ферментирующие глюкозу (с образованием или без образования газа), подвергаются дальнейшему исследованию.
Подозрительные колонии с комбинированной среды пересевают в пробирки со скошенным МПА, а также на среды Гисса с сахарами, 1 %-ную пептонную воду для определения индола и сероводорода.
Сальмонеллы расщепляют маннит с образованием кислоты, вследствие чего меняется цвет среды Гисса.
При исследовании на индол и сероводород из подозрительной колонии микроорганизмы высевают в пробирки с 1 %-ной пептонной водой и термостатируют при 37 °С 24 ч. Затем в пробирку с суточной культурой по стенке добавляют 5 - 10 капель реактива Эрлиха. При наличии индола не позднее чем через 5 мин в пограничном слое образуется ярко-красное кольцо, при отсутствии кольцо остается светло-желтого цвета.
Для определения индолообразования пользуются также реактивом Ковача. К суточной культуре добавляют 0,2 - 0,3 см3 реактива и взбалтывают. Результаты учитывают через 10 мин: реактив поднимается на поверхность среды и при наличии индола окрашивается в темно-красный цвет.
Сальмонеллы индола не образуют.
Для определения сероводорода в пробирку с посевом культуры в 1 %-ную пептонную воду помещают под пробку полоску фильтровальной бумаги, предварительно смоченной уксусно-кислым свинцом и высушенной. Полоска не должна соприкасаться с питательной средой. Посев инкубируют при 37 °С 24 - 72 ч. Если культypa выделяет сероводород, то бумажка с уксусно-кислым свинцом чернеет от образующегося сернистого свинца.
При использовании среды Клиглера об образовании сероводорода судят по почернению среды в столбике.
Сальмонеллы выделяют сероводород.
Из пробирок с комбинированной средой с суточной культурой, показавшей типичную окраску среды для сальмонелл, или из пробирок с суточной культурой, пересеянной на МПА, проводят серологическое исследование. Для этого петлей берут небольшое количество культуры из пробирок, эмульгируют в капле физиологического раствора на предметном стекле. Добавляют каплю поливалентной О-сыворотки к раствору и осторожно покачивают предметное стекло, чтобы смешать жидкости.
Положительная реакция на сальмонеллы (агглютинация) наблюдается в течение 30 - 60 сек Обязательна постановка отрицательной реакции (культура + физиологический раствор). Если при проведении серологического исследования агглютинация не обнаруживается, конечный результат записывают как отсутствие сальмонелл.
Любая агглютинация, которая появляется на стекле, говорит о вероятности присутствия сальмонелл.
По показаниям для полной биохимический типизации сальмонелл проводят посев на расширенный пестрый ряд (ГОСТ 7702.2-74) и реакцию агглютинации не только с О-, но и с Н-сыворотками (ГОСТ 7702.2-74).
СХЕМА
исследования образцов на наличие сальмонелл
Посев проб (25 г или др. навески)
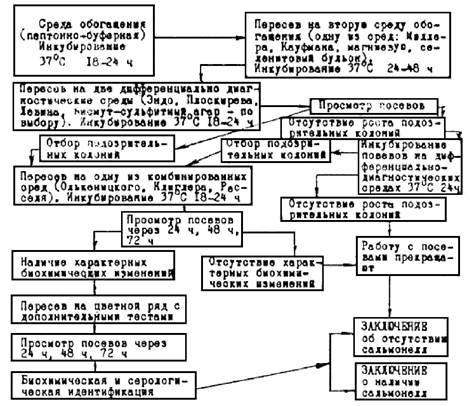
3.4. Определение сульфитредуцирующих клостридий
К сульфитредуцирующим клостридиям относятся облигатные спорообразующие анаэробные бактерии, которые восстанавливают сутьфит натрия (Na2SO3) в сульфид натрия (Na2S), последний, соединяясь с хлорным (или цитратным) железом, образует черное соединение сернистого железа (FeS).
Методы исследования на сульфитредуцирующие клостридии приведены в ГОСТ 9958-81 с изменением № 2, в ГОСТ 10444.9-88. Ниже приведены методические рекомендации с учетом стандартных методик.
Выделение сульфитредуцирующих клостридий из исследуемой пробы проводят в 2 этапа, которые включают в себя обнаружение сульфитредуцирующей способности микроорганизмов и доказательство, что выделенные микроорганизмы являются клостридиями, так как сульфитредуцирующей способностью обладают не только клостридии, но и многие энтеробактерии.
В зависимости от последовательности этапов возможны 2 способа проведения исследований.
Первый способ исследования. Сначала определяют, что микроорганизмы обладают сульфитредуцирующей способностью. Для этого по 1 см3 исходного материала или его разведения производят посев либо в чашки Петри глубинным способом с заливкой средой Вильсон-Блера или другими агаризованными средами с сульфитредуцирующими растворами, либо в стерильные пробирки с заливкой посевного материала названными средами высоким столбиком (10 - 12 см3).
Посевы термостатируют в анаэростате при температуре (37 ± 0,5) °С в течение 48 ч. При отсутствии анаэростата посевы заливают слоем (не менее 2 мм) голодного агара с последующим инкубированием в термостате 24 - 48 ч.
Сульфитредуцирующие микроорганизмы образуют темно-серые или черные колонии и вызывают потемнение среды.
Для подтверждения принадлежности выросших колоний к клостридиям производят пересев в пробирки со средой Китт-Тароцци, прогретые непосредственно перед посевом 25 мин в кипящей водяной бане и охлажденные до 40 - 50 °С. Термостатирование проводят при (37 ± 0,5) °С 24 - 48 ч. Сразу после появления признаков роста (помутнение среды, выделение газа, появление постороннего запаха) проводят микроскопирование, выявляют каталазную активность микроорганизмов с помощью раствора перекиси водорода (30 г/дм3). При наличии в мазках спорообразующих палочек, при отсутствии каталазы, о чем судят по отсутствию пузырьков газа при добавлении к капле культуральной жидкости на предметном стекле такого же количества перекиси водорода, делают заключение о принадлежности микроорганизмов к клостридиям.
В случае отсутствия спор в мазке, положительной пробы на каталазу производят пересев со среды Китт-Тароцци на чашку Петри глубинным способом с заливкой 35 - 40 см3 питательного агара или средой Вильсон-Блера. Застывшую поверхность плотной среды в первом случае накрывают стерильным предметным стеклом, во втором случае (при использовании среды Вильсон-Блера) заливают голодным агаром. Чашки переворачивают и термостатируют 24 - 48 ч при (37 ± 0,5) °С. Появление колоний в глубине агара на 2 - 3 мм от края стекла свидетельствует о том, что микроорганизмы являются клостридиями. Появление в чашках со средой Вильсон-Блера в нижнем слое агара черных или коричневых колоний свидетельствует о присутствии в посевах сульфитредуцирующих клостридий.
Второй способ исследования заключается в первоначальном выделении клостридий, а затем в установлении их сульфитредуцирующей способности. Второй способ отличается от первого только последовательностью посевов в питательные среды. Сначала исследуемый материал высевают в среду Китт-Тароцци, производят микроскопирование, определение каталазы, а затем, установив принадлежность микроорганизмов к клостридиям, производят пересев на среды с сульфитредуцирующими растворами (Вильсон-Блера и др.).
3.5. Методика выделения бактерий рода протей
Из навески продукта готовят исходное и ряд десятикратных разведений так, чтобы можно было определить предполагаемое минимальное количество продукта, содержащее бактерии рода протей.
Из продукта или соответствующих разведений высевают по 1,0 см3 в жидкую среду обогащения (среда жидкая селективная). Посевы ингибируют при (37 ± 0,5) °С в течение 48 ч.
Положительными считают пробирки, в которых наблюдается помутнение среды при росте бактерий, расщепляющих мочевину, наблюдается изменение цвета среды в синий. Отсутствие изменения цвета среды не является показателем отсутствия роста выявляемых бактерий.
Для подтверждения присутствия бактерий рода протей из всех пробирок, в которых наблюдается помутнение среды, делают пересевы на одну из дифференциально-диагностических плотных сред (агар дезоксихолат-цитрат лактозный по Лейфсону в модификации Хайнса, агар дифференциально-диагностический), чтобы получить рост изолированных колоний.
Посевы инкубируют при (37 ± 0,5) °С в течение 48 ч.
На дифференциально-диагностических плотных средах бактерии образуют колонии круглой формы диаметром 1 - 3 мм. Бактерии рода протей обладают свойством роения (ползучим ростом).
Из всех чашек с характерным ростом выбирают не менее 5 колоний для выделения чистых культур и дальнейшего изучения.
Для получения чистых культур используют скошенный в пробирке мясо-пептонный агар или мясо-пептонный бульон. Посевы инкубируют при (37 ± 0,5) °С в течение 24 ч.
Биохимическое подтверждение бактерий рода протей проводят следующим образом: из 24-часовой культуры делают высев штрихами на поверхность скошенного в пробирке агара (среда для расщепления фенилаланина), культивируют при (37 ± 0,5) °С в течение 48 ч, после этого на поверхность агара пипеткой наносят 3 - 5 капель раствора хлорного железа, при этом появление интенсивной зеленой окраски среды свидетельствует о положительной реакции. При отрицательной реакции цвет среды не меняется.
Бактерии рода протей дают положительную реакцию.
Для определения образования сероводорода культуру высевают методом укола в столбик и штрихами на поверхности агаризованной среды (агар тройной сахарный с цитратом железа).
Посевы инкубируют при (37 ± 0,5) °С в течение 48 ч. При образовании сероводорода столбик чернеет. Бактерии рода протей образуют сероводород, при этом в столбике среды появляется газ, что указывает на ферментацию глюкозы с образованием кислоты и газа.
3.6. Определение коагулазоположительных стафилококков (Staphylococcus aureus)
St. aureus - аэробные грамположительные сферические пигментообразующие микроорганизмы, обладающие ферментом коагулазой. Большая часть St. aureus способна к продукции энтеротоксинов.
Метод основан на способности стафилококков расти на питательных средах с повышенным содержанием поваренной соли. Принадлежность к St. aureus определяют по способности коагулировать цитратную плазму крови человека или кролика.
Исследования проводят по ГОСТ 7702.2-74; ГОСТ 9958-81 с учетом нижеизложенных рекомендаций.
При исследовании сухих продуктов перед посевами на питательные среды проводят предварительную инкубацию в фосфатном буферном растворе. Для этого 1 г продукта помещают в 9 см3 раствора, смесь выдерживают при температуре 37 °С в течение 18 - 24 ч. На следующий день пипеткой переносят 1 см3 смеси в пробирку с солевым бульоном.
Несухие продукты без предварительной инкубации в фосфатном буфере сразу высевают (навеску 1 г) в пробирку с 9 см3 солевого бульона. В случае необходимости производят посевы в пробирку с солевым бульоном из серии десятикратных разведений.
После термостатирования при температуре 37 °С в течение 24 ч из солевого бульона производят пересев петлей на чашки Петри с подсушенными средами типа Байрд-Паркер или ЖСА (желточно-солевой агар) для получения изолированных колоний. Чашки с посевами выдерживают в термостате при температуре 37 °С в течение 18 - 24 ч.
На среде Байрд-Паркер St. aureus растут в виде черных блестящих выпуклых колоний в диаметре 1 - 1,5 мм, окруженных зоной просветления среды шириной 1 - 3 мм. Колонии, образовавшие зоны просветления на среде Байрд-Паркер через 24 ч инкубации при 37 °С, в 90 % случаев являются штаммами, образующими энтерококк. Эти колонии не требуют подтверждения в принадлежности к St. aureus и подлежат учету через 24 ч инкубации.
На ЖСА колонии St. aureus имеют форму выпуклых дисков диаметром 2 - 4 мм белого, желтого, кремового, лимонного, золотистого цвета с ровными краями, вокруг колоний образуются радужное кольцо и зона помутнения среды.
Из характерных колоний, подозрительных на St. aureus, готовят мазки-препараты, окрашивают по Граму и микроскопируют. Колонии грамположительных мелких кокков, расположенных в мазке гроздьевидно, отсеивают на сектора чашки Петри или в пробирки со скошенным МПА. Посевы выдерживают в термостате при 37 °С в течение 18 - 24 ч. Из культур, выросших на МПА, после предварительной проверки мазка на чистоту под микроскопом ставят реакцию плазмокоагуляции.
При этом берут две пробирки, в каждой из которых по 0,5 см3 разведенной кроличьей плазмы. В одну пробирку вносят петлей исследуемую суточную агаровую культуру, другую пробирку оставляют незасеянной. Пробирки помещают в термостат при температуре 37 °С. Учитывают результаты через 2 - 4 ч и оставляют до утра при комнатной температуре для окончательного учета.
Пробирки на свертывание плазмы следует просматривать осторожно, чтобы не разрушить начало образования сгустка.
При учете реакции плазмокоагуляции могут наблюдаться три степени активности фермента коагулазы:
++++ - сгусток плотный;
+++ - сгусток, имеющий небольшой отсек;
++ - сгусток в виде взвешенного мешочка.
Все три варианта являются положительным результатом.
Положительная реакция плазмокоагуляции свидетельствует о присутствии коагулазоположительных стафилококков в засеянной массе продукта (в 1 г/см3) 10-1 г и т.д., а отрицательная реакция плазмокоагуляции - об их отсутствии.
СХЕМА
исследования образцов на наличие плазмокоагулирующих стафилококков
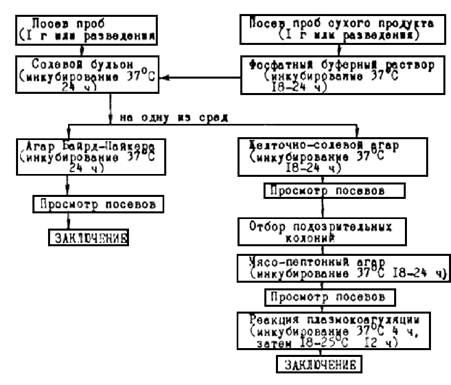
3.7. Определение спор мезофильных и термофильных клостридий, бацилл аэробных и факультативно-анаэробных микроорганизмов
К клостридиям относятся анаэробные бактерии, способные к спорообразованию в строго анаэробных условиях, растущие либо при 30 - 37 °С (мезофилы), либо при 55 - 65 °С (термофилы) и не образующие каталазу.
К бациллам относятся спорообразующие бактерии, способные развиваться как в аэробных, так и в анаэробных условиях (факультативные анаэробы), способные развиваться при 30 - 37 °С (мезофилы) либо при 55 - 65 °С (термофилы).
Подготовка проб для выделения спор. Пробирку с исследуемой навеской продукта или его разведениями помещают в водяную баню с температурой 50 °С. Воду в бане нагревают до достижения нужной температуры внутри продукта, которую определяют в контрольной параллельной пробирке.
Для выявления спор мезофилов пробу прогревают в течение 20 мин при температуре внутри пробирки 80 °С; для спор термофилов - 20 мин при 94 - 96 °С.
Выделение спор клостридий производят путем посева прогретого материала в пробирку с регенерированной средой Китт-Тароцци для термофилов или мезофилов.
Посевы мезофилов термостатируют при 30 °С 48 ч и более (до 5 суток), посевы термофилов - при (58 ± 3) °С 24 - 48 ч (не более 72 ч) при 80 %-ной влажности воздуха (для этого в термостат ставят сосуд с водой с открытой поверхностью).
Признаками роста клостридий являются образование мути, газа, возникновение постороннего запаха.
Посевы сразу после появления роста исследуют под микроскопом. Материал для приготовления препарата берут пипеткой со дна сосуда. При наличии в мазках грамположительных палочек со спорами ставят каталазную пробу (ГОСТ 10444.3-85). Отрицательная проба на каталазу свидетельствует о присутствии в среде облигатных клостридий.
Для окончательного заключения о присутствии клостридий в посевах 1 см3 культуры из пробирки со средой Китт-Тароцци вносят в чашку Петри, заливают 40 см3 питательного агара с глюкозой и тщательно перемешивают. Сразу после застывания агара на его поверхность пинцетом кладут стерильное предметное стекло так, чтобы под ним не было пузырьков воздуха. Затем чашку переворачивают крышкой вниз и ставят в термостат для мезофилов - с температурой 30 °С на 24 - 48 ч; для термофилов - с температурой (58 ± 3) °С на 24 - 48 ч.
Облигатные клостридии растут на чашке под стеклом в центральной части, отступая от края стекла на 1 - 3 мм, образуя под стеклом пузырьки газа и (или) разрывы агара. Факультативные анаэробы растут под стеклом в виде сплошной зоны и по всей поверхности чашки.
Допускается пересев со среды Китт-Тароцци (1 см3 культуральной жидкости) в стерильную пробирку с заливкой высоким столбиком (11 - 12 см) глюкозным питательным агаром. После застывания агара пробирки термостатируют, как описано выше для пересевов в чашки Петри под стекло. В пробирках анаэробы растут в глубине агара, отступая от поверхности 0,5 - 1,5 см, часто с разрывом среды.
Выделение спор бацилл (аэробов и факультативных анаэробов) производят путем глубинного посева прогретого материала в чашки Петри и заливкой агаризованной средой. Для выделения спор бацилл-мезофилов используют питательный агар с глюкозой, для термофилов - картофельно-пептонный агар. Чашки с посевами бацилл-мезофилов термостатируют при 30 °С 72 ч и более (до 5 суток), термофилов - при 58 ± 3 °С не более 72 ч.
При появлении колоний на чашках Петри проводят микрокопирование с окраской мазков по Граму.
При обнаружении в посевах грамположительных споровых палочек проводят реакцию на каталазу (ГОСТ 10444.3-85). Бациллы и мезофилы, и термофилы образуют каталазу.
Для бацилл-термофилов определяют кислотообразующую способность. Для этого либо на стекле готовят водную суспензию из исследуемой колонии и в эту суспензию добавляют каплю индикатора, либо капают индикатором непосредственно на колонию в чашке Петри. В качестве индикатора используют 0,04 %-ный раствор бромкрезолпурпура. Изменение цвета индикатора из сине-фиолетового в желтый указывает на присутствие в посевах кислотообразующих бацилл-термофилов.
Для выявления спор бацилл-мезофилов допускается использование мясо-пептонного бульона, спор бацилл-термофилов-картофельно-пептонного бульона.
4. ПИТАТЕЛЬНЫЕ СРЕДЫ
4.1. Среды для определения общего количества мезофильных аэробных и факультативно-анаэробных микроорганизмов
|
4.1.1. Сухой питательный агар (Даг НПО "Питательные среды") |
- 35,0 г |
|
Сухой экстракт кормовых дрожжей |
- 2,5 г |
|
Глюкоза |
- 1,0 г |
|
Вода дистиллированная |
- 1000 см3 |
Довести pH до 7,0, стерилизовать 20 мин при 121 °С.
4.1.2. Мясо-пептонный (агар) бульон с глюкозой
К 1 дм3 мясо-пептонного бульона (агара) перед стерилизацией добавляют 1 г или 10 г глюкозы, устанавливают pH 7,0 - 7,2 и стерилизуют 20 мин при 121 °С.
4.1.2.1. Мясо-пептонный бульон (агар)
10 г пептона и 5 г хлористого натрия добавляют к 1 дм3 мясной воды. Устанавливают pH 7,0 - 7,2, кипятят, фильтруют через бумажный фильтр. Стерилизуют 20 мин при 121 °С. При выпадении осадка в мясо-пептонном бульоне его вторично фильтруют с последующей стерилизацией. Для приготовления мясо-пептонного агара в 1 дм3 мясо-пептонного бульона перед стерилизацией добавляют 15 - 20 г агара и кипятят на слабом огне при постоянном помешивании до полного растворения агара. Устанавливают pH 7,0 - 7,2, разливают в пробирки или флаконы и стерилизуют 20 мин при 121 °С.
4.2. Среды и реактивы для обнаружения бактерий группы кишечных палочек (колиформных бактерий)
4.2.1. Среда Кесслер (с лактозой)
К 1 дм3 водопроводной воды добавляют 10 г пептона, 50 см3 стерильной бычьей желчи. Смесь кипятят на водяной бане при помешивании 20 - 30 мин. Затем фильтруют ее через ватно-марлевый фильтр, добавляя 2,5 г лактозы; доводят объем водой до 1 дм3. Устанавливают pH 7,4 - 7,6, используя 1 Н растворы NaOH или НСl и проверяя значения pH на потенциометре или универсальной бумагой. Добавляют 2 см3 1 %-ного водного раствора генцианового фиолетового, разливают по 10 см3 в пробирки с поплавками. Стерилизуют 15 мин при 121 °С.
4.2.2. Сухая среда Кесслер (модифицированная) производства Литовского филиала ВНИИМС (ТУ 49 365-76) с учетом изм. № 2 от 01.05.85.
Подготовку среды для посева проводят согласно прописи на этикетке.
4.2.3. Среда Хейфеца (с лактозой)
В 1 дм3 водопроводной воды растворяют 10 г пептона, 5 г хлористого натрия, 5 г лактозы, устанавливают pH 7,4 - 7,6, нагревают до кипения, фильтруют, добавляют 1 см3 5 %-ного спиртового раствора розоловой кислоты и 2,5 см3 0,1 %-ного раствора метиленового голубого. Сразу разливают по 10 см3 в стерильные пробирки с поплавками и стерилизуют 20 мин при 112 °С.
Для приготовления розоловой кислоты 0,5 г порошка заливают 10 см3 этилового ректификованного спирта; через 24 ч раствор готов к употреблению. Раствором можно пользоваться в течение месяца со дня приготовления.
Для приготовления метиленового голубого 0,1 г порошка заливают 100 см3 дистиллированной воды. Через сутки раствор готов к употреблению. При хранении свойства его не изменяются, срок хранения не ограничен.
Краски хранят в темном месте при комнатной температуре.
4.2.4. Среды Эндо, Левина
Среды Эндо и Левина выпускаются в сухом виде Дагестанским НПО "Питательные среды". Их следует готовить согласно прописям, указанным на этикетках банок Изготовленные и разлитые в стерильные чашки Петри среды можно хранить при температуре 4 °С до 10 суток
4.3. Среды и реактивы для определения сальмонелл
4.3.1. Среды предварительного обогащения
4.3.1.1. Пептонно-буферная вода
|
калия дигидрофосфат (KН2РО4) |
- 0,45 г |
|
натрия гидрофосфат, безводный (Na2НРО4) |
- 5,34 г |
|
пептонная вода (1 г пептона + 1000 см3 дистиллированной воды) |
- 1000 см3 |
Приготовление: ингредиенты смешивают, разливают в пробирки или флаконы, стерилизуют в автоклаве при 121 °С 30 мин.
4.3.2. Среды обогащения
4.3.2.1. Среда Мюллера (тетратионатовый бульон Мюллера)
|
мел, стерилизованный сухим жаром |
- 45 г |
|
или кальция карбонат (СаСO3), сухой, стерильный |
- 25 г |
|
бульон Хоттингера, содержащий 120 - 130 мг % аминного азота (или мясо-пептонный бульон) |
- 900 см3 |
|
раствор Люголя |
- 20 см3 |
|
натрия тиосульфат (Na2S2O3∙5Н2О) (часто неправильно именуют гипосульфитом), 50 %-ный стерильный раствор |
- 100 см3 |
Приготовление: в стерильные флаконы помешают по 4,5 г мела, стерилизуют сухим жаром, после чего в каждый флакон наливают по 90 см3 бульона Хоттингера. Стерилизуют при 121 °С 30 мин (pH 7,2 - 7,4). Затем ex tempore асептически добавляют в каждый флакон точно по 2 см3 раствора Люголя и по 10 см3 раствора натрия тиосульфата, хорошо смешивают и разливают по пробиркам. Готовая среда стерилизации не подлежит.
Приготовление раствора Люголя:
|
калия йодид (KI) |
- 20 г |
|
йод кристаллический (I2) |
- 25 г |
|
вода дистиллированная |
- 100 см3 |
Приготовление 50 %-ного раствора натрия тиосульфата
В измерительный цилиндр насыпают 50 г натрия тиосульфата и добавляют воду до 100 см3, растворяют, переливают во флакон, стерилизуют текучим паром 30 мин.
4.3.2.2. Среда Кауфмана
|
среда Мюллера (стерильная) |
- 500 см3 |
|
желчь бычья (стерильная) |
- 250 см3 |
|
бриллиантовый зеленый (0,1 %-ный водный раствор) |
- 50 см3 |
Приготовление: ингредиенты смешивают, асептически разливают в стерильные пробирки по 10 см3, дополнительно не стерилизуют.
Приготовление 20 %-ного желчного бульона
|
бульон мясо-пептонный или Хотгингера |
- 800 см3 |
|
желчь бычья нативная |
- 200 см3 |
Приготовление: pH должен быть равен 7,6. Разливают по 50 см3 во флаконы с поплавками. Стерилизуют текучим паром три дня по 30 мин.
4.3.2.3. Магниевая среда (или хлормагниевая среда)
Среда состоит из трех растворов:
Раствор 1:
|
пептон |
- 4,2 г |
|
натрия хлорид (NaCl) |
- 7,15 г |
|
калия дигидрофосфат (KH2РО4) |
- 1,48 г |
|
дрожжевой диализат |
- 9 см3 |
|
вода дистиллированная |
- 890 см3 |
Раствор II:
|
магния хлорид (MgCl2∙6Н2О) |
- 35,7 см3 |
|
вода дистиллированная |
- 90 см3 |
Раствор III:
|
бриллиантовый зеленый, 0,5 %-ный водный раствор |
- 0,9 см3 |
Приготовление: все три раствора смешивают в указанных количествах, разливают в необходимых объемах в колбы, флаконы или пробирки, стерилизуют при 112 °С 30 мин.
4.3.2.4. Селенитовый бульон
I вариант. Среду готовят из двух основных растворов: А и Б.
Раствор А состоит из 5 г пептона чешской фирмы "Спофа" или венгерской фирмы "Рихтер", 7 г безводного двузамещенного фосфорнокислого натрия, 3 г однозамещенного фосфорнокислого натрия, 4 г х.ч. лактозы, 100 см3 дистиллированной воды, pH 6,9 - 7,1. Раствор стерилизуют 30 мин при температуре 112 °С.
Раствор Б состоит из 10 %-ного раствора кислого селенистокислого натрия, приготовленного на стерильной воде. Раствор готовят непосредственно перед употреблением.
При изменении серии любого из входящих в среду компонентов (пептона, кислого селенистокислого натрия, фосфатов) производят предварительную подтитровку, для чего экспериментально определяют точную пропорцию фосфорнокислого двузамещенного безводного натрия и фосфорнокислого однозамещенного натрия, которая с используемыми образцами пептона и селенистокислого натрия дает pH не выше 6,9 - 7,1, что регулируется изменением соотношения фосфатов.
Для приготовления селенитовой среды в 50 см3 раствора А стерильно добавляют 2 см3 раствора Б. Среду разливают в стерильные пробирки по 5 - 7 см3, но не стерилизуют.
II вариант. Селенитовый бульон с аминопептидом
|
бульон аминопептидный |
- 960 см3 |
|
натрия гидрофосфат (Na2НРО4) |
- 8 г |
|
натрия дигидрофосфат (NaH2РО4) |
- 2 г |
|
натрия гидроселенит (NaHSeO3), 10 %-ный водный раствор |
- 40 см3 |
Приготовление: реакцию среды не устанавливают, т.к pH может колебаться в пределах 7,1 - 7,2. Стерилизуют при 112 °С 20 мин. Непосредственно перед употреблением добавляют 40 см3 стерильного 10 %-ного водного раствора гидроселенита (pH при этом снижается на 0,1 - 0,2), среду хорошо перемешивают и асептически разливают в стерильные пробирки по 5 см3.
Примечание: фосфаты натрия могут быть заменены фосфатами калия в тех же количествах.
Приготовление аминопептидного бульона
|
аминопептид |
- 250 см3 |
|
натрия хлорид (NaCl) |
- 5,5 г |
|
вода дистиллированная |
- 750 см3 |
Приготовление: среду хорошо перемешивают, стерилизуют при 121 °С 20 мин. Готовый бульон можно хранить в бутылях неопределенный срок, желательно при 6 - 10 °С.
4.3.3. Дифференциально-диагностические среды для пересевов со сред обогащения
4.3.3.1. По степени подавления роста посторонней микрофлоры различают среды:
- высокоселективные - висмут-сульфитный агар;
- среднеселективные - среда Плоскирева, слабощелочной питательный агар;
- низкоселективные - среды Эндо, Левина.
4.3.3.2. Среды Эндо, Левина, Плоскирева, висмут-сульфитный агар выпускаются в сухом виде. Способ приготовления указан на этикетке.
4.3.4. Среды для первичной идентификации
4.3.4.1. Комбинированная среда по Олькеницкому
|
агар питательный сухой |
-25 г |
|
лактоза |
- 10 г |
|
аммоний-железо (II) сульфат (FeSO4∙(NaH4)2SO4∙6Н2О) |
- 0,2 г |
|
натрия тиосульфат (Na2S2O3∙5Н2О) |
- 0,3 г |
|
мочевина |
- 10 г |
|
феноловый красный (0,4 %-ный водный раствор) |
- 4 см3 |
|
вода дистиллированная |
- 1000 см3 |
Приготовление: соли предварительно растворяют в небольшом объеме дистиллированной воды. Углеводы и мочевину также растворяют в небольших объемах воды при подогревании в водяной бане. Сухой питательный агар расплавляют в оставшемся объеме воды при нагревании и помешивании. Затем все ингредиенты соединяют, перемешивают с расплавленным агаром, фильтруют через марлевый фильтр, устанавливают pH 7,2 - 7,4, добавляют индикатор и разливают в пробирки по 6 - 7 см3. Среду стерилизуют текучим паром 3 дня подряд по 20 мин и скашивают, оставляя столбик 2 - 2,5 см. Готовая среда бледно-розового цвета.
4.3.4.2. Агар Клиглера
Коммерческую сухую среду готовят в соответствии с указаниями на этикетке препарата. Готовая к употреблению среда имеет красновато-бурый или оранжево-красный цвет, при скашивании следует оставлять столбик высотой 2 - 2,5 см.
4.3.4.3. Среда Ресселя
Приготовление среды Ресселя (сухой) указано на этикетке.
4.3.5. Среды и реактивы для биохимической дифференциации сальмонелл
4.3.5.1. Среды Гисса (среды с углеводами)
Выпускаются коммерческие сухие среды с углеводами (глюкозой, лактозой, мальтозой, сахарозой и маннитом). Их приготовление указано на этикетке.
4.3.5.2. Реактив Эрлиха (на индол)
Взвешивают 5 г парадиметиламидобензальдегида в стеклянном стакане вместимостью 100 см3, помещают в коническую колбу вместимостью 200 см3 и растворяют в 50 см3 этилового спирта. С помощью мерного цилиндра вместимостью 100 см3 медленно добавляют 50 см3 концентрированной соляной кислоты. Раствор хранят в колбе с притертой пробкой при температуре 4 °С.
4.3.5.3. Реактив Ковача (на индол)
В 75 см3 амилового спирта растворяют 5 г парадиметиламидобензальдегида, затем медленно добавляют 25 см3 концентрированной соляной кислоты. Реактив хранят в колбе с притертой пробкой из темного стекла при температуре 4 - 8 °С.
4.3.5.4. Приготовление индикаторной бумаги для определения сероводорода
В 100 см3 дистиллированной воды растворяют 20 г уксусно-кислого свинца и 1 г двууглекислого натрия. Этим раствором пропитывают полоски фильтровальной бумаги, высушивают их при температуре 18 - 23 °С и нарезают на узкие полоски. После приготовления бумага остается белой; при наличии сероводорода чернеет.
4.3.6. Агглютинирующие сальмонеллезные сыворотки
Необходимые разведения сыворотки готовят перед использованием согласно прилагаемой к коробке инструкции.
4.4. Питательные среды и реактивы для определения сульфитредуцирующих клостридий
4.4.1. Среда Китт-Тароцци
|
мясо-пептонный бульон |
- 1000 см3 |
|
глюкоза |
- 10 г |
|
агар |
-1,5 г |
|
кусочки печени или рыбы, или мяса вареные |
- 1 см3 |
Приготовление: стерильные пробирки заполняют на 1 - 1,5 см кусочками вареной печени или мяса, или рыбы и заливают приготовленным мясо-пептонным бульоном с глюкозой и агаром (в 1000 см3 МПБ вносят 10 г глюкозы и 1,5 г агара, который при нагревании постепенно расплавляют). Высота слоя МПБ в пробирках 12 - 13 см. Пробирки со средой стерилизуют 20 мин при 121 °С. pH среды после стерилизации должен быть 7,1.
При приготовлении среды впрок вместо добавления к ней агара на поверхность среды перед стерилизацией в пробирки наслаивают 0,5 - 1,0 см вазелинового масла.
При применении среды Китт-Тароцци без добавления в нее агара или вазелинового масла на поверхность среды после окончания посева наслаивают голодный агар или парафиновую смесь высотой 1,0 - 1,5 см.
При посевах в свежеприготовленную среду Китт-Тароцци (не более 3 сут. с момента приготовления) добавлять агар, вазелиновое масло или наслаивать на ее поверхность голодный агар не обязательно.
4.4.1.1. Приготовление вареной говяжьей печени
500 г говяжьей печени режут на куски массой по 30 - 40 г, заливают водой и кипятят в течение 15 - 20 мин. Воду сливают, куски печени разрезают на кусочки массой 1,5 - 3,0 г, заливают водой, подщелоченной двууглекислым натрием до pH 7,2 - 7,4, и кипятят, не допуская бурного кипения. Общее количество добавленной воды 1000 см3. Затем печень промывают в дуршлаге под струей воды в течение 1 ч и два - три раза дистиллированной водой.
Кусочки печени раскладывают во флаконы, заливают водой и стерилизуют 20 мин при 120 °С.
4.4.1.2. Масло вазелиновое
Масло разливают по 20 - 50 см3 в пробирки или колбы и стерилизуют 20 мин при 120 °С.
Применяют для наслаивания на жидкие питательные среды для анаэробных микроорганизмов.
4.4.1.3. Агар голодный
2,0 г агара растворяют в 98 см3 дистиллированной воды, стерилизуют 20 мин при 120 °С.
4.4.1.4. Парафиновая смесь
Растапливают равные количества парафина и вазелинового масла, смешивают и стерилизует горячим воздухом при температуре 140 °С в течение 60 мин.
Применяют для наслаивания на жидкие питательные среды для анаэробных микроорганизмов.
4.4.2. Среда Вильсон-Блера
На дистиллированной воде готовят 20 %-ный раствор серноватистокислого натрия и 8 %-ный раствор хлористого железа. Оба раствора кипятят.
100 см3 3 %-ного мясо-пептонного агара растапливают на водяной бане и добавляют 1 г глюкозы, 10 см3 20 %-ного раствора серноватистокислого натрия и 1 см3 8 %-ного раствора хлористого железа. Среду разливают в пробирки по 7 см3.
4.4.3. Среда Вильсон-Блера (модифицированная для анаэробов)
|
мясо-пептонный агар с 1 % глюкозы |
- 100 см3 |
|
натрий сернистокислый (Na2SO3), 20 %-ный раствор |
- 10 см3 |
|
железоаммонийные квасцы Fe(KH4)∙(SO4)2∙12Н2O 5 %-ный раствор |
- 1,0 см3 |
К расплавленному и охлажденному до 80 °С мясо-пептонному агару с глюкозой добавляют асептически растворы сернистокислого натрия и железоаммонийных квасцов (растворы сернистокислого натрия и квасцов стерилизуют при температуре (115 ± 1) °С 30 мин либо готовят на горячей (75 ± 5) °С стерильной дистиллированной воде; растворы хранению не подлежат), pH готовой среды при 25 °С составляет 7,7 ± 0,1. Среду разливают по (18 ± 2) см3 в чашки Петри и используют после застывания и подсушивания при температуре (37 ± 1) °С в течение 3 - 4 ч.
4.4.4. Среда Роберта
|
бульон мясо-пептонный стерильный |
- 25 см3 |
|
желатин |
- 30 г |
|
агар |
- 1 г |
|
калий фосфорнокислый двузамещенный (K2НРО4) |
- 2 г |
|
калий азотнокислый (KNO3) |
- 2 г |
|
2,3,5-трифенилтетразолиум хлорид, 1 %-ный водный раствор |
- 10 см3 |
В воду вносят фосфорнокислый калий, азотнокислый калий, агар и желатин, дают набухнуть желатину и нагревают на водяной бане до полного растворения желатина и агара, добавляют стерильный мясо-пептонный бульон и 1 %-ный раствор 2,3,5-трифенилтетразолиум хлорида (1 г 2,3,5-трифенилтетразолиум хлорида вносят в мерную колбу вместимостью 100 см3, доводят объем дистиллированной водой до метки). Устанавливают pH среды таким образом, чтобы после стерилизации он составлял при 25 °С 7,1 ± 0,1. Стерилизуют трое суток подряд при температуре (100 ± 1) °С 20 мин либо однократно при температуре (110 ± 1) °С 15 мин. Готовая среда должна быть бесцветной. Среду хранят при температуре (3 ± 2) °С не более 7 дней.
4.4.5. Среда сульфитжелезная полужидкая
|
МПБ |
- 100 см3 |
|
дрожжевой экстракт сухой или |
- 1 г |
|
жидкий |
- 5 г |
|
сульфит натрия, водный раствор (допускается заменить сульфит натрия Na2SO3 на гипосульфит натрия Na2S2O3∙5Н2О в количестве 1 г на 1000 см3 среды; цитрат железа FeCl3 в тех же концентрациях) |
- 1 см3 |
|
железо лимоннокислое (цитрат) 5 %-ный водный раствор |
- 1 см3 |
К МПБ добавляют дрожжевой экстракт и агар, устанавливают pH таким образом, чтобы после стерилизации его показатель составлял при 25 °С 7,1 ± 0,1, и стерилизуют при температуре (121 ± 1) °С 15 мин. После стерилизации и регенерации добавляют горячие (70 - 80) °С растворы сульфита натрия и лимоннокислого железа, стерилизованные или приготовленные на стерильной дистиллированной воде. Среду перемешивают, разливают в пробирки по 10 - 12 см3 и используют для посева.
4.4.6. Среда улучшенная клостридиальная (A.C.N.)
|
мясной экстракт |
- 10 г |
|
дрожжевой экстракт сухой или |
- 3 г |
|
жидкий |
- 15 г |
|
крахмал растворимый |
- 1 г |
|
глюкоза |
- 5 г |
|
хлорид натрия |
- 5 г |
|
гидрохлорид L-цистенна |
- 0,5 г |
|
уксуснокислый натрий безводный (NaCH3СООН) или |
- 3 г |
|
уксуснокислый натрий водный (NaCH3СООН∙3Н2О) |
- 5 г |
|
агар |
- 15 г |
В воде растворяют все ингредиенты при нагревании, охлаждают до (50 ± 5) °С, устанавливают pH таким образом, чтобы он составлял при 25 °С 7,0 ± 0,1, разливают в пробирки, стерилизуют при температуре (115 ± 1) °С 20 мин. Среду перед высевом регенерируют. Хранят при температуре (6 ± 2) °С не более 7 дней.
4.5. Среды для определения бактерий рода протей
4.5.1. Среда жидкая селективная (Калины Г. и Комаровой Л.)
Основа среды: к 1 дм3 мясо-пептонного бульона добавляют 1 г маннита, 50 см3 натуральной бычьей желчи или эквивалентное количество сухой желчи, 0,8 г калия гидроортофосфата, 2 см3 раствора кристаллического фиолетового (приготовленного: 1 г/дм3∙0,1 г кристаллического фиолетового переносят в мерную колбу вместимостью 100 см3, растворяют в дистиллированной воде; раствор доливают до метки), 2 см3 спиртового раствора бромтимолового синего (1,6 г бромтимолового синего переносят в мерную колбу вместимостью 100 см3 и растворяют в 96 %-ном этаноле; раствор доливают до метки этанолом). Устанавливают pH таким образом, чтобы после стерилизации он составлял 6,9 ± 0,1 при 25 °С. Стерилизуют текучим паром при 100 °С в течение 15 мин.
Для приготовления среды к основе добавляют асептически 10 см3 раствора мочевины (50 г мочевины на 100 см3 дистиллированной воды, раствор доливают до метки) и 100000 ЕД полимиксина В сульфата или 120000 ЕД полимиксина М сутьфата. Среду разливают в стерильные пробирки по 5 см3. Хранят при (3 ± 2) °С не более 7 суток. Готовая среда прозрачная, желто-бурого цвета.
Дифференциально-диагностические плотные среды
4.5.2. Агар дезоксихолат-цитрат лактозный по Leifson в модификации Hynes.
Основа среды: в 1 дм3 кипящей мясной воды растворяют 5 г пептона, 10 г лактозы, 22,5 г агара, охлаждают до (45 - 50) °С, устанавливают pH таким образом, чтобы при 25 °С он составлял 7,4 ± 0,1. Прибавляют 0,03 г нейтрального красного, разливают мерно по колбам, стерилизуют при (115 ± 1) °С в течение 20 мин. Хранят при температуре (3 ± 2) °С не более 7 суток.
Для приготовления питательной среды к расплавленной и охлажденной до (45 - 50) °С основе прибавляют из расчета на 100 см3 основы 5 см3 раствора солей (17 г натрия цитрата, 1 г натрия тиосульфата, 2 г цитрата железа помещают в мерную колбу вместимостью 100 см3, растворяют в дистиллированной воде; раствор доводят до метки и выдерживают на водяной бане при (60 ± 1) °С в течение 1 ч; раствор хранят при комнатной температуре не более 3 мес.) и 5 см3 раствора дезоксихолата натрия (10 г натрия дезоксихолата переносят в мерную колбу вместимостью 100 см3, растворяют в дистиллированной воде; раствор доливают до метки и выдерживают на водяной бане при (60 ± 1) °С в течение 1 ч; раствор хранят при комнатной температуре не более 3 мес.).
Среду перемешивают и разливают по стерильным чашкам Петри по ГОСТ 26670. Среду используют в день ее приготовления.
4.5.3. Агар дифференциально-диагностический (Калина Г. и Комаровой Л.)
К 1 дм3 расплавленного мясо-пептонного агара добавляют 15 см3 дрожжевого экстракта, 10 г маннита, 10 г мальтозы, 80 см3 натуральной бычьей желчи или эквивалентное количество сухой желчи, 2 г железа (III) цитрата, 0,05 г натрия тиосульфата, 0,5 см3 раствора кристаллического фиолетового, 2 см3 щелочного раствора фенолового красного (щелочной раствор фенолового красного массовой концентрацией 16 г/дм3: 1,6 г фенолового красного растворяют в мерной колбе вместимостью 100 см3 в растворе натрия гидроокиси массовой концентрацией 100 г/дм3, раствор доливают раствором натрия гидроокиси до метки); раствор антибиотика (раствор полимиксин В сульфата или полимиксин М сульфата готовят непосредственно перед использованием, для этого во флакон со стерильным антибиотиком вносят 5 или 10 см3 стерильной дистиллированной воды и 120000 ЕД полимиксина М сульфата или 100000 ЕД полимиксина В сульфата).
Среду стерилизуют текучим паром (при 100 °С) в течение 15 мин и разливают после охлаждения по стерильным чашкам Петри. Среду хранят при (4 ± 2) °С не более 7 суток. Готовая среда оранжево-красного цвета.
4.5.4. Среда для расщепления фенилаланина
15 см3 дрожжевого экстракта, 2 г Д-фенилаланина фосфорнокислого двузамещенного, 5 г натрия хлорида, 12 г агара растворяют в 1 дм3 кипящей дистиллированной воды. По 5 см3 среды разливают в пробирки, стерилизуют при (121 ± 1) °С 10 мин, дают застыть в наклонном положении. Среду хранят при (3 ± 2) °С не более 7 суток.
4.5.5. Раствор хлорного железа массовой концентрацией 100 г/дм3; 16,6 г (FeCl3∙6H2O) переносят в мерную колбу вместимостью 100 см3, растворяют в дистиллированной воде. Раствор доливают до метки.
4.5.6. Агар тройной сахарный с цитратом железа
В 1 дм3 мясо-пептонного бульона растворяют при нагревании 15 см3 дрожжевого экстракта, 10 г пептона, 10 г лактозы, 10 г сахарозы, 1 г глюкозы, 0,3 г железа (III) цитрата, 0,3 г натрия тиосульфата, 0,024 г фенолового красного, 15 г агара. Устанавливают pH таким образом, чтобы после стерилизации он составлял при 25 °С 7,4 ± 0,1. Разливают в пробирки по 10 см3 и стерилизуют при температуре (121 ± 1) °С в течение 10 мин, дают застыть в наклонном положении, чтобы максимальная высота столбика составляла 2,5 см. Среда имеет коричнево-красную окраску. Хранят при комнатной температуре не более 7 суток.
4.6. Среды и реактивы для обнаружения плазмокоагулирующих стафилококков
4.6.1. Солевой бульон
К 100 см3 мясо-пептонного бульона (МПБ) с pH 7,2 - 7,4 в колбе вместимостью 200 см3 добавляют 6,5 г хлористого натрия и разливают в пробирки по 10 см3. Стерилизуют в автоклаве при 121 °С в течение 20 мин.
4.6.1.1. Мясо-пептонный бульон по п. 4.1.2.
4.6.2. Желточно-солевой агар (ЖСА)
Основа - солевой агар: к мясо-пептонному бульону (МПБ) с pH 7,2 - 7,4 добавляют 2 % агара и 6,5 % хлористого натрия, расплавляют на водяной бане, при необходимости фильтруют через ватно-марлевый фильтр, разливают мерным цилиндром по 100 см3 в колбы вместимостью 250 см3 и стерилизуют при 121 °С в течение 30 мин. Получают солевой агар. Вместо мясо-пептонного бульона можно использовать сухой питательный агар, добавив к нему 6,5 % хлористого натрия.
ЖСА: на 100 см3 стерильного расплавленного и остуженного до 45 °С солевого агара добавляют 20 см3 эмульсии яичного желтка. После полного размешивания желточно-солевой агар разливают в стерильные чашки Петри по 20 - 25 см3 и хранят в холодильнике до 5 - 7 дней.
4.5.2.1. Эмульсия яичного желтка
На дно стерильной чашки Петри помещают куриное яйцо, которое тщательно протирают ватой, смоченной этиловым спиртом. Стерильным пинцетом пробивают с двух противоположных сторон яйца два отверстия. Через одно из этих отверстий из яйца полностью удаляют белок, а затем, несколько увеличив отверстие, выливают желток в стерильную колбу вместимостью 200 см3. К желтку постепенно добавляют (частями по 20 - 30 см3) 180 - 200 см3 стерильного физиологического раствора, затем содержимое тщательно встряхивают до получения гомогенной массы.
4.6.3. Агар типа Байрд-Паркер
30 г сухого питательного агара на основе ферментативного гидролизата кормовых дрожжей Дагестанского НПО "Питательные среды" размешивают в 1 дм3 дистиллированной воды, добавляют 10 г пирувата натрия, 5 г хлористого лития, тщательно перемешивают и кипятят в течение 1 мин до полного растворения ингредиентов. Устанавливают pH 7,2. Разливают во флаконы объемами 100 - 200 - 300 см3 в зависимости от потребности и стерилизуют при 121 °С 15 мин. Среда может храниться в течение месяца в условиях холодильника. Перед употреблением в растопленную и охлажденную до 45 - 50 °С среду с соблюдением правил асептики прибавляют (из расчета на 100 см3 среды) 0,5 см3 2 % раствора теллурита калия и 5 см3 эмульсии яичного желтка. Среду тщательно перемешивают и разливают в чашки Петри в объеме не менее 20 см3 на чашку. Чашки со средой могут быть использованы в течение 24 ч, максимум 48 ч. Перед посевом чашки со средой подсушивают в термостате общепринятым способом.
4.6.4. Цитратная плазма кролика
Цитратная плазма кролика для реакции плазмокоагуляции выпускается в сухом виде. Готовят непосредственно перед употреблением согласно прописи в прилагаемом наставлении.
4.7. Среды для определения спор клостридий, спор аэробных и факультативно-анаэробных микроорганизмов
4.7.1. Среда Китт-Тароцци по п. 4.4.1
4.7.2. Среда Китт-Тароцци с углекислым кальцием, дрожжевым экстрактом и аскорбиновой кислотой
Готовят среду Китт-Тароцци с углекислым кальцием, но в мясо-пептонный бульон перед фасовкой вносят 2 г сухого дрожжевого экстракта или 10 см3 жидкого дрожжевого экстракта. Перед анализом в регенерированную среду Китт-Тароцци с углекислым кальцием и дрожжевым экстрактом асептически вносят аскорбиновую кислоту из расчета 100 мкг на 1000 см3 среды.
4.7.2.1. Среда Китт-Тароцци с углекислым кальцием
В пробирку или флаконы, предназначенные для среды Тароцци, добавляют на дно щепоту углекислого кальция, стерилизуют горячим воздухом по ГОСТ 26668-85, закладывают в них кусочки мяса или печени и заливают мясо-пептонным бульоном с глюкозой, приготавливая среду далее как просто Китт-Тароцци.
4.7.3. Мясо-пептонный агар (бульон) с глюкозой по п. 4.1.2.
4.7.4. Бульон (агар) картофельно-пептонный
|
картофель |
- 200 г |
|
пептон |
- 5 г |
|
хлорид натрия |
- 5 г |
|
агар (если необходимо) |
- 15 - 20 г |
200 г очищенного и нарезанного кусочками картофеля заливают 1 дм3 водопроводной воды, кипятят 15 - 20 мин, не допуская разваривания кусочков, фильтруют через ватно-марлевый фильтр и доводят объем фильтрата до первоначального. В фильтрате растворяют 5 г пептона, 5 г хлорида натрия и расплавляют при нагревании 15 - 20 г агара. Устанавливают pH 7,1 ± 0,1. Разливают в колбы и пробирки и стерилизуют при температуре (125 ± 1) °С в течение 30 мин.
Рекомендуется контролировать стерильность среды, термостатируя ее при (59 ± 1) °С 48 ч.
4.7.5. Печеночно-глицериновая среда
К 1 дм3 печеночного бульона добавляют 5 г глицерина, 5 г глюкозы, разливают в пробирки или флаконы с кусочками печени (20 - 30 г печени на 100 см3 среды), устанавливают pH 7,0 ± 0,1 и стерилизуют при температуре (121 ± 1) °С в течение 20 мин.
5. ЛАБОРАТОРНАЯ ДОКУМЕНТАЦИЯ
Все данные по микробиологическому контролю производства и санитарного состояния записывают в соответствующие лабораторные журналы.
Лабораторные журналы должны быть прошнурованы, страницы пронумерованы и скреплены печатью вышестоящей организации.
Журналы хранятся у микробиолога. По истечении 3 лет вся документация сдается по акту в архив предприятия. Формы журналов даны в приложениях.
Генеральный директор НПО "Комплекс" В.В. Гущин
Зав. лабораторией санитарно-гигиенической оценки сырья и продуктов А.А. Гусев
6. ПРИЛОЖЕНИЯ
Приложение 1
ЖУРНАЛ микробиологического контроля санитарного состояния производства
|
№ п/п |
Дата анализа |
Наименование исследуемого объекта |
Размер исследуемой поверхности |
БГКП |
ОМЧ (КОЕ/см2) |
Микроорганизмы по показаниям производства и требованиям ветсанслужбы |
Заключение, предложения |
Подпись бактериолога |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
Приложение 2
ЖУРНАЛ микробиологического контроля мяса птицы, потрохов, полуфабрикатов, рецептурных компонентов, используемых в производстве
|
№ п/п |
Дата анализа |
Наименование проб |
Поставщик |
ОМЧ (КОЕ/г) |
Наличие сальмонелл в 25 г |
Протей |
Споры клостридий |
Споры бацилл в 1 г |
Заключение |
Подпись бактериолога |
|||||
|
Среда накопления |
ВСА |
Реакция с поливалентной сывороткой |
СРК |
мезофилов |
термофилов |
мезофилов |
термофилов |
||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
Приложение 3
ЖУРНАЛ микробиологического контроля продуктов сублимационной сушки и готовых колбасно-кулинарных изделий
|
№ п/п |
Дата анализа |
Наименование исследуемого продукта |
Определяемые бактериологические показатели |
Заключение, предложения |
Подпись бактериолога |
||||||||
|
ОМЧ (KOE/г) |
БГКП |
Наличие сальмонелл в 25 г восстановленного продукта |
Сульфитредуцирующие клостридии в 0,1 г |
Патогенные стафилолококки в 1 г продукта |
Наличие протея |
||||||||
|
среда накопления |
ВСА, мазки |
реакция с поливалентной сывороткой |
вегетативные формы |
споровые формы |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
Примечание: О проведении дополнительных исследований по показателям, не указанным в таблице, проводить запись в разделе "Заключение".
Приложение 4
ЖУРНАЛ микробиологического контроля санитарного состояния производства консервов
|
№ п/п |
Дата |
Визуальная оценка санитарного состояния контролируемого цеха, линии, отдельных участков производства |
Место отбора пробы для анализа |
Определяемые бактериологические показатели |
Предложения по улучшению санитарного состояния и подпись микробиолога |
Отметка о принятых мерах и подпись ответственного лица |
|||
|
контролируемый участок или оборудование |
удовлетворительное или неудовлетворительное |
общая обсемененность |
бактерии группы кишечных палочек |
термофилы или другие специфические возбудители порчи в смывах с оборудования |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
Приложение 5
ЖУРНАЛ микробиологического контроля производства консервов
|
№ п/п |
Дата анализа |
Смена и час анализа |
Наименование консервов |
Контрольный этап производства |
pH продукта |
Температура продукта при отборе проб |
Общая обсемененность |
Наличие спор |
Предполагаемые причины повышения бактериологической обсемененности |
Какие меры и кому рекомендованы |
Подпись бактериолога |
||||
|
мезофилы |
термофилы |
||||||||||||||
|
аэробов |
рост на среде Тароцци |
рост на чашках под стеклом |
аэробов |
анаэробов |
|||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
7. СПИСОК ИСПОЛЬЗОВАННОЙ ДОКУМЕНТАЦИИ
1. Временная технологическая инструкция по выработке и использованию мяса цыплят механической обвалки для продуктов детского питания. М: Минмясомолпром СССР, 1983.
2. Временные гигиенические нормативы содержания некоторых химических элементов в основных пищевых продуктах. М: Утверждено Минздравом СССР 30.09.81 г. № 2450-81. 1982.
3. Временные правила сдачи-приемки птицы непосредственно в хозяйствах. - М.: Утверждено Минмясомолпромом РСФСР, Минзаготовок РСФСР. 1979.
4. ГОСТ 4288-76. Изделия кулинарные и полуфабрикаты из рубленого мяса. Правила приемки и методы испытания.
5. ГОСТ 5981-82. Банки металлические для консервов.
6. ГОСТ 18963-73. Вода питьевая. Методы санитарно-бактериологического анализа.
7. ГОСТ 9225-84. Молоко и молочные продукты. Методы микробиологического анализа.
8. ГОСТ 10444.9-88. Продукты пищевые. Метод определения Clostridium perfringens.
9. ГОСТ 10444.7-86 (СТ СЭВ 5211-85). Продукты пищевые. Методы выявления ботулинических токсинов и Clostridium botulinum.
10. Правила ветеринарного осмотра убойных животных и ветеринарно-санитарной экспертизы мяса и мясных продуктов. М.: ВО Агропромиздат. 1988.
11. Временные указания по микробиологическим нормативам для ряда особо скоропортящихся пищевых продуктов и методам их исследования. М., 1982.
12. Ветеринарно-санитарные правила для предприятий (цехов) переработки птицы и производства яйцепродуктов. М., 1987.
13. ГОСТ 10444.0-75. Консервы. Методы микробиологического анализа. Подготовка консервов к анализу.
14. ГОСТ 10444.1-84. Консервы. Приготовление растворов, реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе.
15. ГОСТ 10444.2-75. Консервы. Методы микробиологического анализа. Выявление коагулазоположительных стафилококков.
16. ГОСТ 10444.4-85. Консервы. Методы определения мезофильных анаэробных микроорганизмов.
17. ГОСТ 10444.3-85. Консервы. Методы определения мезофильных аэробных и факультативно-анаэробных микроорганизмов.
18. ГОСТ 10444.5-85. Консервы. Методы определения термофильных аэробных и факультативно-анаэробных микроорганизмов.
19. ГОСТ 10444.6-85. Консервы. Методы определения термофильных анаэробных микроорганизмов.
20. ГОСТ 10444.10-75. Консервы. Методы микробиологического анализа. Выявление Bacillus cereus.
21. ГОСТ 10444.11-75. Консервы. Методы микробиологического анализа. Выявление молочнокислых бактерий.
22. ГОСТ 10444.12-75. Консервы. Методы микробиологического анализа. Выявление дрожжей.
23. ГОСТ 10444.13-75. Консервы. Методы микробиологического анализа. Выявление жизнеспособных плесневых грибов.
24. ГОСТ 10444.14-75. Консервы. Методы микробиологического анализа. Определение содержания плесеней по Говарду.
25. ГОСТ 10444.15-75. Консервы. Методы микробиологического анализа. Определение общего количества микроорганизмов подсчетом на чашках Петри.
26. ГОСТ 25311-82. Мука кормовая животного происхождения. Методы бактериологического анализа.
27. Инструкция по мойке и профилактической дезинфекции на предприятиях мясной и птицеперерабатывающей промышленности. М.: Утверждена Минмясомолпромом СССР 15.01.85. 1985.
28. Инструкция по проведению обязательных медицинских обследований лиц, поступающих на работу и работающих в пищевых предприятиях, на сооружениях по водоснабжению в детских учреждениях и др. М.: Утверждена Главным государственным санитарным инспектором СССР 06.02.61 № 352-61. 1961.
29. Инструкция о порядке санитарно-технического контроля консервов на производственных предприятиях, оптовых базах, в розничной торговле и на предприятиях общественного питания. М.: Утверждена Министерством здравоохранения СССР 18.09.73 № 1121-73. 1973.
30. Инструкция о порядке микробиологического контроля в колбасном производстве. М: Минмясомолпром СССР, 1969.
31. Инструкция по подготовке, наполнению и укупорке консервной тары. М.: Утверждена Минмясомолпромом СССР 23.07.81. 1981.
32. Лабораторная диагностика сальмонеллезов человека и животных, обнаружение сальмонелл в кормах, продуктах питания и объектах внешней среды (Методические указания). М, 1989.
33. Медико-биологические требования и санитарные нормы качества продовольственного сырья и пищевых продуктов. М: Минздрав СССР, 01.08.1989. № 4941-88.
34. Санитарные и ветеринарные требования к проектированию предприятий мясной промышленности. М.: Утверждены Госагропромом СССР 20.04.87 - ВСТП- 06.02.87. 1987.
35. Технологические инструкции по холодильной обработке и хранению мяса и мясопродуктов на мясокомбинатах. М., 1974.
36. Технологическая инструкция по выработке мяса птицы. М.: Минмясомолпром СССР, 1977.
37. Типовые нормы времени и нормативы численности специалистов отделов производственно-ветеринарного контроля предприятий мясной промышленности. М.: ММП ВНИКИМП, 1987.
38. Сборник технологических инструкций по производству мясных консервов. М.: ММ и МП СССР, 1981.
39. Указания о порядке ветеринарно-санитарного осмотра тушек и органов птицы при полном потрошении на конвейерных линиях мясоперерабатывающих предприятий. М.: Утверждены Минсельхозом СССР, 1966.
40. ИСО 2293-76. Мясо и мясные продукты. Контрольный метод определения количества аэробных микроорганизмов при 30 °С.
41. ИСО 3565-75. Мясо и мясные продукты. Определение наличия сальмонелл (контрольный метод).
42. ИСО 3811-79. Мясо и мясные продукты. Обнаружение и подсчет количества предполагаемых колибактерий и кишечной палочки (контрольный метод).
43. ИСО 5552-79. Мясо и мясные продукты. Обнаружение и подсчет энтеробактериазы (контрольный метод).
44. ИСО 4831-78. Микробиология. Общее руководство по подсчету колибактерий. Методика расчета наиболее вероятного значения после инкубации при 30 °С.
45. ИСО 4832-78. Микробиология. Общее руководство по подсчету колиформ. Метод подсчета колоний при температуре 30 °С.
46. ИСО 4833-78. Микробиология. Общее руководство по подсчету микроорганизмов. Метод подсчета колоний при температуре 30 °С.
47. СТ СЭВ 4247-83. Пищевые продукты. Метод определения общего количества мезофильных аэробных и факультативно-анаэробных микроорганизмов посевом в агаризованную среду.
48. СТ СЭВ 4248-83. Пищевые продукты. Метод определения общего количества мезофильных аэробных и факультативно-анаэробных микроорганизмов посевом в жидкие среды.
49. СТ СЭВ 4249-83. Пищевые продукты. Метод определения колиформных бактерий посевом в агаризованную среду.
50. СТ СЭВ 4250-83. Пищевые продукты. Метод определения колиформных бактерий посевом в жидкие среды.
51. СТ СЭВ 5209-85. Продукты пищевые. Метод выявления бактерий рода сальмонелл.
52. СТ СЭВ 5210-85. Продукты пищевые. Метод определения количества Staphilococcus aureus.
53. СТ СЭВ 5211-85. Продукты пищевые. Методы выявления ботулинических токсинов и Cl. botulinum
54. СТ СЭВ 5212-85. Продукты пищевые. Метод определения количества Cl. perftingens.
55. СТ СЭВ 5213-85. Продукты пищевые. Метод определения количества Bac. cereus.
56. СТ СЭВ 5804-86. Пищевые продукты. Метод определения количества бактерий Escherichia coli.
57. СТ СЭВ 5805-86. Продукты пищевые. Метод определения количества бактерий рода Lactobacillus.
58. СТ СЭВ 5806-85. Продукты пищевые. Метод подсчета слизеобразующих бактерий рода Leuconostos.
59. СТ СЭВ 5853-86. Продукты пищевые. Метод определения количества молочнокислых бактерий рода Streptococcus.
60. СТ СЭВ 6075-87. Продукты пищевые. Метод определения количества осмотолерантных дрожжей и плесневых грибов.
61. СТ СЭВ 6076-87. Продукты пищевые. Методы выявления и определения количества бактерий семейства Enterobacteriaceae.
62. СТ СЭВ 6077-87. Продукты пищевые. Методы выявления и определения количества сульфитредуцирующих бактерий.
63. ГОСТ 2874-88. Вода питьевая. Гигиенические требования и контроль за качеством.
64. ГОСТ 10444.12-88. Продукты пищевые. Метод определения дрожжей и плесневых грибов.
СОДЕРЖАНИЕ