ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ
В СФЕРЕ ПРИРОДОПОЛЬЗОВАНИЯ
|
УТВЕРЖДАЮ И. о. директора ФБУ
«Федеральный __________________ А.Б. Сучков «4» июня 2013 г. |
КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ ВОД
МЕТОДИКА ИЗМЕРЕНИЙ МАССОВЫХ
КОНЦЕНТРАЦИЙ ФЕНОЛА И ФЕНОЛОПРОИЗВОДНЫХ
В ПИТЬЕВЫХ, ПРИРОДНЫХ И СТОЧНЫХ ВОДАХ
ГАЗОХРОМАТОГРАФИЧЕСКИМ
МЕТОДОМ
ПНД Ф 14.1:2:4.225-2006
Методика допущена для
целей государственного
экологического контроля
МОСКВА
2006 г.
(Издание 2013 г.)
Методика рассмотрена и одобрена федеральным бюджетным учреждением «Федеральный центр анализа и оценки техногенного воздействия» (ФБУ «ФЦАО»).
Настоящее издание методики действует до выхода нового издания.
Разработчик:
Аналитический центр ЗАО «РОСА»
СОДЕРЖАНИЕ
1 ОБЩИЕ ПОЛОЖЕНИЯ И ОБЛАСТЬ ПРИМЕНЕНИЯ
Настоящий документ устанавливает методику количественного химического анализа различных типов вод с целью определения фенола и фенолопроизводных веществ, (далее - фенолов). Методика предназначена для анализа питьевых вод, в том числе расфасованных в емкости; природных вод, в том числе поверхностных и подземных источников водоснабжения, и морских вод; сточных вод: производственных, хозяйственно-бытовых, ливневых и очищенных. Методика может быть использована для анализа проб талых и технических вод, и проб снежного покрова.
Диапазон измерений массовых концентраций в питьевых и природных водах составляет от 0,0005 до 0,005 мг/дм3, в сточных водах - от 0,001 до 5,0 мг/дм3. Перечень определяемых веществ приведен в таблице 1.
Допускается использовать методику для анализа проб при содержании фенолов в питьевых и природных водах свыше 0,005 мг/дм3, и при содержании в сточных водах свыше 5,0 мг/дм3 при условии разбавления экстракта, но не более, чем в 10 раз.
Блок-схемы проведения анализа питьевой, природной и сточной воды приведены в приложениях 1 и 2.
Продолжительность выполнения анализа одной пробы по определению фенолов - 5 ч., серии из 5 проб - 12 ч.
Таблица 1 - Перечень определяемых веществ
|
Наименование вещества |
|
|
Фенол |
2,3-Ксиленол |
|
о-Крезол |
2,4-Ксиленол |
|
п-Крезол |
2,5-Ксиленол |
|
м-Крезол |
2,6-Ксиленол |
|
о-Этилфенол |
3,4-Ксиленол |
|
п-Этилфенол |
3,5-Ксиленол |
|
2-Изопропилфенол |
2,3,5-Триметилфенол |
|
Фенолы (сумма) |
|
2 НОРМАТИВНЫЕ ССЫЛКИ
ГОСТ 12.0.004-90 Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ 244-76 Натрия тиосульфат кристаллический. Технические условия
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3022-80 Водород технический. Технические условия
ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия.
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 14262-78 Реактивы. Кислота серная особой чистоты. Технические условия
ГОСТ 28311-89 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб
ГОСТ Р 51593-2000 Вода питьевая. Отбор проб
ГОСТ Р 52501-2005 Вода для лабораторного анализа. Технические условия
ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
Примечание - Если ссылочный стандарт заменен (изменен), то следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 ПРИПИСАННЫЕ ХАРАКТЕРИСТИКИ ПОКАЗАТЕЛЕЙ ТОЧНОСТИ
ИЗМЕРЕНИЙ
Настоящая методика обеспечивает получение результатов измерений массовых концентраций фенолов с погрешностями, не превышающими значений, приведенных в таблице 2. Приписанные погрешности измерений не превышают нормы погрешностей, установленные ГОСТ 27384.
Таблица 2 - Диапазон измерений, значения показателей точности, воспроизводимости и повторяемости
|
Диапазон измерений, мг/дм3 |
Показатель повторяемости |
Показатель воспроизводимости |
Показатель точности |
|
Питьевые и природные воды |
|||
|
от 0,0005 до 0,001 вкл. |
18 |
25 |
50 |
|
св. 0,001 до 0,005 вкл. |
14 |
20 |
40 |
|
Сточные воды |
|||
|
от 0,001 до 0,01 вкл. |
18 |
25 |
50 |
|
св. 0,01 до 0,1 вкл. |
14 |
20 |
40 |
|
св. 0,1 до 5 вкл. |
12 |
17,5 |
35 |
|
Примечание - Показатель точности измерений соответствует расширенной неопределенности при коэффициенте охвата k = 2 |
|||
4 МЕТОД ИЗМЕРЕНИЙ
Определение основано на экстракции фенолов из воды диэтиловым эфиром, концентрировании экстракта упариванием и его газохроматографическом анализе с использованием пламенно-ионизационного детектора и альтернативных колонок с последующей идентификацией и определением массовых концентраций индивидуальных веществ по установленной градуировочной характеристике. Для сильно загрязненных вод, например, сточных, требуется предварительная очистка пробы. Для этого проводят предварительную экстракцию пробы воды гексаном.
Примечание - Допускается в качестве экстрагента вместо диэтилового эфира использовать другой растворитель, например, хлористый метилен при условии проведения контроля точности результатов анализа согласно п. 15.1.
5 СРЕДСТВА ИЗМЕРЕНИЙ. ВСПОМОГАТЕЛЬНЫЕ УСТРОЙСТВА.
РЕАКТИВЫ И МАТЕРИАЛЫ
При выполнении измерений применяют следующие средства измерений, вспомогательные устройства, реактивы и материалы:
5.1 Средства измерений, вспомогательное оборудование, лабораторная посуда
5.1.1 Баня песчаная с температурным режимом (50 - 100) °С, снабженная регулятором температуры, например, фирмы «Gerhardt» (Германия).
5.1.2 Весы лабораторные с максимальной нагрузкой 300 г специального или высокого класса точности по ГОСТ Р 53228.
5.1.3 Воронки делительные ВД-3 1000 29/32 по ГОСТ 25336.
5.1.4 Воронки для фильтрования В-75-110 ХС, В-100-150 ХС по ГОСТ 25336.
5.1.5 Государственные стандартные образцы (ГСО) фенолов или вещества гарантированной чистоты с содержанием основного вещества не менее 98 % или аттестованные растворы с относительной погрешностью не более 4 %, например, фирм «Supelco» (США), «ChemService» (США), «Dr. Ehrenstorfer» (Германия) или любой другой. Перечень фенолов приведен в таблице 1.
5.1.6 Дистиллятор или установка любого типа для получения воды дистиллированной по ГОСТ 6709 или воды для лабораторного анализа степени чистоты 2 по ГОСТ Р 52501.
5.1.7 Колбы мерные вместимостью 10 см3 по ГОСТ 1770, класс точности 2.
5.1.8 Колбы конические с притертыми пробками вместимостью 50 и 100 см3 по ГОСТ 25336.
5.1.9 Компрессор сжатого воздуха любой модели, например, «MAXIMA» (Малайзия) для аквариума (сжатый воздух используется для обдува при концентрировании экстракта).
5.1.10 Компьютер персональный, позволяющий работать с программным обеспечением для управления хроматографом, сбора информации и обработки хроматограмм, например, с программой «ChemStation» фирмы «Agilent Technologies» (США).
5.1.11 Мензурки вместимостью 100; 250 и 500 см3 по ГОСТ 1770, класс точности 2.
5.1.12 Микрошприцы вместимостью 0,01; 0,05; 0,10; 0,25; 0,50 и 1,0 см3, например, фирмы «Hamilton» (Австралия).
5.1.13 Пипетки градуированные вместимостью 1; 2; 5 и 10 см3 по ГОСТ 29227, класс точности 2.
Примечание - Допускается использовать дозаторы медицинские лабораторные по ГОСТ 28311.
5.1.14 Пробирки (исполнения 1) вместимостью 10 см3 с ценой деления 0,1 см3 по ГОСТ 1770.
5.1.15 Принтер любой модели.
5.1.16 Стаканы химические вместимостью 25 и 150 см3 по ГОСТ 25336.
5.1.17 Установка для перегонки органических растворителей (гексана), состоящая из круглодонной колбы, дефлегматора, прямого холодильника, приемной колбы, алонжа и водяной бани или колбонагревателя с температурой нагрева от 40 °С до 100 °С, снабженных регулятором температуры.
5.1.18 Устройство для встряхивания емкостей с жидкостью любого типа, например, шюттель-аппарат на 5 мест для делительных воронок вместимостью 1000 см3 фирмы «Agitelec» (Франция).
5.1.19 Флаконы герметично закрывающиеся с завинчивающимися крышками вместимостью 1,5 - 2 см3; 4; 10 и 100 см3, снабженные прокладками с тефлоновым покрытием.
5.1.20 Холодильник двухкамерный бытовой, обеспечивающий температуру холодильной камеры (2 - 10) °С и морозильной камеры минус (12 - 24) °С.
5.1.21 Хроматограф газовый, например, HP 6890 фирмы «Agilent Technologies» (США) в комплекте:
- Детектор пламенно-ионизационный (ПИД), чувствительностью не менее 1×10-8 г/с (по углероду).
- Колонка 1 (основная): хроматографическая капиллярная кварцевая с фазой (50 % цианопропилфенил)-диметилполисилоксан длиной 30 м, внутренним диаметром 0,32 мм, толщиной пленки (0,2 - 0,4) мкм, например, OV-225 фирмы «ВИТОХРОМ» (Россия), или любая другая с фазой, позволяющей разделять фенолы на отдельные компоненты.
- Колонка 2 (альтернативная): хроматографическая капиллярная кварцевая с фазой (5 % фенил)-метилполисилоксан длиной 30 м, внутренним диаметром 0,32 мм и толщиной пленки 0,25 мкм, например, DB-5MS (или DB-5) фирмы «Agilent Technologies» (США).
- Устройство для автоматического отбора и ввода проб, например, HP 6890 Series фирмы «Agilent Technologies».
Примечание - Допускается использовать хроматограф любой другой марки, позволяющий проводить хроматографический анализ в условиях, приведенных в 10.1, с необходимой чувствительностью.
5.1.22 Шкаф сушильный, например, СНОЛ по ТУ 16-681.032.
5.1.23 Цилиндры мерные вместимостью 25 и 50 см3 по ГОСТ 1770, класс точности 2.
Допускается использование средств измерения, вспомогательного оборудования, лабораторной посуды с аналогичными или лучшими метрологическими и техническими характеристиками.
5.2 Реактивы и материалы
5.2.1 Бумага индикаторная универсальная, позволяющая измерять pH в диапазоне от 1 до 12 ед. pH с шагом 1 ед. pH, например, по ТУ 2642-008-11764404 или по ТУ 6-09-1181.
5.2.2 Вата медицинская гигроскопическая по ГОСТ 5556.
5.2.3 Вода дистиллированная по ГОСТ 6709 или вода для лабораторного анализа 2 степени чистоты по ГОСТ Р 52501 (далее - вода дистиллированная).
5.2.4 Водород сжатый по ГОСТ 3022.
5.2.5 Воздух сжатый по ТУ 6 21.
5.2.6 Гелий сжатый по ТУ 51-940.
5.2.7 Гексан (н), ч. по ТУ 2631-03-05807999, очищенный перегонкой (11.1).
5.2.8 Диэтиловый эфир, х.ч. по ТУ 2600-001-45682126.
5.2.9 Кислота серная, ос.ч. по ГОСТ 14262.
5.2.10 Метанол, х.ч. по ГОСТ 6995.
5.2.11 Натрий гидроокись, ч. по ГОСТ 4328.
5.2.12 Натрий серноватистокислый (натрия тиосульфат), стандарт-титр по ТУ 2642-001-07500602 (используют в сухом виде) или ч.д.а. ГОСТ 244.
5.2.13 Натрий сернокислый (натрия сульфат) безводный, ч.д.а. по ГОСТ 4166.
5.2.14 Натрий хлористый (натрия хлорид), х.ч. по ГОСТ 4233.
Допускается использование реактивов более высокой квалификации, а также материалов с аналогичными или лучшими характеристиками.
6 УСЛОВИЯ БЕЗОПАСНОГО ПРОВЕДЕНИЯ РАБОТ
6.1 При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
6.2 При работе с оборудованием необходимо соблюдать правила электробезопасности по ГОСТ Р 12.1.019.
6.3 Обучение работающих безопасности труда должно быть организовано в соответствии с ГОСТ 12.0.004.
6.4 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
7 ТРЕБОВАНИЯ К КВАЛИФИКАЦИИ ОПЕРАТОРА
7.1 К выполнению измерений и обработке их результатов допускают лиц, имеющих специальное среднее или высшее образование химического профиля, владеющих методом хроматографического анализа, знающих конструкцию, принцип действия и правила эксплуатации данного оборудования.
7.2 К выполнению работ по пробоподготовке допускают лиц, имеющих специальное среднее или высшее образование химического профиля, обученных методике подготовки пробы для хроматографического анализа.
8 УСЛОВИЯ ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
температура воздуха от 20 °С до 28 °С
относительная влажность воздуха не более 80 % при 25 °С
напряжение в сети (220 ± 22) В
9 ОТБОР И ХРАНЕНИЕ ПРОБ
9.1 Отбор проб воды осуществляют в соответствии с ГОСТ Р 51592 и ГОСТ Р 51593 в стеклянные герметично закрывающиеся крышками флаконы из темного стекла. Пробы снега в соответствии с ГОСТ 17.1.5.05 переводят в талую воду при температуре окружающей среды. Объем отбираемой пробы питьевой, природной или сточной воды должен быть не менее 0,5 дм3. Рекомендуется отбирать два флакона для обеспечения возможности проведения повторного анализа.
9.2 Пробы воды консервируют на месте отбора тиосульфатом натрия из расчета (80 ± 10) мг соли на 1 дм3 пробы воды и (2 ± 0,5) г гидроокиси натрия.
Примечание - Тиосульфат натрия необходим для связывания остаточного хлора или других окисляющих агентов.
Если проба не была законсервирована на месте отбора, то ее консервируют в лаборатории.
Законсервированную пробу можно хранить при температуре окружающей среды не более 7 суток.
9.3 При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указывается:
- цель анализа;
- место, дата, время отбора;
- шифр пробы;
- должность, фамилия сотрудника, отбирающего пробу.
10 ПОДГОТОВКА К ВЫПОЛНЕНИЮ ИЗМЕРЕНИЙ
10.1 Подготовка аппаратуры
На компьютере в программе управления создают метод анализа с использованием абсолютной градуировки согласно руководству по эксплуатации программного обеспечения. Газовый хроматограф и устройство для автоматического отбора и ввода проб готовят к работе в соответствии с инструкциями по эксплуатации. В качестве газа-носителя используют гелий.
Рекомендуемые параметры газохроматографического анализа:
|
при работе на колонке 1 (основной): |
|
|
Температура детектора |
250 °С |
|
Температура испарителя |
220 °С |
|
Температура термостата колонок |
|
|
начальная |
100 °С |
|
конечная |
145 °С |
|
Время термостатирования при конечной |
|
|
температуре |
3 мин |
|
Расходы газов |
|
|
газа носителя (гелия) |
2 см3/мин |
|
водорода |
30 см3/мин |
|
воздуха |
400 см3/мин |
|
Коэффициент динамического деления потока в инжекторе |
(2 - 20):1 |
|
Скорость потока газа на поддув (гелия) Make up |
33 см3/мин |
|
Скорость подъема температуры |
3,50 °С/мин |
|
Объем хроматографируемой пробы |
0,001 - 0,002 см3 |
|
при работе на колонке 2 (альтернативной): |
|
|
Температура детектора |
300 °С |
|
Температура испарителя |
220 °С |
|
Температура термостата колонок |
|
|
начальная |
60 °С |
|
конечная |
140 °С |
|
Время термостатирования при конечной температуре |
3 мин |
|
Расходы газов |
|
|
газа носителя (гелия) |
1,8 см3/мин |
|
водорода |
30 см3/мин |
|
воздуха |
400 см3/мин |
|
Коэффициент динамического деления потока в инжекторе |
(2 - 20):1 |
|
Скорость потока газа на поддув (гелия) Make up |
33,2 см3/мин |
|
Скорость подъема температуры |
5 °С/мин |
|
Объем хроматографируемой пробы |
(0,001 - 0,002) см3 |
Примечание - Допускается изменять параметры газохроматографического анализа в зависимости от перечня определяемых веществ и используемой хроматографической колонки.
10.2 Подготовка хроматографической колонки
Капиллярные колонки 1 и 2 кондиционируют в соответствии с инструкцией, прилагаемой к колонке, в токе газа-носителя, предварительно отсоединив от детектора. Завершив кондиционирование, колонку подсоединяют к детектору и выводят хроматограф на рабочий режим.
10.3 Приготовление градуировочных растворов
Исходные градуировочные растворы фенола, о-крезола, м-крезола, п-крезола, о-этилфенола, п-этилфенола, 2-изопропилфенола, 2,3-ксиленола, 2,4-ксиленола, 2,5-ксиленола, 2,6-ксиленола, 3,4-ксиленола, 3,5-ксиленола и 2,3,5-триметилфенола с массовой концентрацией 10 мг/см3 в метаноле готовят весовым способом или используют аттестованные растворы (5.1.5).
Срок хранения исходных градуировочных растворов не более 1 года при температуре минус (12 - 24) °С в герметично закрытых флаконах. Перед использованием исходные градуировочные растворы выдерживают при температуре окружающей среды не менее 20 мин.
Основной градуировочный раствор смеси фенолов с массовой концентрацией 0,5 мг/см3 каждого вещества готовят в метаноле. Для этого в мерную колбу вместимостью 10 см3 последовательно вносят по 0,5 см3 исходных растворов фенола, о-крезола, м-крезола, п-крезола, о-этилфенола, п-этилфенола, 2-изопропилфенола, 2,3-ксиленола, 2,4-ксиленола, 2,5-ксиленола, 2,6-ксиленола, 3,4-ксиленола, 3,5-ксиленола и 2,3,5-триметилфенола и доводят объем раствора до метки метанолом.
Основной градуировочный раствор смеси фенолов хранят не более 1 года при температуре минус (12 - 24) °С в герметично закрытых флаконах. Перед использованием основной раствор выдерживают при температуре окружающей среды не менее 20 мин.
Градуировочные растворы смеси фенолов с массовой концентрацией каждого вещества 0,0005-0,0010-0,0050-0,0100-0,0500-0,1000 мг/см3 готовят путем разбавления основного градуировочного раствора смеси фенолов метанолом.
Рекомендуемый порядок приготовления градуировочных растворов представлен в таблице 3. Во флакон вместимостью 1,5 - 2 см3 помещают пипеткой 1 см3 метанола, затем микрошприцем отбирают из этого флакона метанол в объеме, равном объему раствора, который будет добавляться в этот флакон. Например, для приготовления градуировочного раствора № 4 с массовой концентрацией 0,010 мг/см3 вносят пипеткой 1 см3 метанола во флакон, отбирают из него микрошприцем 0,02 см3 метанола и вместо этого объема добавляют микрошприцем 0,02 см3 основного раствора смеси фенолов с массовой концентрацией вещества 0,5 мг/см3.
Приготовленные градуировочные растворы хранят не более 6 месяцев при температуре минус (12 - 24) °С в герметично закрытых флаконах. Перед использованием градуировочные растворы выдерживают при температуре окружающей среды не менее 20 мин.
Таблица 3 - Приготовление градуировочных растворов смеси фенолов
|
Номер раствора |
Массовая концентрация вещества в градуировочном растворе, мг/см3 |
Раствор, используемый для разведения |
Объем метанола, см3 |
Конечный объем градуировочного раствора, см3 |
||
|
Наименование раствора |
Массовая концентрация вещества в растворе, мг/см3 |
Отбираемый объем, см3 |
||||
|
С1 |
0,0005 |
С4 |
0,01 |
0,050 |
0,950 |
1 |
|
С2 |
0,0010 |
С5 |
0,05 |
0,020 |
0,980 |
1 |
|
С3 |
0,0050 |
С6 |
0,10 |
0,050 |
0,950 |
1 |
|
С4 |
0,0100 |
Оси. р-р смеси фенолов |
0,50 |
0,020 |
0,980 |
1 |
|
С5 |
0,0500 |
0,100 |
0,900 |
1 |
||
|
С6 |
0,1000 |
0,200 |
0,800 |
1 |
||
Примечание - Допускается:
- готовить градуировочные растворы с другой массовой концентрацией и в другом объеме с корректировкой схемы их приготовления в указанном диапазоне градуировочной шкалы;
- использовать в качестве растворителей градуировочных растворов диэтиловый эфир, хлористый метилен и другие растворители при условии, что их квалификация не хуже квалификации метанола (5.2.10).
10.4 Установление градуировочных характеристик
Компьютер устанавливают в режим измерения факторов отклика по методу абсолютной градуировки.
Каждый из шести градуировочных растворов анализируют дважды при условиях, указанных в 10.1.
Затем с помощью программного модуля градуировки управляющей программы получают для каждого анализируемого вещества градуировочный график и относительный градуировочный коэффициент Ai, который используют при обработке результатов измерений.
Градуировку хроматографа проводят 1 раз в 6 месяцев, при смене хроматографической колонки или после ремонта оборудования, повлекшего за собой изменение условий хроматографирования (времени выхода и/или нестабильности градуировочной характеристики).
10.5 Контроль стабильности градуировочной характеристики
Проверку стабильности работы хроматографа проводят при выполнении каждой серии проб по результатам анализа одного из градуировочных растворов. Градуировочную характеристику считают стабильной в случае, если измеренное значение массовой концентрации отличается от аттестованного значения не более чем на 20 %, а время удерживания определяемого вещества в градуировочном растворе отклоняется от установленного при градуировке времени удерживания не более чем на 20 с.
Примечание - В случае, если времена удерживания определяемых веществ в растворе метанола (градуировочные растворы) и диэтилового эфира (экстракт) отличаются более чем на 20 с, рекомендуется готовить градуировочные растворы в диэтиловом эфире.
Если условие стабильности градуировочной характеристики не выполняется для одного градуировочного раствора, необходимо выполнить повторное измерение этого градуировочного раствора с целью исключения результата измерения, содержащего грубую погрешность.
Если градуировочная характеристика нестабильна, выясняют и устраняют причины нестабильности и повторяют контроль с использованием других градуировочных растворов, предусмотренных методикой. При повторном обнаружении отклонения результата от градуировочной характеристики ее устанавливают заново.
Примечание - Допускается проводить контроль стабильности градуировочной характеристики по ограниченному перечню веществ. При выборе веществ принимают во внимание следующие факторы: частота обнаружения в реальных пробах; времена удерживания (желательно: начало, середина и конец хроматограммы).
На колонке 1 (OV-225 и DB-5) пики 2,4-ксиленола и 2,5-ксиленола не разделяются. При установлении градуировочной характеристики 2,4-ксиленола и 2,5-ксиленола указывается сумма массовых концентраций этих веществ.
На колонке 2 (DB-5MS) пики м-крезола и п-крезола не разделяются. При установлении градуировочной характеристики м-крезола и п-крезола указывается сумма массовых концентраций этих веществ.
Примеры хроматограмм определяемых соединений на колонках 1 и 2 представлены в приложениях 3 и 4.
10.6 Установление поправочного коэффициента, учитывающего потери при пробоподготовке
Образцы для установления поправочного коэффициента, учитывающего потери при пробоподготовке, представляют собой водные растворы фенолов, аттестованные по процедуре приготовления. Образцы готовят с использованием специально приготовленных проверочных растворов фенолов в органическом растворителе и рабочей пробы питьевой (природной или сточной воды), не содержащей определяемые вещества.
Для приготовления проверочных растворов используют ГСО или вещества гарантированной чистоты. Важно для приготовления проверочных растворов использовать хорошо растворимые в воде растворители, например, метанол или этанол.
Перед приготовлением образцов проводят анализ «холостой пробы»: 0,5 дм3 пробы воды, которую планируют использовать для приготовления образцов, подвергают процедуре подготовки пробы по методике и выполняют измерения. К пробам, содержащим остаточный хлор или другие окисляющие агенты, добавляют тиосульфат натрия из расчета (80 ± 10) мг на 1 дм3. По полученной хроматограмме рассчитывают фоновое значение массовой концентрации определяемого вещества. Полученное значение не должно превышать 30 % нижнего предела определения вещества. При невыполнении данного условия для приготовления образцов отбирают и проверяют другую пробу воды.
Для определения поправочных коэффициентов во всем диапазоне измерений готовят образцы с содержанием каждого фенола вблизи нижней, верхней границ и середины диапазона измерений (например, 0,0005-0,0050-0,1000 мг/дм3). Для каждой выбранной точки диапазона измерений используют не менее 7 образцов с одинаковой массовой концентрацией.
Приготовленные образцы подвергают процедуре пробоподготовки.
Полученный экстракт анализируют и определяют массовую концентрацию каждого определяемого вещества в образце. Затем вычисляют поправочный коэффициент Kni, учитывающий потери при пробоподготовке, как отношение измеренного значения массовой концентрации каждого фенола в образце к аттестованному значению массовой концентрации этого вещества в образце по формуле
|
|
где Xi - измеренное значение массовой концентрации определяемого вещества в i-ом образце, мг/дм3;
Сi - аттестованное значение массовой концентрации определяемого вещества в i-ом образце, мг/дм3;
Далее рассчитывают усредненный поправочный коэффициент Kincp для каждого определяемого вещества во всем диапазоне измерений как среднее арифметическое значение полученных коэффициентов Kni по формуле
|
|
Поправочный коэффициент используют при обработке результатов измерений.
Поправочный коэффициент обязательно устанавливают при внедрении методики.
Поправочный коэффициент проверяют при смене оператора, осуществляющего пробоподготовку. При получении удовлетворительных результатов контроля используют ранее установленный Kincp. В случае получения отрицательных результатов контроля Kni устанавливают заново.
11 ВЫПОЛНЕНИЕ ИЗМЕРЕНИЙ
При выполнении измерений массовых концентраций фенолов выполняют следующие операции:
11.1 Подготовка реактивов
11.1.1 Проверка чистоты новой партии гексана
В коническую колбу вместимостью 50 см3 помещают 25 см3 гексана и упаривают до объема 2 - 4 см3 на песчаной бане при температуре (60 ± 5) °С в токе воздуха. Остаток экстракта переносят в мерную пробирку вместимостью 10 см3 и упаривают до конечного объема (1,0 ± 0,1) см3. Полученный экстракт анализируют в условиях хроматографирования пробы. Гексан считают пригодным при отсутствии на хроматограмме пиков, мешающих определению фенолов.
Примечание - В случае необходимости дополнительной очистки гексана, его перегоняют с помощью установки (5.1.17), отбрасывая первую и последнюю порции отгона
11.1.2 Проверка чистоты новой партии натрия сернокислого
Пропускают 50 см3 диэтилового эфира через коническую воронку с безводным натрием сернокислым (слой ~2 - 3 см), на дно конусной части воронки следует положить немного ваты), собирают эфир в коническую колбу вместимостью 50 см3 и упаривают до объема 2 - 4 см3 на песчаной бане при температуре (60 ± 5) °С. Остаток экстракта переносят в мерную пробирку вместимостью 10 см3 и упаривают до конечного объема (1,0 ± 0,1) см3. Полученный экстракт анализируют в условиях хроматографирования пробы. Натрий сернокислый считают пригодным при отсутствии на хроматограмме пиков, мешающих определению фенолов.
11.1.3 Проверка чистоты новой партии диэтилового эфира
Упаривают 50 см3 диэтилового эфира до объема 2 - 4 см3 на песчаной бане при температуре (60 ± 5) °С. Остаток экстракта переносят в мерную пробирку вместимостью 10 см3 и упаривают до конечного объема (1,0 ± 0,1) см3. Полученный экстракт анализируют в условиях хроматографирования пробы. Диэтиловый эфир считают пригодным при отсутствии на хроматограмме пиков, мешающих определению фенолов.
11.2 Подготовка аппаратуры
Хроматограф и устройство для автоматического отбора и ввода проб выводят на рабочий режим в соответствии с условиями, указанными в п. 10.1. На компьютере в программе управления активизируют метод анализа.
11.3 Приготовление растворов
11.3.1 Раствор гидроксида натрия массовой концентрации 500 г/дм3.
В мензурку вместимостью 100 см3, содержащую 50 см3 дистиллированной воды, помещают (50 ± 1) г гидроокиси натрия (5.2.11), перемешивая стеклянной палочкой до полного растворения. После остывания доводят объем раствора до 100 см3 дистиллированной водой и переливают во флакон из полимерного материала с завинчивающейся крышкой.
Раствор хранят не более 6 месяцев при температуре окружающей среды.
11.3.2 Раствор серной кислоты объемной доли 50 %.
Приготовление раствора проводят в вытяжном шкафу.
В химический стакан вместимостью не менее 200 см3 помещают 50 см3 дистиллированной воды и медленно при перемешивании добавляют 50 см3 концентрированной серной кислоты (5.2.9).
После остывания приготовленный раствор осторожно переливают во флакон с завинчивающейся крышкой.
Раствор хранят не более 1 года при температуре окружающей среды.
11.4 Подготовка пробы
11.4.1 Подготовка пробы питьевой и природной воды
В мензурку вместимостью 0,5 дм3 помещают 0,5 дм3 пробы воды и проверяют значения pH с помощью индикаторной бумаги, подкисляют раствором серной кислоты до значения pH ≤ 3 ед. pH (если проба воды не была законсервирована или была законсервирована гидроокисью натрия) и добавляют 50 - 60 г хлористого натрия (до насыщения раствора). Содержимое мензурки переносят в делительную воронку вместимостью 1 дм3. Мензурку обмывают небольшим количеством диэтилового эфира (5 - 10) см3 и добавляют к пробе, находящейся в делительной воронке. Затем к пробе добавляют 50 см3 диэтилового эфира. Далее воронку с пробой несколько раз интенсивно встряхивают, открывая периодически кран воронки, чтобы выпустить пары эфира, затем делительную воронку устанавливают в кольцо шюттель-аппарата, закрепляют держателем и включают шюттель-аппарат на 10 мин со скоростью 60 - 80 встряхиваний в минуту. После остановки шюттель-аппарата делительную воронку оставляют в покое до разделения слоев (~15 мин), после чего эфирный слой (экстракт) отделяют от водного слоя, пропуская через коническую воронку с безводным натрием сернокислым (слой 2 - 3 см), на дно конусной части воронки следует положить немного ваты, экстракт собирают в коническую колбу вместимостью 50 или 100 см3. Затем делительную воронку обмывают 5 - 10 см3 диэтилового эфира и промывают этим эфиром воронку с натрием сернокислым, смыв присоединяют к экстракту.
Примечание - При ручном способе подготовки пробы экстракцию диэтиловым эфиром проводят трижды порциями по 50 см3, встряхивая делительную воронку в течение 5 минут.
Экстракт упаривают на песчаной бане при температуре (60 ± 5) °С до объема 2 - 4 см3. После этого экстракт переносят в мерную пробирку вместимостью 10 см3, колбу обмывают 1 - 2 см3 эфира, экстракт и смыв объединяют и упаривают до конечного объема (1,0 ± 0,1) см3 (нельзя упаривать досуха!) на песчаной бане. Затем экстракт переносят во флакон вместимостью 2 см3 и герметично закрывают.
11.4.2 Подготовка пробы сточной воды
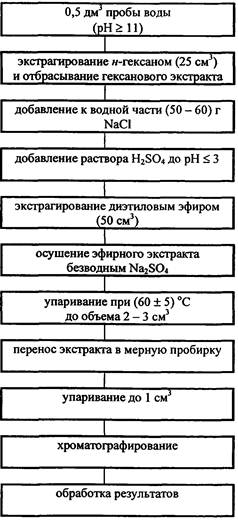
В мензурку вместимостью 0,5 дм3 помещают 0,5 дм3 пробы и проверяют значения pH с помощью индикаторной бумаги (проба должна иметь значение pH ≥ 11 ед. pH). В случае, когда значение pH < 11 ед. pH, добавляют по каплям раствор гидроокиси натрия. Затем пробу воды переносят в делительную воронку вместимостью 1 дм3, добавляют 25 см3 гексана, делительную воронку устанавливают в кольцо шюттель-аппарата и включают его на 10 минут со скоростью 60 - 80 встряхиваний в минуту, содержимому дают отстояться для разделения слоев, отделяют гексановый экстракт и отбрасывают его.
Примечание - При ручном способе подготовки пробы экстракцию гексаном проводят трижды порциями по 25 см3, встряхивая делительную воронку в течение 5 минут.
К водной части добавляют 50 - 60 г хлористого натрия (до насыщения раствора) и подкисляют раствором серной кислоты до значения pH ≤ 3 ед. pH, проверяя значение pH по индикаторной бумаге. Полученный раствор экстрагируют 50 см3 диэтилового эфира в течение 10 минут со скоростью 60 - 80 встряхиваний в минуту, используя шюттель-аппарат. Эфирный экстракт собирают в стакан вместимостью 150 см3 и добавляют небольшими порциями безводный натрий сернокислый при перемешивании до осветления экстракта.
Затем этот экстракт фильтруют через коническую воронку с безводным натрием сернокислым (слой 2 - 3 см), на дно конусной части воронки следует положить немного ваты, и собирают в коническую колбу вместимостью 50 или 100 см3. Воронку с натрием сернокислым промывают 10 - 15 см3 диэтилового эфира и добавляют к экстракту. После этого экстракт упаривают на песчаной бане при температуре (60 ± 5) °С до объема 2 - 4 см3, переносят в мерную пробирку вместимостью 10 см3, колбу обмывают 2 - 5 см3 диэтилового эфира, экстракт и смыв объединяют и упаривают до конечного объема (1,0 ± 0,1) см3 (нельзя упаривать досуха!) на песчаной бане. Затем экстракт переносят во флакон вместимостью 2 см3 и герметично закрывают.
Примечание - При ручном способе подготовки пробы экстракцию диэтиловым эфиром проводят трижды порциями по 50 см3, встряхивая делительную воронку в течение 5 минут.
11.5 Выполнение измерений
Полученные экстракты хроматографируют в тот же день. В случае невозможности немедленного проведения анализа экстракты хранят в герметично закрытых флаконах в морозильной камере при температуре минус (12 - 24) °С не более 12 суток. Экстракты, хранившиеся в холодильнике, перед анализом необходимо выдержать при температуре окружающей среды не менее 20 минут.
В случае, когда массовая концентрация определяемого вещества в экстракте выше массовой концентрации максимальной точки градуировочной характеристики, экстракт следует разбавить растворителем и провести измерение массовой концентрации разбавленного экстракта. При вычислении результатов анализа необходимо учесть степень разбавления.
Фенолы идентифицируют по абсолютным временам удерживания. Для анализа используют хроматографическую колонку 1 (основную). Если на хроматограмме присутствуют определяемые вещества, то проводят хроматографирование на колонке 2 (альтернативной) для повышения надежности идентификации. Обработку результатов измерений массовых концентраций фенолов проводят на основании данных, полученных при анализе на колонке 1 и колонке 2. Если полученные значения массовых концентраций отличаются от среднего не более чем на 25 %, то результат рассчитывают как среднее арифметическое значений, полученных при анализе на колонках 1 и 2. Если полученные значения массовых концентраций отличаются более чем на 25 %, результатом измерения считают меньшее значение массовой концентрации, т.к. завышенные значения, как правило, возникают из-за недостаточного отделения фенолов от примесей на одной из колонок.
Примечание - В случае обнаружения 2,4-ксиленола и 2,5-ксиленола на обеих колонках (на колонке 1 - суммарный пик 2,4-ксиленола и 2,5-ксиленола, а на колонке 2 - отдельные пики 2,4-ксиленола и 2,5-ксиленола) расчеты проводят по результатам, полученным на колонке 2.
В случае обнаружения м-крезола и п-крезола на обеих колонках (на колонке 1 - отдельные пики м-крезола и п-крезола, а на колонке 2-суммарный пик м-крезола и п-крезола) расчеты проводят по результатам, полученным на колонке 1.
12 ОБРАБОТКА РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Обработку результатов измерений массовых концентраций фенолов выполняют с помощью управляющей программы в соответствии с градуировочной характеристикой с учетом концентрирования и потерь при пробоподготовке по формуле
|
|
где:
Xi - массовая концентрация определяемого вещества в пробе, мг/дм3;
Si - площадь пика определяемого вещества в анализируемом экстракте, мВ·с;
Vэ - объем экстракта, см3;
Ai - относительный градуировочный коэффициент, мВ·с·см3/мг (10.4);
Va - объем анализируемой пробы воды, дм3;
Kincp - поправочный коэффициент, учитывающий потери при пробоподготовке (10.6).
13 ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Результаты измерений в протоколе представляют в виде:
|
Xi ± Δi, мг/дм3, Р = 0,95 |
где Δi = 0,01·δi·Xi, δi - значение показателя точности (таблица 2).
Результаты измерений округляют с точностью до:
при массовой концентрации
от 0,0005 до 0,001 мг/дм3 - 0,00001 мг/дм3;
свыше 0,001 до 0,01 мг/дм3 - 0,0001 мг/дм3;
свыше 0,01 до 0,1 мг/дм3 - 0,001 мг/дм3
свыше 0,1 до 5 мг/дм3 - 0,01 мг/дм3
14 ОЦЕНКА ПРИЕМЛЕМОСТИ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
14.1 При получении двух результатов измерений (Х1, Х2) в условиях повторяемости (сходимости) осуществляют проверку приемлемости результатов в соответствии с требованиями ГОСТ Р ИСО 5725-6 (раздел 5).
Результат измерений считают приемлемым при выполнении условия:
|
|
Значения переделов повторяемости (r) приведены в таблице 4.
14.2 При получении результатов измерений в двух лабораториях (Хлаб1, Хлаб2) проводят проверку приемлемости результатов измерений в соответствии с требованиями ГОСТ Р ИСО 5725-6 (раздел 5).
Результат измерений считают приемлемым при выполнении условия:
|
|
Значения пределов воспроизводимости (R) приведены в таблице 4.
Таблица 4 - Пределы повторяемости и воспроизводимости результатов измерений
|
Диапазон измерений, мг/дм3 |
Предел повторяемости (при n = 2 и Р = 0,95), r, % |
Предел воспроизводимости (при n = 2 и Р = 0,95), R, % |
|
Питьевые и природные воды |
||
|
от 0,0005 до 0,001 вкл. |
50 |
69 |
|
св. 0,001 до 0,005 вкл. |
39 |
55 |
|
Сточные воды |
||
|
от 0,001 до 0,01 вкл. |
50 |
69 |
|
св. 0,01 до 0,1 вкл. |
39 |
55 |
|
св. 0,1 до 5 вкл. |
34 |
48 |
15 КОНТРОЛЬ ТОЧНОСТИ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
15.1 В случае регулярного выполнения анализа по методике рекомендуется проводить контроль стабильности результатов измерений путем контроля среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности и погрешности в соответствии с рекомендациями ГОСТ Р ИСО 5725 (часть 6). Образец для контроля готовят с использованием ГСО или вещества гарантированной чистоты и дистиллированной воды. Периодичность контроля регламентируют во внутренних документах лаборатории.
15.2 Оперативный контроль точности результатов измерений рекомендуется проводить с каждой серией проб, если анализ по методике выполняется эпизодически, а также при возникновении необходимости подтверждения результатов измерений отдельных проб (при получении нестандартного результата измерений, результата, превышающего ПДК и т.п.).
В качестве образцов для контроля используют образцы, приготовленные с использованием ГСО или вещества гарантированной чистоты и дистиллированной воды.
Оперативный контроль процедуры измерений проводят путем сравнения результата отдельно взятой контрольной процедуры (Kki) с нормативом контроля (Ki).
Результат контрольной процедуры Kki рассчитывают по формуле
|
Kki = |Xi - Ci|, |
где Xi - результат контрольного измерения массовой концентрации определяемого компонента в образце для контроля;
Сi - аттестованное значение определяемого компонента в образце для контроля.
Норматив контроля Ki рассчитывают по формуле
|
Ki = Δлi, |
где Δлi - характеристика погрешности аттестованного значения определяемого компонента в образце для контроля, установленная в лаборатории при реализации методики.
Примечание - На первом этапе проведения контроля после внедрения методики допускается считать Δлi = 0,84·Δi, где Δi - приписанная характеристика погрешности методики, которую рассчитывают по формуле
|
Δi = 0,01·δi·Ci |
Значения δ приведены в таблице 2.
Качество контрольной процедуры признают удовлетворительным при выполнении условия:
|
Kki ≤ Ki |
При невыполнении условия контроль повторяют. При повторном невыполнении условия выясняют причины, приводящие к неудовлетворительным результатам.
ПРИЛОЖЕНИЕ 1
БЛОК-СХЕМА ПРОВЕДЕНИЯ АНАЛИЗА
ПИТЬЕВОЙ И ПРИРОДНОЙ ВОДЫ

ПРИЛОЖЕНИЕ 2
БЛОК-СХЕМА ПРОВЕДЕНИЯ АНАЛИЗА
СТОЧНОЙ ВОДЫ
ПРИЛОЖЕНИЕ 3
Хроматограмма фенола и фенолопроизводных
на колонке 1 (OV-225)
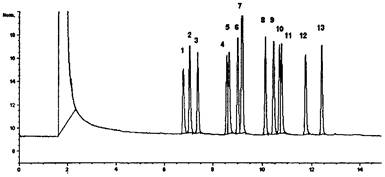
1 - Фенол
2 - 2,6-Ксиленол
3 - о-Крезол
4 - п-Крезол
5 м-Крезол
6 - о-Этилфенол
7 - 2,4-Ксиленол + 2,5-Ксиленол
8 - 2-Изопропилфенол
9 - 2,3-Ксиленол
10 - 3,5-Ксиленол
11 - п-Этилфенол
12 - 3,4-Ксиленол
13 - 2,3,5-Триметилфенол
ПРИЛОЖЕНИЕ 4
Хроматограмма фенола и фенолопроизводных на колонке 2 (DB-5MS)
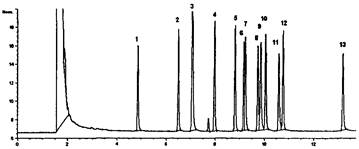
1 - Фенол
2 - о-Крезол
3 - м-Крезол + п-Крезол
4 - 2,6-Ксиленол
5 - о-Этилфенол
6 - 2,4-Ксиленол
7 - 2,5-Ксиленол
8 - п-Этилфенол
9 - 3,5-Ксиленол
10 - 2,3-Ксиленол
11 - 3,4-Ксиленол
12 - 2-Изопропилфенол
13 - 2,3,5-Триметилфенол