МИНИСТЕРСТВО ПРИРОДНЫХ РЕСУРСОВ И ЭКОЛОГИИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральная служба по гидрометеорологии и мониторингу окружающей среды (Росгидромет)
|
РУКОВОДЯЩИЙ ДОКУМЕНТ |
РД |
МАССОВАЯ КОНЦЕНТРАЦИЯ ДИ- И
ПОЛИХЛОРФЕНОЛОВ В ВОДАХ
Методика измерений газохроматографическим методом
Ростов-на-Дону
2012
Предисловие
1 РАЗРАБОТАН федеральным государственным бюджетным учреждением «Гидрохимический институт» (ФГБУ «ГХИ»)
2 РАЗРАБОТЧИКИ Л.В. Боева, канд. хим. наук, Ю.А. Андреев
3 СОГЛАСОВАН с ФГБУ НПО «Тайфун» 01.02.2012
и УМЗА Росгидромета 01.03.2012
4 УТВЕРЖДЕН Заместителем Руководителя Росгидромета 02.03.2012
5 АТТЕСТОВАН ФГБУ «ГХИ», свидетельство об аттестации методики измерений № 507-01.00175-2011 от 11.01.2011
6 ЗАРЕГИСТРИРОВАН ЦМТР ФГБУ «НПО «Тайфун» за номером РД 52.24.507-2012 от 03.03.2012
7 ВЗАМЕН РД 52.24.507-98 «Методические указания. Методика выполнения измерений массовой концентрации ди- и полихлорфенолов в водах газохроматографическим методом».
СОДЕРЖАНИЕ
Введение
Ди- и полихлорфенолы представляют собой производные фенола, содержащие от 2 до 5 атомов хлора в бензольном кольце; бензольное кольцо может содержать также другие заместители.
Ди- и полихлорфенолы, в отличие от их нехлорированных аналогов, имеют исключительно антропогенное происхождение. В природные воды они попадают как непосредственно со сточными водами ряда производств, так и в результате трансформации органических веществ других классов при обеззараживании сточных вод хлорированием. Значительные количества ди- и полихлорфенолов могут содержаться в сточных водах целлюлозно-бумажного производства, использующего хлор для отбеливания целлюлозы; производства пестицидов; ряда химических и электрохимических производств. Полихлорфенолы широко применяются в деревообрабатывающей промышленности для борьбы с насекомыми-вредителями и для консервации древесины, откуда они также могут попадать в водные объекты с ливневым стоком или сточными водами.
Ди- и полихлорфенолы обладают существенно большей устойчивостью в окружающей среде по сравнению с нехлорированными аналогами и большей токсичностью, причем в целом и то и другое возрастает с увеличением числа атомов хлора в молекуле. По этой причине хлорфенолы во многих странах включены в перечни приоритетных загрязняющих веществ.
Биохимическая устойчивость ди- и полихлорфенолов в комплексе с другими физико-химическими свойствами (растворимость в липидах, сорбция на взвешенных частицах, аккумуляция донными отложениями, водными растениями и животными и т.д.) обусловливает их накопление в донных отложениях рек и озер, за счёт чего возникает опасность вторичного загрязнения водных объектов как ди- и полихлорфенолами, так и продуктами их трансформации.
Предельно-допустимые концентрации (ПДК) ди- и полихлорфенолов в природных водах приведены в таблице 1.
Таблица 1 - ПДК ди- и полихлорфенолов
|
ПДК, мг/дм3, для водных объектов |
||
|
рыбохозяйственного назначения |
хозяйственно-питьевого и культурно бытового водопользования |
|
|
2,4 -дихлорфенол |
0,0001 |
0,002 |
|
2,4,6 -трихлорфенол |
0,0001 |
0,004 |
|
2,3,4,6 -тетрахлорфенол |
- |
0,001 |
|
Пентахлорфенолят натрия |
0,0005 |
0,009 |
|
Пентахлорфенол |
- |
0,009 |
РУКОВОДЯЩИЙ ДОКУМЕНТ
МАССОВАЯ КОНЦЕНТРАЦИИИ ДИ- И ПОЛИХЛОРФЕНОЛОВ В ВОДАХ
Методика измерений газохроматографическим методом
Дата введения - 2012-04-02
1 Область применения
1.1 Настоящий руководящий документ устанавливает методику измерений (далее - методика) массовой концентрации 2,3-, 2,4-, 2,5-, 2,6-дихлорфенолов в диапазоне от 0,20 до 8,0 мкг/дм3, 3,4-, 3,5-дихлорфенолов в диапазоне от 0,30 до 12,0 мкг/дм3, три-, тетра- и пентахлорфенолов (далее - полихлорфенолы) в диапазоне от 0,05 до 2,00 мкг/дм3 в пробах природных и очищенных сточных вод газохроматографическим методом.
1.2 Допускается выполнение измерений в пробах с массовой концентрацией ди- и полихлорфенолов, превышающей приведенные в 1.1 верхние границы диапазонов при соответствующем уменьшении объема водной пробы или степени концентрирования гексанового экстракта, подвергаемого газохроматографическому анализу.
1.3 Настоящий руководящий документ предназначен для использования в лабораториях, осуществляющих анализ природных и очищенных сточных вод.
1.4 При наличии соответствующих стандартных образцов или препаратов гарантированной чистоты с помощью данной методики могут быть определены ди- и полихлорпроизводные метилфенолов, этилфенолов и диметилфенолов, а также ди- и полибромпроизводные фенола.
2 Нормативные ссылки
В настоящем руководящем документе использованы ссылки на следующие нормативные документы:
ГОСТ 12.1.005-88 ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 ССБТ. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 17.1.5.04-81 Охрана природы. Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Общие технические условия
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб
МИ 2881-2004 Рекомендация. ГСИ. Методики количественного химического анализа. Процедуры проверки приемлемости результатов анализа
Примечание - Ссылки на остальные нормативные документы приведены в разделах 4 и А.3, А.4 (приложение А).
3 Требования к показателям точности измерений
3.1 При соблюдении всех регламентируемых методикой условий выполнения измерений характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице 2.
Таблица 2 - Диапазон измерений, значения характеристик погрешности и ее составляющих при принятой вероятности Р = 0,95
|
Диапазон измерений массовых концентраций X, мкг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) σr, мкг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) σR, мкг/дм3 |
Показатель правильности (границы систематической погрешности) ± Δc, мкг/дм3 |
Показатель точности (границы погрешности) ± Δ, мкг/дм3 |
|
|
2,3-, 2,4-, 2,5-, 2,6 дихлорфенолы |
От 0,20 до 1,2 включ. |
0,02 + 0,06 ∙ X |
0,03 + 0,08 ∙ X |
0,02 + 0,07 ∙ X |
0,06 + 0,17 X |
|
Св. 1,2 до 8,0 включ. |
0,09 ∙ X |
0,11 ∙ X |
0,08 ∙ X |
0,23 ∙ X |
|
|
3,4-, 3,5- дихлорфенолы |
От 0,30 до 1,8 включ. |
0,03 + 0,09 ∙ X |
0,04 + 0,12 ∙ X |
0,03 + 0,08 ∙ X |
0,09 + 0,25 ∙ X |
|
Св. 1,8 до 12 включ. |
0,09 ∙ X |
0,11 ∙ X |
0,08 ∙ X |
0,23 ∙ X |
|
|
Трихлорфенолы |
От 0,05 до 2,0 включ. |
0,08 ∙ X |
0,10 ∙ X |
0,08 ∙ X |
0,22 ∙ X |
|
Тетра- и пентахлорфенолы |
От 0,05 до 2,0 включ. |
0,01+0,06 ∙ X |
0,02 + 0,08 ∙ X |
0,08 ∙ X |
0,03 + 0,18 ∙ X |
При выполнении измерений в пробах с массовой концентрацией 2,3-, 2,4-, 2,5-, 2,6-дихлорфенолов свыше 8,0 мкг/дм3, 3,4-, 3,5-дихлорфенолов свыше 12,0 мкг/дм3 и полихлорфенолов свыше 2,00 мкг/дм3 при соответствующем изменении объема водной пробы или гексанового экстракта, погрешность измерения не превышает значений, рассчитанных по зависимостям, приведенным в таблице 2.
Предел обнаружения дихлорфенолов газохроматографическим методом в виде ацетильных производных составляет 0,1 мкг/дм3, полихлорфенолов - 0,03 мкг/дм3.
2.2 Значения показателя точности методики используют при:
- оформлении результатов измерений, выдаваемых лабораторией;
- оценке деятельности лабораторий на качество проведения измерений;
- оценке возможности использования результатов измерений при реализации методики выполнения измерений в конкретной лаборатории.
4 Требования к средствам измерений, вспомогательным устройствам, реактивам, материалам
4.1 Средства измерений и вспомогательные устройства
4.1.1 Хроматограф газовый Кристалл 2000М, Хроматэк-Кристалл 5000.2, Цвет-800, или другой с детектором по захвату электронов (ЭЗД, ДПР, ИРД).
4.1.2 Весы высокого (II) класса точности по ГОСТ Р 53228-2008, максимальная нагрузка не более 200 г, дискретность отсчета не более 0,0002 г.
4.1.3 Весы среднего (III) класса точности по ГОСТ 53228-2008, максимальная нагрузка не более 500 г, дискретность отсчета 0,001 г.
4.1.4 рН-метр лабораторный любого типа, снабженный измерительным и вспомогательным электродами.
4.1.5 Государственный стандартный образец (ГСО) состава 2,4-дихлорфенола ГСО 7198-95; 2,4,6-трихлорфенола ГСО 7103-94; пентахлорфенола ГСО 7102-94, гексахлорбензола ГСО 7495-98.
4.1.6 Термометр лабораторный по ТУ 25-2021.007-88 с взаимозаменяемым конусом КШ 14/23, длиной нижней части термометра 60 мм, диапазоном измерения температур от 0 °С до 150 °С и ценой деления шкалы не более 1 °С.
4.1.7 Микрошприцы МШ-10М по ТУ 2-833-106-90 вместимостью 10 мм3 - 2 шт.
4.1.8 Секундомер по ТУ 25.1894.003-90 - 1 шт.
4.1.9 Колбы мерные 2-го класса точности исполнения 2 по ГОСТ 1770-74 вместимостью: 25 см3 - 4 шт., 50 см3 - 10 шт., 100 см3 - 1 шт., 500 см3 - 1 шт.
4.1.10 Пипетки градуированные 2-го класса точности исполнения 1, 2 по ГОСТ 29227-91, вместимостью: 0,5 см3 - 4 шт., 1 см3 - 10 шт., 2 см3 - 15 шт., 5 см3 - 12 шт.
4.1.11 Цилиндры мерные исполнения 1, 3 по ГОСТ 1770-74 вместимостью: 10 см3 - 1 шт., 25 см3 - 4 шт., 50 см3 - 1 шт., 250 см3 - 1 шт., 500 см3 - 2 шт.
4.1.12 Микропробирки конические градуированные со стеклянными пробками вместимостью 2 - 3 см3 или виалы с коническим дном (или микрореакционные сосуды) с завинчивающейся пробкой, имеющей тефлоновую прокладку, вместимостью 1 - 2 см3 с наименьшей ценой деления 0,1 - 0,3 см3 (далее V-виалы) производства фирм Supelco или Wheaton (рисунок 1) - 20 шт.
4.1.13 Колонки кварцевые капиллярные длиной 25 - 30 м, диаметром 0,32 мм с толщиной плёнки неподвижной фазы 0,25 мкм с неподвижной фазой неполярной или слабополярной типа SE-30, SE-54 и полярной неподвижной фазой типа ХЕ-60, OV-225, или другие с аналогичными характеристиками (далее - капиллярные колонки), или колонки хроматографические стеклянные с внутренним диаметром 3 мм длиной 2 м, заполненные носителем типа Хроматон NAW-DMCS (NAW-HMCS, N-Super), фракция 0,16 - 0,20 мм, с 5 % неподвижной фазы типа SE-30, SE-54 и с 5 % неподвижной фазы ХЕ-60, OV-225 или другими с аналогичными характеристиками (далее - набивные колонки).
4.1.14 Колбы типа Кн исполнения 1 с взаимозаменяемым конусом 14/23 и пришлифованной пробкой по ГОСТ 25336-82 вместимостью 25 см3 - 10 шт., 50 см3 - 10 шт.
Рисунок 1 - Микропробирка коническая градуированная (а), V-виала Wheaton (б) и микрореакционный сосуд Supelco (в)
4.1.15 Воронки делительные типа ВД исполнения 1, 3 по ГОСТ 25336-82 вместимостью: 50 см3 - 7 шт., 100 см3 - 2 шт., 500 см3 - 4 шт., 1000 см3 - 1 шт.
4.1.16 Воронки лабораторные типа В по ГОСТ 25336-82 диаметром: 36 мм - 10 шт., 75 мм - 1 шт.
4.1.17 Стаканы, тип В, исполнения 1, ТХС по ГОСТ 25336-82, вместимостью: 25 или 50 см3 - 10 шт., 250 см3 - 1 шт., 1000 см3 - 2 шт.
4.1.18 Установка из стекла группы ТС для перегонки растворителей (круглодонная колба типа К-1 с взаимозаменяемым конусом 29/32, вместимостью 1000 см3, дефлегматор длиной не менее 350 мм с взаимозаменяемыми конусами 19/26 и 29/32, насадка типа Н1 с взаимозаменяемыми конусами 19/26-14/23-14/23, холодильник типа ХПТ-1 длиной не менее 400 мм, алонж типа АИ с взаимозаменяемым конусом муфты 14/23) по ГОСТ 25336-82.
4.1.19 Установка из стекла для получения бидистиллированной воды (плоскодонная колба типа П, исполнения 1, ТХС, с взаимозаменяемым конусом 29/32, вместимостью 1000 см3, насадка типа Н1 с взаимозаменяемыми конусами 19/26-14/23-14/23, холодильник типа ХПТ-1 длиной не менее 400 мм, алонж типа АИ с взаимозаменяемым конусом муфты 14/23) по ГОСТ 25336-82.
4.1.20 Выпарительная чашка № 4 или № 5 по ГОСТ 9147-80 - 1 шт.
4.1.21 Стаканчики для взвешивания (бюксы) по ГОСТ 25336-82: СВ-19/9 - 10 шт., СВ-24/10 - 1 шт., СВ-34/12 - 1 шт.
4.1.22 Пипетки Пастера по ТУ 9464-001-52876351-2000 - 2 шт.
4.1.23 Палочки стеклянные: диаметром - 4 мм, длиной 12 - 15 см - 20 шт.; диаметром 4 или 5 мм, длиной 25 см - 1 шт.
4.1.24 Эксикатор исполнения 2, диаметром корпуса 190 мм по ГОСТ 25336-82.
4.1.25 Склянка для промывания газов типа СПТ по ГОСТ 25336-82.
4.1.26 Флаконы с навинчивающимися пробками и полиэтиленовыми вкладышами, номинальной вместимостью 25 и 50 см3 для хранения аттестованных растворов и экстрактов.
4.1.27 Склянки (в том числе темного стекла) для хранения проб и растворов вместимостью 0,1; 0,25; 0,5 и 1 дм3 с притертыми или завинчивающимися пробками.
4.1.28 Посуда полиэтиленовая для хранения растворов вместимостью 0,5 дм3.
4.1.29 Генератор водорода любого типа, вырабатывающий водород марки «А» по ГОСТ 3022-80.
4.1.30 Микрокомпрессор аквариумный любого типа - 1 шт.
4.1.31 Баня водяная.
4.1.32 Баня песчаная.
4.1.33 Плитка электрическая с регулируемой мощностью нагрева по ГОСТ 14919-83.
4.1.34 Муфельная печь любого типа с регулируемой температурой.
4.1.35 Шкаф сушильный общелабораторного назначения.
4.1.36 Холодильник бытовой.
Примечание - Допускается использование других типов средств измерений, посуды и вспомогательного оборудования, в том числе импортных, с характеристиками не хуже, чем у приведенных в 4.1.
4.2 Реактивы и материалы
4.2.1 Индивидуальные образцы ди- и полихлорфенолов гарантированной степени чистоты, импортные (например, производства фирм Supelco, Sigma-Aldrich, Riedel-de Haёn): 2,4 -дихлорфенол, 2,5 -дихпорфенол; 2,3 -дихлорфенол; 2,6 -дихлорфенол; 3,4 -дихлорфенол; 3,5 -дихлорфенол; 2,4,6 -трихлорфенол; 2,4,5 -трихлорфенол; 2,3,5 -трихлорфенол; 2,3,6 -трихлорфенол; 2,3,4 -трихлорфенол; 3,4,5 -трихлорфенол; 2,3,5,6 -тетрахлорфенол; 2,3,4,5 -тетрахлорфенол; 2,3,4,6 -тетрахлорфенол; пентахлорфенол с содержанием основного вещества не менее 98 %.
4.2.2 2,4,6-трибромфенол по ТУ 6-09-08-1244-77, ч. или импортный.
4.2.3 н-Гексан (далее - гексан) по ТУ 2631-003-05807999-98, х.ч.
4.2.4 Ацетон особой чистоты ос.ч. 9 - 5 ОП-2 по ТУ 2633-039-44493179-00.
4.2.5 Толуол особой чистоты 22 - 5 по ТУ 2632-065-44493179-01 с изм. 1, или толуол по ГОСТ 5789-78, ч.д.а., очищенный перегонкой.
4.2.6 Изопропиловый спирт (2-пропанол) особой чистоты 11 - 5 ОП-1 по ТУ 2632-064-44493179-01 с изм. 1, 2, или по ТУ 6-09-402-85, х.ч.
4.2.7 Ангидрид уксусный по ГОСТ 5815-77, ч.д.а.
4.2.8 Кислота серная по ГОСТ 4204-77, х.ч.
4.2.9 Натрий углекислый безводный (карбонат натрия) по ГОСТ 83-79, ч.д.а.
4.2.10 Натрия гидроокись (гидроксид натрия) по ГОСТ 4328-77, х.ч.
4.2.11 Натрий фосфорнокислый двузамещенный 12-водный (натрия гидрофосфат) по ГОСТ 4172-76, х.ч.
4.2.12 Натрий сернокислый безводный (сульфат натрия) по ГОСТ 4166-76, ч.д.а.
4.2.13 Медь (II) сернокислая 5-водная (сульфат меди) по ГОСТ 4165-78, ч.д.а.
4.2.14 Натрий сернистокислый (сульфит натрия) по ГОСТ 195-77, ч.д.а.
4.2.15 Калий марганцовокислый (перманганат калия) по ГОСТ 20490-75, ч.д.а.
4.2.16 Уголь активный БАУ-А по ГОСТ 6217-74.
4.2.17 Вода дистиллированная по ГОСТ 6709-72.
4.2.18 Бумага индикаторная универсальная по ТУ 6-09-1181-76.
4.2.19 Азот нулевой марка «А» по ТУ 6-21-39-96 или азот газообразный ос.ч. (1 сорт) по ГОСТ 9293-74.
4.2.20 Трубка электроизоляционная из фторопласта Ф-4Д по ГОСТ 22056-76 с внутренним диаметром от 5 до 6 мм.
4.2.21 Трубка из силиконовой резины с внутренним диаметром 5 или 6 мм.
4.2.22 Вата медицинская по ГОСТ 5556-81.
Примечание - Допускается использование реактивов, изготовленных по другой нормативной и технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
5 Метод измерения
Выполнение измерений массовой концентрации ди- и полихлорфенолов газохроматографическим методом основано на извлечении их из воды толуолом, реэкстракции из толуола раствором карбоната натрия или буферным раствором с рН 10,7, ацилировании уксусным ангидридом, экстракции ацетильных производных гексаном, либо подкислении реэкстракта и экстрации гексаном неацилированных ди- и полихлорфенолов и количественном их определении с детектором по захвату электронов на капиллярной или набивной колонке.
Идентификацию индивидуальных ди- и полихлорфенолов проводят по временам удерживания. В случае неоднозначной идентификации используют две колонки разной полярности.
Расчет количественного содержания ди- и полихлорфенолов осуществляют по высотам или площадям их пиков на хроматограмме с использованием внутреннего стандарта.
6 Требования безопасности, охраны окружающей среды
6.1 При выполнении измерений массовой концентрации ди- и полихлорфенолов в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в национальных стандартах и соответствующих нормативных документах.
6.2 По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся к 1, 2, 3 и 4-му классам опасности по ГОСТ 12.1.007.
6.3 Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005.
6.4 Оператор, выполняющий измерения на хроматографе должен знать правила безопасности при работе с электрооборудованием, сжатыми и горючими газами.
6.5 Работу с сухими препаратами ди- и полихлорфенолов следует проводить в вытяжном шкафу с использованием средств индивидуальной защиты - респиратора, резиновых перчаток. При попадании ди- и полихлорфенолов на кожу, их следует немедленно снять сухим ватным тампоном, затем протереть ватным тампоном, смоченным изопропиловым спиртом, после чего тщательно промыть водой с мылом.
6.6 Градуировочные растворы и экстракты, содержащие ди- и полихлорфенолы, а также сливы органических растворителей собирают в герметично закрывающуюся посуду и утилизируют согласно установленным правилам.
6.8 Сливы толуола, не содержащие ди- и полихлорфенолы, допускается собирать в отдельные склянки с этикетками «Слив толуола для регенерации» и регенерировать для повторного использования.
7 Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются лица с высшим профессиональным образованием или со средним профессиональным образованием и стажем работы в лаборатории не менее 3 лет, владеющие техникой газохроматографического анализа и освоившие методику.
8 Требования к условиям измерений
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
- температура воздуха (20 ± 5) °С;
- атмосферное давление от 84,0 до 106,7 кПа (от 630 до 800 мм рт.ст.);
- влажность воздуха не более 80 % при 25 °С;
- напряжение в сети (220 ± 10) В;
- частота переменного тока (50 ± 1) Гц.
9 Порядок выполнения измерений
9.1 Отбор и хранение проб
Отбор проб производят в соответствии с ГОСТ 17.1.5.05 и ГОСТ Р 51592. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04 и ГОСТ Р 51592. Пробы отбирают в склянки вместимостью 0,25 дм3 с притертыми стеклянными или завинчивающимися пробками с плотными полиэтиленовыми вкладышами. Экстракция проб должна быть выполнена в течение суток с момента отбора пробы.
При необходимости более длительного хранения пробы консервируют, добавляя по 2 см3 раствора серной кислоты, 2 моль/дм3, 10 %-ного раствора сульфата меди и 10 %-ного раствора сульфита натрия. Законсервированные таким образом пробы можно хранить в темном прохладном месте до трех недель.
Хранение проб в течение месяца возможно в виде толуольных экстрактов во флаконах с завинчивающимися пробками с плотным полиэтиленовым вкладышем или колбах с притертыми пробками вместимостью 25 см3. Хранить экстракты следует в темноте.
9.2 Приготовление растворов и реактивов
9.2.1 Раствор серной кислоты, 2 моль/дм3
К 480 см3 дистиллированной воды в термостойком стакане вместимостью 1000 см3 осторожно при непрерывном перемешивании прибавляют 27 см3 концентрированной серной кислоты. После охлаждения раствор переносят в стеклянную склянку с притертой или полиэтиленовой пробкой.
9.2.2 Раствор карбоната натрия, 0,15 моль/дм3
Растворяют 7,95 г карбоната натрия в 500 см3 бидистиллированной воды. Раствор хранят в стеклянной посуде с притертой или полиэтиленовой пробкой не более 10 дней.
9.2.3 Раствор гидрофосфата натрия, 0,15 моль/дм3
Переносят 26,85 г Na2HPO4 ∙ 12 H2O (или эквивалентную массу соли с другим содержанием кристаллизационной воды) в мерную колбу вместимостью 500 см3, растворяют в небольшом количестве бидистиллированной воды и после полного растворения соли доводят до метки.
9.2.4 Раствор гидроксида натрия, 0,15 моль/дм3
Растворяют 3,0 г гидроксида натрия в 500 см3 бидистиллированной воды.
9.2.5 Фосфатный буферный раствор, рН 10,7
Фосфатный буферный раствор готовят смешиванием 1 объёма раствора гидроксида натрия с двумя объёмами раствора гидрофосфата натрия с концентрациями 0,15 моль/дм3 каждого. При необходимости величину рН корректируют добавлением соответствующих растворов гидроксида или гидрофосфата натрия до значения в пределах от 10,65 до 10,8. После приготовления фосфатный буферный раствор очищают интенсивным встряхиванием с гексаном из расчета 20 см3 гексана на 500 см3 буферного раствора. После расслоения водный слой сливают в склянку с притертой пробкой и используют в течение 10 дней. По прошествии этого срока оставшийся раствор можно использовать после контроля рН и повторной очистки гексаном.
9.2.6 Уксусный ангидрид
Около 20 см3 уксусного ангидрида помещают в чистую сухую делительную воронку вместимостью 50 - 100 см3, добавляют 10 см3 гексана и встряхивают в течение 2 мин. После расслоения фаз уксусный ангидрид (нижний слой) сливают в чистую сухую колбу с хорошо притертой пробкой. Хранят очищенный уксусный ангидрид при комнатной температуре в темном месте не более 10 дней. При использовании уксусный ангидрид следует тщательно оберегать от попадания посторонних веществ, особенно воды, раствора карбоната натрия и буферного раствора.
9.2.7 Раствор сульфата меди, 10 %-ный
Растворяют 15 г сульфата меди (CuSO4 ∙ 5H2O) в 85 см3 дистиллированной воды.
9.2.8 Раствор сульфита натрия, 10 %-ный
Растворяют 10 г сульфита натрия в 90 см3 дистиллированной воды. Хранят в темной, плотно закрытой склянке не более месяца.
9.2.9 Очистка растворителей
Для очистки растворителей (гексана, толуола и изопропилового спирта) используют одно- или двукратную перегонку в установке с дефлегматором. Степень чистоты растворителей контролируют холостым опытом.
При регенерации толуола перед перегонкой его промывают раствором карбоната натрия из расчета 100 см3 карбоната на 500 см3 толуола, а затем трижды по 50 см3 бидистиллированной воды.
9.2.10 Сульфат натрия, безводный
Сульфат натрия прокаливают в муфельной печи при температуре от 450 °С до 500 °С в течение 5 - 6 ч. Хранят в склянке с хорошо притертой пробкой в течение месяца.
9.2.11 Вода бидистиллированная
Для получения бидистиллированной воды в перегонную колбу наливают дистиллированную воду, добавляют от 0,1 до 0,2 г перманганата калия на 1 дм3 воды и несколько капель концентрированной серной кислоты. Колбу нагревают, кипятят 15 мин, затем воду перегоняют. Первую порцию отгона отбрасывают (не менее 50 см3), оставляя после перегонки в колбе около 10 % от первоначального объема дистиллированной воды. Хранят бидистиллированную воду в склянке с притертой стеклянной или завинчивающейся полипропиленовой пробкой.
9.3 Приготовление градуировочных растворов
9.3.1 Градуировочные растворы ди- и полихлорфенолов готовят из ГСО или соответствующих реактивов гарантированной степени чистоты.
Приготовление аттестованных растворов индивидуальных ди- и полихлорфенолов из ГСО, содержащих сухие вещества, или реактивов гарантированной степени чистоты проводят согласно приложению А.
В качестве растворителя для приготовления растворов применяют чистый изопропиловый спирт.
9.3.2 Для приготовления основного раствора смеси ди- и полихлорфенолов с массовой концентрацией 2,3-, 2,4-, 2,5-, 2,6-дихлорфенолов 200 мкг/см3; 3,4-, 3,5-дихлорфенолов - 300 мкг/см3; три-, тетра- и пентахлорфенолов - 50 мкг/см3 рассчитывают объемы аттестованных растворов индивидуальных веществ, необходимые для приготовления 25 см3 смеси, по формуле
![]() (1)
(1)
где V - объем аттестованного раствора индивидуального ди- и полихлорфенола, см3;
C1 - массовая концентрация ди- и полихлорфенола в основном растворе смеси, мкг/см3;
С2 - массовая концентрация индивидуального ди- и полихлорфенола в аттестованном растворе, мг/см3.
Рассчитанный объем раствора каждого ди- и полихлорфенола отмеривают градуированными пипетками соответствующей вместимости и помещают в одну мерную колбу вместимостью 25 см3, затем доводят до метки изопропиловым спиртом и перемешивают. Хранят в холодильнике во флаконе с хорошо пришлифованной пробкой или завинчивающейся пробкой с герметизирующим вкладышем с тефлоновым покрытием не более 3 мес.
Поскольку некоторые изомеры ди- и полихлорфенолов могут иметь одинаковые времена удерживания на используемой колонке, следует готовить две или три смеси, так, чтобы в каждой смеси присутствовали вещества с разными временами удерживания.
9.3.3. Для приготовления рабочего раствора смеси ди- и полихлорфенолов с массовой концентрацией 2,3-, 2,4-, 2,5-, 2,6-дихлорфенолов 8,00 мкг/см3; 3,4-, 3,5-дихлорфенолов 12,0 мкг/см3; три-, тетра- и пентахлорфенолов 2,00 мкг/см3 отбирают 1,00 см3 основного раствора смеси ди- и полихлорфенолов пипеткой вместимостью 1 см3, помещают в мерную колбу вместимостью 25 см3, доводят до метки изопропиловым спиртом и перемешивают. Хранят в холодильнике во флаконе с хорошо пришлифованной пробкой или завинчивающейся пробкой с герметизирующим вкладышем с тефлоновым покрытием не более недели.
9.3.4 Для приготовления градуировочного раствора смеси ди- и полихлорфенолов № 1 с массовой концентрацией 2,3-, 2,4-, 2,5-, 2,6-дихлорфенолов 0,80 мкг/см3; 3,4-, 3,5-дихлорфенолов 1,20 мкг/см3; три-, тетра- и пентахлорфенолов 0,20 мкг/см3 градуированной пипеткой вместимостью 5 см3 отбирают 2,5 см3 рабочего раствора смеси ди- и полихлорфенолов, помещают его в мерную колбу вместимостью 25 см3, доводят до метки изопропиловым спиртом и перемешивают. Хранят в холодильнике не более 2 сут.
9.3.5 Для приготовления градуировочного раствора смеси ди- и полихлорфенолов № 2 с массовой концентрацией 2,3-, 2,4-, 2,5-, 2,6-дихлорфенолов 0,40 мкг/см3; 3,4-, 3,5-дихлорфенолов 0,60 мкг/см3; три-, тетра- и пентахлорфенолов 0,10 мкг/см3 градуированной пипеткой вместимостью 5 см3 отбирают 2,5 см3 рабочего раствора смеси ди- и полихлорфенолов, помещают его в мерную колбу вместимостью 50 см3, доводят до метки изопропиловым спиртом и перемешивают. Хранят в холодильнике не более 2 сут.
9.4 Приготовление растворов внутреннего стандарта (2,4,6-трибромфенола и гексахлорбензола)
9.4.1 Для приготовления основного раствора внутреннего стандарта взвешивают в бюксе 0,100 г 2,4,6-трибромфенола или гексахлорбензола. Растворяют навеску в изопропиловом спирте, количественно переносят ее в мерную колбу вместимостью 100 см3, доводят изопропиловым спиртом до метки и перемешивают. Переносят раствор во флакон с плотным тефлоновым или полиэтиленовым вкладышем и хранят в холодильнике не более 6 мес.
Массовая концентрация 2,4,6-трибромфенола и гексахлорбензола в полученных растворах составляет 1,00 мг/см3.
9.4.2 Для приготовления промежуточных растворов внутреннего стандарта с массовой концентрацией 2,4,6-трибромфенола или гексахлорбензола 10 мкг/см3 отбирают 0,5 см3 основного раствора с помощью градуированной пипетки вместимостью 1 см3, помещают его в мерную колбу вместимостью 50 см3, доводят до метки изопропиловым спиртом и перемешивают. Хранят не более месяца в холодильнике во флаконе с плотно закрывающейся пробкой.
9.4.3 Для приготовления рабочего раствора внутреннего стандарта с массовой концентрацией 2,4,6-трибромфенола 0,10 мкг/см3 градуированной пипеткой вместимостью 0,5 см3 отбирают 0,50 см3 промежуточного раствора внутреннего стандарта с массовой концентрацией 10 мкг/см3, помещают его в мерную колбу вместимостью 50 см3, доводят до метки изопропиловым спиртом и перемешивают. Хранят в холодильнике не более 5 сут.
9.4.4 Для приготовления рабочего раствора внутреннего стандарта с массовой концентрацией гексахлорбензола 0,040 мкг/см3 градуированной пипеткой вместимостью 0,5 см3 отбирают 0,20 см3 промежуточного раствора внутреннего стандарта с массовой концентрацией 10 мкг/см3, помещают его в мерную колбу вместимостью 50 см3, доводят до метки изопропиловым спиртом и перемешивают. Хранят в холодильнике не более 5 сут.
9.5 Приготовление фильтра для очистки воздуха
Для очистки воздуха при упаривании экстрактов его пропускают через фильтр с активным углем. В качестве фильтра применяют склянку для очистки газов СПТ. Входной и выходной отростки склянки заполняют медицинской ватой (входной толщиной около 2 см, выходной - около 4 см), наполняют склянку активным углем доверху и закрывают пробкой. Уровень активного угля не должен доходить до выходного отростка примерно на 2 см. После этого входной отросток склянки соединяют с аквариумным микрокомпрессором, а выходящий из выходного отростка очищенный воздух используют для отдувки растворителя. На выходной отросток надевают фторопластовую трубку необходимой длины, в другой конец которой вставляют стеклянный капилляр (пипетку Пастера), как показано на рисунке 2.
1 - микрокомпрессор; 2 - фильтр с активным углем; 3 - фторопластовая соединительная трубка; 4 - пипетка Пастера; 5 - микропробирка (или V-виала); 6 - песчаная или водяная баня; 7 - нагреватель (электроплитка).
Рисунок 2 - Схема установки для упаривания экстрактов
9.6 Подготовка хроматографа
Подготовку хроматографа к работе осуществляют в соответствии с руководством по его эксплуатации.
Режим работы для определения ди- и полихлорфенолов при работе с капиллярной колонкой с фазой типа SE-54 или SE-30 устанавливают следующий:
-температура испарителя ...............................................250 °С;
- температура детектора.................................................300 °С;
- температура термостата колонок 50 °С в течение 1 мин, затем повышение температуры со скоростью 15 °С/мин до 270 °С и выдержка 2 мин при 270 °С;
- расход газа-носителя (водорода) через колонку 1,6 - 2,0 см3 /мин, деление потока 1:8 - 1:10.
При работе с набивной колонкой:
-температура испарителя ...............................от 240 °С до 250 °С;
- температура детектора...................................................280 °С;
- температура термостата колонок 150 °С - 5 мин., затем повышение температуры со скоростью 15 °С/мин до 240 °С и выдержка при этой температуре в течение 5 мин;
- расход газа-носителя (азота) через колонку от 30 до 40 см3/мин;
- расход азота на поддув детектора - в соответствии с руководством по эксплуатации хроматографа;
- рабочий предел измерений на усилителе - в зависимости от определяемых концентраций;
- скорость диаграммной ленты (при использовании самописца) 600 мм/ч.
При идентификации ди- и полихлорфенолов на колонке с полярной фазой типа ХЕ-60, OV-225 или аналогичной:
- максимальная температура................................................. 230 °С;
- выдержка.............................................................................. от 5 до 7 мин;
- температура испарителя...................................................... 240 °С;
- детектора............................................................................... 280 °С.
Примечание - Приведенные параметры в каждом конкретном случае могут корректироваться для достижения наилучшего разделения пиков на хроматограмме и наиболее высокой чувствительности измерения.
9.7 Установление градуировочных зависимостей и определение времени удерживания индивидуальных ди- и полихлорфенолов по отношению к внутреннему стандарту
9.7.1 Для установления градуировочных зависимостей с использованием ацилирования готовят градуировочные образцы - экстракты ацетатов ди- и полихлорфенолов с различным их содержанием и одинаковым содержанием внутреннего стандарта. Для этого в делительные воронки вместимостью 50 см3 помещают 20 см3 раствора карбоната натрия, 0,15 моль/дм3, добавляют 1,0 см3 рабочего раствора внутреннего стандарта с массовой концентрацией 2,4,6-трибромфенола 0,10 мкг/см3, добавляют градуировочный раствор смеси ди- и полихлорфенолов в соответствии с таблицей 3, приливают 4 - 5 см3 очищенного гексана и встряхивают содержимое воронки в течение 0,5 мин.
После расслоения переносят водную фазу в другую воронку такой же вместимости, добавляют 0,4 см3 уксусного ангидрида, далее проводят все операции по извлечению ацетатов ди- и полихлорфенолов и обработке экстракта, описанные в 10.1.2 и 10.1.3, и записывают хроматограммы.
9.7.2 При выполнении измерений без ацилирования для приготовления градуировочных образцов в делительные воронки вместимостью 50 см3 помещают 20 см3 фосфатного буферного раствора, приливают градуировочный раствор смеси ди- и полихлорфенолов в соответствии с таблицей 3, добавляют 4 - 5 см3 очищенного гексана и встряхивают содержимое воронки в течение 0,5 мин. После расслоения переносят водную фазу в другую воронку такой же вместимости, приливают 1,0 см3 рабочего раствора внутреннего стандарта с массовой концентрацией гексахлорбензола 0,040 мкг/см3, добавляют 0,5 см3 раствора серной кислоты (1:4), далее проводят все операции по извлечению ди- и полихлорфенолов и обработке экстракта, описанные в 10.2.2 и 10.2.3, и записывают хроматограммы.
Таблица 3 - Схема приготовления и состав градуировочных образцов ди- и полихлорфенолов
|
Номер градуировочного образца |
Объем градуировочного раствора смеси ди- и полихлорфенолов, см3 |
Содержание ди- и полихлорфенолов в градуировочном образце, мкг |
|||
|
№ 2 |
№ 1 |
2,3-; 2,4-; 2,5-; 2,6- дихлорфенолы |
3,4-; 3,5-дихлорфенолы |
Три-, тетра- и пентахлорфенолы |
|
|
1 |
0,20 |
- |
0,080 |
0,12 |
0,020 |
|
2 |
0,40 |
- |
0,16 |
0,24 |
0,040 |
|
3 |
0,60 |
- |
0,24 |
0,36 |
0,060 |
|
4 |
0,80 |
- |
0,32 |
0,48 |
0,080 |
|
5 |
1,00 |
- |
0,40 |
0,60 |
0,100 |
|
6 |
- |
1,0 |
0,80 |
1,2 |
0,20 |
|
7 |
- |
1,5 |
1,2 |
1,8 |
0,30 |
|
8 |
- |
2,0 |
1,6 |
2,4 |
0,40 |
|
9 |
- |
2,5 |
2,0 |
3,0 |
0,50 |
При хранении в темном прохладном месте полученные экстракты можно использовать в течение месяца. Во время хранения не следует допускать полного испарения гексана, это делает образец непригодным для дальнейшего использования.
Примеры хроматограмм ди- и полихлорфенолов и их ацетатов приведены в приложении Б.
9.7.3 При проведении расчетов используют высоты или площади пиков. Находят отношения Кхп высоты (или площади) пика каждого ди- и полихлорфенола к высоте (или площади) внутреннего стандарта на той же хроматограмме по формулам
![]() (2)
(2)
![]() (3)
(3)
где hx - высота пика ди- и полихлорфенола, мм;
hв - высота пика внутреннего стандарта, мм;
Sx - площадь пика ди- и полихлорфенола, мм2;
Sв - площадь пика внутреннего стандарта, мм2.
По полученным данным методом наименьших квадратов устанавливают две градуировочные зависимости для каждого ди- и полихлорфенола в координатах: содержание ди- и полихлорфенола в конкретном градуировочном образце (см. таблицу 3) - величина Кхп для этого же образца. Первую градуировочную зависимость устанавливают по образцам № 1 - № 5, вторую - № 5 - № 9. Допускается устанавливать одну градуировочную зависимость по образцам № 1 - № 5, если концентрация дихлорфенов в анализируемых пробах воды не превышает 2 мкг/дм3, полихлорфенолов - 0,4 мкг/дм3.
Для определения времени удерживания ди- и полихлорфенолов относительно внутреннего стандарта используют градуировочный образец № 5. Проверку времени удерживания осуществляют перед анализом каждой серии проб.
9.7.4 Контроль стабильности градуировочной характеристики следует проводить не реже одного раза в неделю при ежедневной работе, либо при анализе каждой серии проб при периодической работе на приборе. Для контроля стабильности используют градуировочные образцы по 9.7.1 или 9.7.2 (не менее 2 образцов для каждой градуировочной зависимости). Градуировочную характеристику признают стабильной, если выполняется условие
|qx - qr| ≤ 0,10 ∙ qr, (4)
где qx - результат контрольного измерения содержания ди- и полихлорфенола в образце, мкг;
qr - приписанное образцу содержание ди- и полихлорфенола, мкг.
Если условие стабильности не выполняется для одного градуировочного образца, необходимо выполнить повторное измерение этого образца для исключения результата, содержащего грубую погрешность. При повторном невыполнении условия, выясняют причины нестабильности, устраняют их и повторяют измерения с использованием других образцов, предусмотренных методикой. Если градуировочная характеристика вновь не будет удовлетворять условию (4), устанавливают новую градировочную зависимость.
9.8 Холостая проба
Перед анализом проб природной или очищенной сточной воды следует проверить чистоту используемых растворов, реактивов, посуды. Для этого берут 250 см3 бидистиллированной воды и проводят все операции, описанные в разделе 10.
Если на хроматограмме холостой пробы практически отсутствуют пики, совпадающие по времени выхода с определяемыми соединениями (допускается наличие незначительных пиков, высота которых не превышает 3 % от высоты внутреннего стандарта), то все растворы и реактивы могут использоваться для анализа. В противном случае следует выяснить, какой из реактивов вносит загрязнение и очистить или заменить его.
10 Порядок выполнения измерений
10.1 Выделение ди- и полихлорфенолов из воды и концентрирование при выполнении измерений с ацилированием
10.1.1 В делительную воронку вместимостью 500 см3 полностью переносят пробу из склянки, в которую ее поместили после отбора, стенки склянки тщательно ополаскивают дважды по 2 - 3 см3 ацетона, который присоединяют к пробе. Если проба не была законсервирована, добавляют 2 см3 раствора серной кислоты 2 моль/дм3, 2 см3 10 %-ного раствора сульфата меди, 1,0 см3 рабочего раствора внутреннего стандарта 2,4,6-трибромфенола (0,10 мкг), 15 см3 толуола и экстрагируют ди- и полихлорфенолы в течение 2 мин. После расслоения фаз водный слой почти полностью переносят в другую воронку вместимостью 500 см3, круговыми движениями несколько раз перемешивают экстракт, дают еще несколько минут отстояться и как можно полнее отделяют воду. Экстракт переносят в делительную воронку вместимостью 100 см3. Воронку, в которой проводили экстракцию, споласкивают 5 см3 толуола и переносят его в воронку с водной пробой. Повторяют экстракцию в течение 1 мин, после расслаивания водную пробу отбрасывают (если при отборе пробы объем ее не был измерен, то предварительно переносят пробу в мерный цилиндр вместимостью 500 см3, измеряют и записывают объем воды с поправкой на добавленные реактивы).
К реэкстракту приливают 5 см3 гексана и встряхивают в течение 0,5 мин. После отстаивания переносят водный слой в другую делительную воронку вместимостью 50 см3, добавляют 0,4 см3 уксусного ангидрида, перемешивают от 10 до 15 с и дают постоять еще 30 с, затем приливают 10 см3 гексана, закрывают воронку пробкой, встряхивают ее и, перевернув пробкой вниз, открывают кран, чтобы сбросить избыточное давление паров гексана. Повторяют этот прием еще два - три раза, затем экстрагируют ацетаты ди- и полихлорфенолов в течение 1,5 мин.
После отстаивания в течение 10 - 15 минут удаляют прозрачный водный слой. Если гексановый экстракт эмульгирован, после удаления водного слоя экстракт несколько раз перемешивают плавными круговыми движениями и дают возможность еще отстояться несколько минут. После этого водную фазу удаляют как можно полнее, а гексановый экстракт переносят в сухой стакан вместимостью 25 или 50 см3. В делительную воронку добавляют для споласкивания 3 см3 гексана.
10.1.3 К экстракту в стакане добавляют небольшими порциями безводный сульфат натрия, перемешивая стеклянной палочкой, до полного осушения экстракта. Прозрачный экстракт переносят в коническую градуированную микропробирку или V-виалу (см. рисунок 1), предварительно сполоснув их гексаном, и упаривают при температуре от 50 °С до 60 °С на песчаной или водяной бане (см. рисунок 2) под струей очищенного воздуха, продуваемого микрокомпрессором через угольный фильтр.
Экстракт переносят в микропробирку (V-виалу) частями, по мере упаривания. После переноса всего экстракта в стакан с сульфатом натрия приливают гексан, использованный для споласкивания воронки и промывают сульфат натрия, тщательно перемешивая его палочкой. Эту порцию гексана также переносят в микропробирку или V-виалу с экстрактом и упаривают содержимое до объема примерно 0,2 см3.
10.2 Выделение ди- и полихлорфенолов из воды и концентрирование при выполнении измерений без ацилирования
10.2.1. Выполняют экстракцию ди- и полихлорфенолов из воды согласно 10.1.1, но не добавляя раствор 2,4,6-трибромфенола. К объединенному экстракту приливают 20 см3 фосфатного буферного раствора и реэкстрагируют ди- и полихлорфенолы в течение 2 мин. Дают возможность фазам расслоиться, нижний водный слой переносят в делительную воронку вместимостью 50 см3, толуол отбрасывают.
10.2.2 К реэкстракту приливают 5 см3 гексана и встряхивают воронку в течение 0,5 мин. После отстаивания переносят водный слой во вторую воронку вместимостью 50 см3, гексан отбрасывают. В воронку с водным раствором приливают 1,0 см3 рабочего раствора внутреннего стандарта гексахлорбензола (0,040 мкг), добавляют 0,5 см3 раствора серной кислоты (1:4), тщательно перемешивают круговыми движениями, затем приливают 10 см3 гексана и экстрагируют ди- и полихлорфенолы в течение 3 мин.
После расслоения фаз прозрачный водный слой возвращают в первую воронку вместимостью 50 см3. Если гексановый экстракт эмульгирован, после удаления водного слоя экстракт несколько раз перемешивают плавными круговыми движениями и дают возможность еще отстояться несколько минут. После этого отделившуюся воду присоединяют к основной порции, а гексановый экстракт переносят в сухой стакан вместимостью 25 или 50 см3. Ополаскивают делительную воронку 5 см3 гексана, переносят его в воронку с водным раствором и повторяют экстракцию в течение 2 мин. После отстаивания водный слой отбрасывают, а гексановые экстракты объединяют в стакане. В воронку, где проводилась повторная экстракция приливают 3 см3 гексана и ополаскивают ее.
10.2.3 К экстракту в стакане добавляют небольшими порциями безводный сульфат натрия, перемешивая стеклянной палочкой, до полного осушения экстракта. Прозрачный экстракт переносят в коническую градуированную микропробирку или V-виалу (см. рисунок 1), предварительно сполоснув их гексаном, и упаривают при температуре от 50 °С до 60 °С на песчаной или водяной бане (рисунок 2) под струей очищенного воздуха, продуваемого микрокомпрессором через угольный фильтр.
Экстракт переносят в микропробирку (V-виалу) частями, по мере упаривания. После переноса всего экстракта в стакан с сульфатом натрия приливают гексан, использованный для споласкивания воронки и промывают сульфат натрия, тщательно перемешивая его палочкой. Эту порцию гексана также переносят в микропробирку или V-виалу с экстрактом и упаривают содержимое до объема примерно 0,1 - 0,2 см3.
10.3 Хроматографирование экстрактов
Устанавливают условия хроматографирования в соответствии с 9.6. Вводят в испаритель хроматографа гексановый экстракт (2 мм3 при работе с капиллярной колонкой и 5 мм3 при работе с набивной колонкой), записывают хроматограмму. Повторяют измерения 2 - 3 раза.
В приложении Б приведены в качестве примера хроматограммы экстракта воды речной воды без добавки и с добавкой ди- и полихлорфенолов при выполнении измерений с ацилированием.
Идентификацию ди- и полихлорфенолов осуществляют сравнением времени удерживания относительно внутреннего стандарта на хроматограмме градуировочного образца ди- и полихлорфенолов или их ацетатов и анализируемой пробы. Если на хроматограмме пробы имеются пики, соответствующие по времени удерживания ди- и полихлорфенолам или их ацетатам, особенно при появлении пиков соответствующих веществам с одинаковыми временами удерживания, либо при анализе сильно загрязненных проб, где возможно наложение пиков посторонних веществ, следует проверить корректность идентификации хроматографированием пробы на колонке с более полярной фазой. Следует иметь в виду, что некоторые изомеры трудно разделить на любой фазе, например, 2,4- и 2,5-дихлорфенолы. Соединение можно считать идентифицированным только в том случае, если соответствующий ему пик выходит на обеих колонках, в противном случае делают вывод об отсутствии данного соединения в пробе.
При анализе однотипных проб, состав которых не подвергается резким изменениям, либо когда известно заранее, какие из ди- и полихлорфенолов могут содержаться в пробе, идентификация с использованием полярной колонки не является обязательной для каждой пробы, а может быть проведена для одной - двух проб из однотипной серии.
Мешающее влияние посторонних веществ в основном устраняется при выполнении операций, предусмотренных методикой, лишь при анализе сильно загрязненных вод могут появиться дополнительные пики на хроматограммах, затрудняющие идентификацию и расчет количественного содержания ди- и полихлорфенолов. Для устранения таких помех достаточно использовать дополнительную идентификацию определяемых соединений на колонке с полярной фазой.
Примечание - При анализе с ацилированием очищенных сточных вод, в которых вероятно присутствие соединений брома, либо природных вод, загрязняемых такими сточными водами, следует удостовериться в отсутствии 2,4,6-трибромфенола в анализируемой воде, либо использовать в качестве внутреннего стандарта гексахлорбензол. В этом случае внутренний стандарт добавляют в реэкстракт перед добавлением уксусного анагидрида.
11 Вычисление результатов измерений
11.1 Для расчета используют хроматограммы полученные на колонке с неполярной фазой (SE-54, SE-30 или аналогичными), однако в том случае когда в пробе имеются соединения, времена удерживания которых на этих фазах совпадают, для расчета используют также результаты, полученные на колонке с полярной фазой.
Находят отношения высот (площадей) пиков ди- и полихлорфенолов на хроматограмме к высоте (площади) пика внутреннего стандарта на этой же хроматограмме. Если это отношение составляет менее 0,2, массовую концентрацию каждого ди- и полихлорфенола X, мкг/дм3 в анализируемой пробе воды рассчитывают по формулам
![]() (5)
(5)
![]() (6)
(6)
где qx1 - содержание ди- и полихлорфенола в аликвоте пробы, найденное по градуировочной зависимости, мкг;
bx - коэффициент, учитывающий потери ди- и полихлорфенолов в процессе анализа (таблица 4);
V - объем пробы воды, взятый для анализа, дм3;
Кх1 - отношение высоты (площади) пика определяемого ди- и полихлорфенола к высоте площади) пика внутреннего стандарта в градуировочном образце № 1 (см. 9.7.1 и 9.7.2).
Таблица 4 - Коэффициенты, учитывающие потери ди- и полихлорфенолов в процессе анализа
|
Коэффициент bx |
||
|
Выполнение измерений с ацилированием |
Выполнение измерений без ацилирования |
|
|
2,3-, 2,5-дихлорфенолы |
1,0 |
0,80 |
|
2,4-, 2,6-дихлорфенолы |
1,0 |
0,90 |
|
3,5-дихлорфенол |
0,95 |
0,70 |
|
3,4-дихлорфенол |
0,90 |
0,50 |
|
2,4,6-, 2,3,4-, 2,3,5-, 2,4,5-трихлорфенолы |
1,0 |
0,90 |
|
2,3,6-трихлорфенол |
1,0 |
1,0 |
|
3,4,5-трихлорфенол |
0,95 |
0,70 |
|
2,3,4,5-тетрахлорфенол |
0,95 |
1,0 |
|
2,3,5,6-, 2,3,4,6-тетрахлорфенолы |
1,0 |
0,90 |
|
Пентахлорфенолы |
1,0 |
0,90 |
11.2 Если отношение высоты (площади) пика определяемого ди- и полихлорфенола к внутреннему стандарту составляет величину 0,2 или более, содержание его в аликвоте пробы, взятой для анализа, находят по соответствующей градуировочной зависимости. Массовую концентрацию ди- и полихлорфенола в анализируемой пробе воды рассчитывают по формуле
![]() (7)
(7)
12 Оформление результатов измерений
12.1 Результат измерения в документах, предусматривающих его использование, представляют в виде:
Х ± Δ, мкг/дм3 (Р = 0,95), (8)
где ± Δ - границы характеристики погрешности результата измерения для данной массовой концентрации ди- и полихлорфенолов, мкг/дм3 (см. таблицу 2).
Численные значения результата измерения должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности, последние не должны содержать более двух значащих цифр.
12.2 Допустимо представлять результат в виде
Х ± Δл (Р = 0,95) при условии Δл < Δ, (9)
где ± Δл - границы характеристик погрешности результатов измерений, установленные при реализации методики в лаборатории и обеспечиваемые контролем стабильности результатов измерений.
12.3 Результаты измерений оформляют протоколом или записью в журнале по формам, приведенным в Руководстве по качеству лаборатории.
13 Контроль качества результатов измерений при реализации методики в лаборатории
13.1 Общие положения
13.1.1 Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
- оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
13.1.2 Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
13.2 Алгоритм оперативного контроля процедуры выполнения измерений с использованием метода добавок
13.2.1 Оперативный контроль процедуры выполнения измерений проводят с использованием рабочих проб природной или очищенной сточной воды, законсервированных в соответствии с подразделом 9.1. В качестве добавок используют градуировочный раствор ди- и полихлорфенолов № 1.
Контроль исполнителем процедуры выполнения измерений проводят путем сравнения результатов отдельно взятой контрольной процедуры Кк с нормативом контроля К.
13.2.2 Результат контрольной процедуры Кк, мкг/дм3, рассчитывают по формуле
Кк = |Х' - Х - Сд|, (10)
где X' - результат контрольного измерения массовой концентрации фенола в пробе с известной добавкой, мкг/дм3;
Сд - концентрация добавки, мкг/дм3.
13.2.3 Норматив контроля погрешности К, мкг/дм3, рассчитывают по формуле
![]() (11)
(11)
где Δлх' - значения характеристики погрешности результатов измерений, установленные при реализации методики в лаборатории, соответствующие массовой концентрации ди- и полихлорфенолов в пробе с добавкой, мкг/дм3;
Δлх - значения характеристики погрешности результатов измерений, установленные при реализации методики в лаборатории, соответствующие массовой концентрации ди- и полихлорфенолов в рабочей пробе, мкг/дм3.
Примечание - Допустимо для расчета норматива контроля использовать значения характеристик погрешности, полученные расчетным путем по формулам Δлх' = 0,84 ∙ Δх' и Δлх = 0,84 ∙ Δх.
13.2.4 Если результат контрольной процедуры удовлетворяет условию
процедуру анализа признают удовлетворительной.
При невыполнении условия (12) контрольную процедуру повторяют. При повторном невыполнении условия (12), выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
14 Проверка приемлемости результатов, полученных в условиях воспроизводимости
14.1 Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости R. При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение предела воспроизводимости рассчитывают по формуле
R = 2,77 ∙ σR. (13)
14.2 При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно разделу 5 ГОСТ Р ИСО 5725 - 6 или МИ 2881.
14.3 Проверка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Приложение
А
(рекомендуемое)
Методика приготовления аттестованных растворов индивидуальных ди- и полихлорфенолов АР-ХФН-Х для установления градуировочных характеристик приборов и контроля точности результатов измерений массовой концентрации ди- и полихлорфенолов газохроматографическим методом
А.1 Назначение и область применения
Настоящая методика регламентирует процедуру приготовления аттестованных растворов индивидуальных ди- и полихлорфенолов, предназначенных для установления градуировочных характеристик приборов и контроля точности результатов измерений массовой концентрации ди- и полихлорфенолов в природных и очищенных сточных водах газохроматографическим методом.
А.2 Метрологические характеристики
А.2.1 Аттестованное значение массовой концентрации ди- и полихлорфенола в аттестованном растворе АР-ХФН-Х составляет 2,00 мг/см3.
А.2.2 Абсолютная величина погрешности аттестованного значения массовой концентрации ди- и полихлорфенола в аттестованном растворе АР-ХФН-Х с вероятностью 0,95 не превышает 0,040 мг/см3.
А.3 Средства измерений, вспомогательные устройства, реактивы
А.3.1 Весы высокого (II) класса точности по ГОСТ Р 53228-2008, максимальная нагрузка не более 200 г, дискретность отсчета не более 0,0002 г.
А.3.2 Колбы мерные 2 класса точности исполнения 2, 2а по ГОСТ 1770-74 вместимостью 50 см3 - 10 шт.
А.3.4 Пипетка градуированная 2-го класса точности по ГОСТ 29227-91 вместимостью 5 см3 - 1 шт.
А.3.5 Стаканчики для взвешивания (бюксы) СВ-19/9 по ГОСТ 25336-82 - 10 шт.
А.3.6 Воронки лабораторные, тип В, диаметром 36 мм по ГОСТ 25336-82 - 10 шт.
А.3.7 Палочки стеклянные диаметром 4 мм длиной от 12 до 15 см - 10 шт.
А.3.8 Шпатель.
А.3.9 Склянки для хранения аттестованных растворов вместимостью 50 см3 с завинчивающейся пробкой и плотным полиэтиленовым вкладышем или склянки с притертыми стеклянными пробками вместимостью 50 см3 - 16 шт.
А.4 Исходные компоненты аттестованных растворов
А.4.1 ГСО состава 2,4-дихлорфенола ГСО 7198-95; 2,4,6-трихлорфенола ГСО 7103-94; пентахлорфенола ГСО 7102-94 или индивидуальные образцы ди- и полихлорфенолов гарантированной степени чистоты, импортные (например, производства фирм Supelco, Sigma-Aldrich, Riedel-de Haёn): 2,4-дихпорфенол, 2,5-дихпорфенол; 2,3-дихлорфенол; 2,6-дихлорфенол; 3,4-дихлорфенол; 3,5-дихлорфенол; 2,4,6-трихлорфенол; 2,4,5-трихлорфенол; 2,3,5-трихлорфенол; 2,3,6-трихлорфенол; 2,3,4-трихлорфенол; 3,4,5-трихлорфенол; 2,3,5,6-тетрахлорфенол; 2,3,4,5-тетрахлорфенол; 2,3,4,6-тетрахлорфенол; пентахлорфенол с содержанием основного вещества не менее 98 %.
А.4.2 Изопропиловый спирт (2-пропанол) особой чистоты 11-5 ОП-1 по ТУ 2632-064-44493179-01 с изм. 1, 2, или по ТУ 6-09-402-85, х.ч.
А.5 Процедура приготовления аттестованных растворов ди- и полихлорфенолов АР-ХФН-Х
На весах высокого класса точности взвешивают в бюксе 0,10 г каждого из ди- и полихлорфенолов с точностью до четвертого знака после запятой. В бюкс приливают пипеткой 5 - 7 см3 изопропилового спирта и перемешивают чистой палочкой до растворения навески. Количественно (по палочке!) через воронку переносят раствор фенола в мерную колбу вместимостью 50 см3, трижды ополаскивают бюкс, палочку и воронку изопропиловым спиртом, сливая его в ту же мерную колбу, доводят раствор в колбе до метки изопропиловым спиртом и перемешивают. Переносят раствор в склянку с плотно закрывающейся пробкой вместимостью 50 см3. Полученным растворам приписывают массовую концентрацию ди- и полихлорфенола 2,0 мг/см3.
А.6 Расчет метрологических характеристик аттестованных растворов
А.6.1 Аттестованное значение массовой концентрации каждого ди- и полихлорфенола в растворе АР-ХФН-Х С, мг/см3, рассчитывают по формуле
![]() (A.1)
(A.1)
где m - масса навески ди- и полихлорфенола, г;
V - вместимость мерной колбы, см3.
А.6.2 Расчет погрешности приготовления аттестованного раствора АР-ХФН-Х Δ, мг/см3, выполняют по формуле
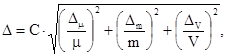 (А.2)
(А.2)
где Δµ - предельное значение возможного отклонения массовой доли основного вещества в реактиве от приписанного значения µ, %;
µ - массовая доля основного вещества (ди- и полихлорфенола), приписанная используемому реактиву, %;
Δm - предельная возможная погрешность взвешивания, г;
ΔV - предельное значение возможного отклонения вместимости мерной колбы от номинального значения, см3.
Погрешность приготовления аттестованного раствора АР-ХФН-Х равна
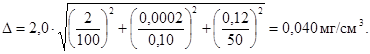
А.7 Требования безопасности
А.7.1 При приготовлении аттестованных растворов ди- и полихлорфенолов соблюдают требования безопасности, установленные в национальных стандартах и соответствующих нормативных документах.
А.7.2 По степени воздействия на организм вредные вещества, используемые при приготовлении аттестованных растворов, относятся к 1-му и 3-му классам опасности по ГОСТ 12.1.007.
А.7.3 Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005.
А.7.4 Взвешивание препаратов ди- и полихлорфенолов следует проводить с использованием средств индивидуальной защиты - респиратора и резиновых перчаток. При попадании ди- и полихлорфенолов на кожу, их следует немедленно снять сухим ватным тампоном, затем протереть тампоном, смоченным изопропиловым спиртом и тщательно промыть водой с мылом.
А.8 Требования к квалификации операторов
Аттестованные растворы может готовить инженер или лаборант со средним профессиональным образованием, прошедший специальную подготовку и имеющий стаж работы в химической лаборатории не менее года.
А.9 Требования к маркировке
На склянки с аттестованными растворами должны быть наклеены этикетки с указанием условного обозначения раствора, наименования конкретного ди- и полихлорфенола, содержащегося в данном растворе, массовой концентрации ди- и полихлорфенола, погрешности ее установления и даты приготовления.
А.10 Условия хранения
Аттестованные растворы ди- и полихлорфенолов хранят в герметично закрытых флаконах в холодильнике в течение 6 мес.
Приложение
Б
(справочное)
Примеры хроматограмм ди- и полихлорфенолов и их ацетатов
На рисунке Б.1 приведена хроматограмма ряда ацетатов ди- и полихлорфенолов, полученная на капиллярной колонке с неподвижной фазой SE-54, а на рисунке Б.2 хроматограмма тех же соединений на набивной колонке с неподвижной фазой ХЕ-60.
На рисунках Б.3 и Б.4 приведены хроматограммы не ацилированных ди- и полихлорфенолов на капиллярной колонке HP 50+.
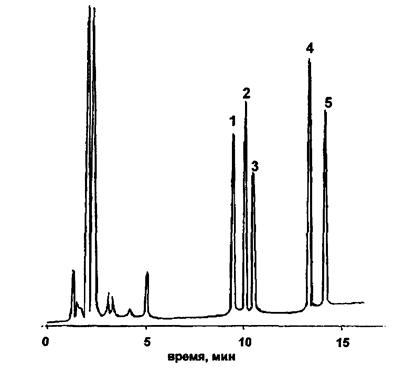
1 - 2,4-дихлорфенол (0,4 мкг); 2 - 3,4 дихлорфенол (0,6 мкг); 3 - 2,4,6 - трихлорфенол (0,1 мкг); 4 - 2,4,6 -трибромфенол (0,1 мкг); 5 - пентахлорфенол (0,1 мкг)
Рисунок Б.1 - Хроматограмма ацетильных производных ди- и полихлорфенолов на капиллярной колонке с неподвижной фазой SE-54
1 - 2,4-дихлорфенол (0,4 мкг); 2 - 2,4,6-трихлорфенол (0,1 мкг); 3 - 3,4-дихлорфенол (0,6 мкг); 4 - 2,4,6-трибромфенол (0,1 мкг); 5 - пентахлорфенол (0,1 мкг)
Рисунок Б.2 - Хроматограмма ацетильных производных ди- и полихлорфенолов на набивной колонке с неподвижной фазой ХЕ-60
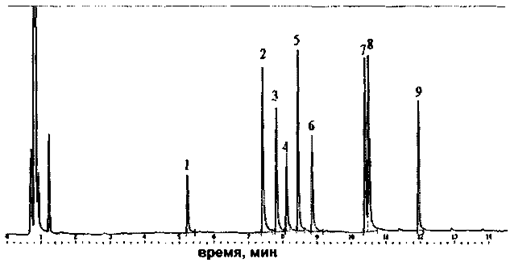
1 - 2,4-дихлорфенол (0,4 мкг); 2 - 2,3-дихлорфенол (0,4 мкг); 3 - 2,6-дихлорфенол (0,4 мкг); 4 - 2,4,6-трихлорфенол (0,1 мкг); 5 - 2,3,4-трихлорфенол (0,1 мкг); 6 - 2,3,5,6-тетрахлорфенол (0,1 мкг); 7 - 3,4,5-трихлорфенол (0,1 мкг); 8 - гексахлорбензол (0,04 мкг); 9 - пентахлорфенол (0,1 мкг)
Рисунок Б.3 - Хроматограмма неацилированных ди- и полихлорфенолов на капиллярной колонке HP 50+
1 - 2,5-дихлорфенол (0,4 мкг); 2 - 2,3,5-трихлорфенол (0,1 мкг); 3 - 2,4,5-трихлорфенол (0,1 мкг); 4 - 3,5-дихлорфенол (0,6 мкг); 5 - 2,3,6-трихлорфенол (0,1 мкг); 6 - 3,4-дихлорфенол (0,6 мкг); 7 - 2,3,4,5-тетрахлорфенол (0,1 мкг) 8 - 2,3,4,6-тетрахлорфенол (0,1 мкг); 9 - гексахлорбензол (0,04 мкг)
Рисунок Б.4 - Хроматограмма неацилированных ди- и полихлорфенолов на капиллярной колонке HP 50+
На рисунках Б.5 и Б.6 приведены хроматограммы экстрактов речной воды без добавок и с добавкой градуировочного раствора ди- и полихлорфенолов при выполнении измерений с ацилированием.
Рисунок Б.5 - Хроматограмма экстракта пробы речной воды на капиллярной колонке с неподвижной фазой SE-54 (с ацилированием)
1 - 2,4-дихлорфенол (1,2 мкг/дм3); 2 - 3,4-дихлорфенол (1,8 мкг/дм3); 3 - 2,4,6-трихлорфенол (0,3 мкг/дм3) 4 - пентахлорфенол (0,3 мкг/дм3)
Рисунок Б.6 - Хроматограмма экстракта пробы речной воды с добавкой ди- и полихлорфенолов на капиллярной колонке с неподвижной фазой SE-54 (с ацилированием)
Лист регистрации изменений
|
Номер изменения |
Номер страницы |
Номер документа (ОРН) |
Подпись |
Дата |
||||
|
измененной |
замененной |
новой |
аннулированной |
внесения изменения |
введения изменения |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
МИНИСТЕРСТВО ПРИРОДНЫХ РЕСУРСОВ И ЭКОЛОГИИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральная служба по гидрометеорологии и мониторингу окружающей среды
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ УЧРЕЖДЕНИЕ «ГИДРОХИМИЧЕСКИЙ ИНСТИТУТ»
|
344090, г. Ростов-на-Дону пр. Стачки, 198 |
Факс: (863) 222-44-70 Телефон (863) 297-51-63, E-mail ghi@aaanet.ru |
СВИДЕТЕЛЬСТВО
об аттестации методики измерений № 507.01.00175-2011
Методика измерений массовой концентрации ди- и полихлорфенолов в водах газохроматографическим методом
разработанная федеральным государственным бюджетным учреждением «Гидрохимический институт» (ФГБУ «ГХИ»), пр-т Стачки, д. 198, г. Ростов-на-Дону (36 с.)
и регламентированная РД 52.24.507-2012. Массовая концентрация ди- и полихлорфенолов в водах. Методика измерений газохроматографическим методом
аттестована в соответствии с ГОСТ Р 8.563-96.
Аттестация осуществлена по результатам экспериментальных исследований.
В результате аттестации установлено, что методика измерений соответствует предъявляемым к ней метрологическим требованиям и обладает метрологическими характеристиками, приведенными в таблицах 1 и 2.
Таблица 1 - Диапазон измерений, значения характеристик погрешности и ее составляющих при принятой вероятности Р = 0,95
|
Диапазон измерений массовых концентраций X, мкг/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости) σr, мкг/дм3 |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) σR, мкг/дм3 |
Показатель правильности (границы систематической погрешности) ±Δc, мкг/дм3 |
Показатель точности (границы погрешности) ±Δ, мкг/дм3 |
|
|
2,3-, 2,4-, 2,5-, 2,6 дихлорфенолы |
От 0,20 до 1,2 включ. |
0,02 + 0,06 ∙ X |
0,03 + 0,08 ∙ X |
0,02 + 0,07 ∙ X |
0,06 + 0,17 ∙ X |
|
Св. 1,2 до 8,0 включ. |
0,09 ∙ X |
0,11 ∙ X |
0,08 ∙ X |
0,23 ∙ X |
|
|
3,4-, 3,5-дихлорфенолы |
От 0,30 до 1,8 включ. |
0,03+0,09 ∙ X |
0,04 + 0,12 ∙ X |
0,03 + 0,08 ∙ С |
0,09 + 0,25 ∙ X |
|
Св. 1,8 до 12 включ. |
0,09 ∙ С |
0,11 ∙ С |
0,08 ∙ С |
0,23 ∙ X |
|
|
Трихлорфенолы |
От 0,05 до 2,0 включ. |
0,08 ∙ X |
0,10 ∙ X |
0,08 ∙ X |
0,22 ∙ X |
|
Тетра- и пентахлорфенолы |
От 0,05 до 2,0 включ. |
0,01+0,06 ∙ X |
0,02+0,08 ∙ X |
0,08 ∙ X |
0,03+0,18 ∙ X |
Таблица 2 - Диапазон измерений, значения пределов повторяемости и воспроизводимости при принятой вероятности Р = 0,95
|
Диапазон измерений массовых концентраций X, мкг/дм3 |
Предел повторяемости (для двух результатов параллельных определений) r, % |
Предел воспроизводимости (значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях, при вероятности Р = 0,95) R, % |
|
|
2,3-, 2,4-, 2,5-, 2,6 дихлорфенолы |
От 0,20 до 1,2 включ. |
0,06 + 0,17 ∙ X |
0,08 + 0,22 ∙ X |
|
Св. 1,2 до 8,0 включ. |
0,25 ∙ X |
0,30 ∙ X |
|
|
3,4-, 3,5- дихлорфенолы |
От 0,30 до 1,8 включ. |
0,08 + 0,025 ∙ X |
0,11 + 0,33 ∙ X |
|
Св. 1,8 до 12 включ. |
0,25 ∙ С |
0,30 ∙ С |
|
|
Трихлорфенолы |
От 0,05 до 2,0 включ. |
0,22 ∙ X |
0,28 ∙ X |
|
Тетра- и пентахлорфенолы |
От 0,05 до 2,0 включ. |
0,03 + 0,17 ∙ X |
0,06 + 0,22 ∙ X |
При реализации методики в лаборатории обеспечивают:
- оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля погрешности).
Алгоритм оперативного контроля исполнителем процедуры выполнения измерений приведен в РД 52.24.507-2012.
Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
Дата выдачи 11.01.2011.
|
Директор |
A.M. Никаноров |
|
|
Главный метролог |
А.А. Назарова |