ГОСТ Р 58505-2019
ГОСТ Р 58505-2019
Информатизация здоровья. Элементы данных и их метаданные для описания структурированной информации о клиническом геномном секвенировании в электронных медицинских картах
| Обозначение: |  ГОСТ Р 58505-2019 ГОСТ Р 58505-2019 |
| Обозначение англ: |  GOST R 58505-2019 GOST R 58505-2019 |
| Статус: | введен впервые |
| Название рус.: | Информатизация здоровья. Элементы данных и их метаданные для описания структурированной информации о клиническом геномном секвенировании в электронных медицинских картах |
| Название англ.: | Health informatics. Data elements and their metadata for describing structured clinical genomic sequence information in electronic health records |
| Дата добавления в базу: | 01.02.2020 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.05.2020 |
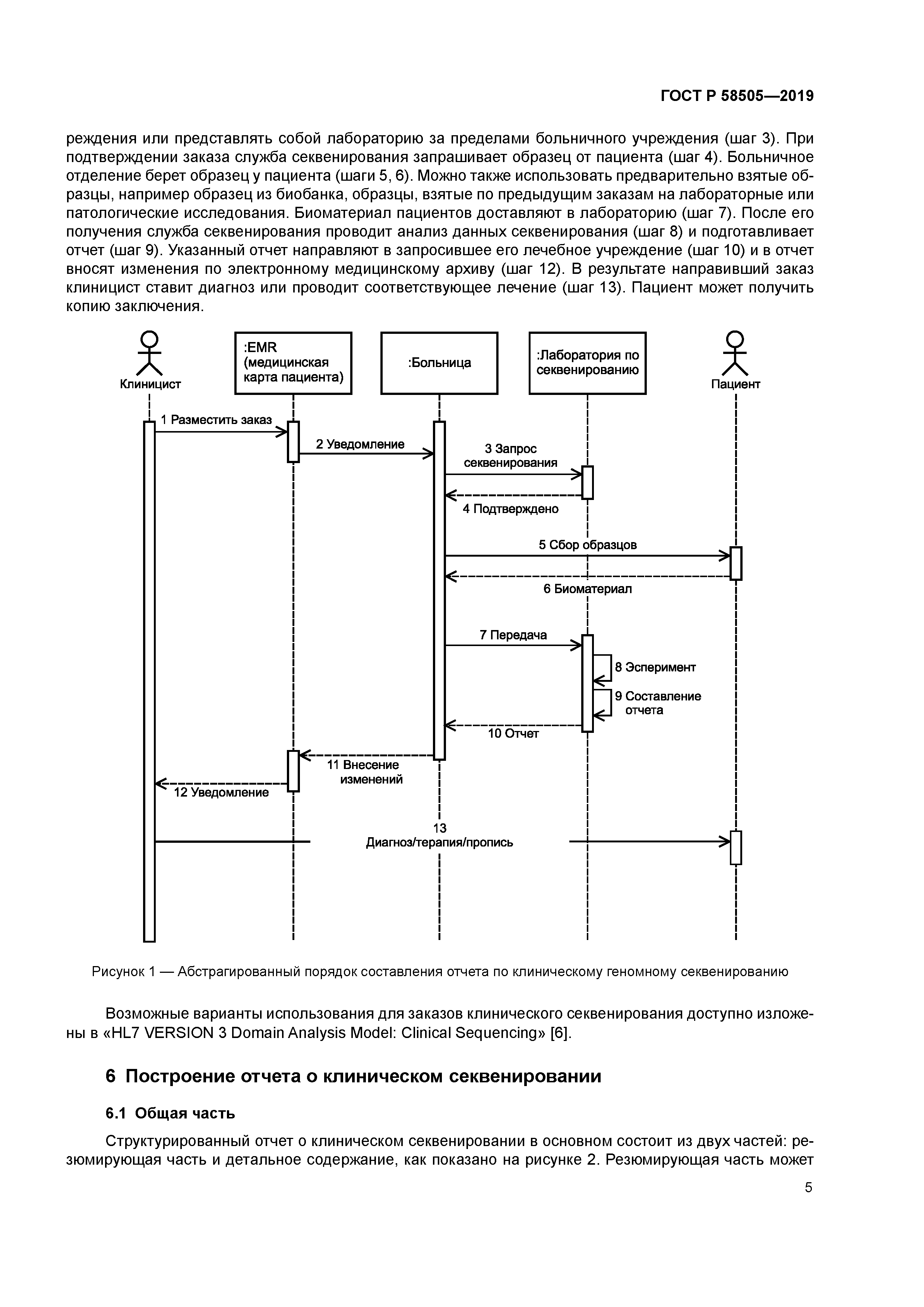
| Область применения: | Стандарт определяет элементы данных и необходимые для них метаданные для выполнения структурированного отчета о клиническом геномном секвенировании для занесения в электронный медицинский архив с упором на геномные данные, созданные посредством технологии секвенирования нового поколения. Стандарт: - определяет построение структурированного отчета о клиническом геномном секвенировании; - определяет поля необходимых данных и их метаданных для структурированного отчета о клиническом геномном секвенировании; - определяет дополнительные данные; - охватывает изменчивость на уровне ДНК по образцам, взятым у человека, с использованием полногеномного секвенирования, полноэкзомного секвенирования и таргетного секвенирования (таргетные генетические панели, направленные на конкретное заболевание) при помощи технологий секвенирования нового поколения. Несмотря на то что транскриптомное секвенирование и иные технологии важны для обеспечения лучшего ухода за пациентом и позволяют проведение прецизионной медицины, стандарт касается исключительно изменчивости на уровне ДНК; - охватывает в основном применение в медицинской практике и клинические исследования, например клинические испытания и прикладные исследования с использованием клинических данных с учетом, в частности, деидентификации или согласия пациента. Фундаментальные исследования и иные научные направления не включены в объем стандарта; - не охватывает другие биологические виды, например геномы вирусов и микробов, а также - не охватывает методики секвенирования по Сенгеру. |
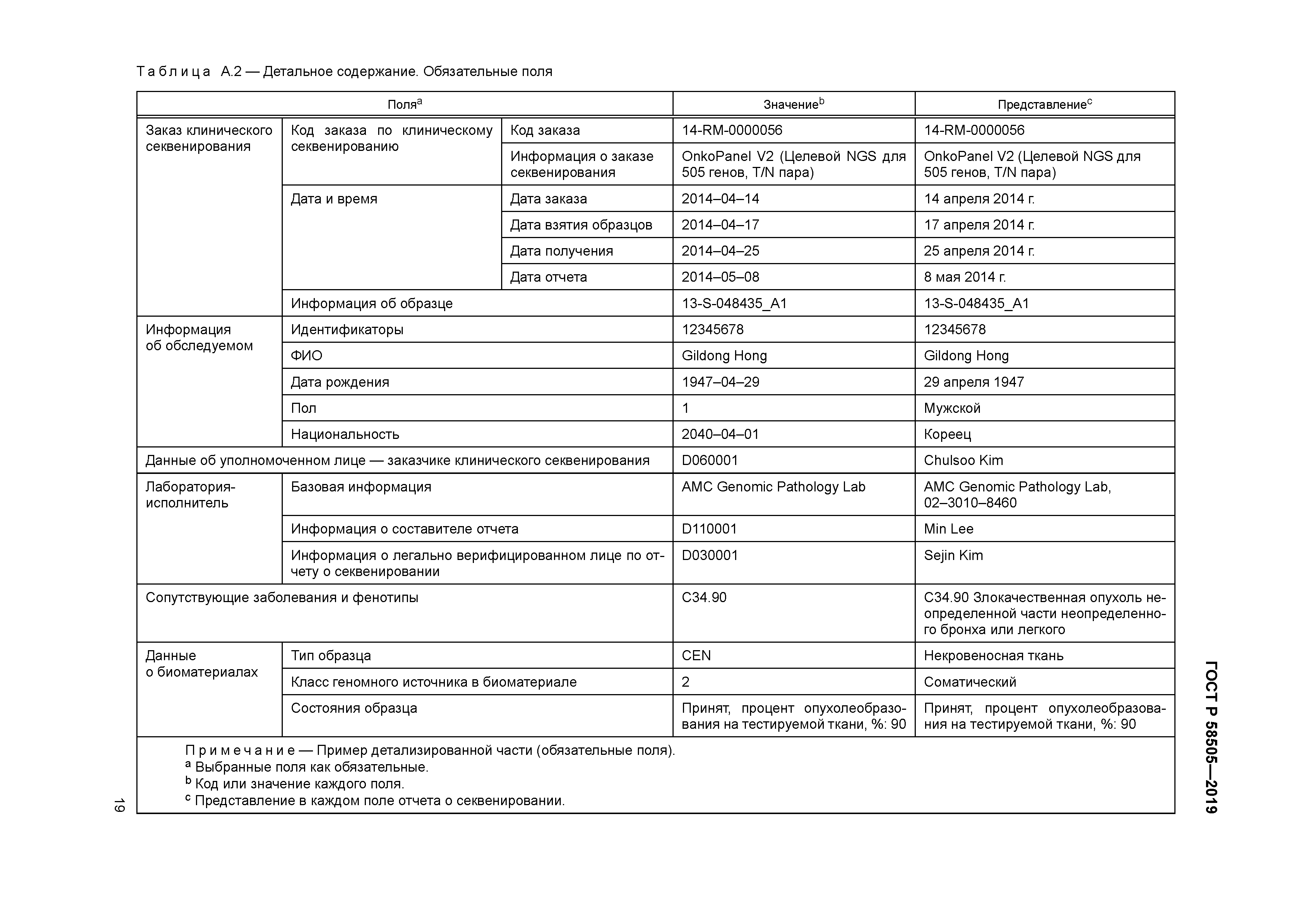
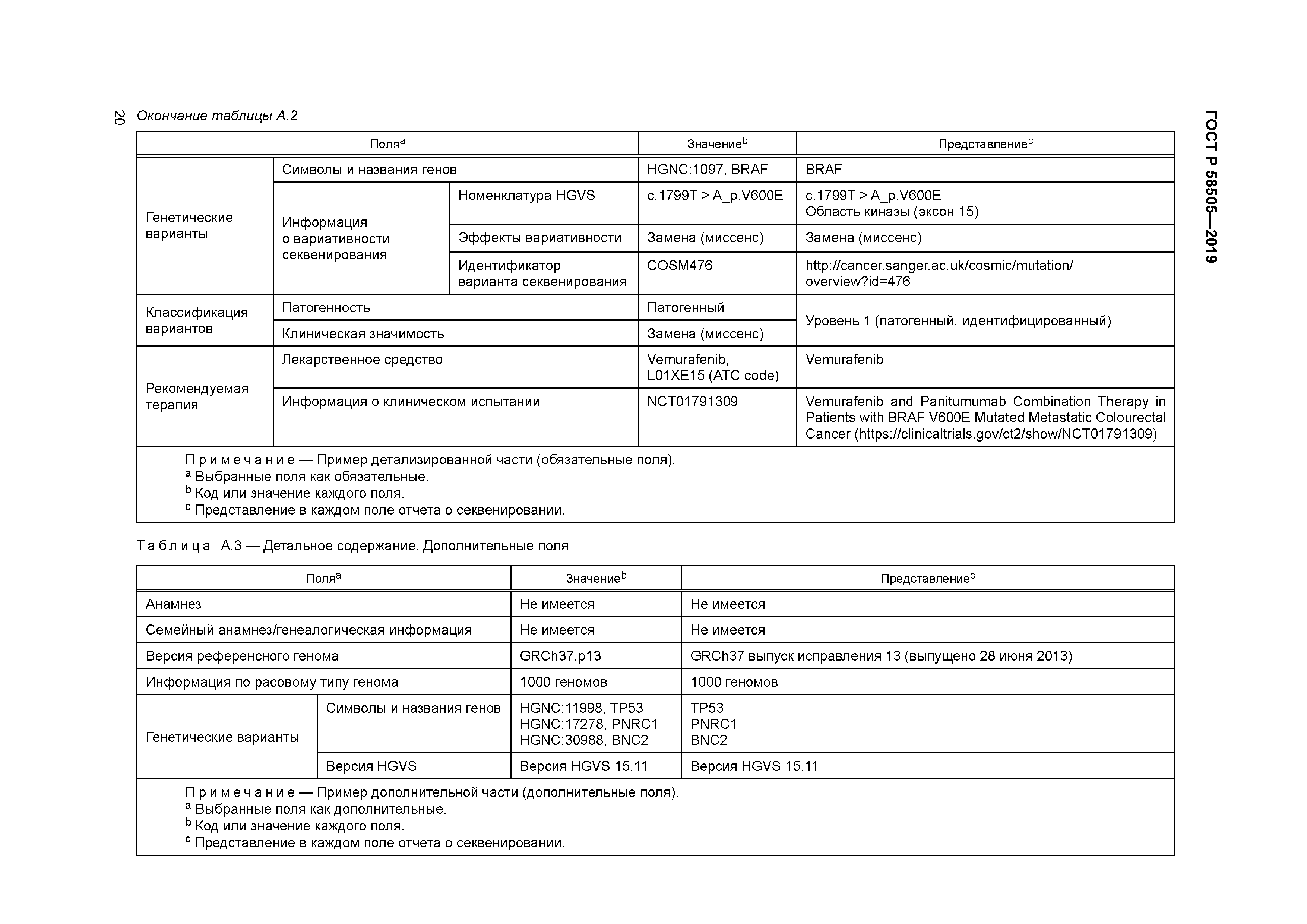
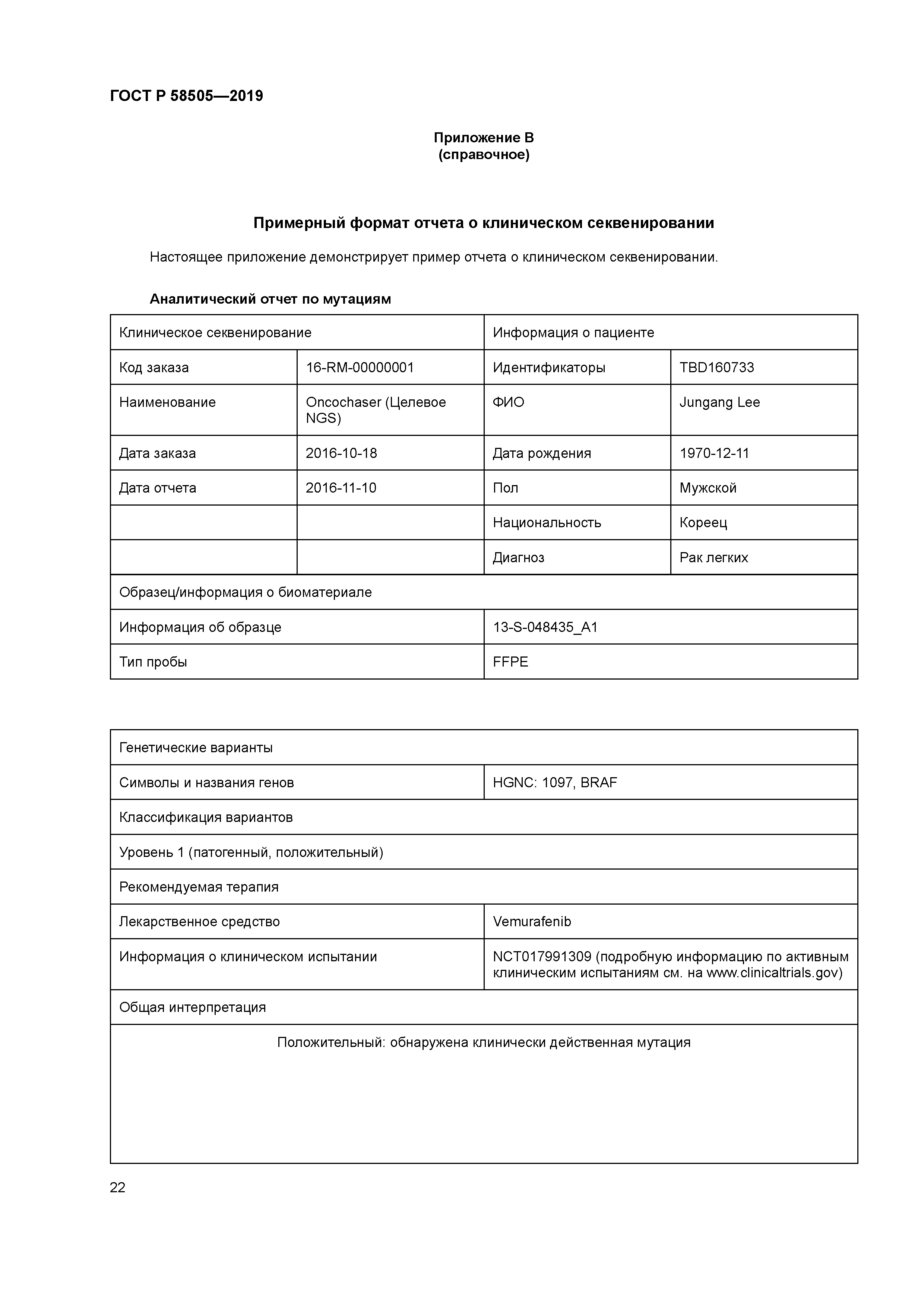
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Сокращения 5 Сценарий варианта использования 6 Построение отчета о клиническом секвенировании 6.1 Общая часть 6.2 Общая интерпретация в резюмирующей части 6.3 Детальное содержание 7 Поля и их номенклатура обязательных данных 7.1 Общая часть 7.2 Заказы на клиническое секвенирование 7.3 Информация об обследуемом 7.4 Информация по легально уполномоченному лицу, заказывающему клиническое секвенирование 7.5 Лаборатория-исполнитель 7.6 Сопутствующие заболевания и фенотипы 7.7 Информация о биоматериале 7.8 Генетические варианты 7.9 Классификация вариантов 7.10 Рекомендуемая терапия 7.11 дополнение 8 Поля и их номенклатура дополнительных данных 8.1 Общая часть 8.2 Анамнез 8.3 Семейный анамнез/генеалогическая информация 8.4 Версия референсного генома 8.5 Информация по расовому типу генома 8.6 Генетические варианты 8.7 детальная информация по секвенированию 8.8 Ссылки Приложение А (справочное) Примерная структура отчета о клиническом секвенировании Приложение В (справочное) Примерный формат отчета о клиническом секвенировании Библиография |
| Разработан: | ФГУП СТАНДАРТИНФОРМ |
| Утверждён: | 29.08.2019 Федеральное агентство по техническому регулированию и метрологии (575-ст) |
| Издан: | Стандартинформ (2019 г. ) |
| Расположен в: |