

 ГОСТ Р ИСО 15378-2017
ГОСТ Р ИСО 15378-2017
Первичные упаковочные материалы для лекарственных средств. Частные требования по применению ИСО 9001:2008 с учетом надлежащей производственной практики (GMP)
| Обозначение: |   ГОСТ Р ИСО 15378-2017 ГОСТ Р ИСО 15378-2017 |
| Обозначение англ: |   GOST R ISO 15378-2017 GOST R ISO 15378-2017 |
| Статус: | взамен |
| Название рус.: | Первичные упаковочные материалы для лекарственных средств. Частные требования по применению ИСО 9001:2008 с учетом надлежащей производственной практики (GMP) |
| Название англ.: | Primery packaging materials for medicinal products. Particular requirements for the application of ISO 9001:2008 with reference to good manufacturing practice (GMP) |
| Дата добавления в базу: | 01.01.2019 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.07.2018 |
| Область применения: | Стандарт устанавливает требования, предъявляемые к системе менеджмента качества в тех случаях, когда организации требуется продемонстрировать способность производить первичные упаковочные материалы для лекарственных средств, которые стабильно соответствуют требованиям потребителя, в том числе регуляторным требованиям и международным стандартам, применимым к первичной упаковке. В стандарте неоднократно используется выражение «если это целесообразно». В том случае, если определенное требование сопровождается данной фразой, это означает, что данное требование является «целесообразным», за исключением случаев, когда организация может документально обосновать иное. |
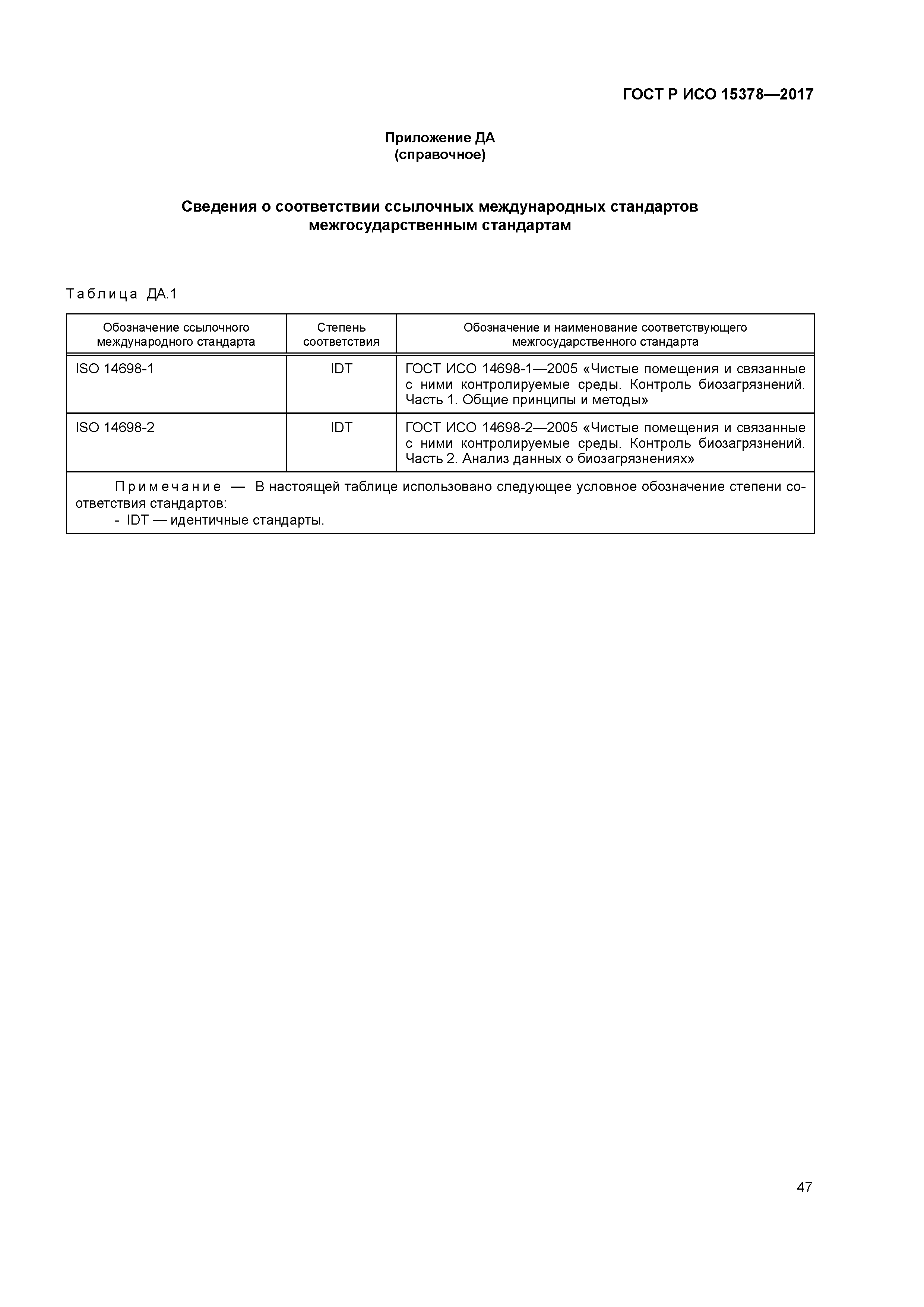
| Оглавление: | 1 Область применения 1.1 Общие положения 1.2 Применение 2 Нормативные ссылки 3 Термины и определения 3.1 Термины, связанные с качеством 3.2 Термины, связанные с менеджментом 3.3 Термины, связанные с организацией 3.4 Термины, связанные с процессами и продукцией 3.5 Термины, относящиеся к характеристикам 3.6 Термины, связанные с соответствием 3.7 Термины, связанные с документацией 3.8 Термины, связанные с испытаниями 3.9 Термины, связанные с управлением рисками 4 Система менеджмента качества 4.1 Общие требования 4.2 Требования, предъявляемые к документации 5 Ответственность руководства 5.1 Обязательства руководства 5.2 Ориентация на потребителя 5.3 Политика в области качества 5.4 Планирование 5.5 Ответственность, полномочия и обмен информацией 5.6 Анализ со стороны руководства 6 Управление ресурсами 6.1 Обеспечение ресурсами 6.2 Персонал 6.3 Инфраструктура 6.4 Производственная зона 6.5 Работы по техническому обслуживанию и уборке 7 Процессы жизненного цикла продукции 7.1 Планирование процессов жизненного цикла продукции…. 7.2 Процессы, связанные с потребителем 7.3 Проектирование и разработка 7.4 Закупки 7.5 Производство и обслуживание 7.6 Управление оборудованием для мониторинга и измерения. 8 Измерение, анализ и улучшение 8.1 Общие положения 8.2 Мониторинг и измерение 8.3 Управление несоответствующей продукцией 8.4 Анализ данных 8.5 Улучшение Приложение А (обязательное) Требования ОМР к печатным материалам для первичной упаковки Приложение В (справочное) Руководство по требованиям, предъявляемым к верификации, квалификации и валидации первичных упаковочных материалов Приложение С (справочное) Взаимосвязь между пунктами настоящего стандарта и структурами более высокого уровня Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов межгосударственным стандартам Библиография |
| Разработан: | ГБОУ ВПО Первый Московский Государственный медицинский Университет им. И.М. Сеченова |
| Утверждён: | 12.09.2017 Росстандарт (1076-ст) |
| Издан: | Стандартинформ (2017 г. ) |
| Расположен в: | |
| Заменяет собой: | |
| Нормативные ссылки: |
|





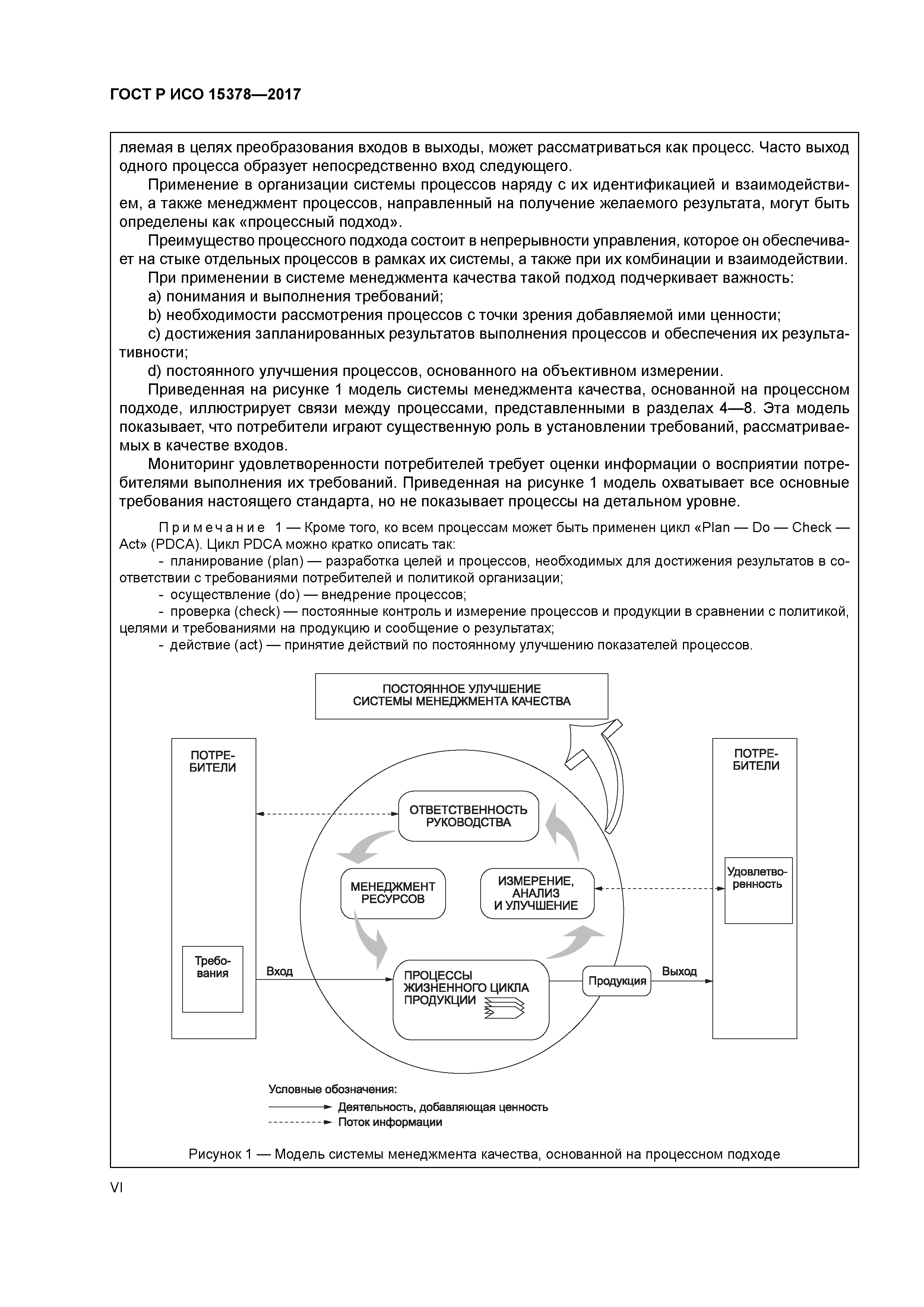




































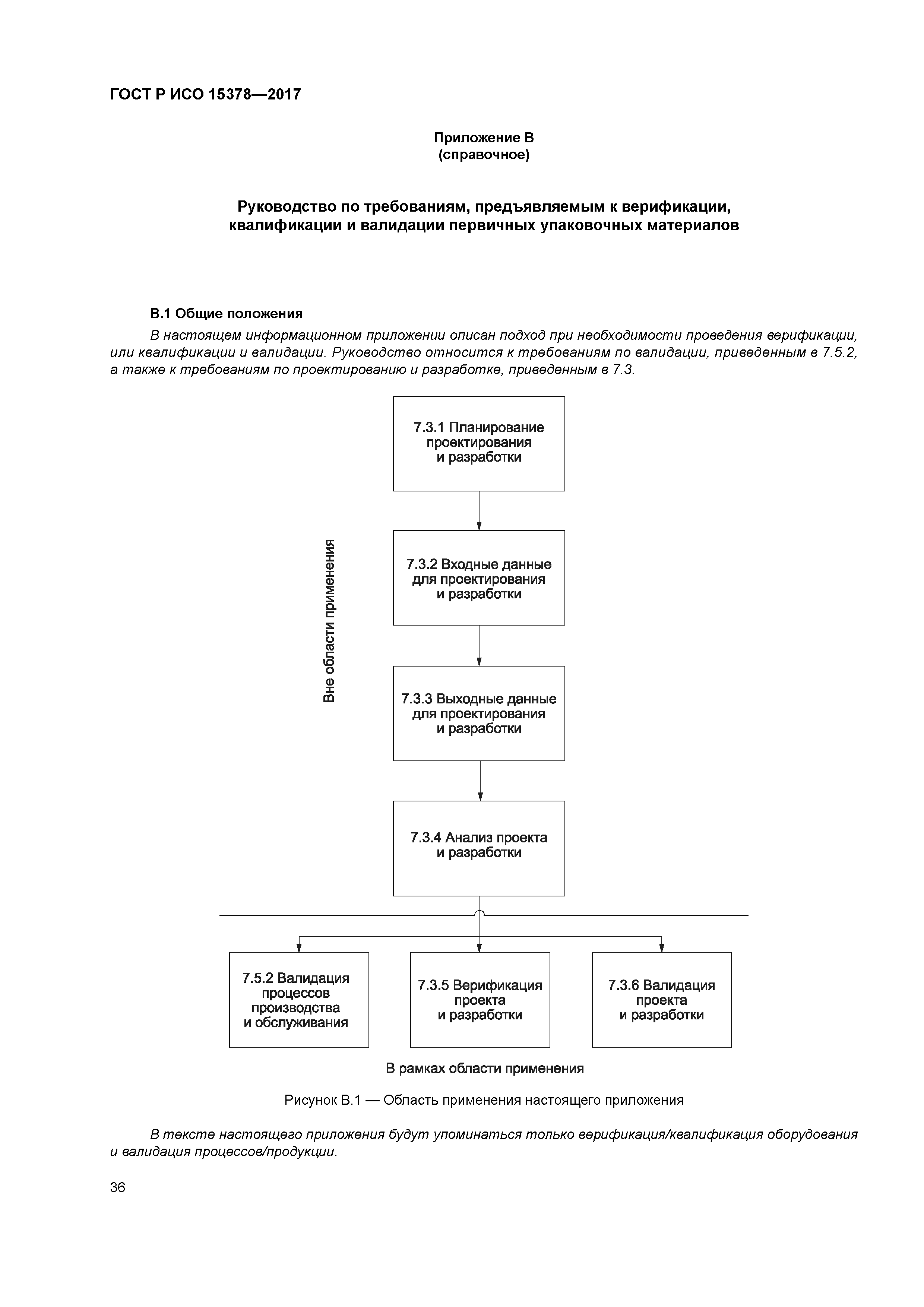



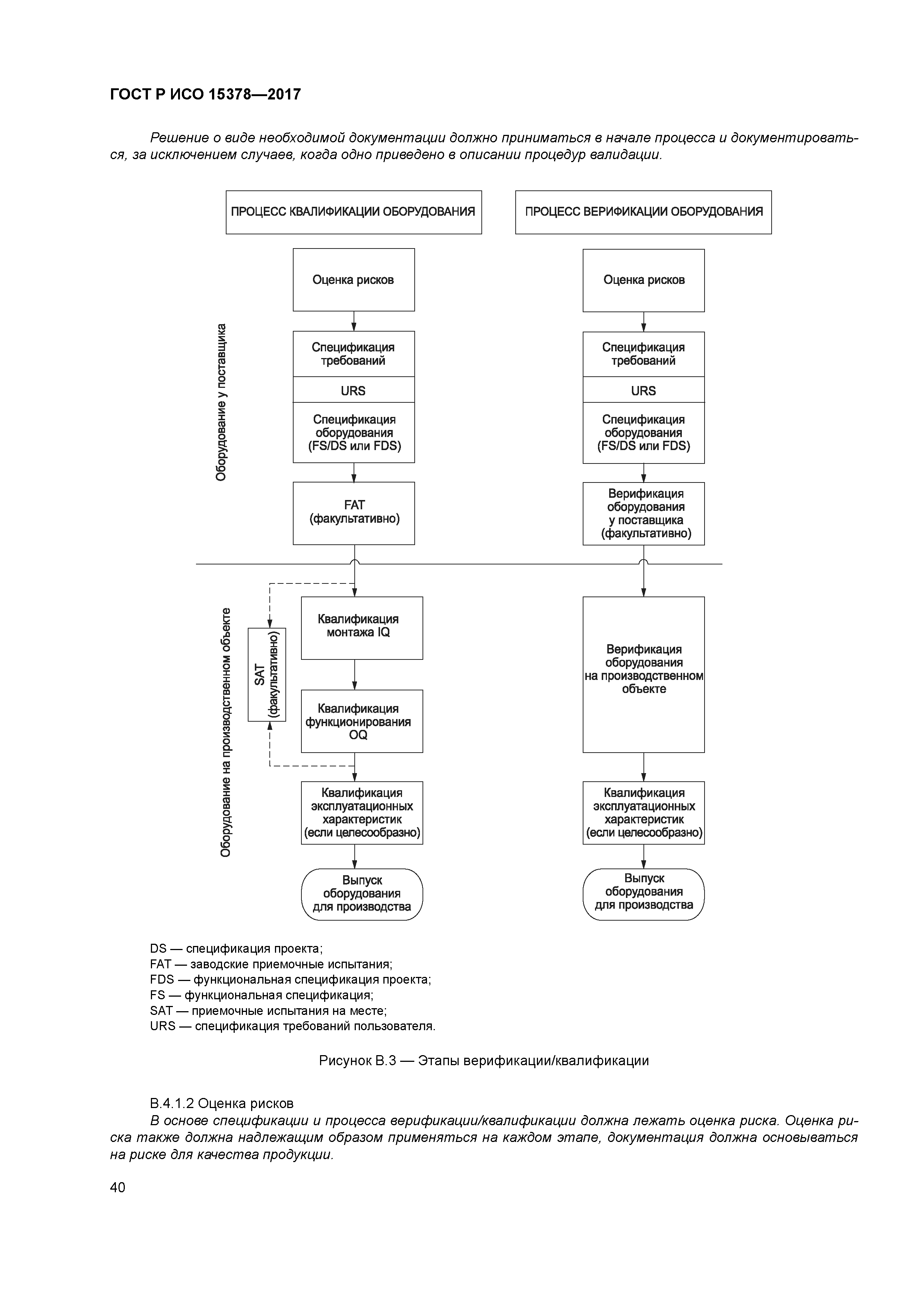

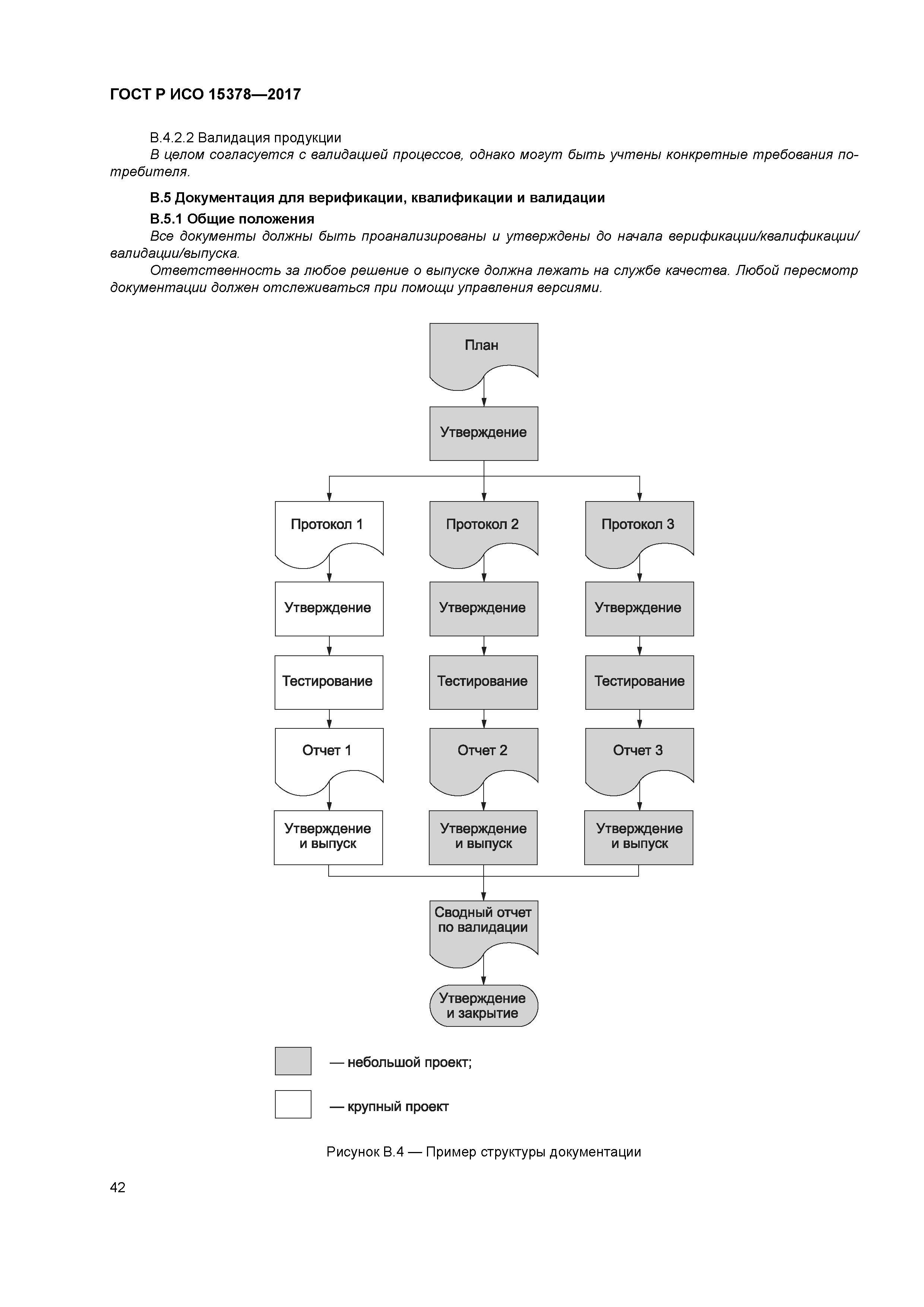






 ГОСТ Р 53699-2009 «Первичные упаковочные материалы для лекарственных средств. Частные требования по применению ГОСТ Р ИСО 9001-2008 с учетом правил GMP»
ГОСТ Р 53699-2009 «Первичные упаковочные материалы для лекарственных средств. Частные требования по применению ГОСТ Р ИСО 9001-2008 с учетом правил GMP»