ГОСТ Р ИСО 11615-2014
ГОСТ Р ИСО 11615-2014
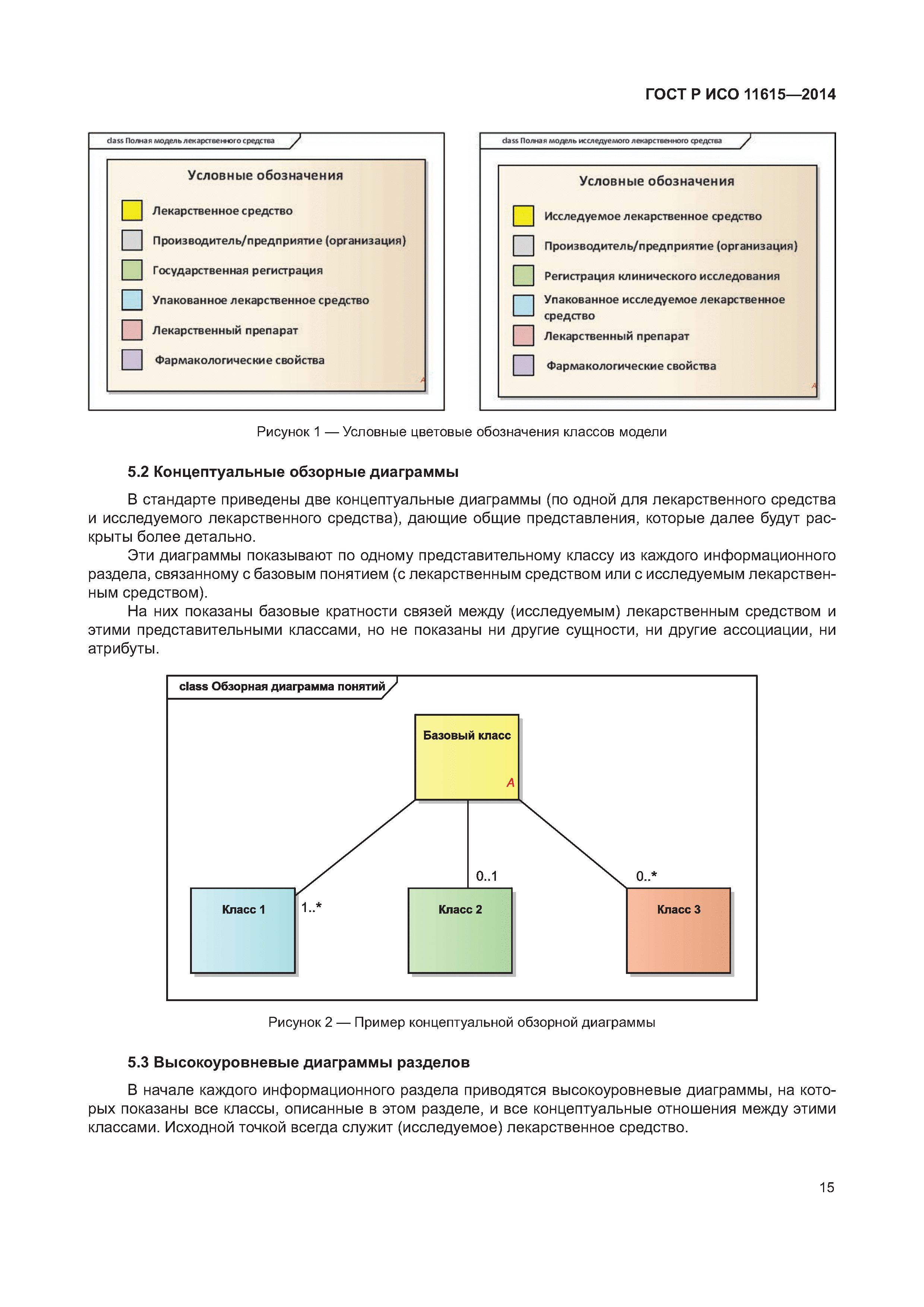
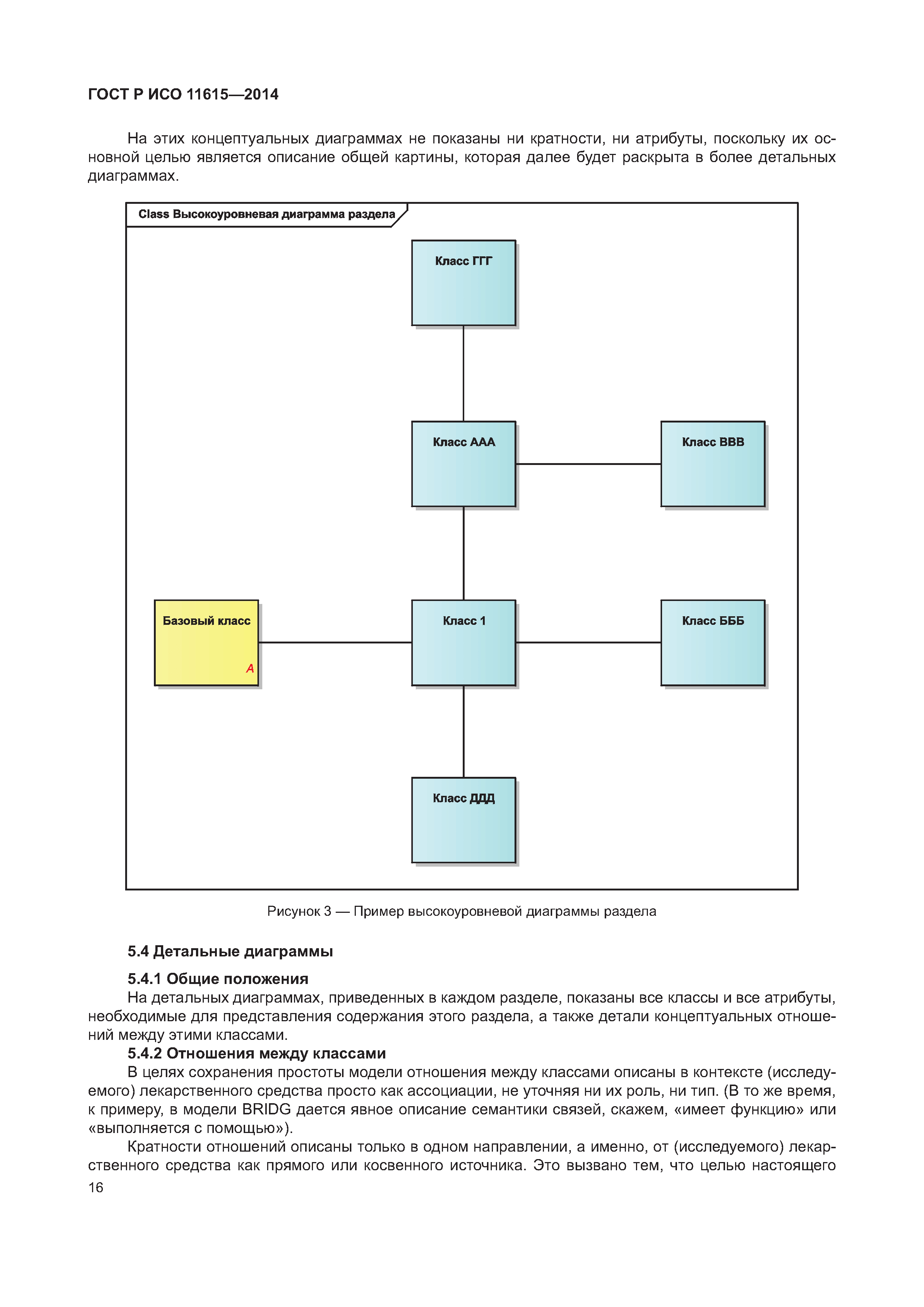
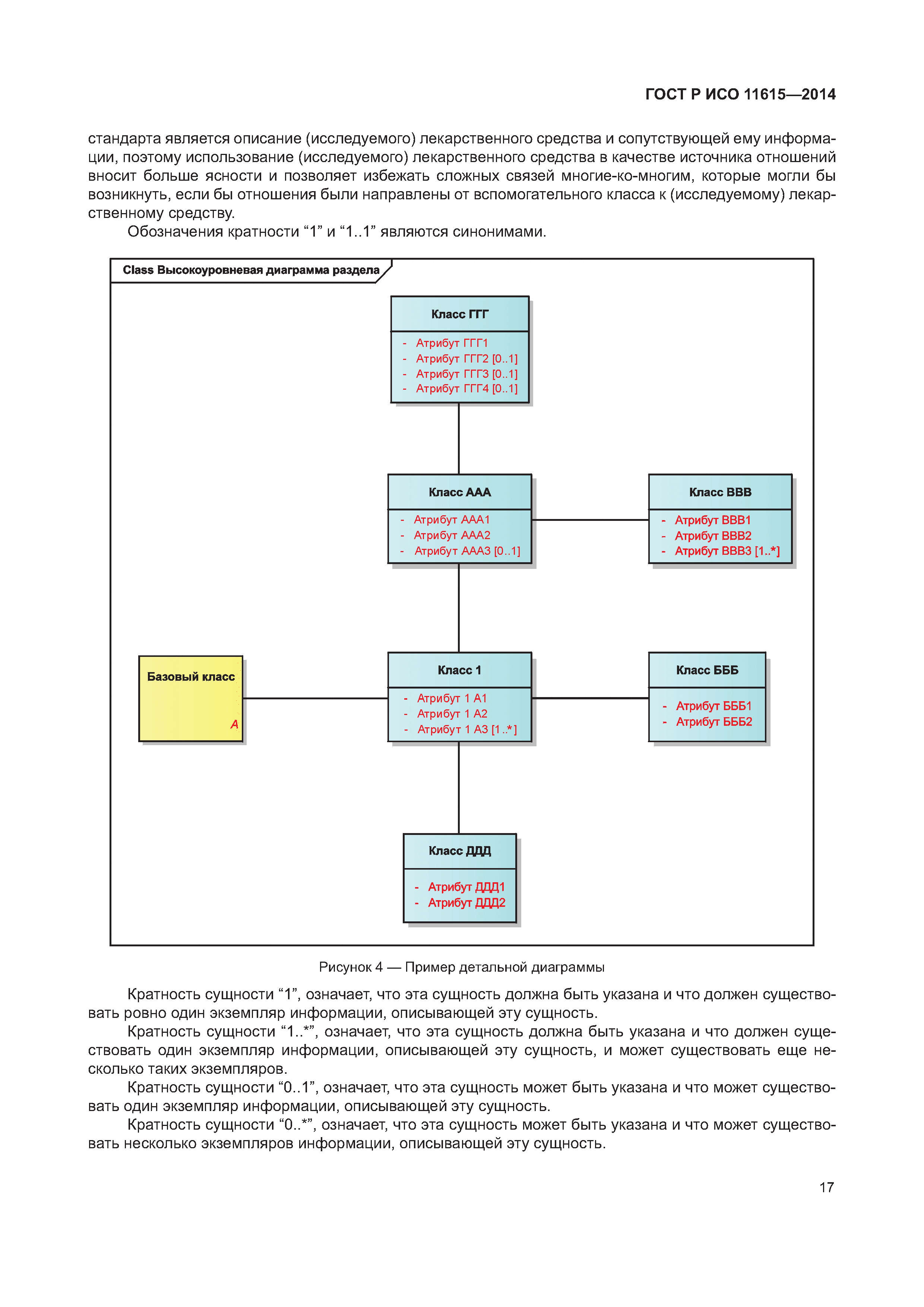
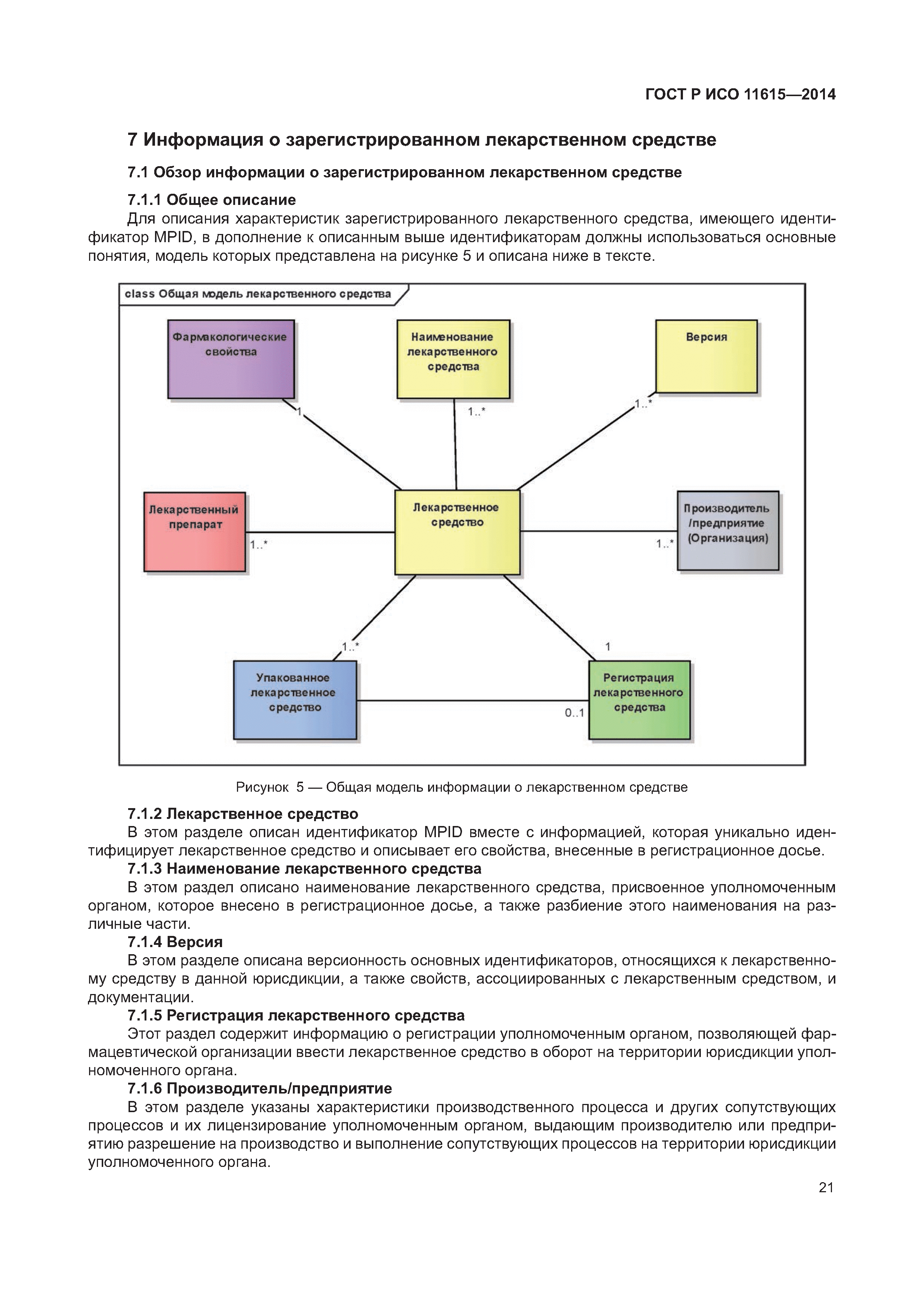
Информатизация здоровья. Идентификация лекарственных средств. Элементы данных и структуры для уникальной идентификации и обмена информацией о регистрируемых лекарственных средствах
| Обозначение: |  ГОСТ Р ИСО 11615-2014 ГОСТ Р ИСО 11615-2014 |
| Обозначение англ: |  GOST R ISO 11615-2014 GOST R ISO 11615-2014 |
| Статус: | введен впервые |
| Название рус.: | Информатизация здоровья. Идентификация лекарственных средств. Элементы данных и структуры для уникальной идентификации и обмена информацией о регистрируемых лекарственных средствах |
| Название англ.: | Health informatics. Identification of medicinal products. Data elements and structures for the unique identification and exchange of regulated medicinal product information |
| Дата добавления в базу: | 12.02.2016 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.10.2015 |
| Область применения: | В стандарте описаны определения и понятия, а также элементы данных и их структурные отношения, необходимые для уникальной идентификации и детального описания лекарственных средств. Стандарты, перечисленные во введении, в своей совокупности представляют собой информационную модель, предназначенную для описания характеристик и уникальной идентификации регистрируемых лекарственных средств для применения человеком в течение всего их жизненного цикла, то есть по мере необходимости от разработки до регистрации, проведения пострегистрационных исследований, обновления или снятия с рынка. Кроме того, для обеспечения возможности успешного обмена информацией, связанной с уникальной идентификацией и характеристиками лекарственных средств, в стандарте описан контекст применения других стандартов обмена данными группы IDMP. |
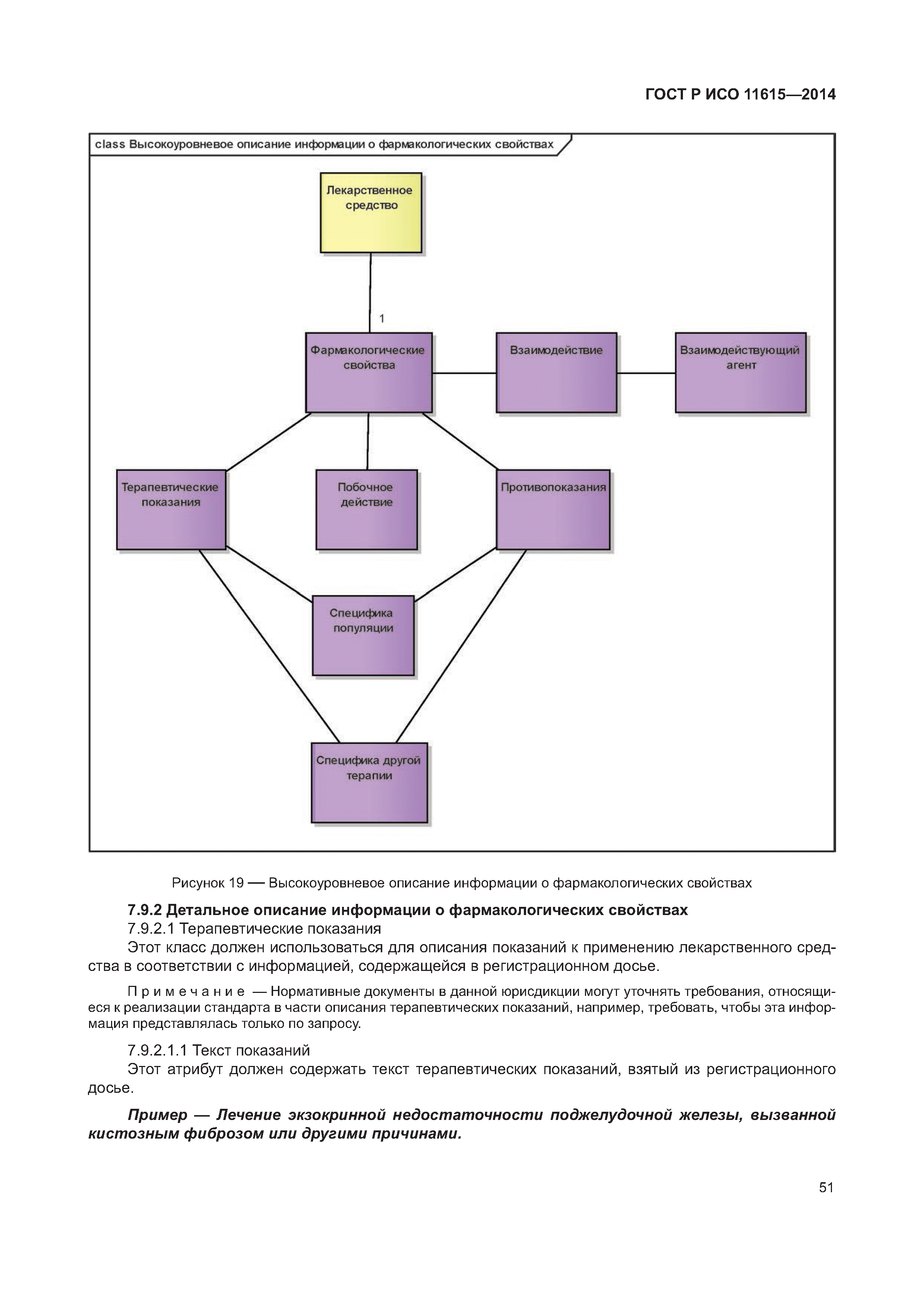
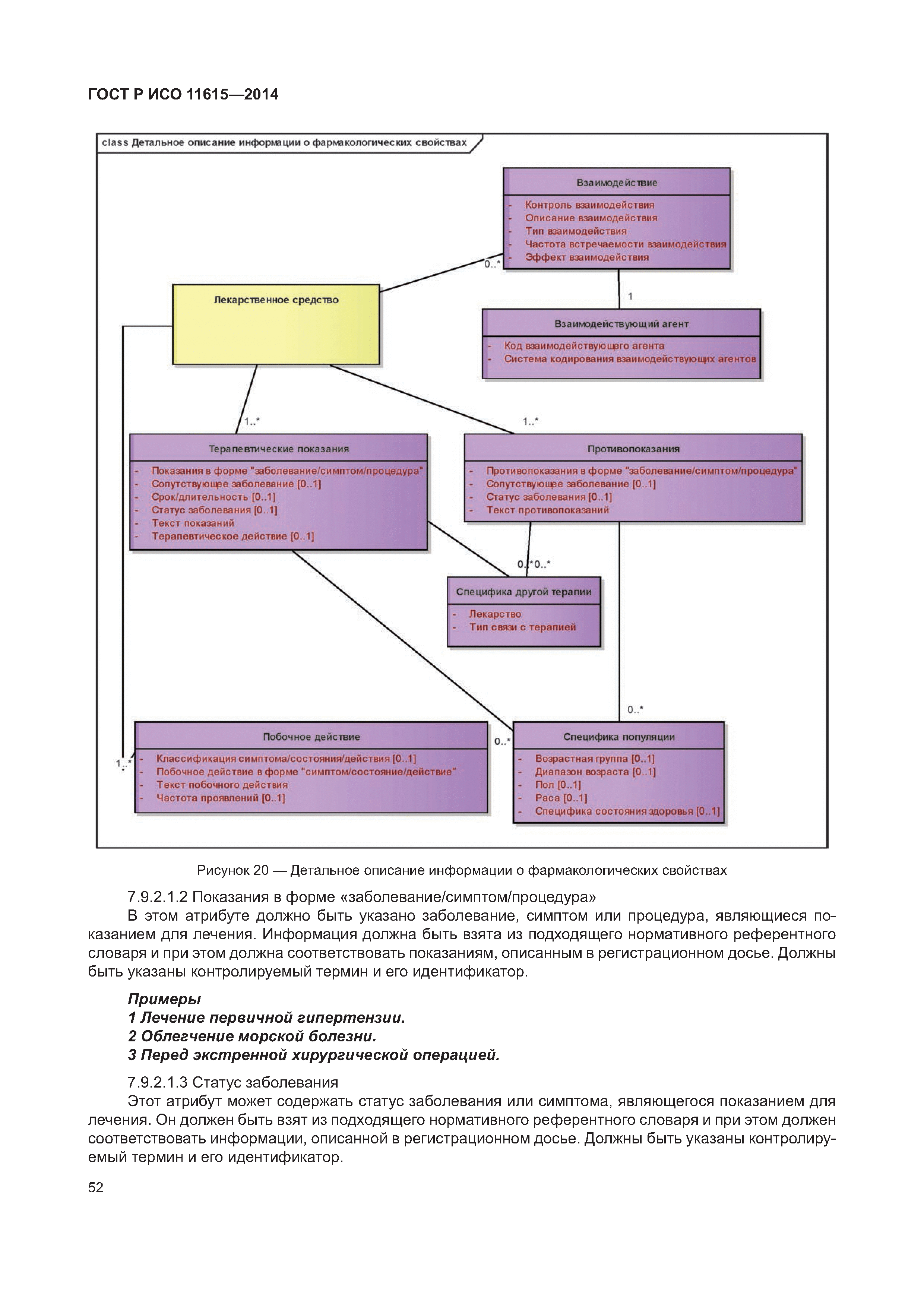
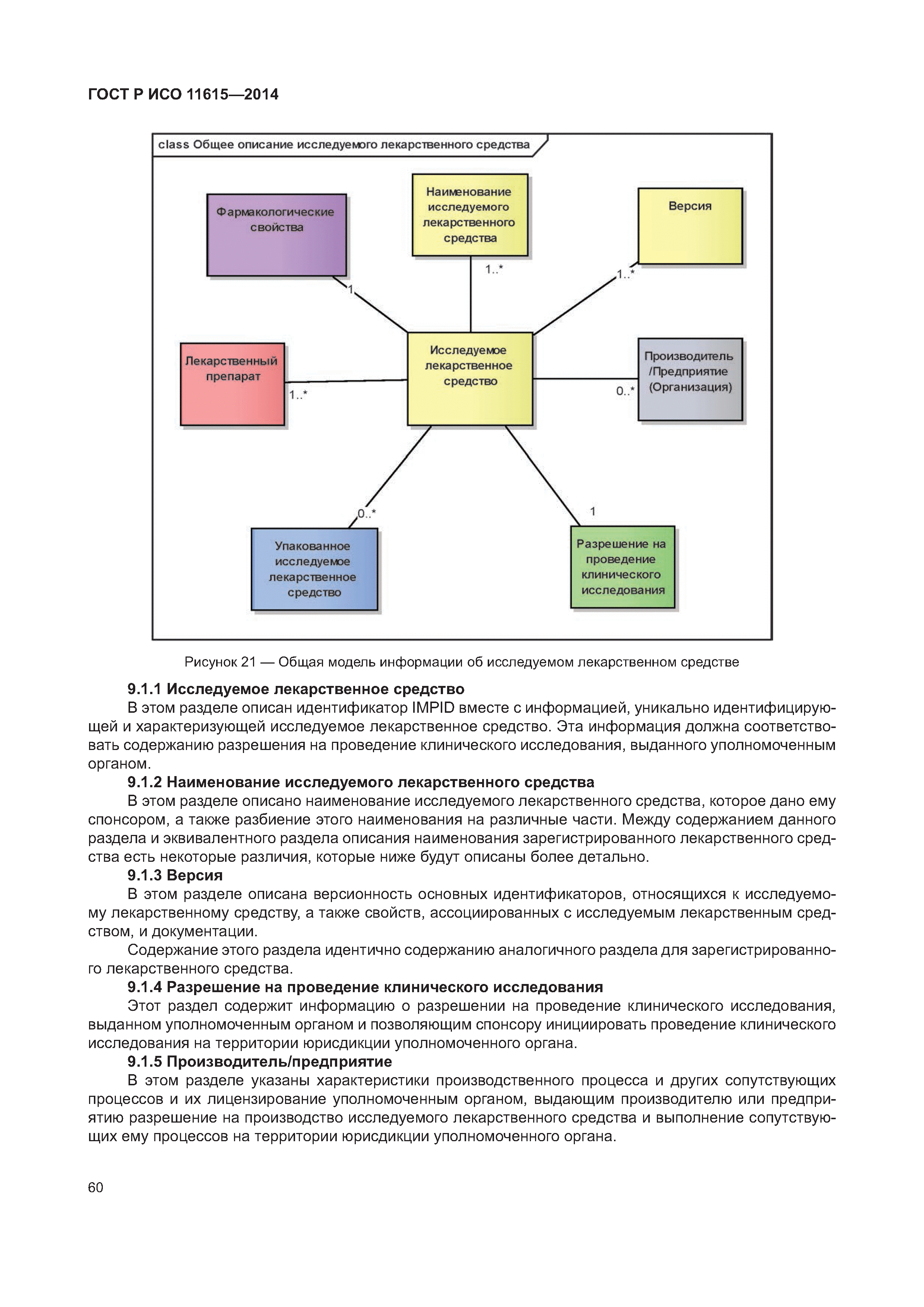
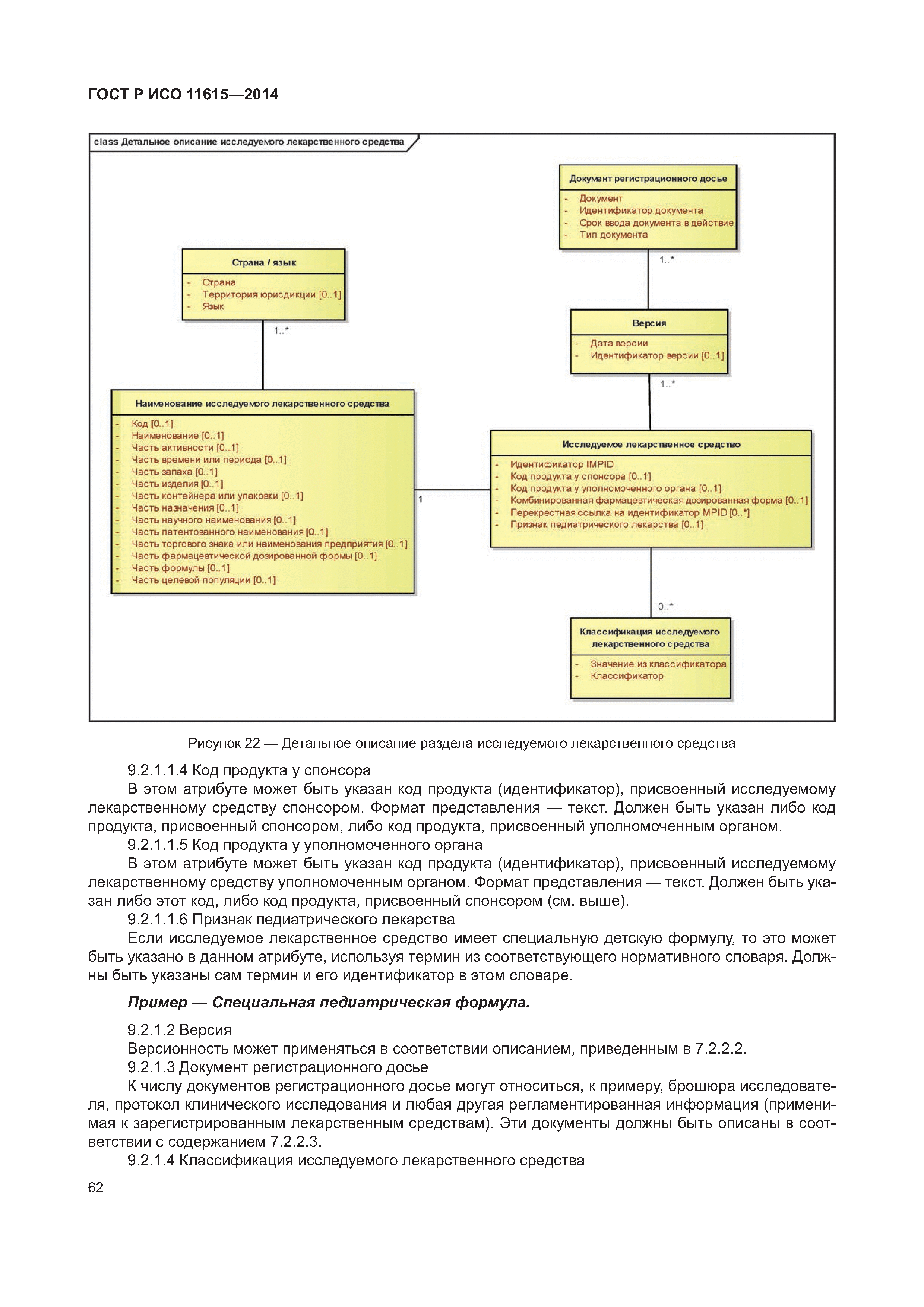
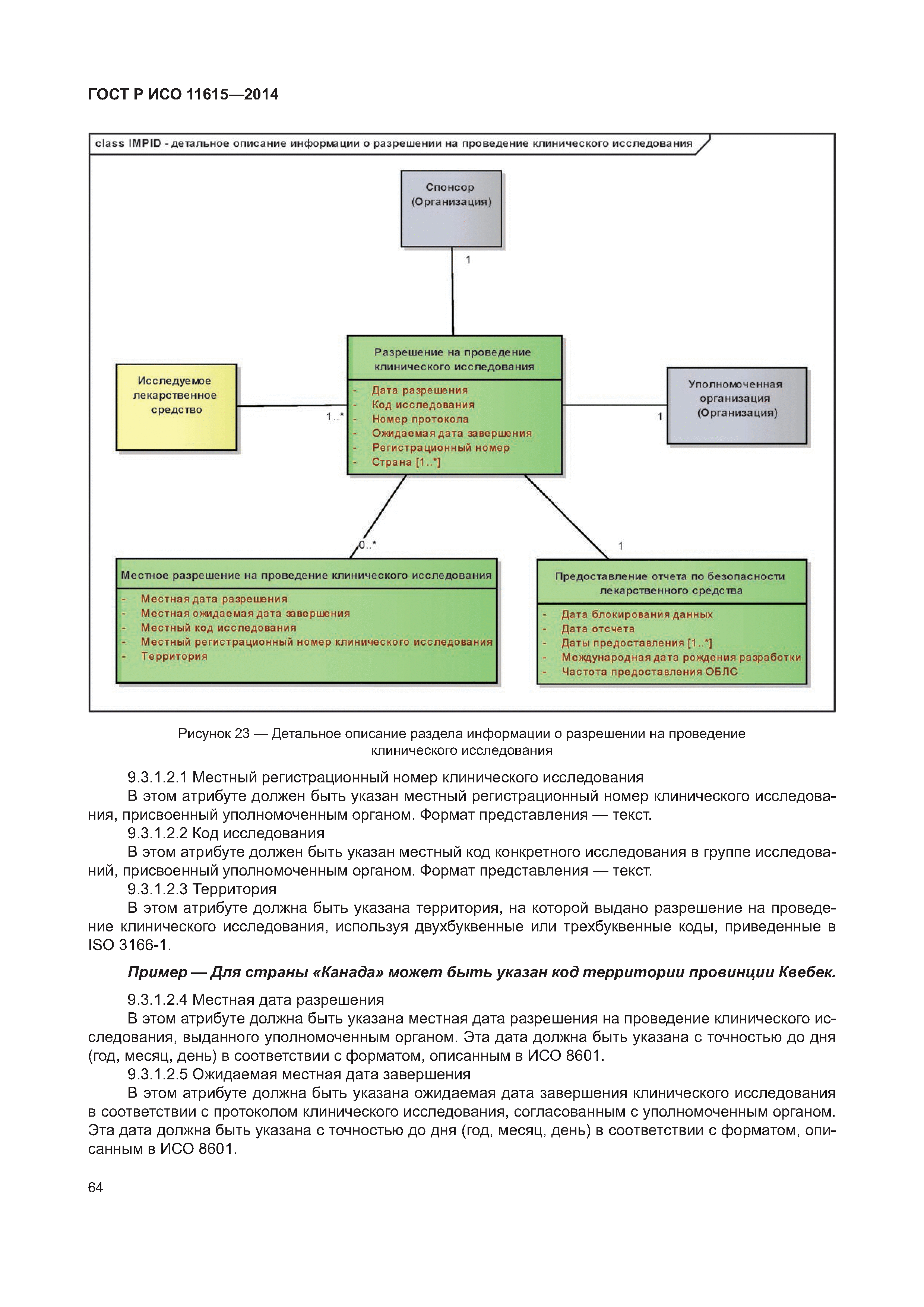
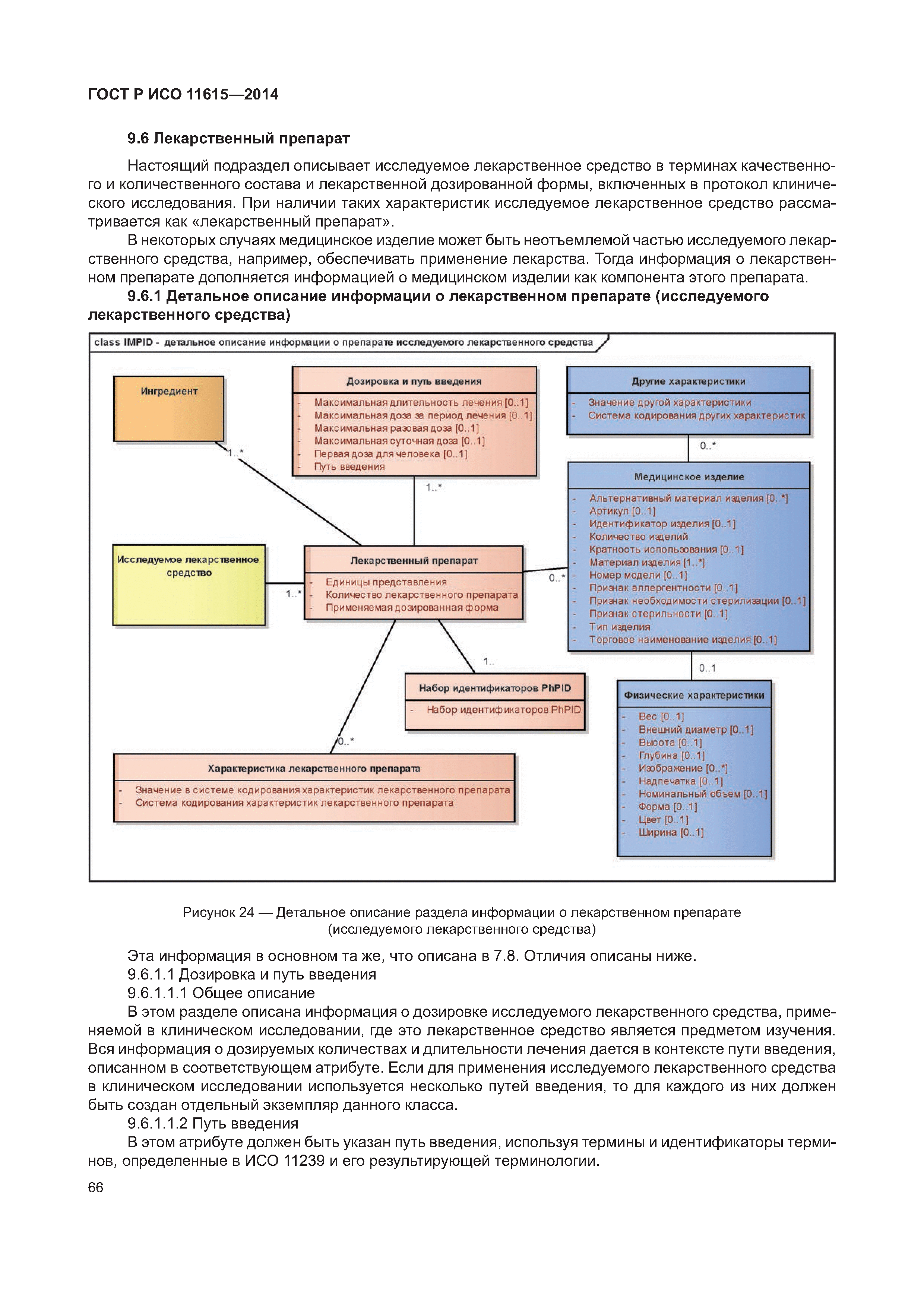
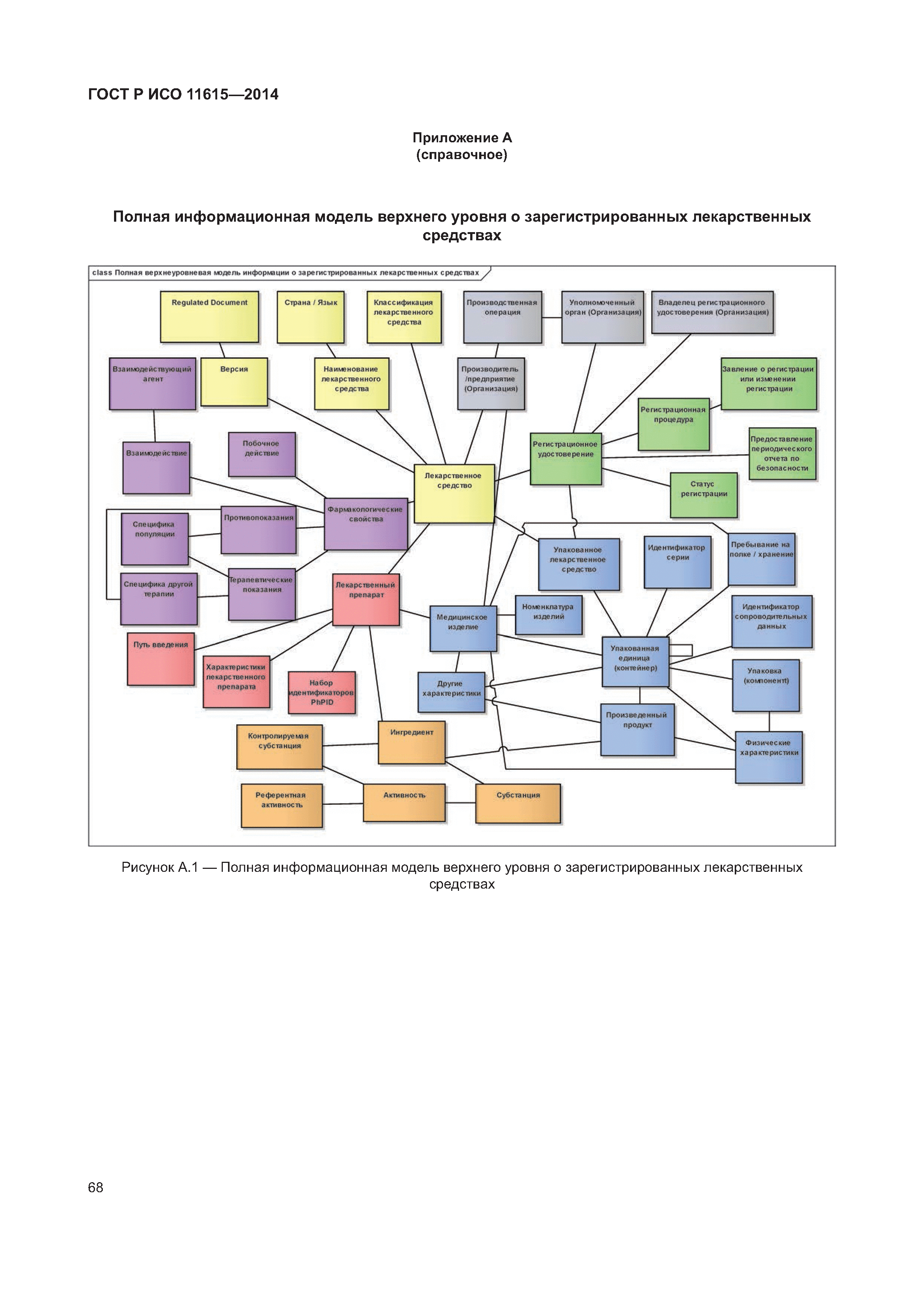
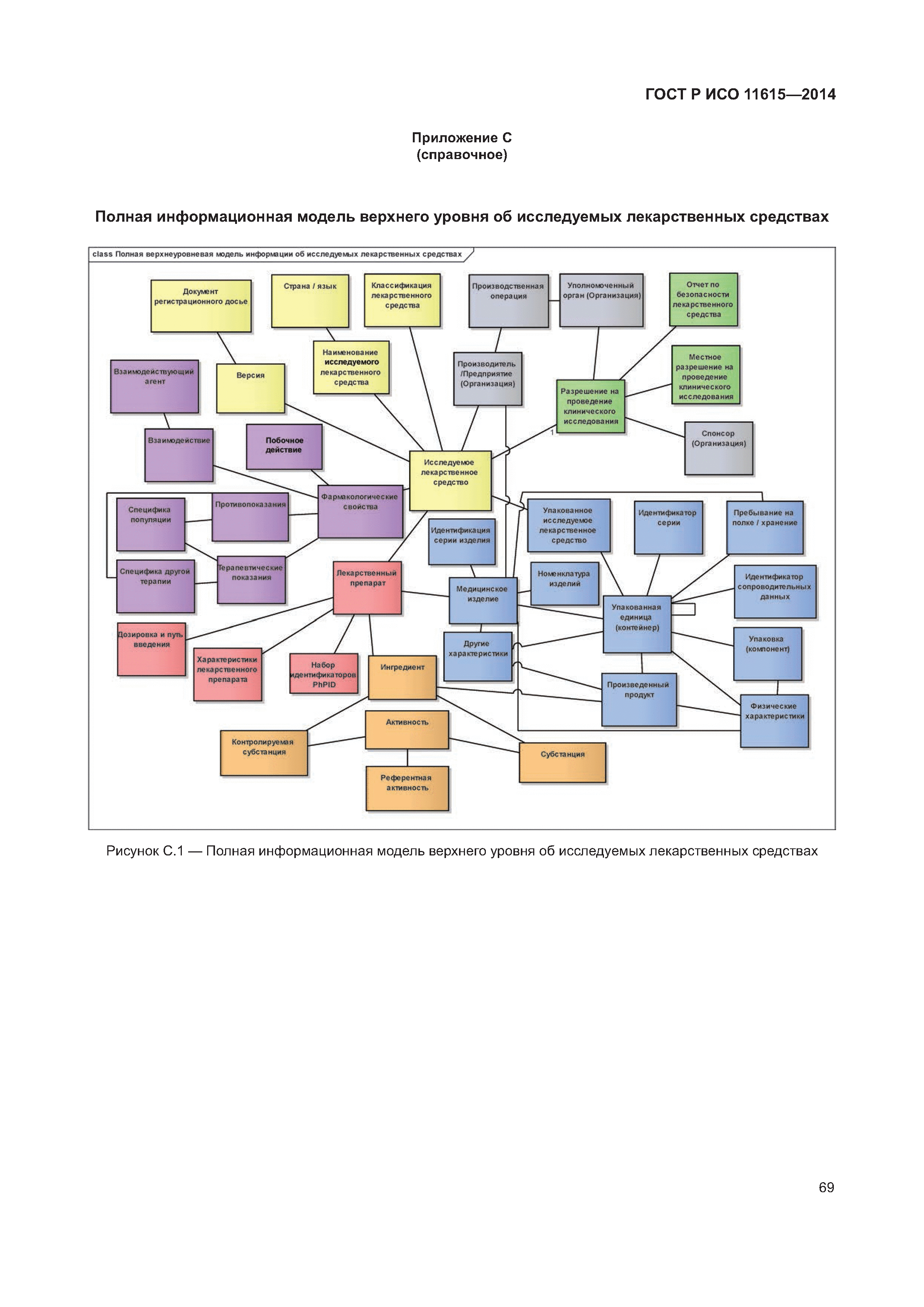
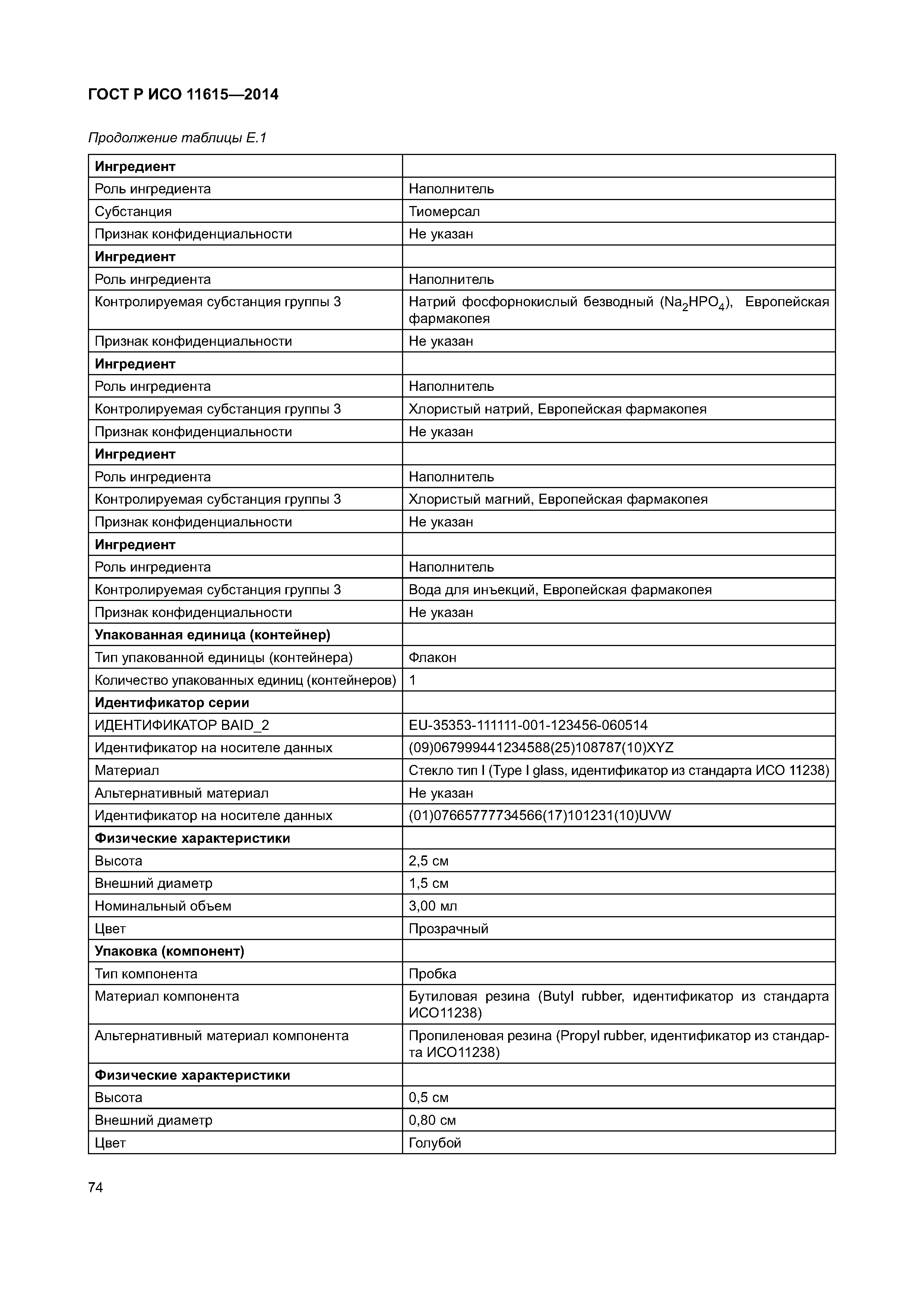
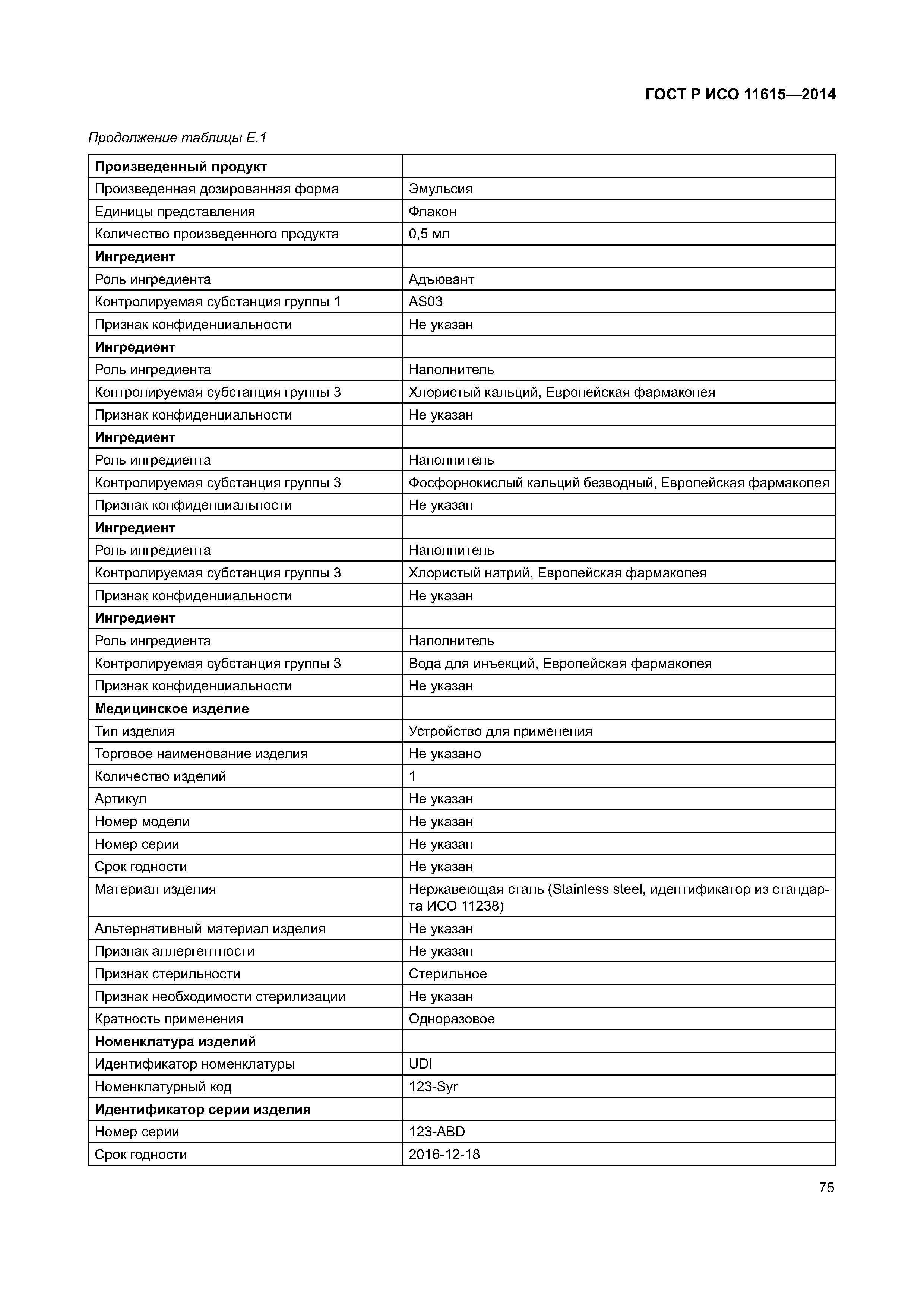
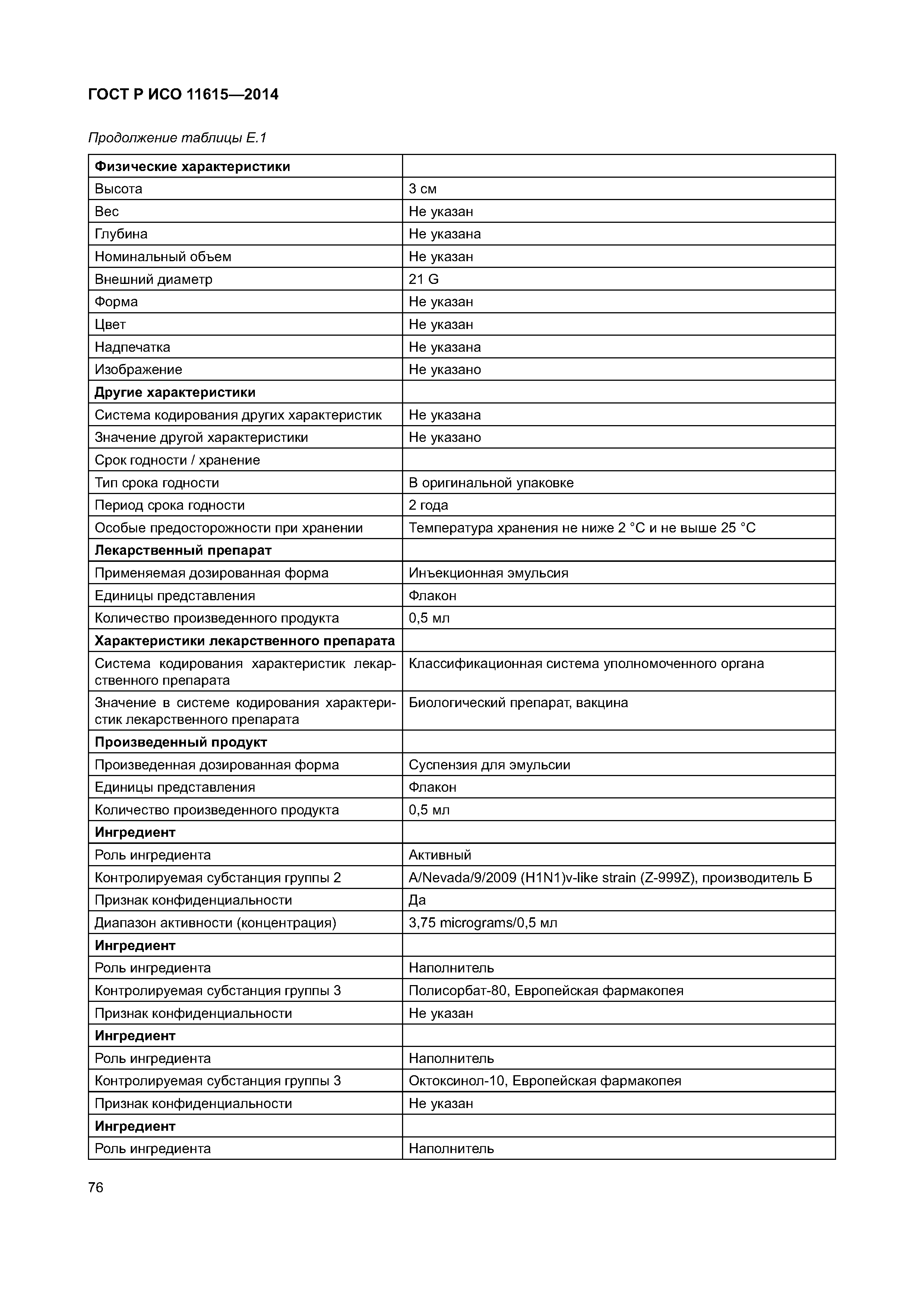
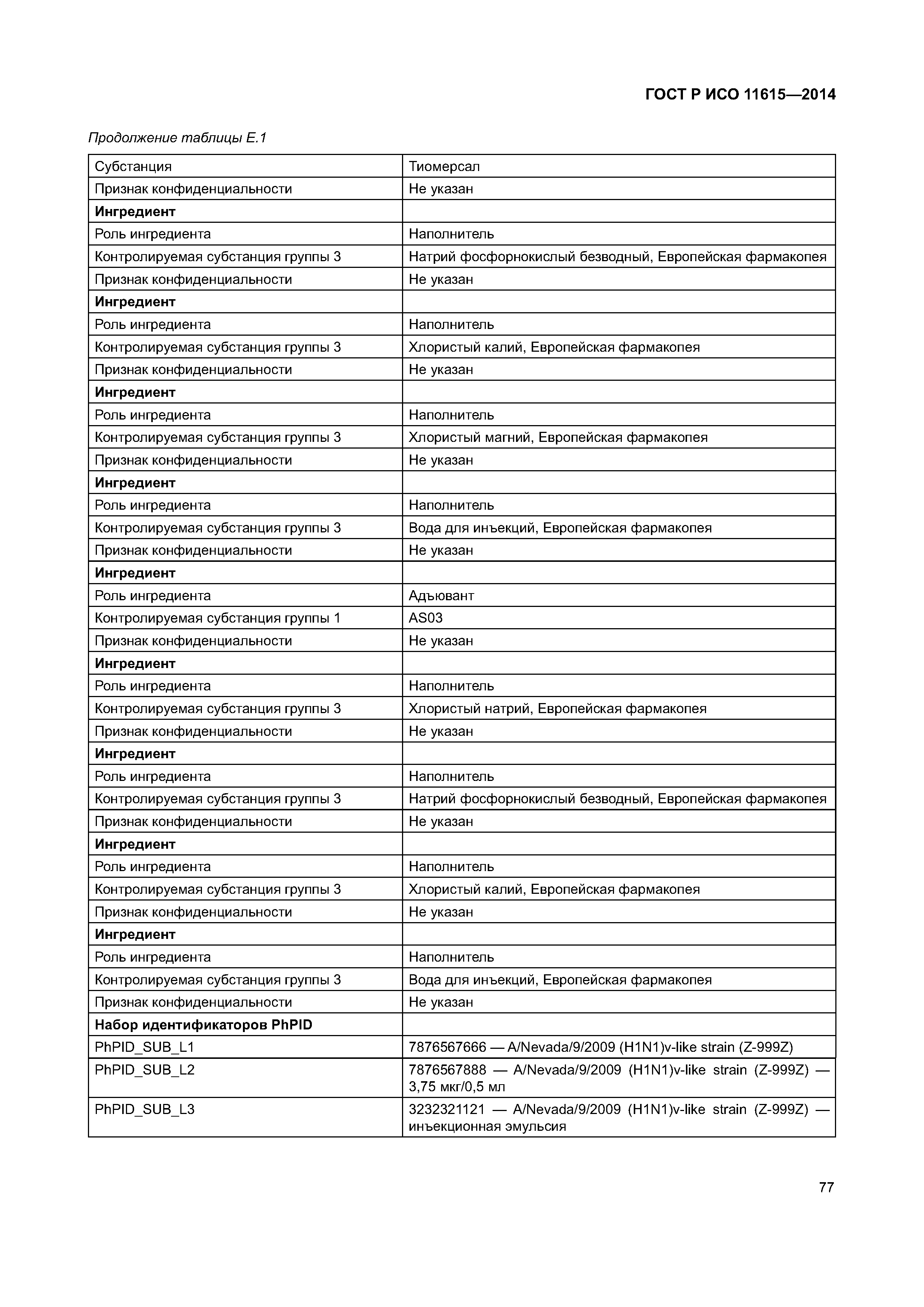
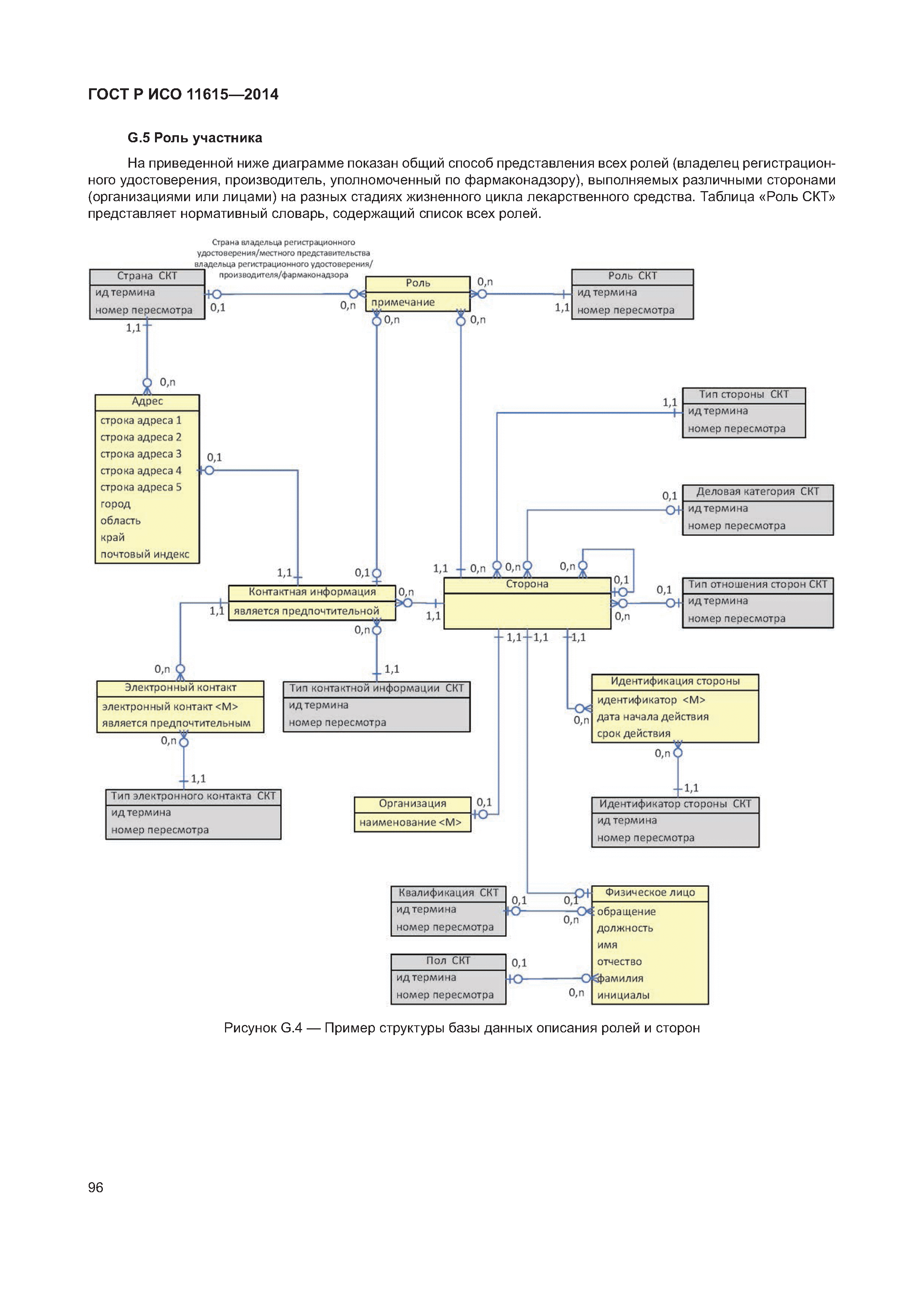
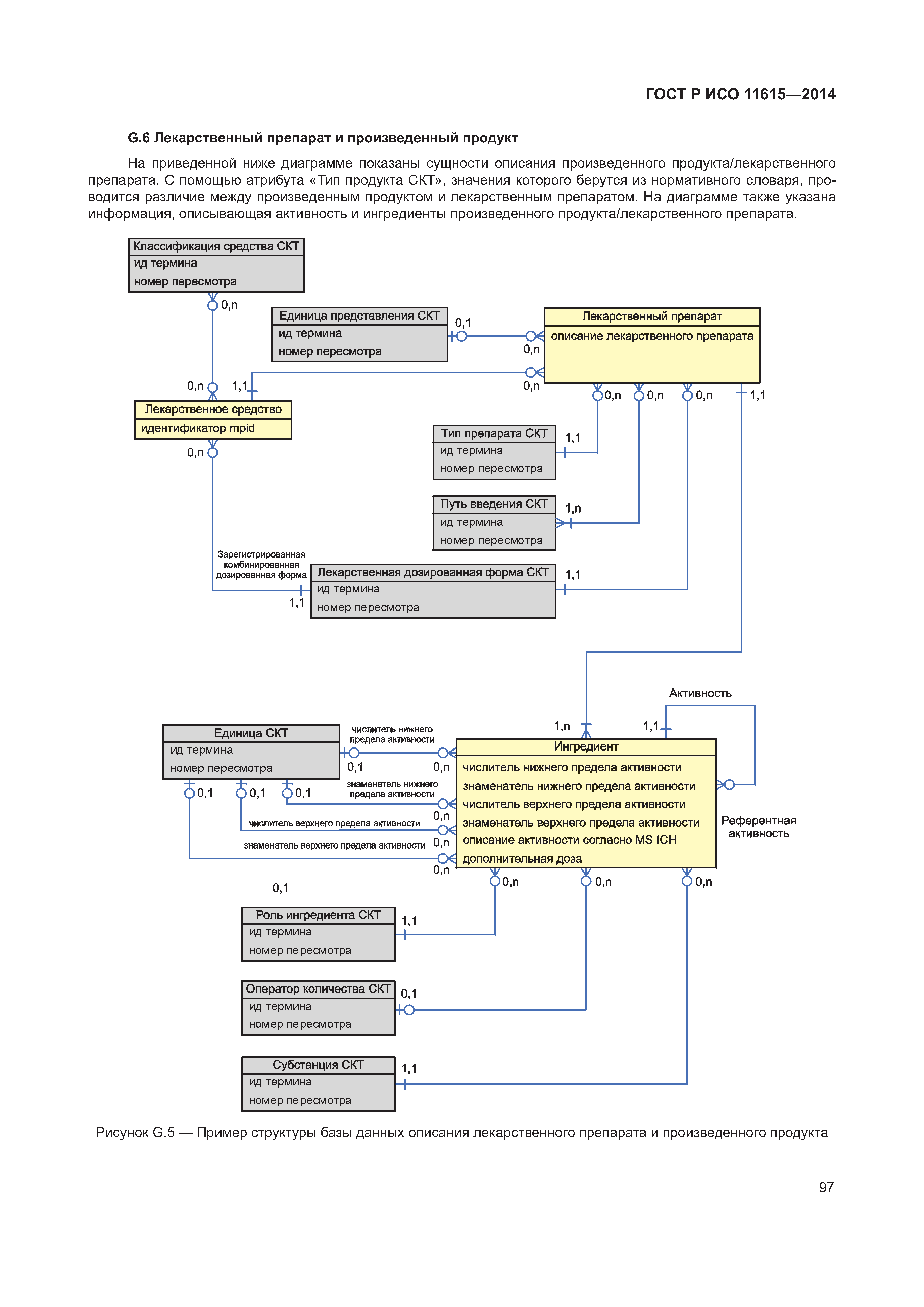
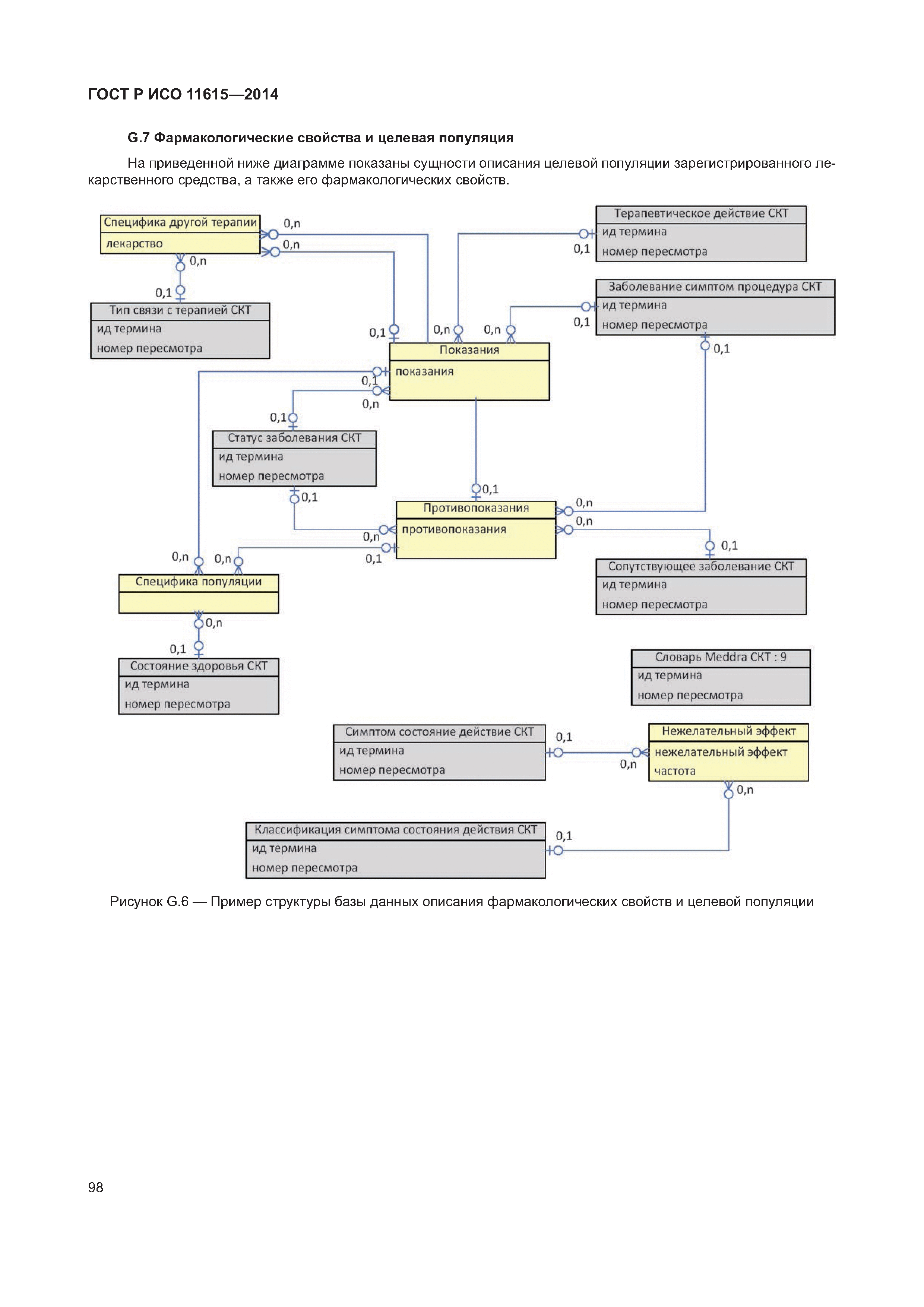
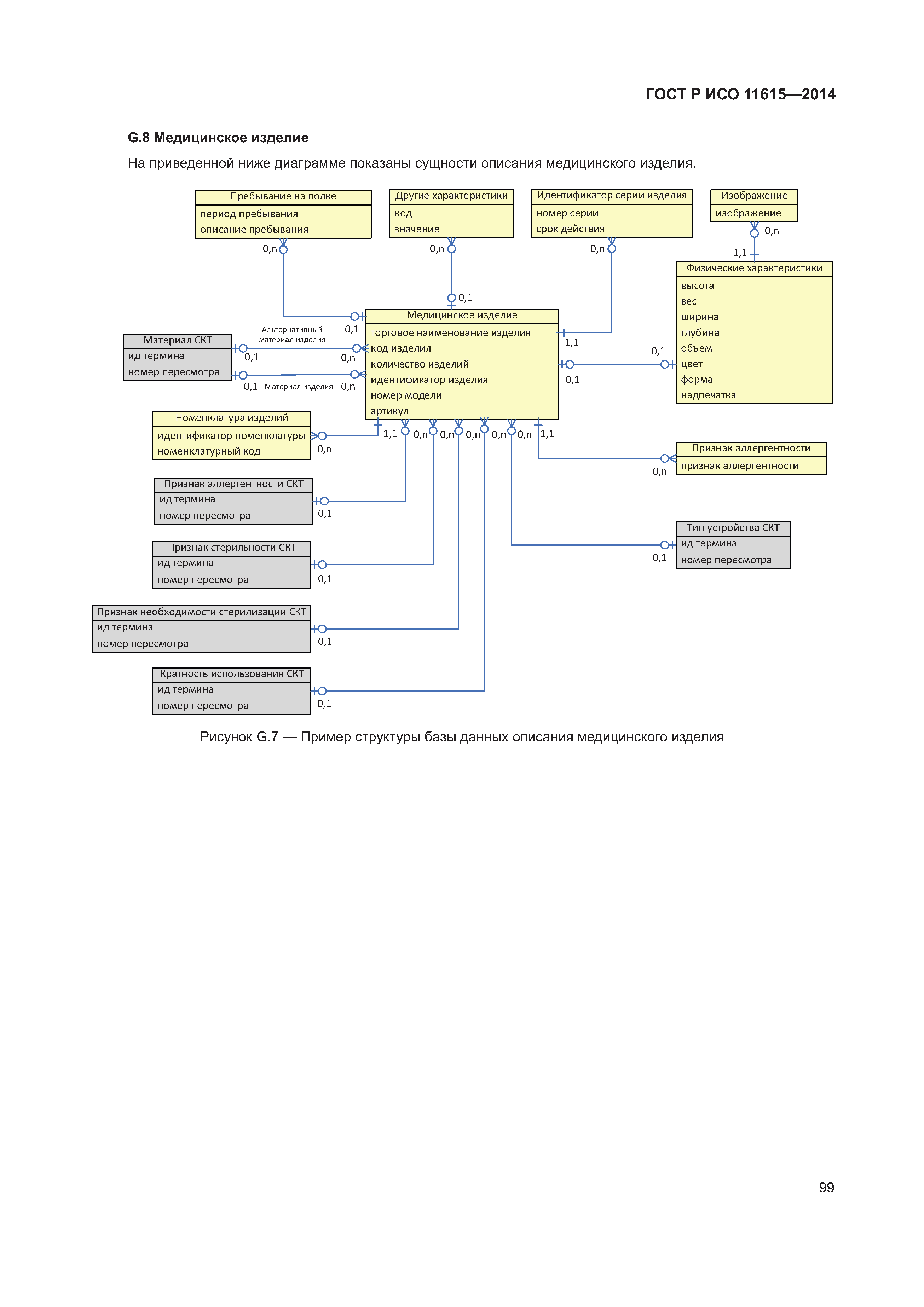
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины, определения и сокращения 3.1 Термины и определения 3.2 Сокращения 4 Требования 4.1 Понятия, необходимые для уникальной идентификации лекарственных средств 5 Описание принципов и методов информационного моделирования 5.1 Общие положения 5.2 Концептуальные обзорные диаграммы 5.3 Высокоуровневые диаграммы разделов 5.4 Детальные диаграммы 6 Идентифицирующие характеристики зарегистрированных лекарственных средств 6.1 Первичные идентификаторы 6.2 Идентификатор лекарственного средства (MPID) 6.3 Идентификатор упакованного лекарственного средства (PCID) 6.4 Идентификатор серии лекарственного средства (BAID_1) 6.5 Идентификатор серии лекарственного средства (BAID_2) 7 Информация о зарегистрированном лекарственном средстве 7.1 Обзор информации о зарегистрированном лекарственном средстве 7.2 Лекарственное средство 7.3 Регистрация лекарственного средства 7.4 Организация 7.5 Производитель/предприятие 7.6 Упакованное лекарственное средство, включая произведенный продукт и медицинское изделие 7.7 Ингредиент, субстанция и активность 7.8 Лекарственный препарат и медицинское изделие 7.9 Фармакологические свойства 8 Идентифицирующие характеристики исследуемых лекарственных средств 8.1 Общие положения 8.2 Первичные идентификаторы 8.3 Идентификатор исследуемого лекарственного средства (IMPID) 8.4 Идентификатор упакованного исследуемого лекарственного средства (IPCID) 8.5 Идентификатор серии исследуемого лекарственного средства (IBAID_1) 8.6 Идентификатор серии исследуемого лекарственного средства (IBAID_2) 9 Информация об исследуемом лекарственном средстве 9.1 Обзор информации об исследуемом лекарственном средстве 9.2 Исследуемое лекарственное средство 9.3 Разрешение на проведение клинического исследования 9.4 Производитель/предприятие 9.5 Упакованное исследуемое лекарственное средство 9.6 Лекарственный препарат 9.7 Ингредиент 9.8 Фармакологические свойства Приложение А (справочное) Полная информационная модель верхнего уровня о зарегистрированных лекарственных средствах Приложение В (справочное) Полная подробная информационная модель о зарегистрированных лекарственных средствах (см. вкладку) Приложение С (справочное) Полная информационная модель верхнего уровня об исследуемых лекарственных средствах Приложение D (справочное) Полная подробная информационная модель об исследуемых лекарственных средствах (см. вкладку) Приложение Е (справочное) Рабочий пример в табличной форме Приложение F (справочное) Списки классов и атрибутов Приложение G (справочное) Пример реализации информации о лекарственном средстве Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов и документов национальным стандартам Российской Федерации Библиография |
| Разработан: | ООО Корпоративные электронные системы ФБГУ ЦНИИОИЗ Минздрава |
| Утверждён: | 17.11.2014 Федеральное агентство по техническому регулированию и метрологии (1621-ст) |
| Издан: | Стандартинформ (2015 г. ) |
| Расположен в: |