Государственное санитарно-эпидемиологическое нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение концентраций действующих
веществ пестицидов в воде, почве, зеленой
массе, зерне и соломе зерновых культур,
семенах и масле рапса, зерне гороха,
семенах и масле льна
Сборник методических указаний
по методам контроля
МУК
4.1.3020-12; 4.1.3022-12;
4.1.3042-12; 4.1.3045-12
Москва 2013
1. Разработаны сотрудниками ГНУ «Всероссийский НИИ защиты растений» Россельхозакадемии, ФГУП «Всероссийский научно-исследовательский институт метрологии им. Д.И. Менделеева».
2. Введены в действие с момента утверждения.
3. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Руководитель Федеральной службы потребителей и благополучия человека, Главный государственный санитарный Г.Г. Онищенко 3 июля 2012 г. Дата введения: с момента утверждения |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение остаточных количеств
эсфенвалерата
в семенах и масле рапса
методом газожидкостной хроматографии
Методические
указания
МУК 4.1.3022-12
Свидетельство о метрологической аттестации от 24.02.2012 № 01.5.04.068/01.00043/2012.
Настоящие методические указания устанавливают метод газожидкостной хроматографии для определения в семенах рапса (горчицы) массовой концентрации эсфенвалерата в диапазоне концентраций 0,01 - 0,1 мг/кг, в масле - 0,02 - 0,2 мг/кг.
Название действующего вещества по ИСО: эсфенвалерат.
Название действующего вещества по ИЮПАК: (S)-α'-циано-3-феноксибензил-(S)-2-(4-хлорфенил)-3-метилбутират.
Структурная формула:
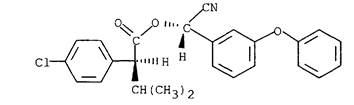
Эмпирическая формула: С25Н22ClNO3.
Молекулярная масса: 419,9.
Химически чистый препарат - бесцветное кристаллическое вещество (до 23 °С).
Температура плавления: 59,0 - 60,2 °С.
Давление паров при 25 °С - 2 ∙ 10-4 mPa.
Коэффициент распределения н-октанол/вода: Kow log P = 6,22 (25 °С).
Растворимость: в воде при 25 °С - 0,002 мг/л; в н-гексане - 10 - 50; метаноле - 70 - 100; в ксилоле, ацетоне, хлороформе, этилацетате, DMSO, DMFA - > 600 (в г/кг при 25 °С).
Вещество относительно стабильно на свету, стабильно к гидролизу при рН 5,7 и 9 (25 °С).
Краткая токсикологическая характеристика
Класс токсичности по ВОЗ - II, ЕПА - II.
Острая пероральная токсичность (LD50) для крыс 75 - 88 мг/кг.
Область применения
Инсектицид широкого спектра действия (группа пиретроидов), применяется на зерновых, масличных, плодовых и других культурах.
1. Погрешность измерений
Методика обеспечивает выполнение измерений с погрешностью, не превышающей ± 25 %, при доверительной вероятности 0,95.
Метрологическая характеристика метода представлена в табл. 1 и 2.
Таблица 1
Метрологические параметры
|
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr, % |
Показатель промежуточной прецизионности (относительное среднеквадратическое отклонение в условиях вариации факторов «время», «оператор» в одной лаборатории), σRл, % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), σR, % |
Показатель точности* (границы относительной погрешности при вероятности Р = 0,95), ± δ, % |
|
|
Семена от 0,01 до 0,1 вкл. |
7 |
9 |
12 |
25 |
|
Масло от 0,02 до 0,1 вкл. |
7 |
9 |
12 |
25 |
|
Масло от 0,1 до 0,2 вкл. |
8 |
9 |
11 |
22 |
|
* Соответствует расширенной неопределенности Uотн. при коэффициенте охвата k = 2 |
||||
Полнота извлечения вещества, стандартное отклонение, доверительный интервал среднего результата для полного диапазона концентраций (n = 20, Р = 0,95) приведены в табл. 2.
Таблица 2
Полнота определения эсфенвалерата в семенах и масле рапса (N = 5 для каждой концентрации)
|
Предел обнаружения, мг/кг |
Диапазон определяемых концентраций, мг/кг |
Среднее значение определения, % |
Стандартное отклонение, S, % |
Доверительный интервал среднего результата, ±, % |
|
|
Семена |
0,01 |
0,01 - 0,1 |
82,4 |
4,6 |
4,2 |
|
Масло |
0,02 |
0,02 - 0,2 |
77,4 |
4,9 |
4,5 |
2. Метод измерений
Методика основана на извлечении эсфенвалерата из семян и масла рапса (горчицы) водно-ацетоновым раствором или ацетонитрилом с последующей очисткой перераспределением между двумя несмешивающимися жидкостями и на колонке с флорисилом. Количественное определение проводят методом газожидкостной хроматографии с использованием электронозахватного детектора.
Нижний предел измерения эсфенвалерата в пробе семян 0,01 мг/кг, масла - 0,02 мг/кг, средняя полнота извлечения из семян 82,4 % и из масла 77,4 %.
3. Средства измерений, вспомогательные устройства, реактивы и материалы
3.1. Средства измерений
|
Газовый хроматограф Цвет-550 М или аналогичный с ДЭЗ (ДПР) |
|
|
Весы аналитические ВЛА-200 |
|
|
Цилиндры мерные на 100 см3 |
ГОСТ 1774-74Е |
|
Колбы мерные на 25, 50, 100 см3 |
|
|
Пипетки на 1, 2, 5,10 см3 |
Примечание. Допускается использование средств измерения иных производителей с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Аналитический стандарт эсфенвалерата 99,8 % |
|
|
Ацетон, чда |
|
|
Ацетонитрил, хч |
ТУ 6-09-3534-87 |
|
Азот газообразный в баллонах с редуктором |
ТУ 6-16-40-14-88 |
|
Бумажные фильтры «красная лента» |
ТУ 6.091678-86 |
|
Вода дистиллированная |
ГОСТ 6709-79 |
|
Гексан, хч |
ТУ 2631-003-05807999-98 |
|
Насадка для колонки: хроматон N-Super (0,125 - 0,160 мм) с 5 % SE-30 или ХЕ-60 (Чехия) |
|
|
Натрий сернокислый безводный, ч, свежепрокаленный |
|
|
Флорисил 150 - 250 µm (Merck, Германия), содержание воды ≤ 2,5 % |
|
|
Хлороформ, чда |
ТУ 2631-020-11291058-96 |
|
Этиловый эфир уксусной кислоты, чда |
|
|
Элюент для колоночной хроматографии № 1: гексан-этилацетат (50:50 по объему) |
|
|
Элюент для колоночной хроматографии № 2: гексан-этилацетат (20:80 по объему) |
Примечание. Допускается использование реактивов иных производителей с более высокой квалификацией, не требующих дополнительной очистки растворителей.
3.3. Вспомогательные устройства, материалы
|
Аналитическая стеклянная насадочная колонка длиной 1 м, внутренним диаметром 3 мм |
|
|
Мельница лабораторная зерновая ЛМЗ |
ТУ 1-01-0593-79 |
|
Установка ультразвуковая «Серьга» |
ТУ 3.836.008 |
|
Ротационный вакуумный испаритель Büchi R-200/205 (Швейцария) или аналогичный |
|
|
Микрошприц МШ-10, МШ-10М |
ТУ 2-833-106 |
|
Насос водоструйный |
МРТУ 42 861-64 |
|
Колбы плоскодонные на шлифах КШ500 29/32 ТС |
|
|
Колбы круглодонные на шлифах КШ50 29-32 ТС |
|
|
Воронки лабораторные В-75-110 |
|
|
Воронки делительные ВД-3-500 |
ГОСТ 8613-75 |
|
Стаканы химические |
|
|
Колонка стеклянная хроматографическая длиной 25 см, диаметром 10 мм |
Примечание. Допускается применение оборудования иных производителей с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При проведении работы необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими, легковоспламеняющимися веществами (ГОСТ 12.1.007-76).
При выполнении измерений с использованием газового хроматографа и работе с электроустановками соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019-2009 и инструкциями по эксплуатации приборов.
4.2. Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать ПДК (ОБУВ), установленных ГН 2.2.5.1313-03 и 2.2.5.2308-07. Организация обучения работников безопасности труда - по ГОСТ 12.0.004-90.
4.3. При работе с газами, находящимися в баллонах под давлением до 15 мПа (150 кгс/см2) необходимо соблюдать «Правила устройства и безопасной эксплуатации стационарных компрессорных установок, воздуховодов и газопроводов под давлением» ПБ 03-576-03. Запрещается открывать вентиль баллона, не установив на нем понижающий редуктор.
5. Отбор и хранение проб
Отбор проб семян и масла рапса (горчицы) - ГОСТ 10852-86 «Семена масличные. Правила приемки и методы отбора проб».
Для длительного хранения семена рапса (горчицы) подсушивают при комнатной температуре в отсутствие света. Сухие образцы могут храниться в течение года. Перед анализом пробы семян доводят до стандартной влажности и измельчают. Пробы масла рапса хранят в холодильнике при 0 - 4 °С в закрытой стеклянной таре не более 2 месяцев.
6. Подготовка к определению
6.1. Подготовка и очистка реактивов и растворителей
Перед началом работы рекомендуется проверить чистоту применяемых органических растворителей. Для этого 100 мл растворителя упаривают в ротационном вакуумном испарителе при температуре 40 °С до объема 1,0 см3 и хроматографируют. При обнаружении мешающих определению примесей очистку растворителей производят в соответствии с общепринятыми методиками.
6.2. Кондиционирование колонки
Перед началом анализа колонку, заполненную хроматоном N-Super (0,125 - 0,160 мм) с 5 % SE-30, не присоединяя к детектору, кондиционируют в токе инертного газа (азот) при температуре 250 °С в течение 8 - 10 ч.
6.3. Приготовление стандартного и градуировочных растворов
Берут точную навеску эсфенвалерата (50 мг), переносят в мерную колбу на 50 см3, растворяют навеску в ацетоне и доводят до метки (стандартный раствор с концентрацией 1,0 мг/см3). Градуировочные растворы с концентрациями 0,1; 0,2; 0,5; 1,0 и 2,0 мкг/см3 готовят методом последовательного разбавления по объему, используя для разбавления гексан. Стандартный раствор можно хранить в холодильнике при температуре 0 - 4 °С в течение 6 месяцев, градуировочные растворы - в течение недели.
Для внесения в образец при определении полноты извлечения используют градуировочные растворы.
6.4. Построение градуировочного графика
Для построения градуировочного графика (площадь пика - концентрация эсфенвалерата в растворе) в хроматограф вводят по 1 мм3 градуировочных растворов (не менее 3 параллельных измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых концентраций), измеряют высоты или площади пиков и строят график зависимости среднего значения высоты (площади) пика от концентрации эсфенвалерата в градуировочном растворе (мкг/см3).
Методом наименьших квадратов рассчитывают градуировочный коэффициент (К) в уравнении линейной регрессии:
С = KS, где
S - площадь пика градуировочного раствора.
Градуировку признают удовлетворительной, если значение коэффициента линейной корреляции оказывается не ниже 0,99.
Градуировочную характеристику необходимо проверять при замене реактивов, хроматографической колонки или элементов хроматографической системы, а также при отрицательном результате контроля градуировочного коэффициента.
Градуировочную зависимость признают стабильной при выполнении следующего условия:
![]() где
где
С - аттестованное значение массовой концентрации эсфенвалерата в градуировочном растворе;
Ск - результат контрольного измерения массовой концентрации эсфенвалерата в градуировочном растворе;
λконтр. - норматив контроля градуировочного коэффициента, % (λконтр. = 10 % при P = 0,95).
6.5. Подготовка колонки с флорисилом для очистки экстракта
В нижнюю часть стеклянной колонки длиной 25 см и внутренним диаметром 1 см помещают тампон из стекловаты и вносят суспензию 4,5 г флорисила в 20 см3 смеси гексан-этилацетат (1:1, по объему), дают растворителю стечь до верхнего края сорбента. Колонку промывают 25 см3 этой же смеси со скоростью 1 - 2 капли в секунду, после чего она готова к работе.
6.6. Проверка хроматографического поведения эсфенвалерата на колонке с флорисилом
В круглодонную колбу емкостью 10 см3 отбирают 0,5 см3 стандартного раствора эсфенвалерата с концентрацией 1 мкг/см3. Отдувают растворитель током теплого воздуха, остаток растворяют в 2 см3 элюента № 1 и вносят в колонку. Колбу обмывают еще 2 см3 элюента № 1 и также вносят в колонку. Затем промывают колонку 25 см3 гексана и элюируют эсфенвалерат 60 см3 элюента № 2 со скоростью 1 - 2 капли в секунду. Отбирают фракции по 10 см3 каждая, упаривают досуха, остаток растворяют в 2 см3 гексана и анализируют на содержание эсфенвалерата по п. 2.6.4. Фракции, содержащие эсфенвалерат, объединяют, упаривают досуха, остаток растворяют в 2 см3 гексана и анализируют по п. 2.6.4. Рассчитывают содержание эсфенвалерата в элюате, определяя полноту вымывания вещества из колонки и необходимый для этого объем элюента.
Примечание. Профиль вымывания эсфенвалерата может меняться при использовании новой партии сорбента.
6.7. Подготовка приборов и средств измерения
Установка и подготовка всех приборов и средств измерения проводится в соответствии с требованиями технической документации.
7. Проведение определения
7.1. Экстракция эсфенвалерата из семян рапса
Навеску измельченных на лабораторной мельнице семян массой 10 г помещают в коническую колбу на 250 см3, заливают 50 - 100 см3 смеси растворителей ацетон-вода (в соотношении 1:1) и экстрагируют эсфенвалерат в ультразвуковой ванне в течение 15 мин. Экстракт фильтруют через бумажный фильтр («красная лента»). Экстракцию повторяют дважды 30 см3 той же смеси. Объединенный фильтрат помещают в делительную воронку и переэкстрагируют эсфенвалерат гексаном трижды порциями по 30 см3. Объединенные гексановые экстракты фильтруют через слой безводного сернокислого натрия. Полученный раствор выпаривают на ротационном испарителе при температуре бани 50 °С до полного удаления гексана. Далее проводят очистку экстрактов по п. 7.3.
7.2. Экстракция эсфенвалерата из рапсового масла
Навеску масла 10 г растворяют в 60 см3 гексана и экстрагируют эсфенвалерат 50 см3 ацетонитрила в УЗ-ванне в течение 15 мин. Полученную смесь помещают в делительную воронку объемом 250 см3. После расслоения* нижний ацетонитрильный слой сливают, из верхнего гексанового слоя экстрагируют эсфенвалерат ацетонитрилом еще дважды порциями по 30 см3. К объединенному ацетонитрильному экстракту добавляют воду в соотношении ацетонитрил-вода (1:4) и переэкстрагируют эсфенвалерат хлороформом трижды порциями по 30 см3. Объединенные хлороформные экстракты сушат над безводным серно-кислым натрием и выпаривают досуха на ротационном испарителе при температуре 50 °С. Сухой остаток растворяют в 5 см3 ацетона и помещают в морозильную камеру с температурой -18 °С на 2 ч. Охлажденный ацетоновый раствор декантируют в круглодонную колбу на 10 см3 через фильтр «красная лента», после чего фильтр промывают 2 см3 ацетона. Полученный раствор упаривают на ротационном испарителе при температуре бани не выше 40 °С до полного удаления ацетона. Далее очистку проводят по п. 7.3.
______________
* В случае образования сравнительно стойких эмульсий можно добавить несколько мл насыщенного раствора хлористого натрия или этилового спирта.
7.3. Очистка экстрактов на колонке с флорисилом
Остаток в колбе, полученный при упаривании очищенных по пп. 7.1 и 7.2 экстрактов семян или масла, количественно переносят двумя порциями по 2 см3 смеси гексан-этилацетат (1:1, по объему) в кондиционированную хроматографическую колонку (п. 6.2). Промывают колонку 25 см3 гексана, элюат отбрасывают. Эсфенвалерат элюируют 60 см3 элюента № 2 (гексан-этилацетат = 2:8). Весь элюат собирают в грушевидную колбу емкостью 100 см3. Раствор выпаривают досуха на ротационном испарителе при температуре не выше 50 °С. Сухой остаток растворяют в 1 - 2 см3 гексана и 1 мм3 раствора вводят в хроматограф.
7.4. Условия хроматографирования
Газовый хроматограф «Цвет-550М» с ДПР (ДЭЗ).
Колонка стеклянная 1 м×3 мм, заполненная хроматоном N-Super (0,125 - 0,160 мм) с 5 % SE-30.
Температура колонки 240 °С, испарителя 250 °С, детектора 320 °С.
Скорость газа-носителя (азот) через колонку 46 см3/мин.
Шкала электрометра 8 ∙ 1010 (16 ∙ 1010).
Объем вводимой пробы 1 мкл.
Время удерживания эсфенвалерата 3 мин 20 с.
Линейный диапазон детектирования 0,1 - 2 нг.
7.5. Обработка результатов анализа
Количественное определение проводят методом абсолютной калибровки, содержание эсфенвалерата в образце семян или масла (X, мг/кг) вычисляют по формуле:
![]() где
где
Н1 - высота (площадь) пика эсфенвалерата в стандартном растворе, мм (мв ∙ с);
Н2 - высота (площадь) пика эсфенвалерата в анализируемой пробе, мм (мв ∙ с);
V - объём экстракта, подготовленного для хроматографирования, см3;
Р - навеска анализируемого образца, г;
С - концентрация эсфенвалерата в стандартном растворе, мкг/см3.
Содержание остаточных количеств эсфенвалерата в анализируемом образце вычисляют как среднее из 2 параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор эсфенвалерата 2 мкг/см3, разбавляют.
8. Проверка приемлемости результатов параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предел повторяемости:
X1, X2 - результаты параллельных определений, мг/кг;
r - значение предела повторяемости (r = 2,8σr).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
9. Оформление результатов
Результат анализа представляют в виде:
![]() (X ± Д) мг/кг при
вероятности Р = 0,95, где
(X ± Д) мг/кг при
вероятности Р = 0,95, где
![]() - среднее
арифметическое результатов определений, признанных приемлемыми, мг/кг;
- среднее
арифметическое результатов определений, признанных приемлемыми, мг/кг;
Δ - граница абсолютной погрешности, мг/кг:
![]() где
где
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае, если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
содержание вещества в пробе «менее нижней границы определения» (например: менее 0,01 мг/кг*, где «*» - 0,01 мг/кг - предел обнаружения в семенах рапса).
10. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1 - 6-2002 «Точность (правильность и прецизионность) методов и результатов измерений».
10.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
10.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Сд должна удовлетворять условию:
![]() где
где
![]()
![]() - характеристика
погрешности (абсолютная погрешность) результатов анализа, соответствующая
содержанию компонента в испытуемом образце (расчетному значению содержания
компонента в образце с добавкой соответственно), мг/кг, при этом:
- характеристика
погрешности (абсолютная погрешность) результатов анализа, соответствующая
содержанию компонента в испытуемом образце (расчетному значению содержания
компонента в образце с добавкой соответственно), мг/кг, при этом:
Δл = ±0,84Δ, где
Δ - граница абсолютной погрешности, мг/кг:
![]() где
где
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк рассчитывают по формуле:
Кк = Х' - Х - Сд, где
X', X, Сд - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п. 4) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
![]()
Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
10.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предел воспроизводимости (R):
![]() где (3)
где (3)
X1, Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций), %.
11. Требования к квалификации оператора
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы методом газожидкостной хроматографии, ознакомленный с руководством по эксплуатации хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п. 10.
12. Разработчики
Цибульская И.А., Копытова Ф.И., Долженко О.В. (ГНУ «Всероссийский научно-исследовательский институт защиты растений» Россельхозакадемии (ГНУ ВИЗР), Санкт-Петербург, Пушкин).