Государственное
санитарно-эпидемиологическое нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
ОПРЕДЕЛЕНИЕ
ОСТАТОЧНЫХ
КОЛИЧЕСТВ ПЕСТИЦИДОВ
В ПИЩЕВЫХ ПРОДУКТАХ,
СЕЛЬСКОХОЗЯЙСТВЕННОМ СЫРЬЕ
И ОБЪЕКТАХ ОКРУЖАЮЩЕЙ СРЕДЫ
Сборник методических указаний
МУК 4.1.1941 - 4.1.1954-05
Москва, 2009
1. Сборник подготовлен Федеральным научным центром гигиены им. Ф.Ф. Эрисмана (академик РАМН, проф. В.Н. Ракитский, проф. Т.В. Юдина); при участии специалистов Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Разработчики методов указаны в каждом из них.
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека.
3. Утверждены Главным государственным санитарным врачом Российской Федерации, Первым заместителем Министра здравоохранения Российской Федерации, академиком РАМН Г.Г. Онищенко.
4. Введены впервые.
УТВЕРЖДАЮ
Главный государственный санитарный врач
Российской Федерации,
Руководитель Федеральной службы
по надзору в сфере защиты прав потребителей и
благополучия человека
____________________ Г.Г. Онищенко
18 января 2005 г.
МУК 4.1.1942-05
Дата введения 18.04.05
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
ПО ОПРЕДЕЛЕНИЮ ОСТАТОЧНЫХ КОЛИЧЕСТВ ГАЛОКСИФОП-Р-
МЕТИЛА В РЕПКАХ ЛУКА
МЕТОДОМ КАПИЛЛЯРНОЙ
ГАЗОЖИДКОСТНОЙ ХРОМАТОГРАФИИ
1. Вводная часть.
1.1. Краткая характеристика препарата.
Фирма-изготовитель: Дау АгроСаенсес.
Торговое название: Зеллек-супер.
Действующее вещество: галоксифоп-Р-метил.
Название по номенклатуре ИЮПАК: (R)-2-[4-(3-хлоро-5-трифторометил-2-пиридилокси)фенокси]пропионовой кислоты метиловый эфир.
Структурная формула:
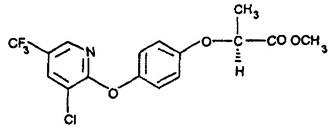
Эмпирическая формула: C16H13ClF3NO4.
Молекулярная масса: 375,7.
Химически чистый метиловый эфир галоксифоп-Р кислоты представляет собой светло-коричневую жидкость. В биологических средах легко гидролизуется до галоксифоп-Р кислоты.
Название галоксифоп-Р кислоты по номенклатуре ИЮПАК: (R)-2-[4-(3-хлоро-5-трифторометил-2-пиридилокси)фенокси]пропионовая кислота.
Структурная формула:
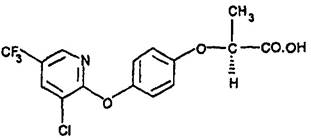
Эмпирическая формула: C15H11ClF3NO4.
Молекулярная масса: 361,7.
Химически чистое вещество: бесцветные кристаллы.
Температура плавления: 107 - 108 °С.
Растворимость (г/л) при 25 °С: в воде - 0,043, хорошо растворяется в большинстве органических растворителях.
1.2. Краткая токсикологическая характеристика галоксифоп-Р-метила.
LD50 для крыс - 393 - 599 мг/кг, для кроликов - > 5000 мг/кг. Не оказывает раздражающего действия на кожу, слабо раздражает глаза.
Гигиенические нормативы: ПДК в воде водоемов - 0,001 мг/л, ОДК в почве - 0,15 мг/кг, МДУ в свекле сахарной и кормовой, подсолнечнике и сое (семена), масле растительном - 0,05 мг/кг, в рапсе (семена) - 0,2 мг/кг, ВМДУ в картофеле - 0,01 мг/кг.
1.3. Область применения препарата.
Гербицид для борьбы с однолетними и многолетними злаковыми сорными растениями.
2. Метод определения галоксифоп-Р-метила в репках лука с применением капиллярной газожидкостной хроматографии.
2.1. Основные положения.
2.1.1. Принцип метода.
Метод основан на извлечении остаточных количеств галоксифоп-Р кислоты из анализируемого объекта органическими растворителями, проведении очистки экстракта перераспределением в системе несмешивающихся растворителей и метилированной галоксифоп-Р кислоты диазометаном.
Количественное определение проводят методом внешнего стандарта с применением капиллярной газожидкостной хроматографии и использованием детектора электронного захвата (ДЭЗ).
2.1.2. Избирательность метода.
Метод специфичен в присутствии других применяемых пестицидов. Проведение очистки экстрактов, а также использование капиллярной колонки и селективного детектора позволяет устранять влияние коэкстрактивных веществ на результаты анализа.
2.1.3. Метрологическая характеристика метода.
Диапазоны измеряемых концентраций, пределы обнаружения и другие метрологические параметры метода представлены в таблицах 1 и 2.
Таблица 1.
Метрологические параметры метода.
|
Анализируемые объекты: |
|
|
Репки лука |
|
|
Предел обнаружения, мг/кг |
0,01 |
|
Диапазон определяемых концентраций, мг/кг |
0,01 - 0,08 |
|
Среднее значение определения, % |
82,7 |
|
Стандартное отклонение, % |
5,2 |
|
Относительное стандартное отклонение, % |
2,8 |
Таблица 2.
Полнота определения галоксифоп-Р-метила в модельных пробах (n = 6).
|
Внесено, мг/кг |
Извлечено, % |
Доверительный интервал среднего результата, % |
|
|
Репки лука |
0,01 |
75,5 |
±6,8 |
|
0,02 |
80,3 |
±5,2 |
|
|
0,04 |
85,4 |
±4,5 |
|
|
0,08 |
89,7 |
±4,1 |
2.2. Реактивы, растворы, материалы.
Аналитический стандарт галоксифоп-Р кислоты.
Азот газообразный высокой чистоты, ТУ 301-07-25-89.
Ацетон, осч, ТУ 2633-004-11291058-94.
Вода дистиллированная и перегнанная над КМnО4 и щелочью.
н-Гексан, хч, ТУ 6-09-3375-78.
Дихлорметан, хч, ТУ 6-09-2662-77.
Изооктан эталонный, ГОСТ 12433-83.
Калия гидроокись, чда, ГОСТ 24363-80.
Натрий сернокислый б/в (сульфат), чда, ГОСТ 4166-76.
Натрий хлористый, чда, ГОСТ 4233-77.
N-Нитрозометилмочевина, хч, ТУ 6-09-11-1643-82.
Серная кислота, осч, ГОСТ 14262-78.
Смесь н-гексан : этиловый эфир, 70:30, по объему.
Фильтры бумажные, красная лента, ТУ 2642-001-42624157-98.
Фильтры бумажные, белая лента, ТУ 2642-001-42624157-98.
Фильтры бумажные, синяя лента, ТУ 2642-001-42624157-98.
Эфир этиловый (серный), ОСТ 84-2006-88.
2.3. Приборы, аппаратура, посуда.
Газовый хроматограф с ДЭЗ.
Колонка хроматографическая кварцевая капиллярная длиной 30 м, внутренним диаметром 0,32 мм с неподвижной фазой ВР-50 (OV-17, HP-17, DB-17), толщина слоя 0,5 мкм.
Аппарат для встряхивания, ТУ 64-1-1081-73 или аналогичный.
Весы аналитические типа ВЛА-200, ГОСТ 34104-80.
Весы лабораторные типа ВЛКТ-500, ГОСТ 24104-80.
Воронки делительные емкостью 500 мл, ГОСТ 25336-82.
Воронки химические конусные, ГОСТ 25336-82.
Индикаторная бумага универсальная, ТУ 6-09-1181-76.
Колбы-концентраторы емкостью 150 и 250 мл, ГОСТ 25336-82.
Колбы плоскодонные емкостью 250 мл, ГОСТ 25336-82.
Колбы мерные со шлифом емкостью 25, 50, 100 мл, ГОСТ 1770-74.
Колпачки алюминиевые для герметизации флаконов, ГОСТ Р 51314-99.
Микрошприц МШ-10, ТУ 2-833-106.
Насос водоструйный, ГОСТ 10696-75.
Ротационный вакуумный испаритель типа ИР-1 или аналогичный.
Пипетки мерные емкостью 1, 2, 5 и 10 мл, ГОСТ 20292-74.
Приспособление для обжима колпачков на флаконах, ТУ 42-2-2442-73.
Пробирки мерные со шлифом емкостью 5,0 мл, ГОСТ 1770-74.
Стаканы химические емкостью 500 мл, ГОСТ 25336-82.
Установка для перегонки растворителей при атмосферном давлении.
Установка для упаривания растворителей в токе азота.
Установка ультразвуковая «Серьга» УЗМ002 или аналогичная.
Флаконы стеклянные (типа пенициллиновых) емкостью 5,0 мл, ТУ 64-2-10-87.
Электроплитка, ГОСТ 14919-83.
2.4. Подготовка к определению.
2.4.1. Подготовка и очистка растворителей.
Перед началом работы рекомендуется проверить чистоту применяемых органических растворителей. Для этого 100 мл растворителя упаривают в ротационном вакуумном испарителе при температуре +40 °C до объема 1,0 мл и хроматографируют. При обнаружении мешающих определению примесей очистку растворителей производят в соответствии с общепринятыми методиками.
2.4.2. Приготовление стандартных растворов.
Основной раствор галоксифоп-Р кислоты с содержанием 100 мкг/мл готовят растворением в ацетоне 0,01 г аналитического стандарта в мерной колбе емкостью 100 мл. Раствор хранят в холодильнике при температуре +4 - 6 °С не более трех месяцев.
Рабочие стандартные растворы с концентрациями 1,6, 0,8, 0,4 и 0,2 мкг/мл готовят из основного стандартного раствора галоксифоп-Р кислоты последовательным разбавлением ацетоном. Рабочие растворы хранят в холодильнике при температуре +4 - 6 °С не более месяца.
Для приготовления калибровочных растворов в мерные пробирки со шлифом емкостью 5,0 мл вносят по 1,0 мл рабочих растворов галоксифоп-Р кислоты с концентрациями 0,2, 0,4, 0,8 и 1,6 мкг/мл. Растворитель в пробирках упаривают в токе азота досуха и проводят метилирование галоксифоп-Р кислоты по п. 2.4.3.
2.4.3. Метилирование галоксифоп-Р кислоты.
В пробирки с сухим остатком добавляют по 2,0 мл свежеприготовленного по п. 2.4.5 эфирного раствора диазометана. Пробирки закрывают пробками и ставят на 12 - 14 часов (на ночь) в холодильник с температурой +4 - 6 °С. После этого эфир в пробирках упаривают досуха в токе азота и сухой остаток растворяют в 1,0 мл изооктана.
2.4.4. Построение калибровочного графика.
Для построения калибровочного графика в инжектор хроматографа (п. 2.6.3) вводят по 1 мкл приготовленных по п. 2.4.3 растворов, содержащих галоксифоп-Р-метил в концентрациях 0,2, 0,4, 0,8 и 1,6 мкг/мл. Осуществляют не менее трех параллельных измерений и находят среднее значение высоты (площади) хроматографического пика для каждой концентрации. Строят калибровочный график зависимости высоты (площади) хроматографического пика в мм (мм2) от концентрации галоксифоп-Р-метила в рабочем растворе в мкг/мл.
N-Нитрозометилмочевину массой 0,5 г помещают во флакон емкостью 2,0 - 3,0 мл и герметизируют резиновой пробкой и колпачком с помощью приспособления для обжима колпачков на флаконах. Этиловый эфир количеством 4,0 мл вносят в другой флакон емкостью 5,0 мл, герметизируют резиновой пробкой и колпачком и охлаждают в морозильной камере холодильника в течение 30 минут.
После этого флаконы через предварительно проколотые пробки соединяют гибкой тефлоновой трубкой (внутр. диам. ~ 1,5 - 2,0 мм), одним концом погружая ее в этиловый эфир на всю глубину (флакон с охлажденным этиловым эфиром обязательно должен еще иметь свободный выход в атмосферу). Во флакон с нитрозометилмочевиной, используя шприц с тонкой иглой и прокалывая пробку, добавляют по каплям по стенке 50 % водный раствор гидроокиси калия (~ 0,5 мл) до прекращения реакции. Этиловый эфир при насыщении диазометаном окрашивается в ярко желтый цвет.
Внимание! Приготовление эфирного раствора диазометана и процедуру метилирования необходимо обязательно проводить в работающем вытяжном шкафу.
2.5. Отбор, первичная обработка и хранение проб.
Отбор проб для анализа проводят в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции, продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов», утвержденными заместителем Главного государственного санитарного врача СССР 21.08.1979 г., № 2051-79.
Репки лука после отбора проб моют, обсушивают фильтровальной бумагой, удаляют шелуху и из каждой репки по осевой линии вырезают 1/4 часть. Полученную среднюю пробу измельчают, перемешивают и выделяют аналитические пробы длительного хранения, аналитические пробы репок лука помещают в морозильную камеру с температурой -18 °С и хранят в закрытой стеклянной или полиэтиленовой таре.
2.6. Проведение определения.
2.6.1. Экстрагирование галоксифоп-Р кислоты.
Аналитическую пробу репок лука массой 20 ± 0,1 г помещают в плоскодонную колбу емкостью 250 мл, добавляют 150 мл ацетона, слегка встряхивают и подвергают обработке ультразвуком в УЗ-бане в течение 10 мин. После этого содержимое колбы фильтруют через бумажный фильтр красная лента в колбу-концентратор емкостью 250 мл. Содержимое колбы с пробой промывают 50 мл ацетона, который также фильтруют в колбу-концентратор.
При использовании аппарата для встряхивания в плоскодонную колбу с аналитической пробой вносят 150 мл ацетона и встряхивают в течение 60 минут. После этого содержимое колбы фильтруют через бумажный фильтр красная лента в колбу-концентратор емкостью 250 мл. Содержимое колбы с пробой промывают 50 мл ацетона, который также фильтруют в колбу-концентратор.
Колбу-концентратор с объединенным экстрактом подсоединяют к ротационному вакуумному испарителю и упаривают растворитель до объема 10 - 20 мл при температуре +40 °С. В колбу-концентратор добавляют 200 мл бидистиллированной воды, 2,0 мл 5,0 % водного раствора серной кислоты и содержимое колбы перемешивают встряхиванием. Колбу-концентратор помещают в холодильник и выдерживают при температуре +4 - 6 °С в течение 4 - 5 часов. После этого содержимое колбы фильтруют через бумажный фильтр белая лента в делительную воронку емкостью 500 мл. В воронку добавляют 10 % водный раствор гидроокиси калия до рН 9 - 10, 20 мл насыщенного водного раствора хлористого натрия и после перемешивания 75 мл дихлорметана. Содержимое воронки энергично встряхивают в течение 2-х минут. После 15-ти минутного отстаивания нижний дихлорметановый слой сливают и отбрасывают. Процедуру очистки экстракта с использованием 50 мл дихлорметана повторяют. Далее в воронку добавляют 30 мл насыщенного водного раствора хлористого натрия и после перемешивания 75 мл н-гексана. Содержимое воронки энергично встряхивают в течение 2-х минут. После 5-ти минутного отстаивания нижний ацетоно-водный слой сливают в химический стакан емкостью 500 мл, а верхний гексановый слой сливают и отбрасывают.
Водный раствор пробы, находящийся в химическом стакане, подкисляют концентрированной серной кислотой до рН 2,0 и переносят в чистую делительную воронку емкостью 500 мл. В воронку добавляют 100 мл смеси гексан : этиловый эфир (70:30) и встряхивают в течение 2-х минут. После полного разделения слоев нижний водный слой сливают и отбрасывают. В делительную воронку добавляют 200 мл бидистиллированной воды, 1,0 мл 5,0 % водного раствора серной кислоты и 10 мл насыщенного водного раствора хлористого натрия. Содержимое воронки встряхивают в течение 2-х минут. После полного разделения слоев нижний водный слой сливают и отбрасывают. Данную процедуру очистки экстракта повторяют еще один раз. После этого верхний гексано-эфирный слой фильтруют через фильтр синяя лента со слоем безводного сульфата натрия (толщина слоя ~ 1,0 - 1,5 см) в колбу-концентратор емкостью 150 мл.
Колбу-концентратор с объединенным гексано-эфирным экстрактом подсоединяют к ротационному вакуумному испарителю и упаривают растворители при температуре +40 °С до объема 3 - 5 мл. Остаток экстракта переносят в мерную пробирку со шлифом емкостью 5,0 мл и упаривают растворители в токе азота досуха при температуре +40 °С.
2.6.2. Метилирование галоксифоп-Р кислоты.
В пробирку с сухим остатком добавляют 2,0 мл свежеприготовленного по п. 2.4.5 эфирного раствора диазометана. Пробирку закрывают притертой пробкой и ставят на 12 - 14 часов (на ночь) в холодильник с температурой +4 - 6 °С. После этого эфир в пробирке упаривают досуха в токе азота и сухой остаток растворяют в 1,0 мл изооктана. Газохроматографический анализ на содержание галоксифоп-Р-метила проводят по п. 2.6.3.
2.6.3. Условия хроматографирования.
Газовый хроматограф с ДЭЗ.
Колонка хроматографическая капиллярная длиной 30 м, внутренним диаметром 0,32 мм с неподвижной фазой ВР-50 (OV-17, НР-17, DB-17), толщина слоя - 0,5 мкм.
Температура колонки: программирование от 100 °С (3 мин) до 280 °С (25 мин) со скоростью 8,0 °С/мин.
Температура испарителя: 240 °С.
Температура детектора: 300 °С.
Расход газов: газа-носителя (азот в/ч) - 1,5 см3/мин, дополнительного газа (азот в/ч) к ДЭЗ - 40 см3/мин.
Объем вводимой пробы: 1 мкл.
Время удерживания галоксифоп-Р-метила: 23,2 ± 0,05 мин.
Предел детектирования: 0,1 нг.
Линейный диапазон детектирования: 0,2 - 2,0 нг.
2.6.4. Обработка результатов анализа.
Содержание галоксифоп-Р-метила рассчитывают методом внешнего стандарта по формуле:
|
|
где
X - содержание галоксифоп-Р-метила в пробе, мг/кг,
Н - высота (площадь) пика анализируемого вещества, мм (мм2),
Q - концентрация стандартного раствора галоксифоп-Р-метила, мкг/мл,
V - количество экстракта, подготовленного для хроматографирования, мл,
Нот - высота (площадь) пика стандартного вещества, мм (мм2),
m - масса (г) аналитической пробы.
3. Требования техники безопасности.
Необходимо соблюдать общепринятые правила техники безопасности при работе с органическими растворителями, токсичными веществами, электронагревательными приборами и сжатыми газами, а также требования, изложенные в документации к приборам.
4. Контроль погрешности измерений.
Оперативный контроль погрешности и воспроизводимости результатов измерений осуществляется в соответствии с рекомендациями МИ 2335-95 «Внутренний контроль качества результатов количественного химического анализа».
5. Разработчики.
П.А. Тарарин, Т.А. Маханькова, Л.В. Григорьева (ВНИИ защиты растений).
СОДЕРЖАНИЕ