4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
ОПРЕДЕЛЕНИЕ ОСТАТОЧНЫХ КОЛИЧЕСТВ ПЕСТИЦИДОВ
В ПИЩЕВЫХ ПРОДУКТАХ, СЕЛЬСКОХОЗЯЙСТВЕННОМ
СЫРЬЕ И ОБЪЕКТАХ ОКРУЖАЮЩЕЙ СРЕДЫ
Определение остаточных
количеств квизалофоп-П-
тефурила
и его метаболитов в клубнях картофеля, ботве
и корнеплодах сахарной и столовой свеклы, моркови и
луке методом газожидкостной хроматографии
СБОРНИК МЕТОДИЧЕСКИХ УКАЗАНИЙ
МУК 4.1.1138-02
ВЫПУСК 1
МОСКВА
2004
1. Сборник подготовлен: Федеральным научным центром гигиены им. Ф.Ф. Эрисмана (чл.-корр. РАМН, проф. В.Н. Ракитский, проф. Т.В. Юдина); Московской сельскохозяйственной академией им. К.А. Тимирязева (проф. В.А. Калинин, к. хим. н. Довгилевич А.В.); Всероссийским НИИ фитопатологии (А.М. Макеев и др.); Всероссийским НИИ защиты растений (В.И. Долженко и др.); Санкт-Петербургским НИИ лесного хозяйства (Маслаков С.Е., Л.В. Григорьева и др.), при участии Департамента Госсанэпиднадзора Минздрава России (А.П. Веселов).
2. Методические указания рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию при Минздраве России.
3. Утверждены и введены в действие Главным государственным санитарным врачом Российской Федерации, Первым заместителем Министра здравоохранения Российской Федерации, академиком РАМН Г.Г. Онищенко.
4. Введены впервые.
Главный государственный санитарный
врач Российской Федерации, Первый
заместитель Министра здравоохранения
Российской Федерации
Г.Г. Онищенко
Дата введения: 1 января 2003 г.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств квизалофоп-П-
тефурила и его метаболитов в
клубнях картофеля, ботве
и корнеплодах сахарной и столовой свеклы, моркови и
луке методом газожидкостной хроматографии
Методические указания
МУК 4.1.1138-02
1. Вводная часть
Фирма производитель: Юнироял Кемикал Ко. Инк.
Торговое наименование препарата: ПАНТЕРА, КЭ.
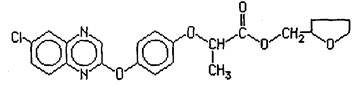
Действующее вещество (д. в.): квизалофоп-П-тефурил
Название д. в. по номенклатуре ИЮПАК: (R)-2-[4-(6-=хлорхиноксалин-2-илокси)фенокси]пропионовой кислоты тетрагидрофурфуриловый эфир.
C22H21N2ClO5 M. м. 428
Кристаллический порошок белого цвета без запаха.
Давление паров: < 5,9 × 10-8 мм Hg при 25 °С.
Растворимость (мг/л при 25 °С): в воде - 3,753, метаноле - 6439, толуоле - 65170, н-гексане - 1243.
Температура плавления: 72,5 - 74,5 °С.
Коэффициент распределения в системе октанол/вода: logp - 4,3222.
Основным продуктом гидролитического разложения (метаболитом) квизалофоп-П-тефурила является 2-[4-(6-хлорхиноксалин-2-илокси)фенокси]пропионовая кислота.
Токсикологическая характеристика: ДСД для массы тела человека 0,004 мг/кг.
Гигиенические нормативы
МДУ в сельскохозяйственной продукции: свекла, картофель 0,04 мг/кг; лук - 0,06 мг/кг.
ПАНТЕРА, КЭ - послевсходовый гербицид для борьбы с однолетними и многолетними злаковыми сорными растениями при возделывании овощных и технических культур.
2. Методика определения остаточных количеств квизалофоп-П-тефурила и его метаболитов в клубнях картофеля, ботве и корнеплодах сахарной и столовой свеклы, моркови и луке с применением газожидкостной хроматографии
2.1. Основные положения
2.1.1. Принцип метода
Метод основан на извлечении остаточных количеств квизалофоп-П-тефурила и его метаболитов из анализируемого объекта метанолом, последующем гидролизе квизалофоп-П-тефурила и метаболитов с дериватизацией (метанолиз) до конечного продукта 2-метокси-6-хлорхиноксалина, проведении очистки экстрактов на колонке с оксидом алюминия и концентрирования конечных реэкстрактов.
Количественное определение проводят методом внешнего стандарта с применением газожидкостной хроматографии с использованием термоионного детектора (ТИД) или детектора электронного захвата (ДЭЗ), набивной или капиллярной колонки с неподвижной фазой типа SE-30.
2.1.2. Избирательность метода
Прочие пестициды, применяемые в интенсивной технологии выращивания овощей, определению не мешают. Использование колоночной хроматографии для очистки экстрактов, а также селективных детекторов позволяет устранить влияние возможных мешающих анализу примесей.
2.1.3. Метрологическая характеристика метода
Полнота определения квизалофоп-П-тефурила в модельных пробах (п = 6)
|
Внесено, мг/кг |
Извлечено, % |
Доверительный интервал среднего результата, % |
|
|
Клубни картофеля |
0,025 |
78 |
± 8,7 |
|
0,05 |
80 |
± 8,1 |
|
|
0,1 |
85 |
± 6,2 |
|
|
0,5 |
91 |
± 4,9 |
|
|
Корнеплоды сахарной свеклы |
0,025 |
80 |
± 8,1 |
|
0,05 |
85 |
± 6,8 |
|
|
0,1 |
90 |
± 5,0 |
|
|
0,5 |
93 |
± 4,3 |
|
|
Корнеплоды столовой свеклы |
0,025 |
82 |
± 7,4 |
|
0,05 |
86 |
± 6,8 |
|
|
0,1 |
92 |
± 5,0 |
|
|
0,5 |
95 |
± 4,7 |
|
|
Ботва свеклы |
0,025 |
80 |
± 9,3 |
|
0,05 |
83 |
± 8,4 |
|
|
0,1 |
88 |
± 6,6 |
|
|
0,5 |
90 |
± 6,0 |
|
|
Морковь |
0,025 |
75 |
± 11,2 |
|
0,05 |
78 |
± 10,5 |
|
|
0,1 |
83 |
± 10,2 |
|
|
0,5 |
90 |
± 9,3 |
|
|
Репка лука |
0,05 |
60 |
± 19,2 |
|
0,1 |
65 |
± 14,8 |
|
|
0,5 |
72 |
± 12,1 |
2.2. Реактивы, растворы и материалы
|
Аналитический стандарт квизалофоп-П-тефурила |
|
|
Ацетон, ч |
|
|
Вода дистиллированная |
ГОСТ 7602-76 |
|
н-Гексан, хч |
ТУ 6-09-3375-78 |
|
Кислота соляная, осч. 23-4 |
ТУ 6-09-01-794-90 |
|
Метилен хлористый, хч |
ТУ 6-09-06-856-77 |
|
Натрия гидроокись, чда |
|
|
Натрий сернокислый, безводный, чда |
|
|
Натрий хлористый, чда |
|
|
Оксид алюминия для хроматографии, ч, размер частиц 100 - 200 мкм, 1-й степени активности по Брокману, нейтральный |
|
|
Оксид алюминия для хроматографии, ч, размер частиц 100 - 200 мкм, 4-й степени активности по Брокману, нейтральный |
|
|
Спирт метиловый, хч, (перегнанный) |
ТУ 6-09-1709-77 |
2.3. Приборы, аппаратура, посуда
|
Хроматографическая колонка кварцевая капиллярная длиной 10 м и внутренним диаметром 0,53 мм с неподвижной фазой типа SE-30 |
|
|
Хроматографическая колонка насадочная длиной 2,0 м и внутренним диаметром 4,0 мм с неподвижной фазой 3 % SE-30 на хроматоне N-AW, 0,125 - 0,160 мм |
|
|
Ротационный испаритель ИР-1М или аналогичного типа |
ТУ 25-11-917-76 |
|
Микрошприц МШ 10А |
ТУ 64-1-2850 |
|
Весы аналитические |
ТУ 64-1-1065 |
|
Пробирки мерные конические на 10 мл |
ГОСТ 1770-7420 |
|
Воронки делительные на 500 мл |
|
|
Воронки для фильтрования стеклянные |
ГОСТ 8613 |
|
Колбы мерные на 10, 50, 100 мл |
|
|
Концентраторы грушевидные (конические) НШ19, КГУ-100-14/19, ТС |
ГОСТ 10394 |
|
Пипетки мерные на 0,1; 1,0; 5,0 мл |
|
|
Стаканы стеклянные на 100 мл |
ГОСТ 6236 |
|
Фильтры бумажные «красная лента» |
ТУ 6-09-2670 |
|
Колбы круглодонные на 500 мл со шлифом |
|
|
Колбы плоскодонные на 500 мл |
|
|
Гомогенизатор |
МРТУ 42-15.05-63 |
|
Чашка фарфоровая |
2.4. Отбор проб
Отбор проб для анализа проводят в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов», утвержденными 21.08.79 № 2051-79.
2.5. Подготовка к определению
2.5.1. Подготовка и очистка растворителей
Перед началом работы рекомендуется проверить чистоту применяемых органических растворителей. Для этого 100 мл растворителя упаривают в ротационном испарителе при температуре 40 °С до объема 1,0 мл и хроматографируют. При обнаружении мешающих определению примесей очистку растворителей производят в соответствии с общепринятыми методиками.
2.5.2. Подготовка и кондиционирование колонки
Подготовленной насадкой (3 % SE-30 на хроматоне N-AW или другом носителе) заполняют стеклянную колонку и уплотняют ее под вакуумом. Колонку устанавливают в термостате хроматографа, не подсоединяя к детектору, и кондиционируют ее при рабочем расходе газа-носителя и температуре 260 °С в течение 8 - 10 ч.
2.5.3. Приготовление стандартных растворов
Основной раствор 2-метокси-6-хлорхиноксалина с концентрацией 100 мкг/мл готовят в мерной колбе растворением 0,01 г стандартного вещества в 100 мл н-гексана. Раствор хранят в холодильнике не более 3 месяцев. Рабочие стандартные растворы с концентрациями 2,0; 5,0; 10,0 и 25,0 мкг/мл готовят из основного стандартного раствора 2-метокси-6-хлорхиноксалина соответствующим последовательным разбавлением н-гексаном. Рабочие растворы хранят в холодильнике не более месяца.
При определении в модельных пробах полноты извлечения квизалофоп-П-тефурила используют соответствующие растворы вещества в ацетоне.
2.5.4. Построение калибровочного графика
Для построения калибровочного графика в инжектор хроматографа вводят по 1 - 3 мкл рабочего стандартного раствора 2-метокси-6-хлорхиноксалина с концентрацией 2,0; 5,0; 10,0 и 25,0 мкг/мл. Осуществляют не менее 5 параллельных измерений и находят среднее значение высоты (площади) хроматографического пика для каждой концентрации. Строят калибровочный график зависимости высоты (площади) хроматографического пика в мм (мм2) от концентрации 2-метокси-6-хлорхиноксалина в растворе в мкг/мл.
2.5.5. Подготовка хроматографических колонок с оксидом алюминия 1-й и 4-й степени активности по Брокману для очистки экстрактов
Оксид алюминия прогревают в фарфоровой чашке в термостате при 150 °С в течение 5 ч и охлаждают до комнатной температуры (1-я степень активности по Брокману). Для приготовления оксида алюминия 4-й степени активности по Брокману внутреннюю поверхность колбы со шлифом объемом 0,5 л увлажняют 11,1 мл дистиллированной воды и добавляют в колбу 100 г активированного оксида алюминия. Содержимое колбы тщательно перемешивают. Колбы с подготовленным оксидом алюминия хранят герметично закрытыми.
Стеклянную колонку размером 30,0×1,0 см заполняют (при легком встряхивании) 5,0 г оксида алюминия (высота слоя ~ 7,0 см). Над слоем оксида алюминия помещают слой безводного сульфата натрия высотой 2,0 см и содержимое колонки перед использованием промывают 30,0 мл н-гексана.
2.5.6. Подготовка проб к определению
Клубни картофеля, корнеплоды моркови и свеклы промывают водой для удаления остатков почвы и обсушивают фильтровальной бумагой. Из каждого неочищенного клубня, корнеплода или репки лука берут сегменты (1/4 часть) по осевой линии. Сегменты нарезают ножом, гомогенизируют и после тщательного перемешивания выделяют средний образец. Ботву свеклы нарезают ножом, гомогенизируют, перемешивают и выделяют средний образец.
2.6. Проведение определения
2.6.1. Обработка проб для газохроматографического анализа с использованием ДЭЗ
2.6.1.1. Проведение экстракции и метанолиза. Образец массой 10,0 ± 0,1 г помещают в круглодонную колбу со шлифом емкостью 250 мл, добавляют 25 мл метилового спирта и 5 мл 40 %-ного водного раствора гидроокиси натрия, слегка встряхивают и добавляют 25 мл (вторая порция) метилового спирта. Колбу помещают на водяную баню, присоединяют обратный холодильник и содержимое колбы кипятят в течение 90 мин. Затем обратный холодильник отсоединяют, колбу закрывают пробкой и охлаждают в струе проточной холодной воды. Сразу же после этого содержимое колбы фильтруют через складчатый бумажный фильтр «красная лента» в делительную воронку емкостью 500 мл. Внутренние стенки колбы и фильтр промывают 15 мл метилового спирта. Затем в воронку добавляют 50 мл дистиллированной воды, 10 мл насыщенного водного раствора хлористого натрия и с использованием концентрированной соляной кислоты (~ 3 мл) доводят содержимое воронки до рН 5 - 6. В воронку приливают 30 мл н-гексана и встряхивают в течение 3 мин. После 5-минутного отстаивания нижний водно-метанольный слой сливают в плоскодонную колбу емкостью 500 мл.
Гексановый экстракт, оставшийся в делительной воронке, пропускают через коническую воронку с ватным тампоном и слоем безводного сульфата натрия (толщина 1,0 - 1,5см) в грушевидную колбу-концентратор емкостью 100 мл. Экстрагирование с использованием 30 мл н-гексана повторяют еще раз. Воронку и сульфат натрия промывают 5 мл н-гексана. Объединенный гексановый экстракт упаривают на ротационном вакуумном испарителе при температуре 40 °С до объема 5,0 мл.
Водно-метанольный слой отбрасывают.
2.6.1.2. Проведение очистки экстрактов корнеплодов и ботвы свеклы, корнеплодов моркови и клубней картофеля на колонке с оксидом алюминия 4-й степени активности по Брокману. Остаток гексанового экстракта объемом 5 мл количественно переносят из колбы-концентратора в подготовленную колонку с оксидом алюминия. Элюирование 2-метокси-6-хлорхиноксалина осуществляют 20 мл н-гексана со скоростью ~ 60 кап./мин в грушевидную колбу-концентратор.
Элюат после очистки концентрируют на ротационном вакуумном испарителе при температуре 40 °С до объема 1,5 - 2,0 мл. Остаток количественно переносят в мерную коническую пробирку емкостью 10 мл и упаривают н-гексан в токе азота досуха. Сухой остаток в пробирке растворяют в 0,5 мл н-гексана и хроматографируют.
2.6.1.3. Проведение очистки экстрактов репок лука на колонке с оксидом алюминия 1-й степени активности по Брокману. При проведении анализа проб репок лука остаток гексанового экстракта репок лука объемом 5 мл количественно переносят в колонку с оксидом алюминия 1-й степени активности по Брокману.
Колонку с нанесенным экстрактом промывают 30 мл смеси н-гексан-метилен хлористый (98 : 2) и элюат отбрасывают. После этого проводят элюирование 2-метокси-6-хлорхиноксалина 15 мл смеси н-гексан-метилен хлористый (93 : 7) со скоростью ~ 60 кап./мин в грушевидную колбу-концентратор.
Элюат после очистки концентрируют на ротационном вакуумном испарителе при температуре 40 °С до объема 1,5 - 2,0 мл. Остаток количественно переносят в мерную коническую пробирку емкостью 10 мл и упаривают н-гексан в токе азота досуха. Сухой остаток в пробирке растворяют в 0,5 мл н-гексана и хроматографируют.
2.6.2. Обработка проб для газохроматографического анализа с использованием ТИД
Образец массой 10,0 ± 0,1 г помещают в круглодонную колбу со шлифом емкостью 250 мл, добавляют 25 мл метилового спирта и 5 мл 40 %-ного водного раствора гидроокиси натрия, слегка встряхивают и добавляют 25 мл (вторая порция) метилового спирта. Колбу помещают на водяную баню, присоединяют обратный холодильник и содержимое колбы кипятят в течение 90 мин. Затем обратный холодильник отсоединяют, колбу закрывают пробкой и охлаждают в струе проточной холодной воды. Сразу же после этого содержимое колбы фильтруют через складчатый бумажный фильтр «красная лента» в делительную воронку емкостью 500 мл. Внутренние стенки колбы и фильтр промывают 15 мл метилового спирта. Затем в воронку добавляют 50 мл дистиллированной воды, 10 мл насыщенного водного раствора хлористого натрия и с использованием концентрированной соляной кислоты (~ 3 мл) доводят содержимое воронки до рН 5 - 6. В воронку приливают 30 мл н-гексана и встряхивают в течение 3 мин. После 5-минутного отстаивания нижний водно-метанольный слой сливают в плоскодонную колбу емкостью 500 мл.
Гексановый экстракт, оставшийся в делительной воронке, пропускают через коническую воронку с ватным тампоном и слоем безводного сульфата натрия (толщина 1,0 - 1,5 см) в грушевидную колбу-концентратор емкостью 100 мл. Экстрагирование с использованием 30 мл н-гексана повторяют еще раз. Воронку и сульфат натрия промывают 5 мл н-гексана. Водно-метанольный слой отбрасывают.
Объединенный гексановый экстракт упаривают на ротационном вакуумном испарителе при температуре 40 °С до объема 5,0 мл. Остаток количественно переносят в мерную коническую пробирку емкостью 10 мл и упаривают н-гексан в токе азота досуха. Сухой остаток в пробирке растворяют в 0,5 мл н-гексана и хроматографируют.
2.7. Условия газохроматографического анализа
2.7.1. При использовании насадочной колонки
|
«Цвет-500» или другой с ДПР (ДЭЗ), ТИД |
|
|
Колонка |
насадочная с н. ф. типа SE-30 |
|
Длина, внутренний диаметр колонки |
2,0 м×4,0 мм |
|
Рабочая шкала электрометра |
2 × 10-10А |
|
Скорость протяжки ленты самописца |
0,5 см/мин |
|
Скорость потока гелия (азота) |
40 см3/мин |
|
Скорость потока воздуха (ТИД) |
350 см3/мин |
|
Скорость потока водорода (ТИД) |
35 см3/мин |
|
Режим хроматографирования |
изотермический |
|
Температура колонки |
150 °С |
|
Температура испарителя |
250 °С |
|
Температура детектора |
280 °С |
|
Объем вводимой пробы |
2,0 - 3,0 мкл |
|
Время удерживания 2-метокси-6-хлорхиноксалина |
5,6 ± 0,25 мин |
|
Линейный диапазон определения |
5,0 - 50 нг |
Примечание: после выполнения 5 - 7 анализов насадочную колонку следует прогреть при температуре 260 °С в течение 1 ч.
2.7.2. При использовании капиллярной колонки
|
«Цвет-500» или другой с ТИД |
|
|
1 |
2 |
|
Колонка |
кварцевая капиллярная с н. ф. SE-30 |
|
Толщина слоя неподвижной фазы |
2,65 мкм |
|
Длина, внутренний диаметр колонки |
10 м × 0,53 мм |
|
Рабочая шкала электрометра |
2 × 10-10А |
|
Скорость протяжки ленты самописца |
0,5 см/мин |
|
Скорость потока гелия (азота) |
7 см3/мин |
|
Скорость потока дополнительного газа - гелия (азота) к детектору |
30 см3/мин |
|
Скорость потока воздуха |
350 см3/мин |
|
Скорость потока водорода |
35 см3/мин |
|
Режим хроматографирования |
программирование температуры |
|
Температура колонки начальная |
80 °С |
|
Время хроматографирования при начальной температуре |
3 мин |
|
Температура колонки конечная |
280 °С |
|
Время хроматографирования при конечной температуре |
20 мин |
|
Скорость подъема температуры |
20 °С/мин |
|
Температура испарителя |
250 °С |
|
Температура детектора |
280 °С |
|
Объем вводимой пробы |
1,0 - 2,0 мкл |
|
Время удерживания 2-метокси-6-хлорхиноксалина |
9,0 ± 0,1 мин |
|
Линейный диапазон определения |
2,0 - 20 нг |
2.7.3. Расчет суммарного содержания квизалофоп-П-тефурила и его метаболитов
Расчет проводят по стандартному раствору 2-метокси-6-хлорхиноксалина, высота (площадь) пика которого наиболее близка высоте (площади) пика в рабочей пробе. Расчет суммарного содержания квизалофоп-П-тефурила и его метаболитов производят по следующей формуле:
![]() [мг/кг],
где
[мг/кг],
где
С - концентрация стандартного раствора 2-метокси-6-хлорхиноксалина, нг/мкл;
Н1 - высота (площадь) пика 2-метокси-6-хлорхиноксалина в анализируемой пробе, мм (мм2);
Нст - высота (площадь) пика 2-метокси-6-хлорхиноксалина в стандартном растворе, мм (мм2);
V1 - объем анализируемой пробы, введенной в хроматограф, мкл;
Vcm - объем пробы стандартного раствора, введенного в хроматограф, мкл;
V2 - общий объем анализируемой пробы, мкл;
Р - навеска исследуемого образца пробы, г;
К - коэффициент пересчета, равный 2,75, учитывающий соотношение молекулярных масс квизалофоп-П-тефурила и 2-метокси-6-хлорхиноксалина, а также степень извлечения анализируемых компонентов из матрицы.
Для получения достоверных результатов измерений конечный результат записывается следующим образом:
![]()
![]() ,
где
,
где
X - содержание остаточных количеств квизалофоп-П-тефурила и его метаболитов в анализируемой пробе в пересчете на действующее вещество;
х - среднее из трех параллельных результатов измерений;
Δ - показатель погрешности измерений, соответствующий диапазону, в который попадает величина х.
3. Требования техники безопасности
Необходимо соблюдать общепринятые правила техники безопасности при работе с органическими растворителями, токсичными веществами, электронагревательными приборами и сжатыми газами, а также требования, изложенные в документации на приборы.
4. Разработчики
Долженко В.И., Крылов А.И., Григорьева Л.В., Тарарин П.А., Николаев М.Я. (ВНИИ защиты растений, 189620, Санкт-Петербург - Пушкин, шоссе Подбельского, 3).
СОДЕРЖАНИЕ
|
2.2. Реактивы, растворы и материалы.. 3 2.3. Приборы, аппаратура, посуда. 3 2.5. Подготовка к определению.. 4 2.6. Проведение определения. 5 2.7. Условия газохроматографического анализа. 6 |