Унифицированная методика контроля токсичности серийно выпускаемых полимерных изделий медицинского назначения однократного применения
| Статус: | действует |
| Название рус.: | Унифицированная методика контроля токсичности серийно выпускаемых полимерных изделий медицинского назначения однократного применения |
| Дата добавления в базу: | 01.01.2018 |
| Дата актуализации: | 01.01.2021 |
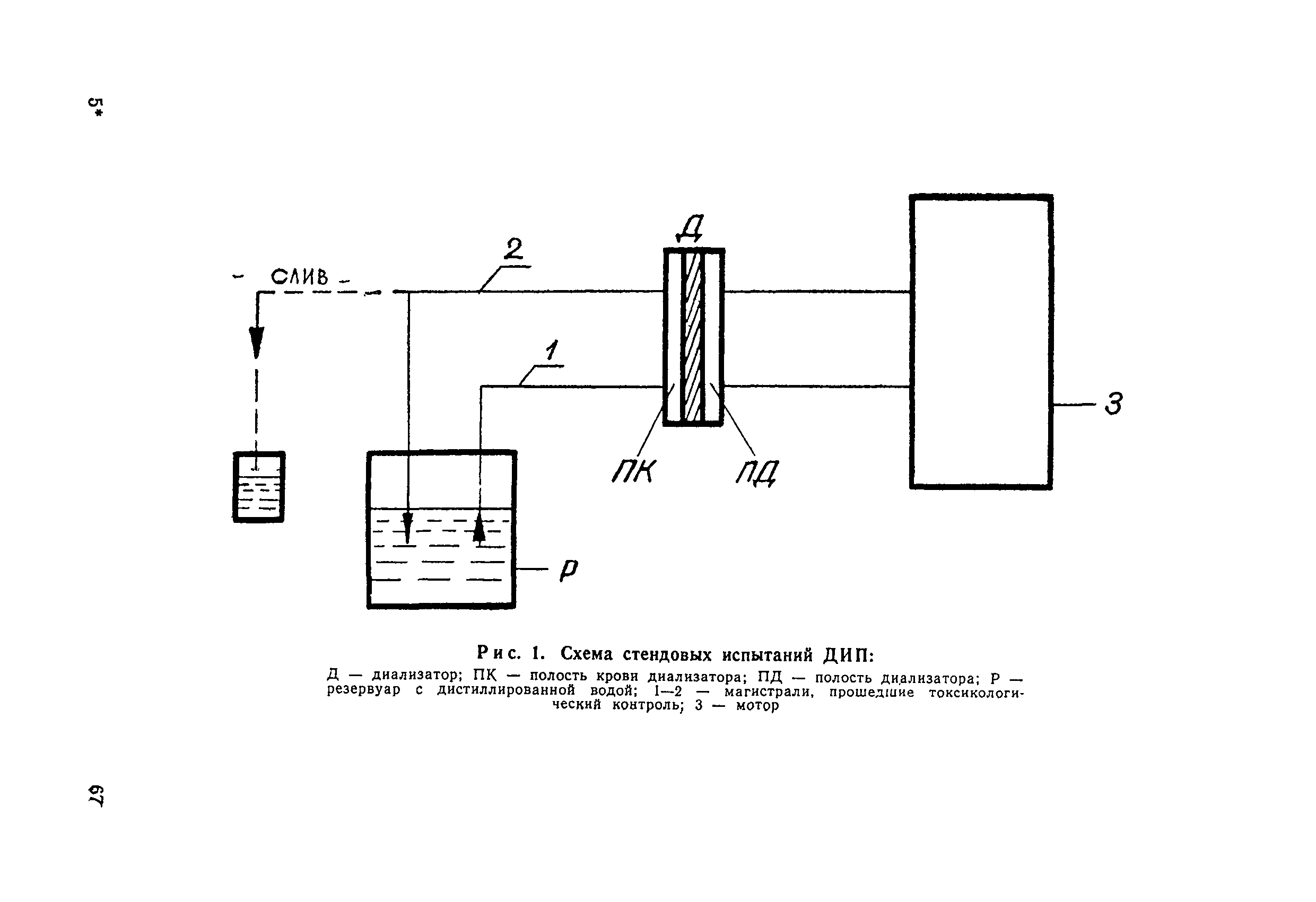
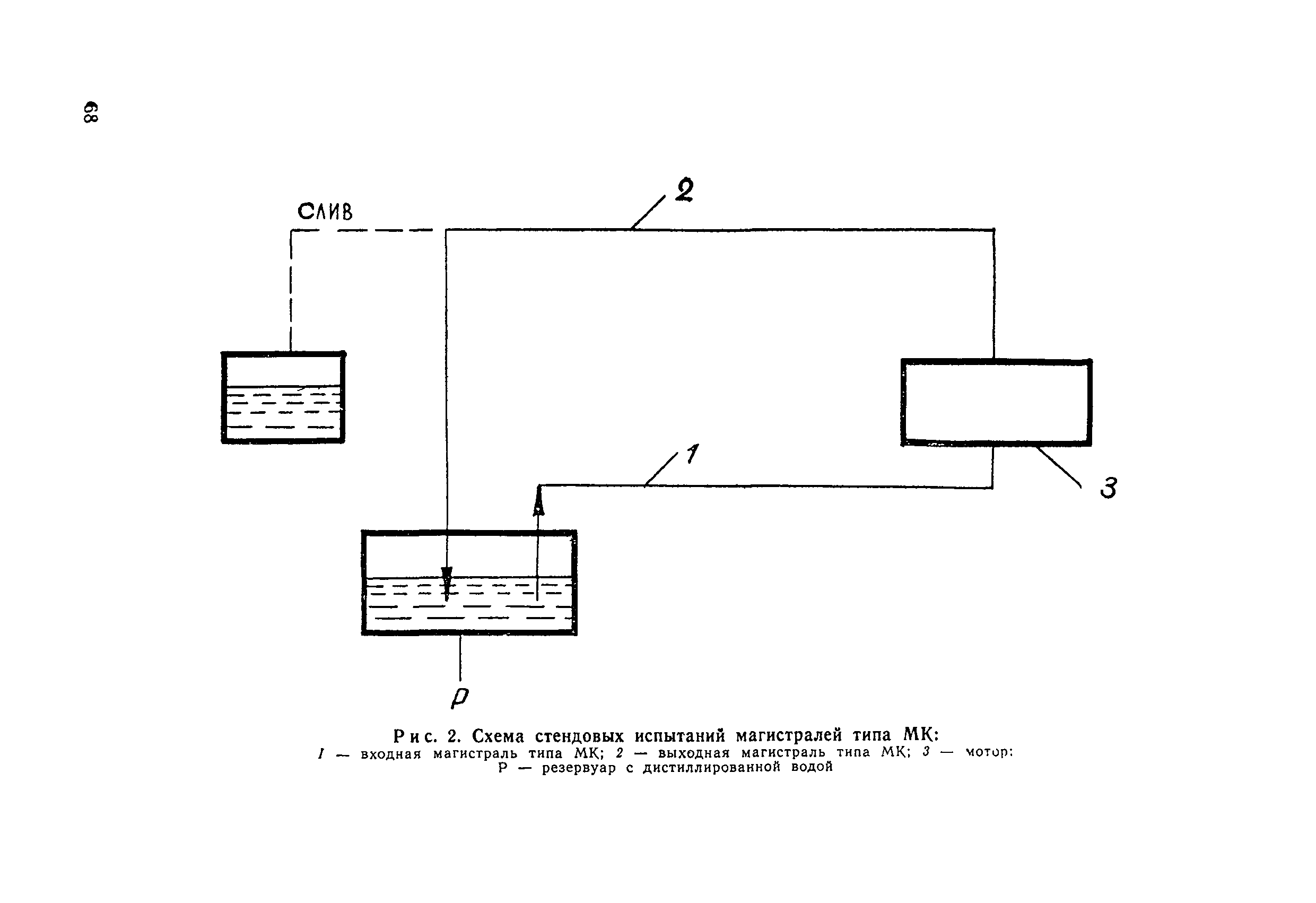
| Область применения: | Методика распространяется на следующие серийно выпускаемые полимерные изделия: - системы инфузионные, трансфузионные, эксфузионные (методика контроля утв. 30.3.78 г.); - шприцы инъекционные (методика контроля утв. 30.3.78 г.) - иглы для родничковой пункции (методика контроля утв. 10.8.79); - катетеры внутривенные, эпидуральные, пупочные детские желудочные детские, носовые детские, кишечные (методика контроля утв. 21.5.80 г.); - контейнеры и их комплекты для взятия, транспортировки, хранения и переливания крови и ее компонентов типа "Компопласт" и "Гемакон" (методика контроля утв. 26.6.85 г.); - диализаторы одноразовые типа ДИП (методика контроля утв. 29.8.83 г.); - магистрали кровопроводящие типа МК (методика контроля утв. 29.8.83); - флаконы для кровезаменителей (методика контроля утв. 29.8.83); - фильтры крови типа ФК (методика контроля утв. 24.5.83) - оксигенаторы типа "Север" (методика контроля утв. 29.8.83) |
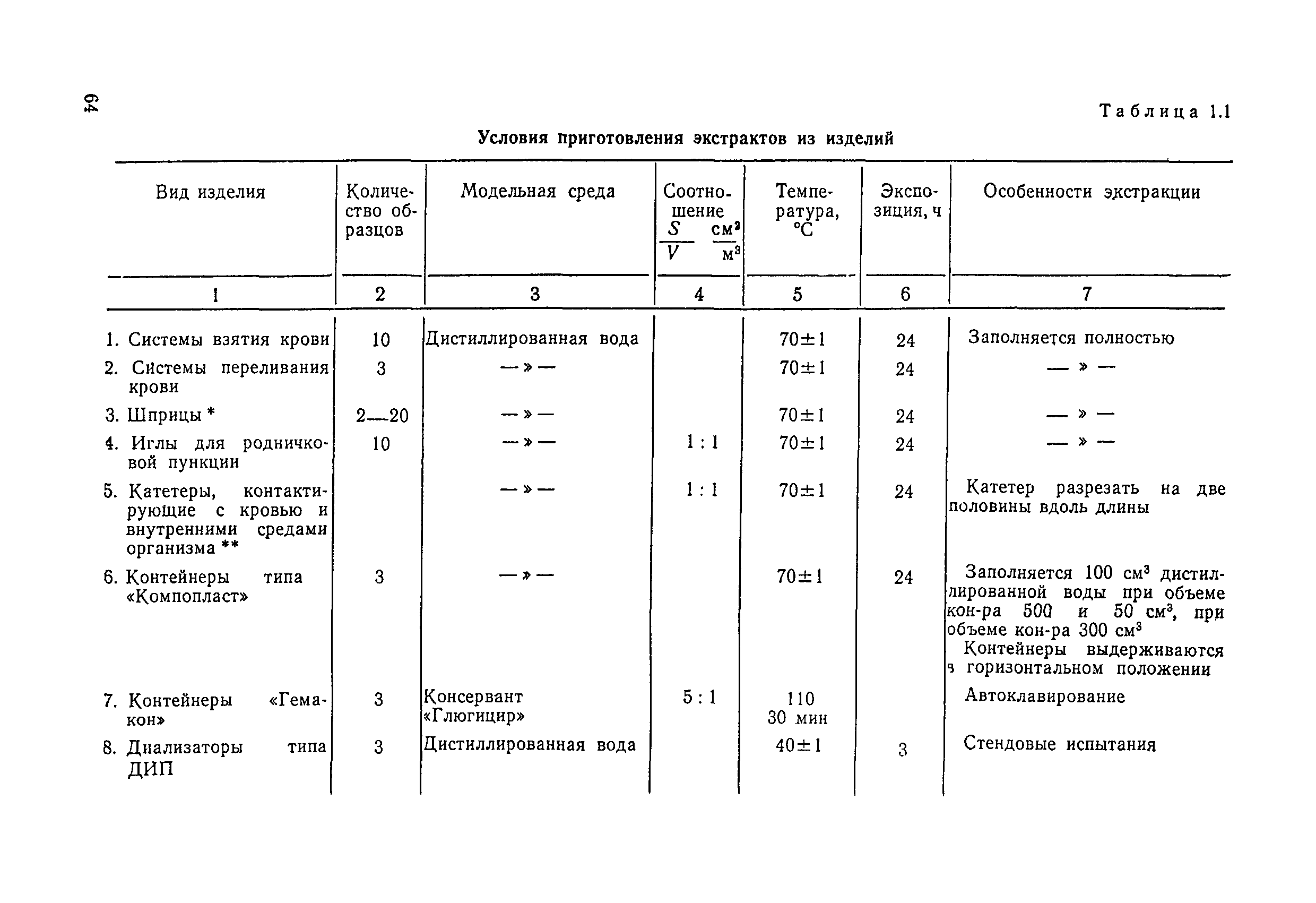
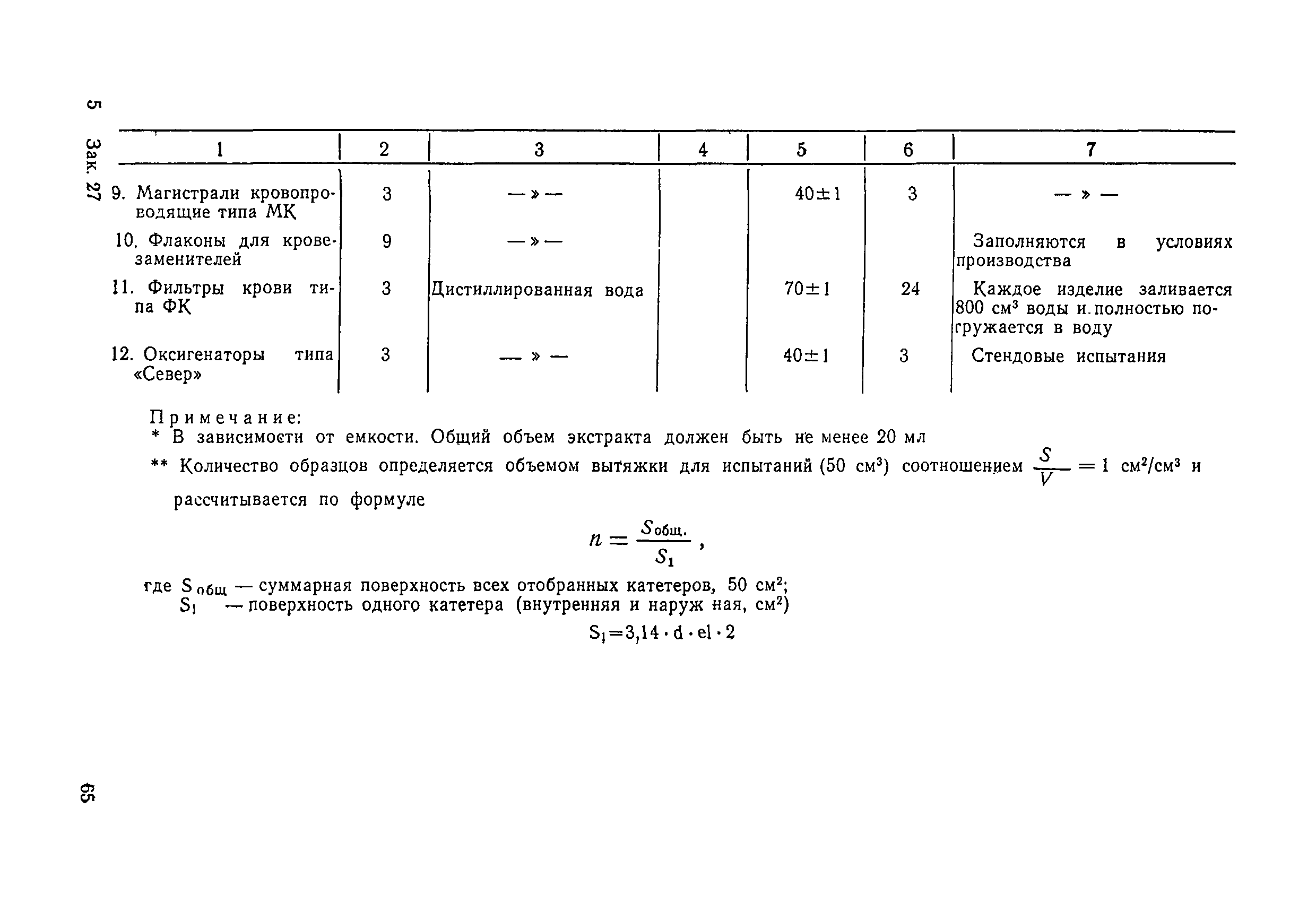
| Оглавление: | 1.1. Общие положения 1.2. Порядок отбора изделий 1.3. Условия приготовления экстрактов из изделий 1.4. Санитарно-химические испытания изделий 1.5. Гемолитический тест 1.6. Токсикологические испытания изделий на мышах 1.7. Оценка результатов испытаний Перечень литературных и справочных источников |
| Разработан: | Московский медицинский стоматологический институт имени Н.А. Семашко Киевский медицинский институт Институт органической химии АН УССР ВНИИИ медицинской техники Минздрава СССР |
| Утверждён: | 27.11.1985 Начальник Управления по внедрению новых лекарственных средств и медицинской техники |
| Расположен в: | |
| Нормативные ссылки: |
|



















 ГОСТ 12.1.007-76 «Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности»
ГОСТ 12.1.007-76 «Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности»