
 ГОСТ Р ИСО 22442-1-2011
ГОСТ Р ИСО 22442-1-2011
Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 1. Менеджмент риска
| Обозначение: |  ГОСТ Р ИСО 22442-1-2011 ГОСТ Р ИСО 22442-1-2011 |
| Обозначение англ: |  GOST R ISO 22442-1-2011 GOST R ISO 22442-1-2011 |
| Статус: | введен впервые |
| Название рус.: | Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 1. Менеджмент риска |
| Название англ.: | Medical devices utilizing animal tissues and their derivatives. Part 1. Application of risk management |
| Дата добавления в базу: | 01.09.2013 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.03.2012 |
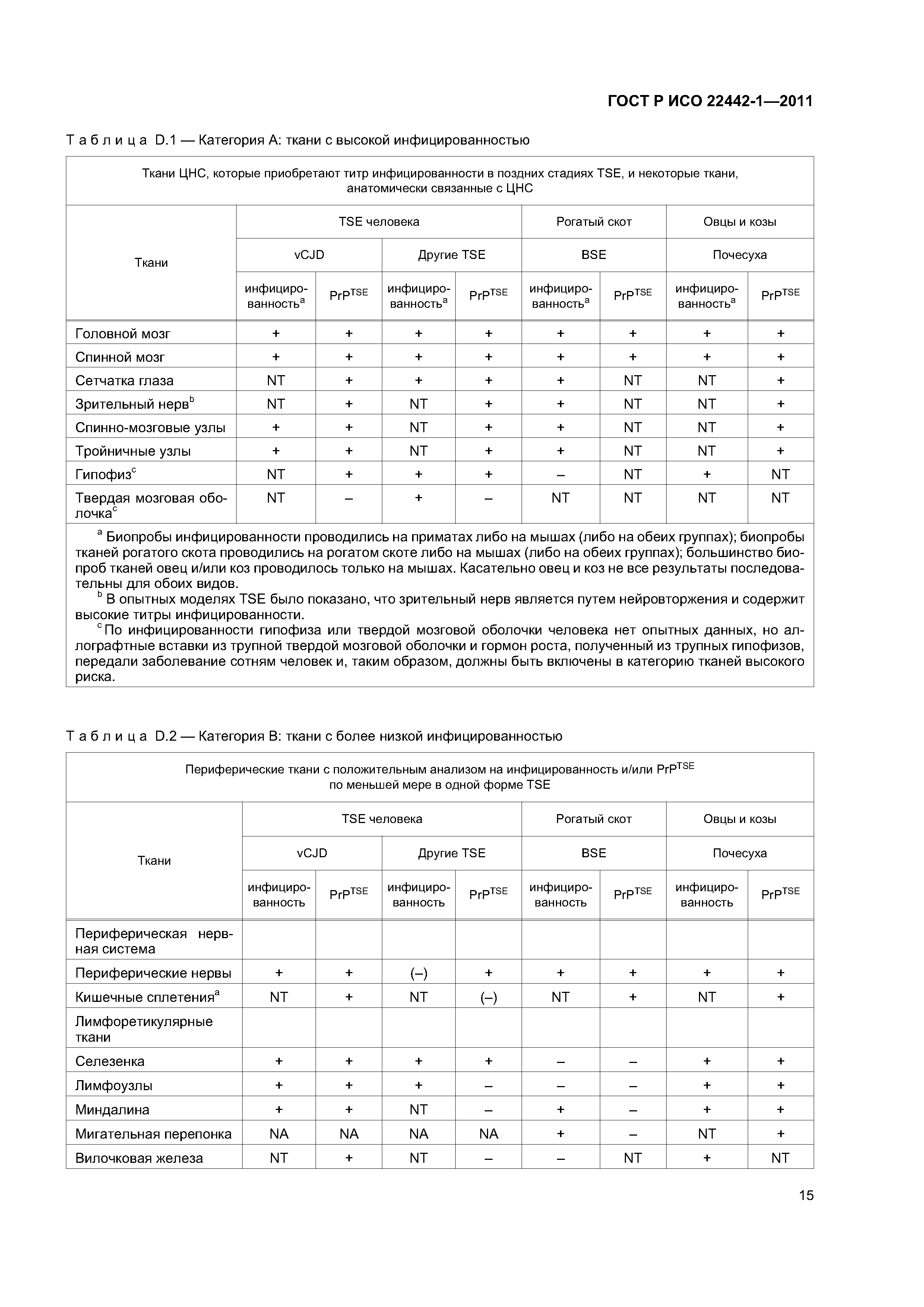
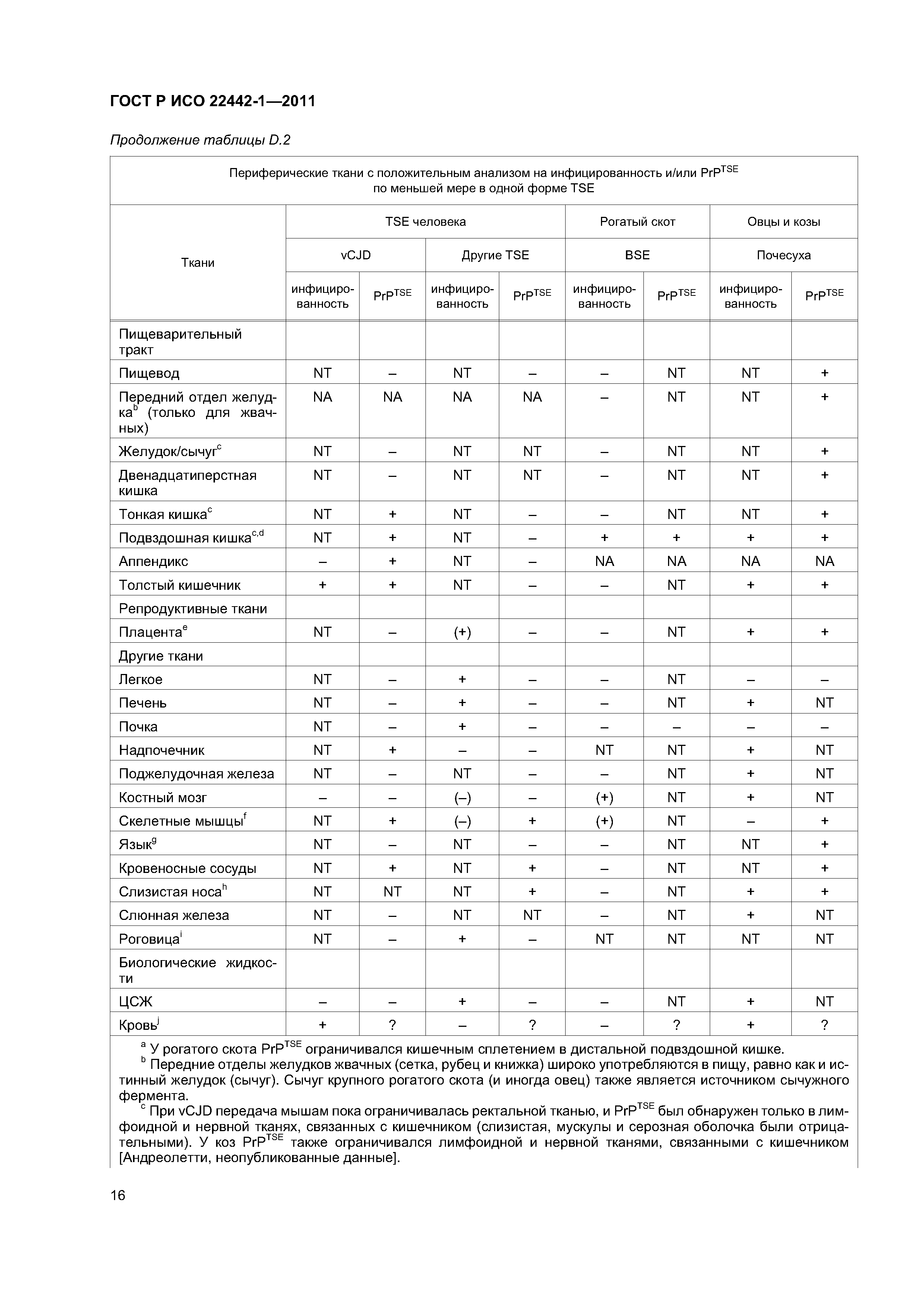
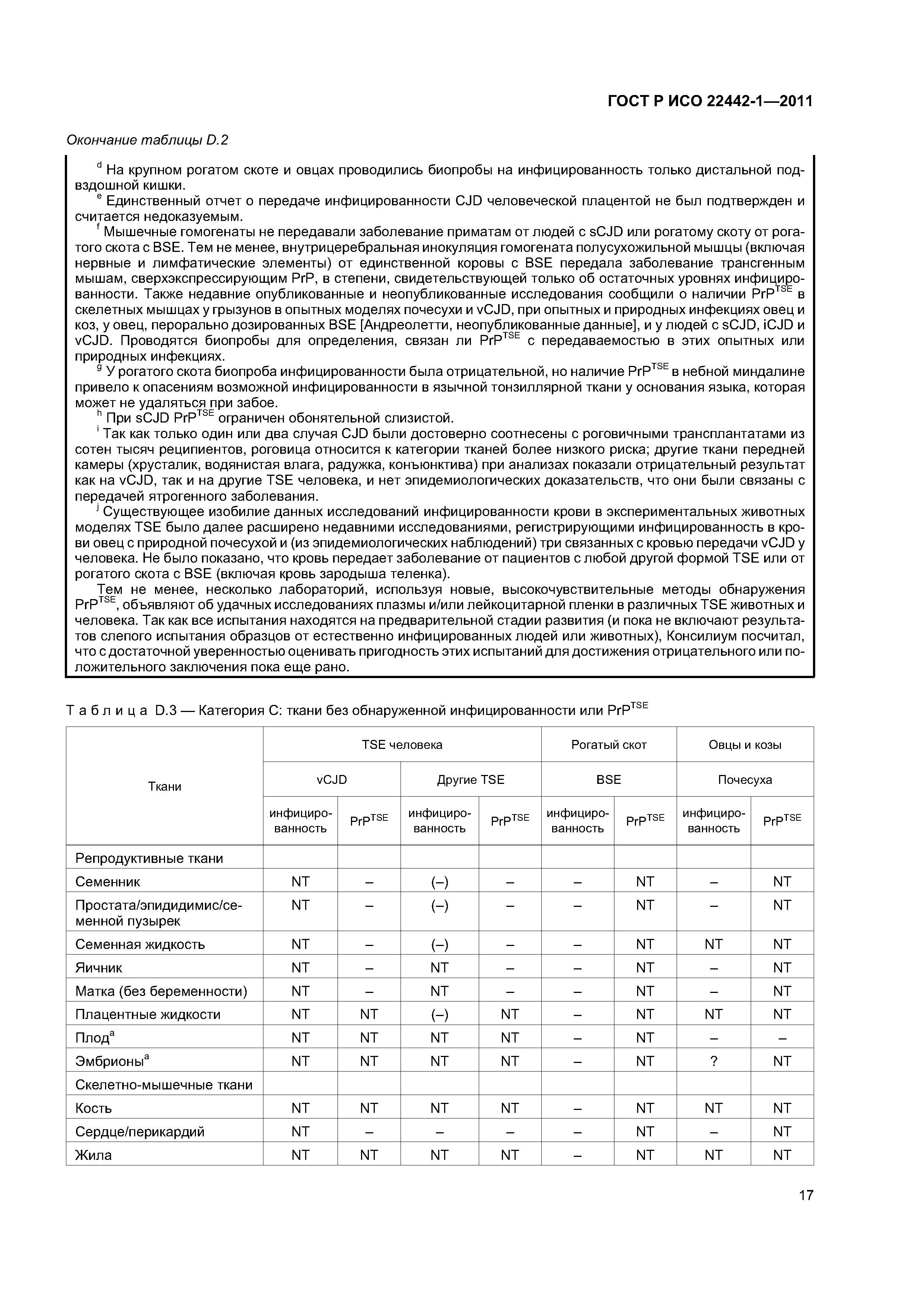
| Область применения: | Стандарт распространяется на медицинские изделия, за исключением диагностических медицинских изделий in vitro, изготовленных с использованием материалов животного происхождения, являющихся нежизнеспособными или приведенными в нежизнеспособное состояние. Стандарт в сочетании с ИСО 14971 определяет процедуру для установления опасности и опасных ситуаций, связанных с такими изделиями, для расчета и оценки возможного риска, контроля такого риска и наблюдения за эффективностью такового контроля. Также стандарт устанавливает процесс принятия решения для допустимости остаточного риска, учитывая баланс остаточного риска, как определено в ИСО 14971, и ожидаемое медицинское преимущество по сравнению с существующими альтернативами. Предназначением стандарта является предоставление требований и рекомендаций по контролю риска, связанного с опасностями, характерными для медицинских изделий, произведенных с использованием животных тканей или их производных, такими как: a) контаминация бактериями, плесневыми или дрожжевыми грибами; b) контаминация вирусами; c) контаминация агентами, вызывающими инфекционные губчатые энцефалопатии (TSE); d) материал, вызывающий нежелательные пирогенные, иммунологические или токсикологические реакции. Схожие принципы могут быть применимы для паразитов и других неклассифицированных патогенных единиц. Стандарт не определяет систему контроля качества для регулирования всех стадий производства медицинских изделий. Стандарт не касается использования тканей человека в медицинских изделиях. |
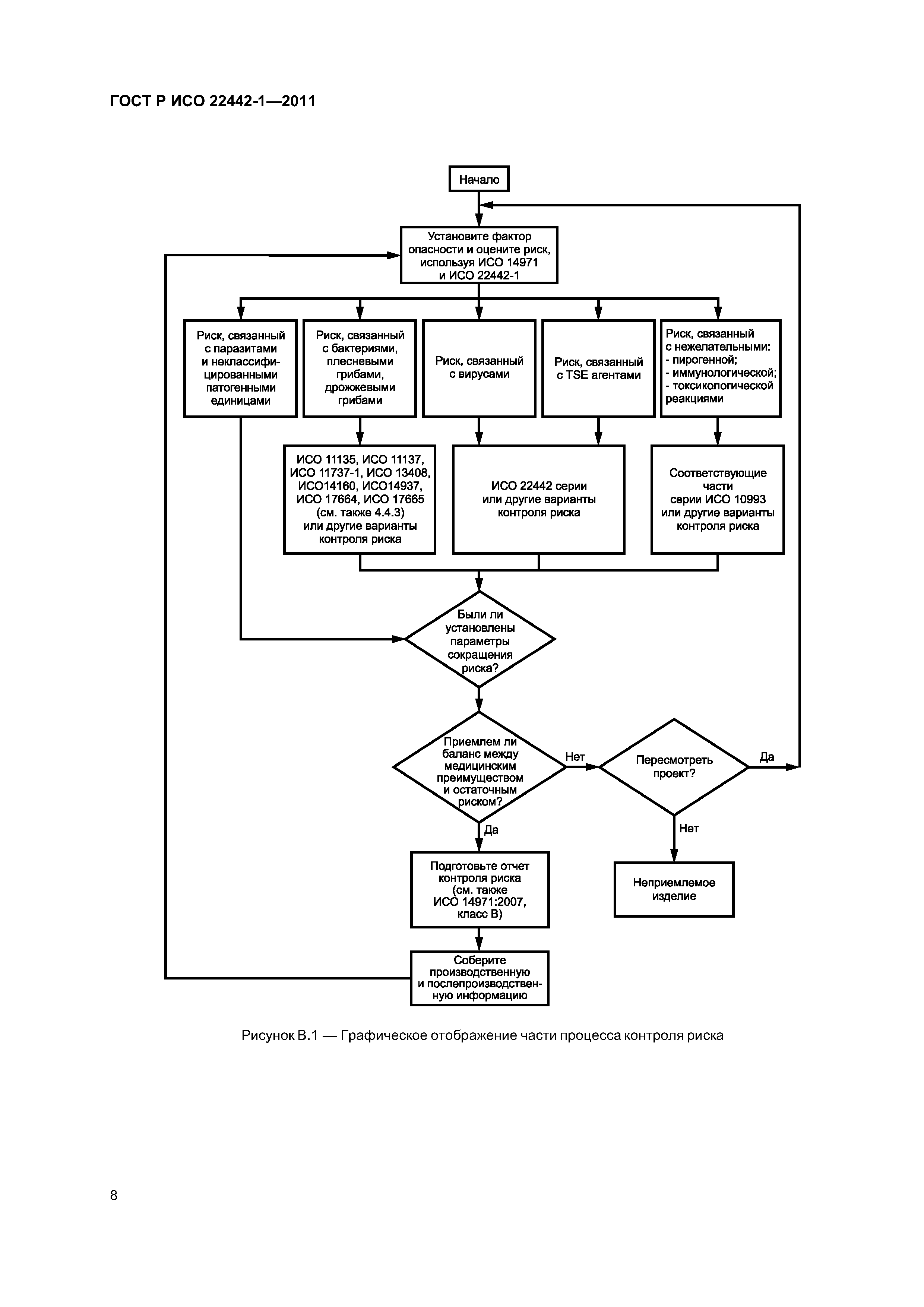
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Процесс контроля риска 4.1 Общая часть 4.2 Анализ риска 4.3 Оценка риска 4.4 Контроль риска 4.5 Оценка приемлемости общего остаточного риска 4.6 Производственная и постпроизводственная информационные системы Приложение А (справочное) Рекомендации по применению настоящего стандарта Приложение В (справочное) Графическое отображение части процесса контроля риска для медицинских изделий, использующих животный материал Приложение С (справочное) Специальные требования для некоторых животных материалов с учетом контроля риска агентов ТSЕ Приложение D (справочное) Информация, связанная с контролем риска ТSЕ Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации Библиография |
| Разработан: | АНО ИМБИИТ |
| Утверждён: | 15.06.2011 Федеральное агентство по техническому регулированию и метрологии (124-ст) |
| Издан: | Стандартинформ (2011 г. ) |
| Расположен в: | |
| Нормативные ссылки: |
|























 ГОСТ Р ИСО 10993-1-2009 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования»
ГОСТ Р ИСО 10993-1-2009 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования»