
 ГОСТ Р 53133.2-2008
ГОСТ Р 53133.2-2008
Технологии лабораторные клинические. Контроль качества клинических лабораторных исследований. Часть 2. Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов
| Обозначение: |  ГОСТ Р 53133.2-2008 ГОСТ Р 53133.2-2008 |
| Обозначение англ: |  GOST R 53133.2-2008 GOST R 53133.2-2008 |
| Статус: | введен впервые |
| Название рус.: | Технологии лабораторные клинические. Контроль качества клинических лабораторных исследований. Часть 2. Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов |
| Название англ.: | Medical laboratory technologies. Quality control of clinical laboratory tests. Part 2. Rules for intra-laboratory quality control of quantitative methods of clinical laboratory tests using control materials |
| Дата добавления в базу: | 01.09.2013 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.01.2010 |
| Область применения: | Стандарт устанавливает общие требования к проведению внутрилабораторного контроля качества количественных исследований, выполняемых в клинико-диагностических лабораториях, организациях здравоохранения, в составе которых действуют указанные лаборатории. Стандарт предназначен для применения всеми организациями, учреждениями и предприятиями, а также индивидуальными предпринимателями, деятельность которых связана с оказанием медицинской помощи гражданам Российской Федерации |
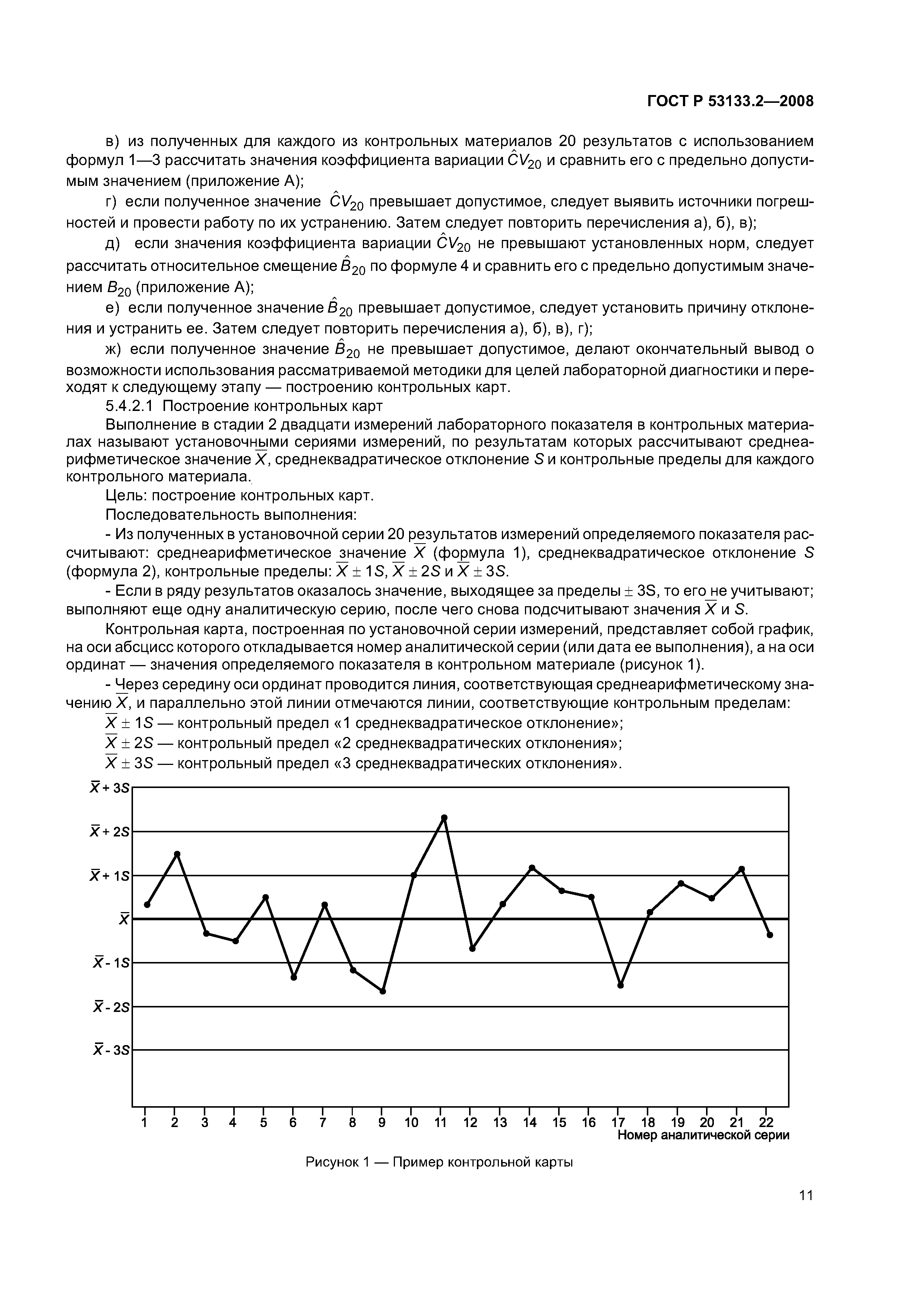
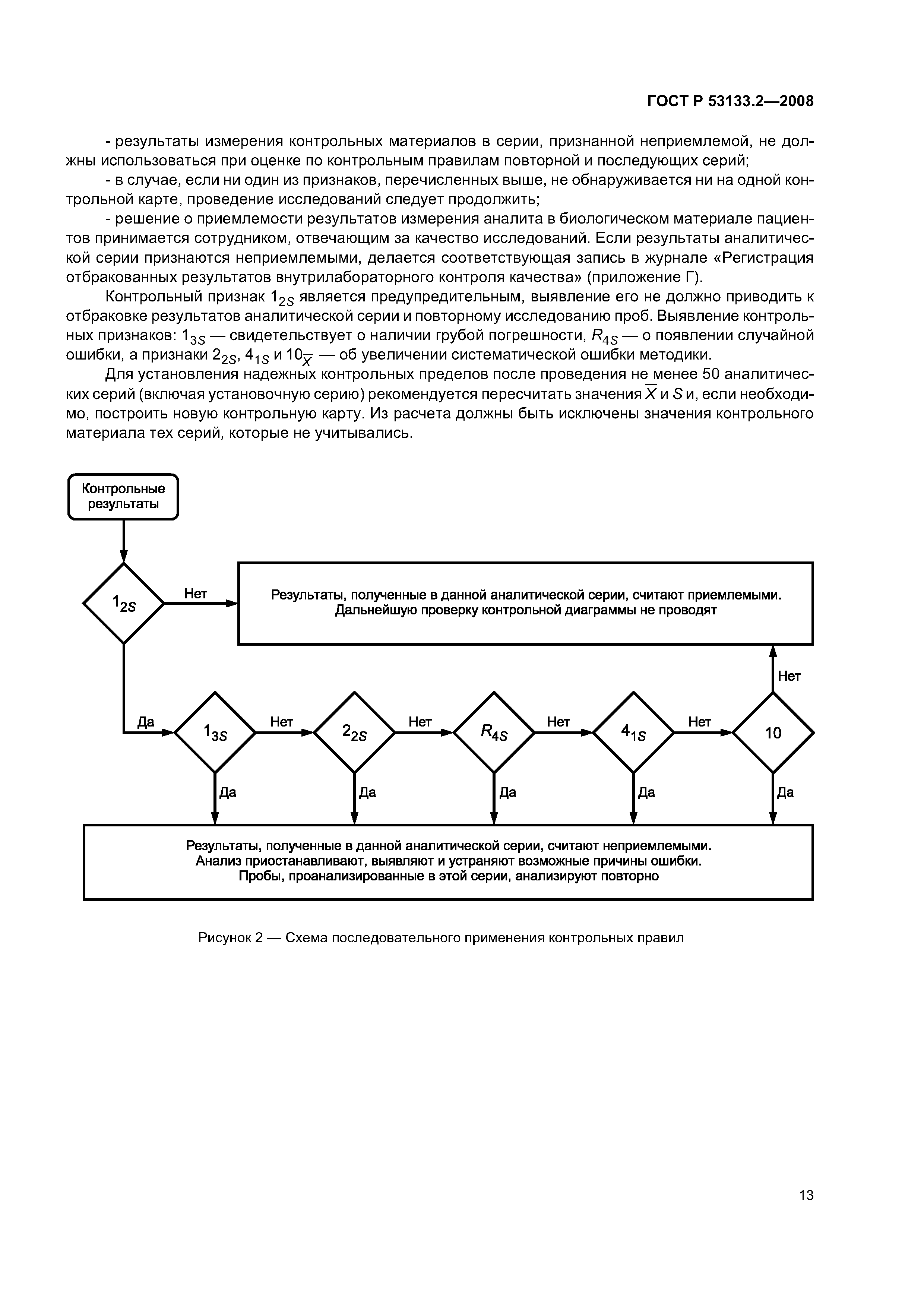
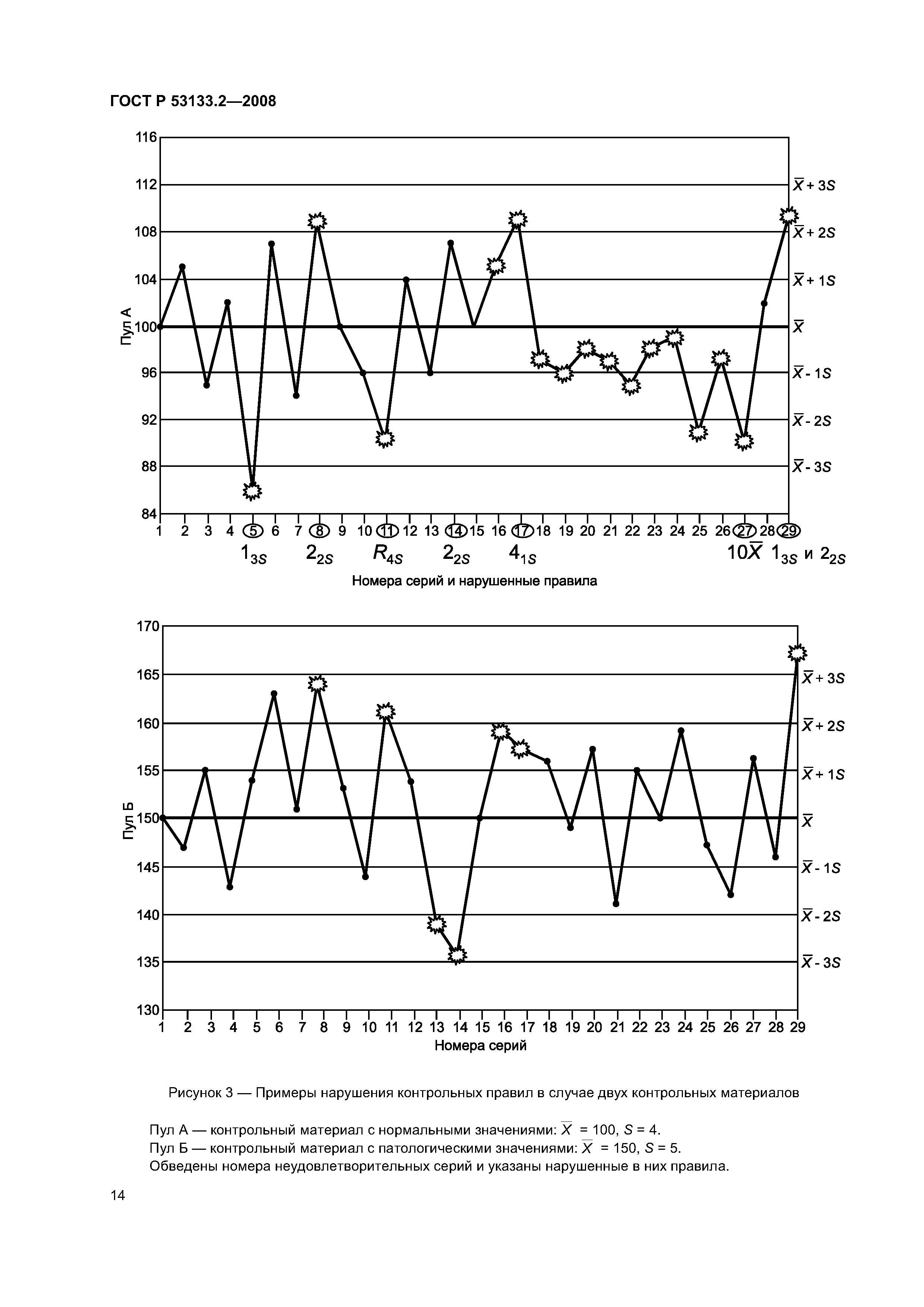
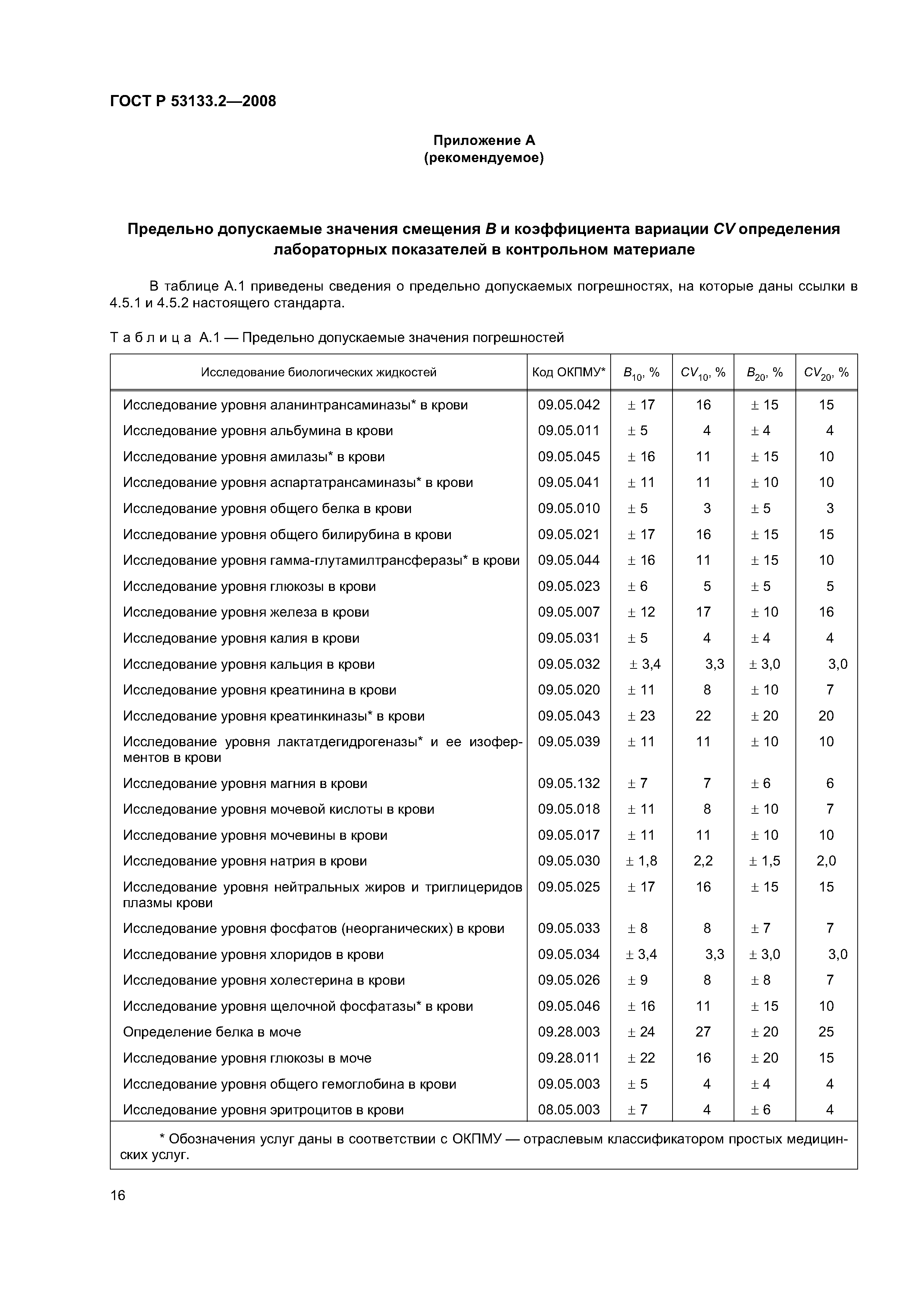
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Внутрилабораторный контроль в системе управления качеством клинических лабораторных исследований 4.1 Общие положения 4.2 Общие принципы организации и проведения внутрилабораторного контроля качества в клинико-диагностических лабораториях 5 Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов 5.1 Контрольные материалы 5.2 Использование контрольных материалов 5.3 Статистические основы оценки погрешностей количественных методов исследования с применением контрольных материалов 5.4 Порядок проведения внутрилабораторного контроля качества Приложение А (рекомендуемое) Предельно допускаемые значения смещения В и коэффициента вариации CVопределения лабораторных показателей в контрольном материале Приложение Б (рекомендуемое) Форма регистрации результатов оценки повторяемости результатов измерения Приложение В (рекомендуемое) Форма регистрации результатов установочных серий измерений показателя в контрольных материалах Приложение Г (рекомендуемое) Форма регистрации отбракованных результатов внутрилабораторного контроля качества Библиография |
| Разработан: | Лаборатория проблем клинико-лабораторной диагностики Московской медицинской академии им. И.М. Сеченова Росздрава Государственный научный центр профилактической медицины Научно-исследовательский институт нейрохирургии Российской академии медицинских наук ЗАО Аналитика |
| Утверждён: | 18.12.2008 Федеральное агентство по техническому регулированию и метрологии (559-ст) |
| Издан: | Стандартинформ (2009 г. ) |
| Расположен в: | |
| Нормативные ссылки: |
|




















 ГОСТ Р ИСО 5725-1-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения»
ГОСТ Р ИСО 5725-1-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения»