
 ГОСТ Р ИСО 14708-1-2012
ГОСТ Р ИСО 14708-1-2012
Имплантаты хирургические. Активные имплантируемые медицинские изделия. Часть 1. Общие требования к безопасности, маркировке и информации, предоставляемой изготовителем
| Обозначение: |  ГОСТ Р ИСО 14708-1-2012 ГОСТ Р ИСО 14708-1-2012 |
| Обозначение англ: |  GOST R ISO 14708-1-2012 GOST R ISO 14708-1-2012 |
| Статус: | введен впервые |
| Название рус.: | Имплантаты хирургические. Активные имплантируемые медицинские изделия. Часть 1. Общие требования к безопасности, маркировке и информации, предоставляемой изготовителем |
| Название англ.: | Implants for surgery. Active implantable medical devices. Part 1. General requirements for safety, marking and for information to be provided by the manufacturer |
| Дата добавления в базу: | 01.10.2014 |
| Дата актуализации: | 01.01.2021 |
| Дата введения: | 01.01.2014 |
| Область применения: | Стандарт устанавливает общие требования к активным имплантируемым медицинским изделиям. Методы испытаний, приведенные в стандарте, предназначены для оценки соответствия на образцах изделий и не предназначены для испытаний изготавливаемой продукции. Стандарт применим к активным имплантируемым медицинским изделиям, приводимых в действие не только силой электрического тока, но и с помощью других источников энергии. Стандарт также применим к некоторым видам неимплантируемых частей медицинских изделий и принадлежностей к ним. |
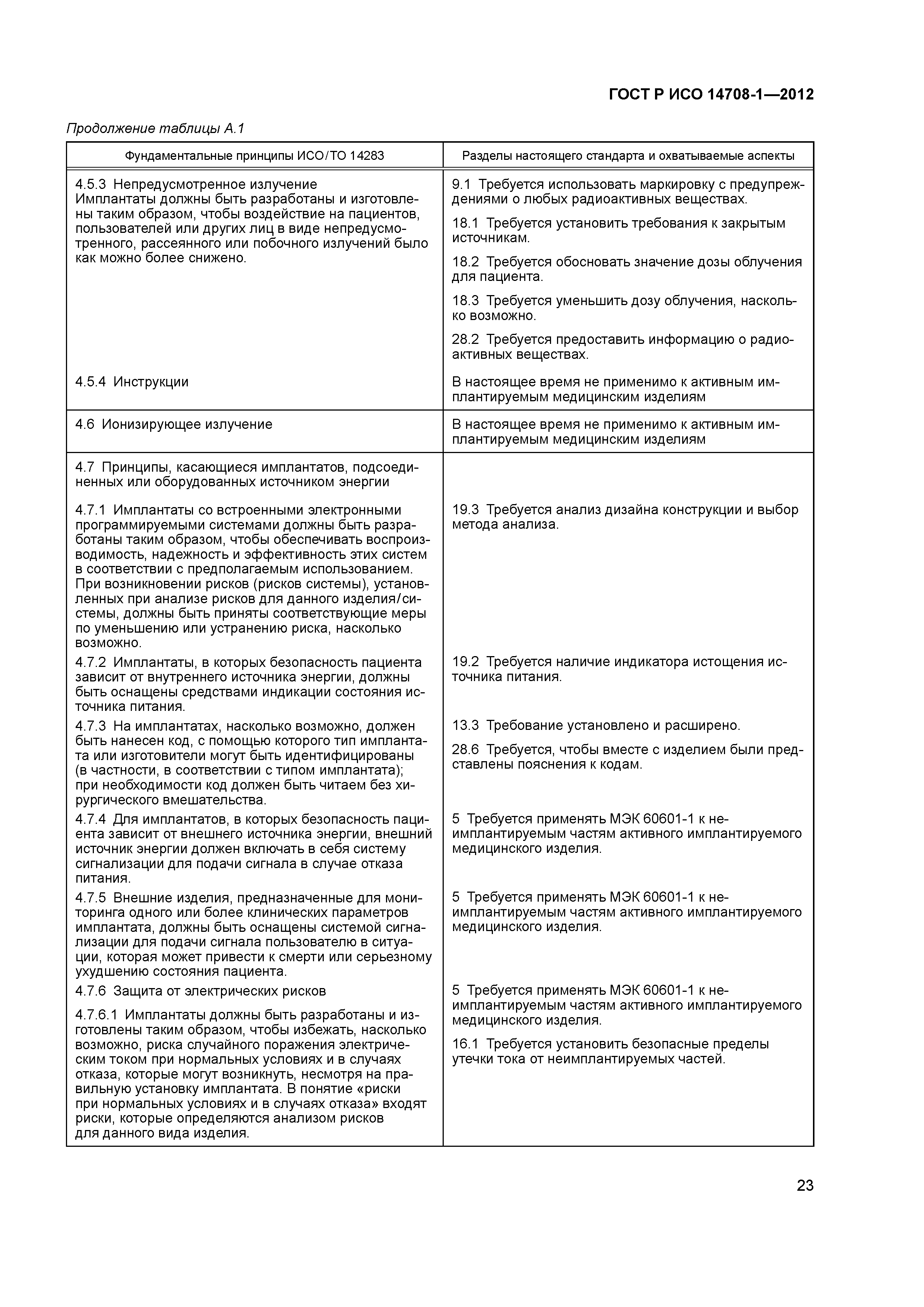
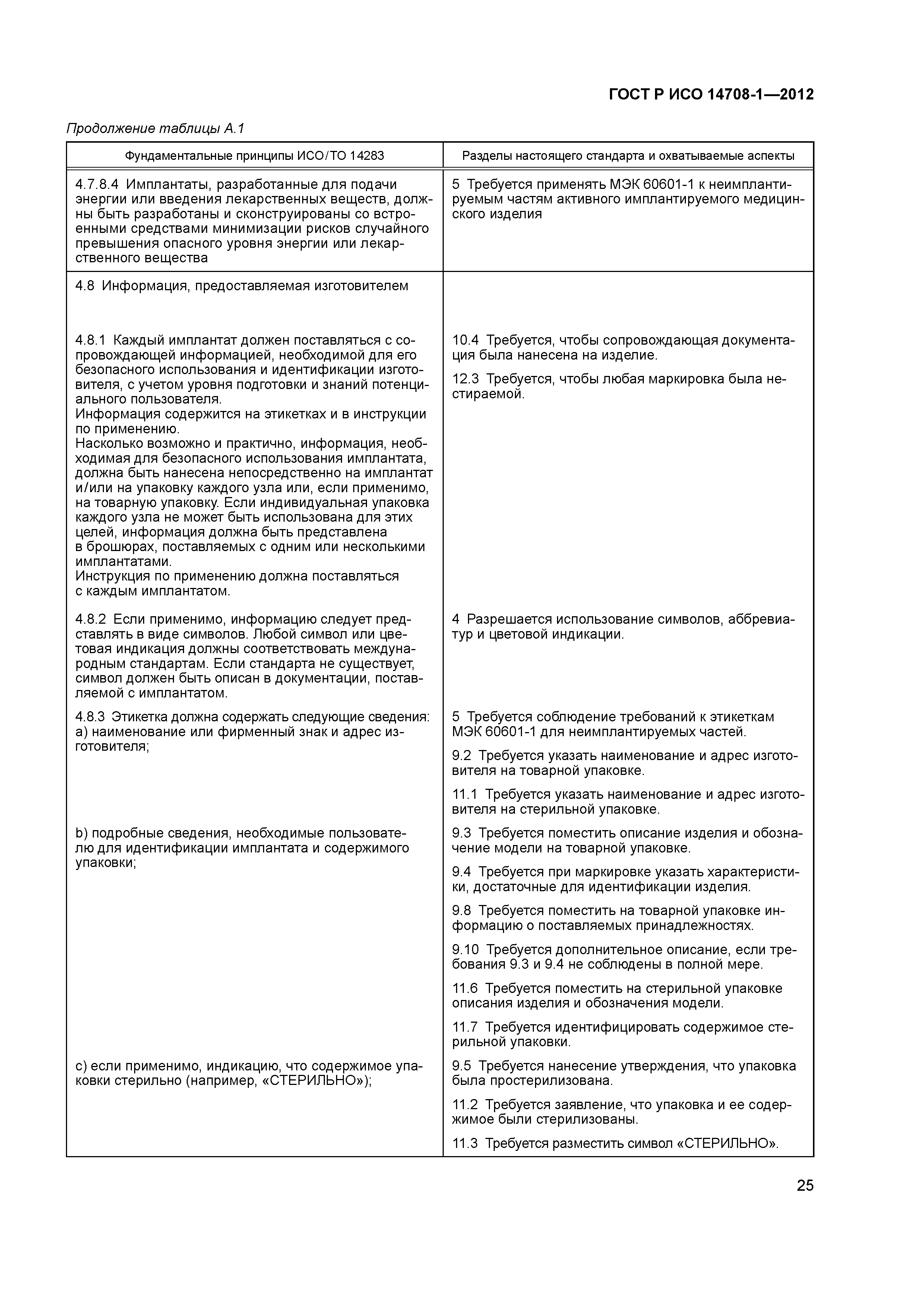
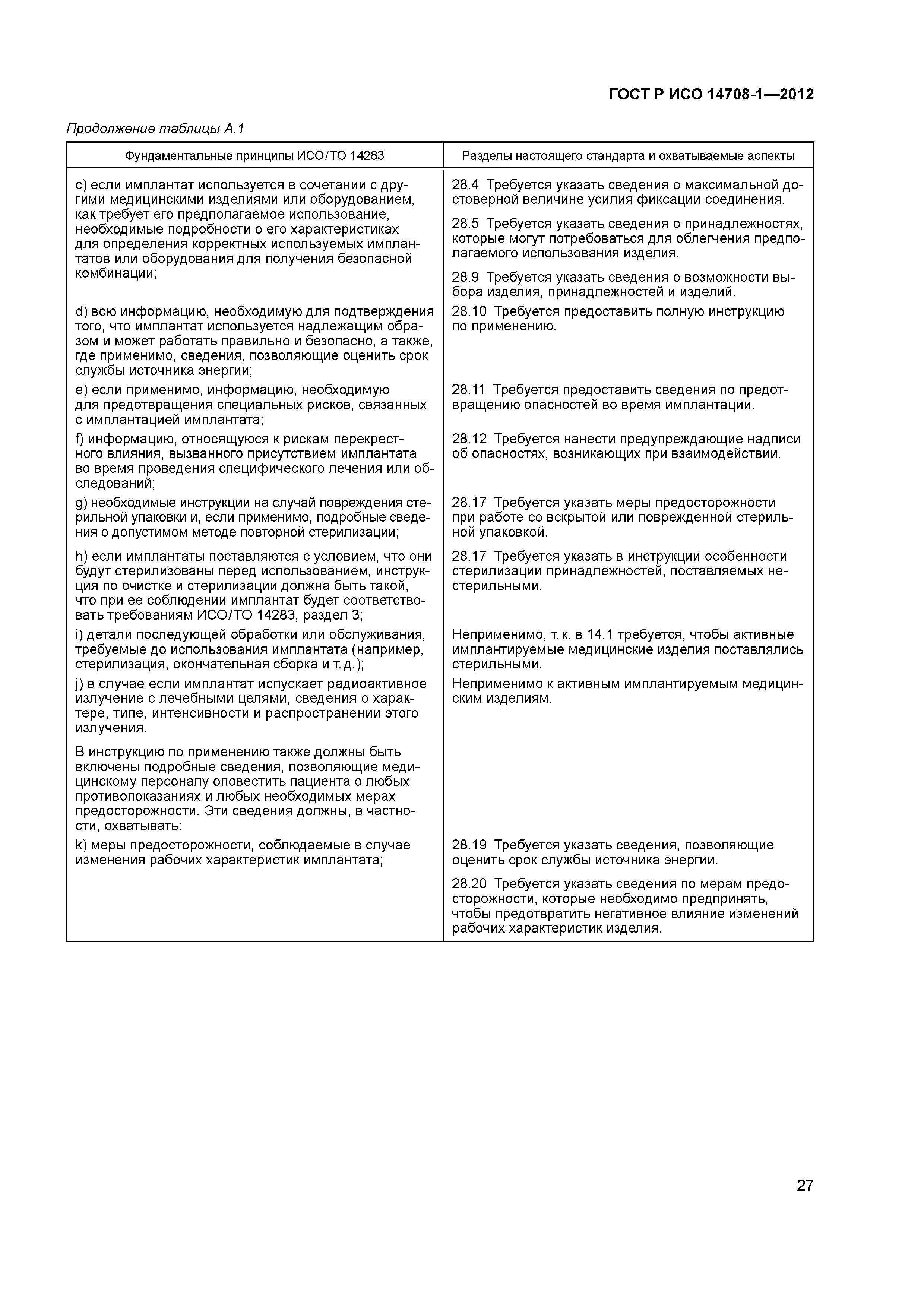
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Символы и аббревиатуры 5 Общие требования к неимплантируемым частям 6 Требования к активным имплантируемым медицинским изделиям определенных видов 7 Общие требования к упаковке 8 Общая маркировка активных имплантируемых медицинских изделий 9 Маркировка товарной упаковки 10 Конструкция товарной упаковки 11 Маркировка стерильной упаковки 12 Конструкция одноразовой упаковки 13 Маркировка активных имплантируемых медицинских изделий 14 Защита от непреднамеренных биологических воздействий, вызванных активным имплантируемым медицинским изделием 15 Защита пациента или пользователя от вреда, вызванного внешними физическими особенностями активного имплантируемого медицинского изделия 16 Защита пациента от вреда, вызванного электрическим током 17 Защита пациента от вреда, вызванного тепловыделениями 18 Защита от ионизирующего излучения, выделяемого или испускаемого активным имплантируемым медицинским изделием 19 Защита от непреднамеренных воздействий, вызванных изделием 20 Защита изделия от повреждений, вызванных применением наружных дефибрилляторов 21 Защита изделия от изменений, вызванных электрическими полями высокой энергии, приложенными непосредственно к пациенту 22 Защита активного имплантируемого медицинского изделия от изменений, вызванных применением разнородных видов лечения 23 Защита активного имплантируемого медицинского изделия от воздействия механических сил 24 Защита активного имплантируемого медицинского изделия от повреждений, вызванных электростатическим разрядом 25 Защита активного имплантируемого медицинского изделия от повреждений, вызванных изменениями атмосферного давления 26 Защита активного имплантируемого медицинского изделия от повреждений, вызванных перепадами температур 27 Защита активного имплантируемого медицинского изделия от электромагнитного неионизирующего излучения 28 Сопровождающая документация Приложение А (справочное) Соответствие между фундаментальными принципами ИСО/ТО 14283 и разделами настоящего стандарта Приложение В (справочное) Связь между разделами настоящего стандарта и фундаментальными принципами, перечисленными в приложении А Приложение С (справочное) Обоснование Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации Библиография |
| Разработан: | ФГБУ НЦССХ им. А.Н. Бакулева РАМН |
| Утверждён: | 30.08.2012 Федеральное агентство по техническому регулированию и метрологии (265-ст) |
| Издан: | Стандартинформ (2014 г. ) |
| Расположен в: | |
| Нормативные ссылки: |
|













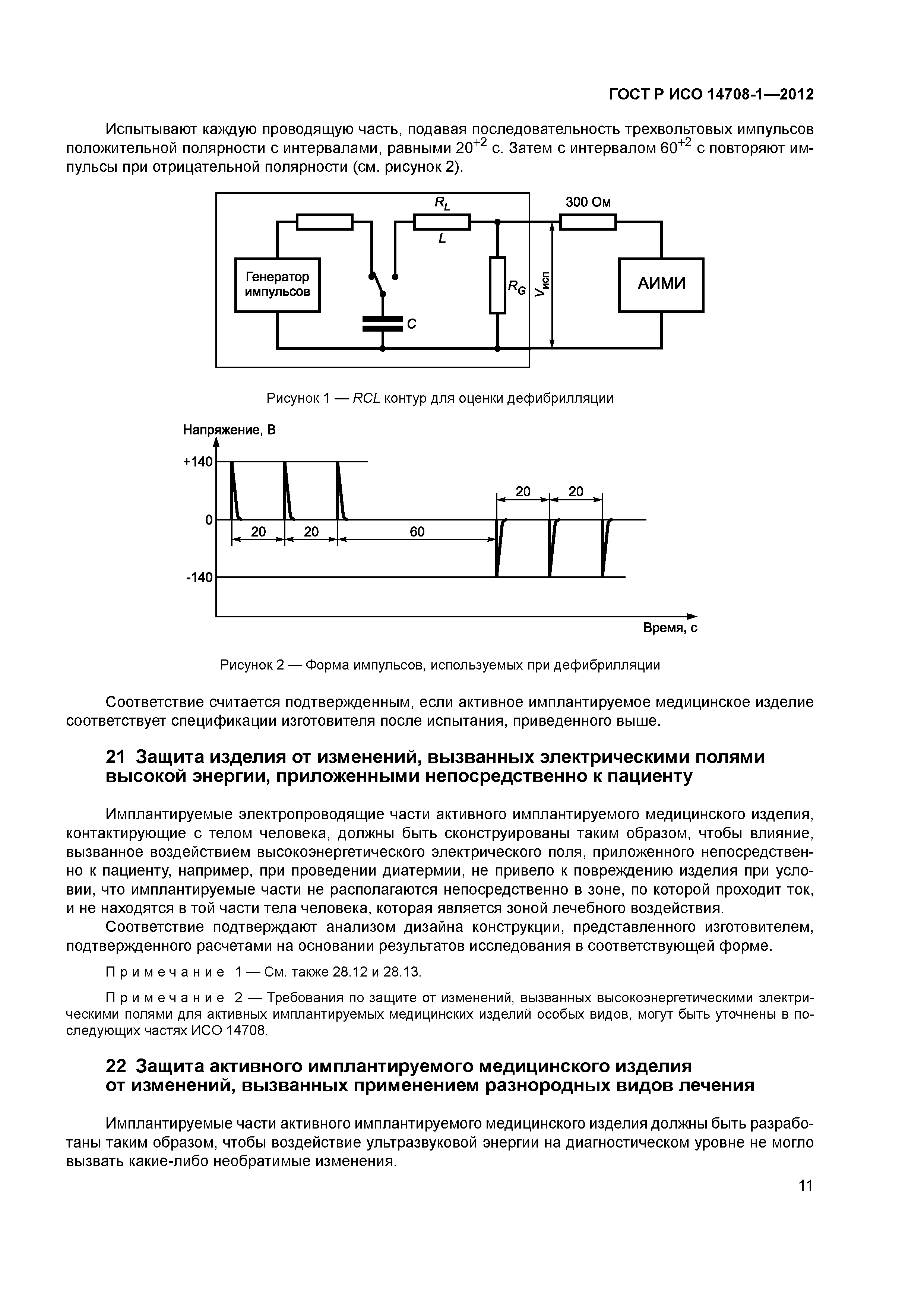






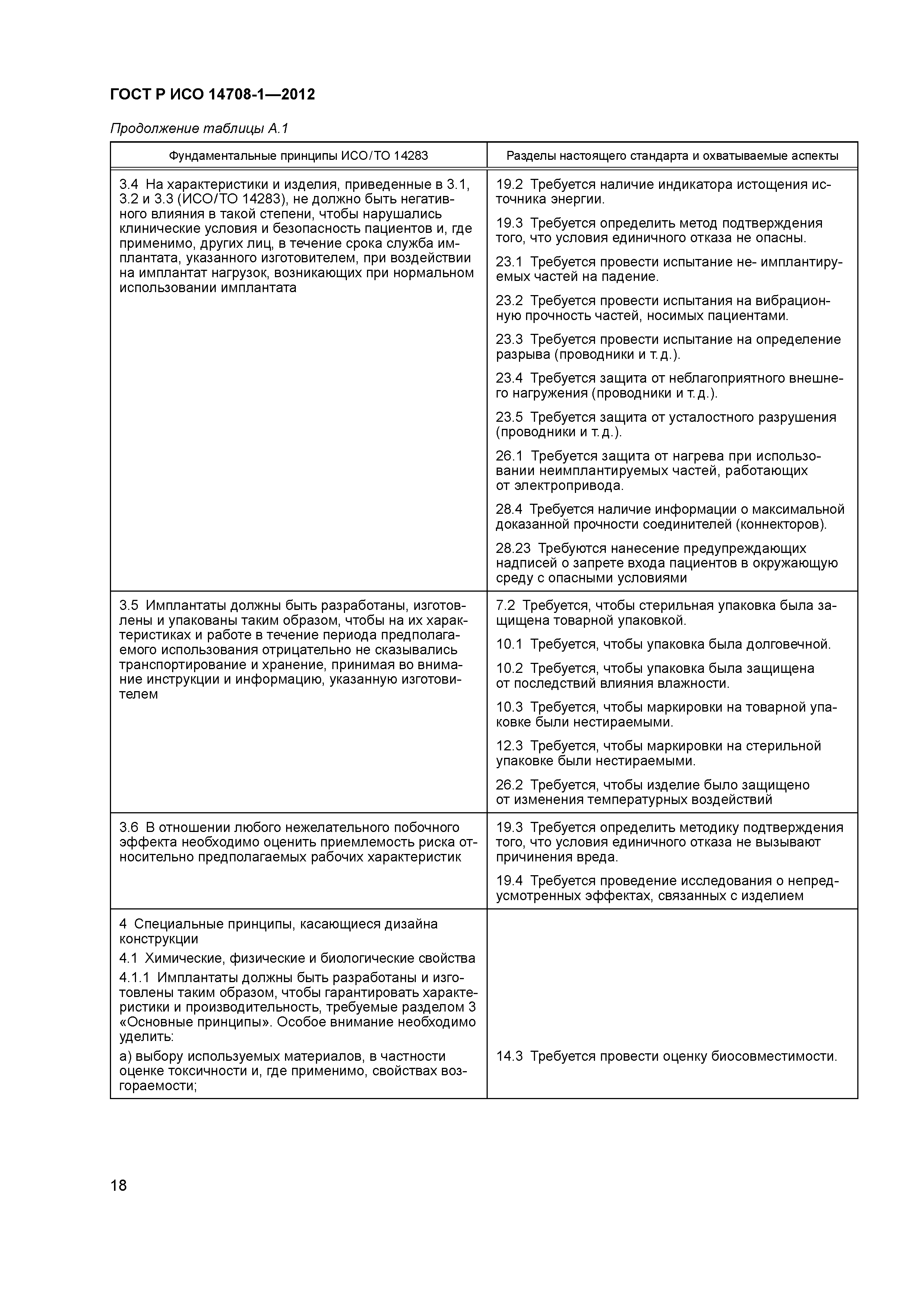
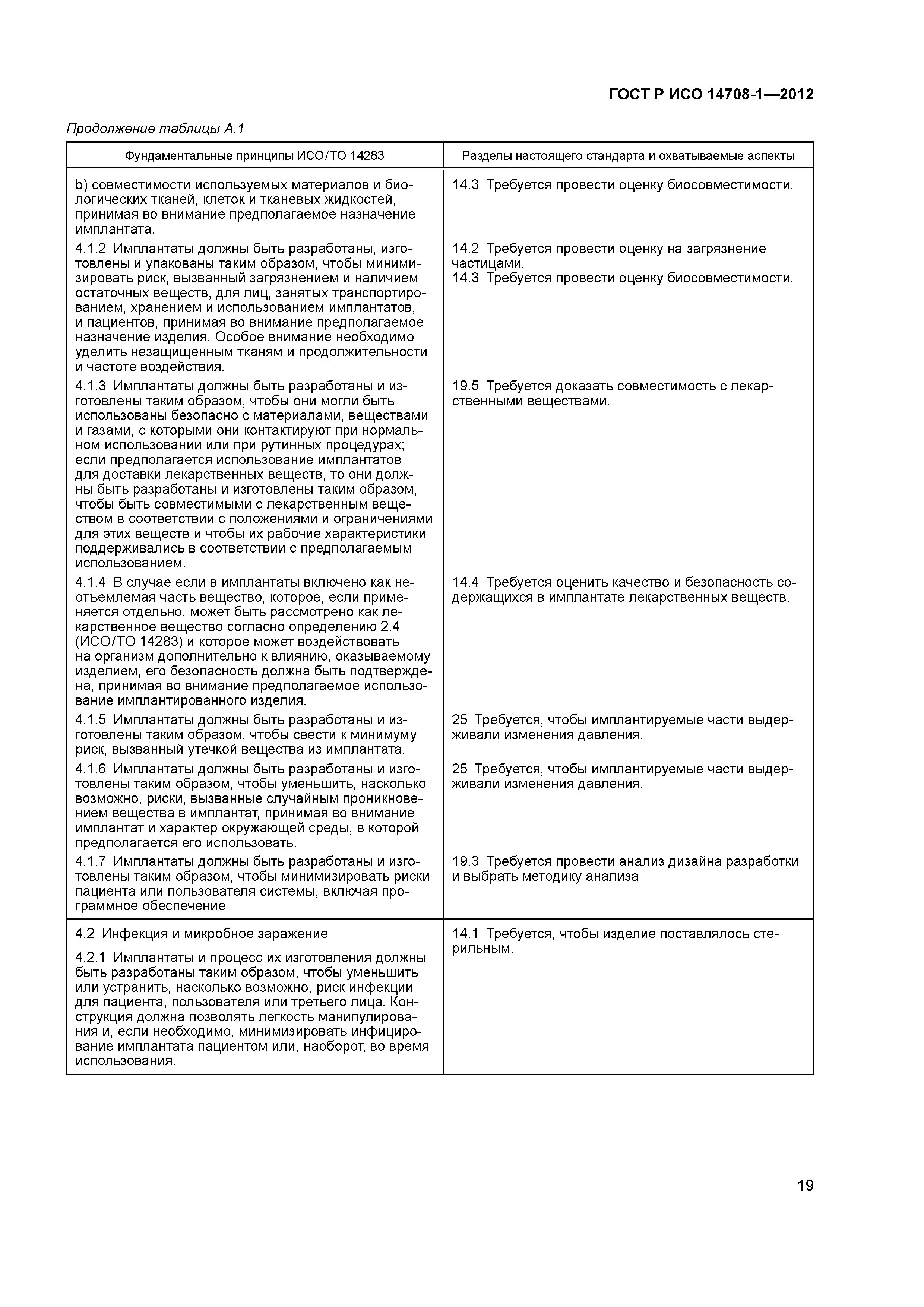

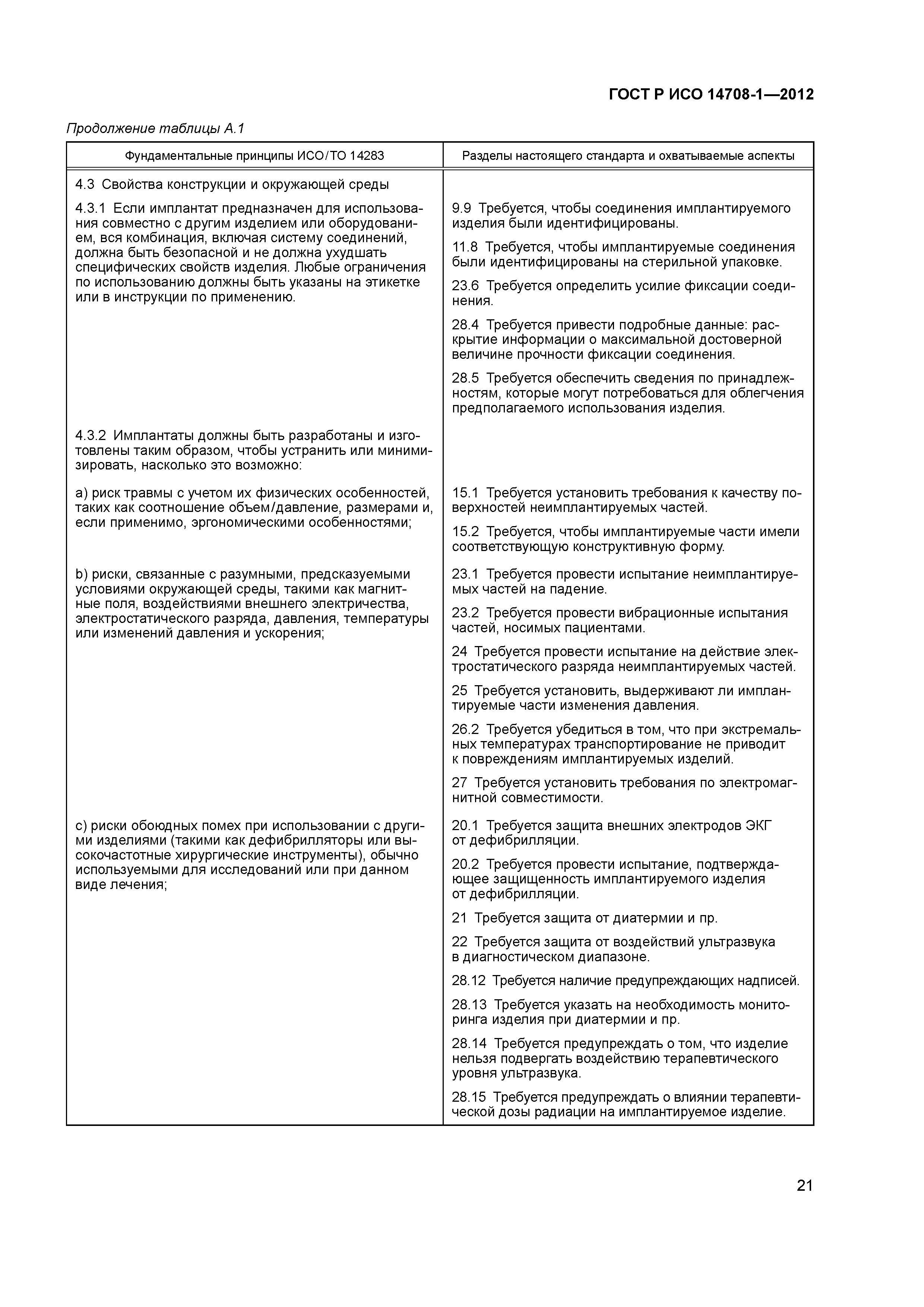












 ГОСТ Р ИСО 11607-2003 «Упаковка для медицинских изделий, подлежащих финишной стерилизации. Общие требования»
ГОСТ Р ИСО 11607-2003 «Упаковка для медицинских изделий, подлежащих финишной стерилизации. Общие требования»